Изобретение относится к способу получения новых производных 1,5-бенз оксатиепина или их солей, которые проявляют высокую активность блокирования cepoTOHHHOBbDcSj-рецепторов, а также антагонизм действию кальция, вызывают облегчение спазмов сосудов головного мозга, улучшают ренальную циркуляцию, проявляют диуретическую и противотромбозную активность и являются полезными в качестве профилактических и терапевтических агентов против игаемических сердечных отклонений, таких как пекторальная анги- на и инфаркты миокарда, тромбозы, гипертония, и церебральных циркулярных расстройств, таких как спазмы сосудов головного мозга.
Целью изобретения является полу- чение новых производных 1,5-бензокса- тиепина, обладающих ценными фармакологически активными свойствами, новыми в этом ряду соединений.
Способ иллюстрируется следующими примерами.
Пример 1. В 350 мл ацетона растворяют 44,7 г 2-меркапто-4-мет- оксифенола и 88 г метилбромацетата и к раствору добавляют 88 г безводно- го калия с последующим перемешиванием при комнатной температуре в течение 5 ч и нагреванием при кипячении с обратным холодильником в течение 5 ч После охлаждения смеси неорганическое вещество отфильтровьшают и фильтрат концентрируют при пониженном давлении Остаток перекристаллизовывают из смеси этилацетата и гексана.
Получают 65 г бесцветных кристал- лов метил-4-метокси-2-метокси-карбо- нилметилтиофеноксиацетата, т.пл. 78°С.
Вычислено, %: С 51,99; Н 5,37.
С 13 Н 16 OgS
Найдено, % С 52,18; Н 5,37.
Пример 2. В 300 мл М,М-ди- метилформамида растворяют 94,4 г метил-4-метокси-2-метоксикарбонил- метилтиофеноксиацетата и к раствору по каплям добавляют 67 г 28%-ного метилата натрия при охлаждении льдом и перемешивании. Реакционную смесь перемешивают в течение 1 ч и выливают в охлажденную льдом воду, содержащую разбавленную соляную кислоту, осадок собирают фильтрованием, промывают водой, сушат и затем перекрис-
д
о
5
о
„
5
5
0
5
таллизовывают из смеси этилацетата и гексана.
Получают 58,7 г бесцветных кристаллов метил-7-метокси-3-оксо- 3,4- ДИГИДРО-2Н-1,5-бензоксатиепин-4- карбоксилата, т.пл. 79-81°С.
Вычислено, %: С 53,72; Н 4,51.
C,H,0,S
Найдено, %: С 53,72; Н 4,40.
Пример 3. В 600 мл ацетона растворяют 60 г 2-меркапто-4-метокси- фенола и 67 г хлорацетонитрила и к раствору при комнатной -температуре в потоке азотного газа при перемешивании добавляют 125 г безводного карбоната калия с последующим перемешиванием при комнатной температуре в течение 3 ч и нагреванием при кипячении с обратным холодильником в течение 5 ч. После охлаждения реакционной смеси неорганическое вещество отфиль- тровьшают и фильтрат концентрируют при пониженном давлении. Остаток перекристаллизовьшают из этанола.
Получают бесцветные призмы 2-циа- нометилтио-4-метоксифеноксиацетонит- рила. Выход 65 г, т.пл. 53-54 С.
Вычислено, %: С 56,39; Н 4,30; N 11,96.
С, N,
Найдено, %: С 56,57; Н 4,32; N 11,78.
Пример 4. В 120 мл М,М-ди- метилформамида растворяют 30 г 2-циа- нометилтио-4-метоксифеноксиацетонит- рила и к раствору по каплям добавляют 30 г 28%-ного метилата натрия при охлаждении льдом и в потоке азотного газа при перемешивании, перемешивание продолжают в течение 2ч. Реакционную смесь выливают в охлажденную льдом воду, содержащую 12 г уксусной кислоты, осадок собирают фильтрованием, промьшают водой и перекристал- лизовьшают из хлороформа.
Получают бесцветные призмы 3-ами- но-7-метокси-2Н-1,5-бензоксатиепин- 4-карбонитрила. Выход 19,5 г, т.пл. 203-205°С.
Пример 5. В 60 мл этанола суспендируют 6,0 г З-амино-7-метокси- 2Н-1,5-бензоксатиепин-4-карбонитрШ1а, к суспензии добавляют 18 мп концентрированной соляной кислоты с последующим перемешиванием при 80-90 С в течение 30 мин. После охлаждения реакционной смеси выделившийся хлористьш аммоний отфильтровывают и фильтрат
концентрируют при пониженном давлении. Остаток перекристаллизовывают из смеси этилацетат - гексан.
Получают бесцветные призмы 7-мет- окси-3-оксо-3,4-ДИГИДРО-2Н-I,5-бенз- оксатиепин-А-карбонитрила. Выход 5,1 г, т.пл. .
Вычислено, %: С 56,16; Н 3,86; N 5,95.
С„ Н,ГШз5
Найдено, %: С 56,08; Н 3,79; N 5,85.
Пример 6. В 200 мл метанола растворяют 15 г 7-метокси-З-оксо- 3,4-ДИГИДРО-2Н-1,5-бензоксатиепин-4- карбонитрила,раствор насыщают высушенным хлористым водородом и вьщержи вают при комнатной температуре в течение 4 дней. К реакционному раствору добавляют 10 мл воды, смесь оставляют стоять в течение ночи и концентрируют ее при пониженном дав- лении. Остаток счищают с помощью хроматографии на силикагельной колонке (элюент - хлороформ).
Получают 6,0 г метил 7-метокси-З- оксо-3,4-дигидро-2Н-1,5-бензоксатие- пин-4-карбоксш1ата (см. пример 2) вместе с 6,0 г исходного материала, который выделяют.
Пример 7. Смесь 30 г метил- 7-метокси-З-оксо-З,4-дигидро-2Н-1,5- бензоксатиепин-4-карбоксилата, 50 г 1-бром-З-хлорпропана, 46 г безводног карбоната калия, 10 г йодистого калия, 1,0 г йодистого тетрабутиламмо- ния и 300 мл ацетонитрила нагревают при кипячении с обратным холодильником в течение 4 ч. После охлаждения смеси неорганическое вещество отфиль тровьшают и фильтрат концентрируют при пониженном давлении. Получающийс в результате остаток растворяют в этилацетате, раствор промывают водой и сушат. Растворитель выпаривают при пониженном давлении, остаток очищают с помощью хроматографии на силикагел ной колонке (элюент - гексан:этилацетат :метиленхлорид 10:1:10).
Перекристаллизация из этанола дает бесцветные призмы метш1-4-(3- хлорпропил)-7-метокси-З-оксо-З,4-ди- ГИДРО-2Н-1,5-бензоксатиепин-4-карбок силата. Выход 17 г, т.пл. 64-65 С.
Вычислено, %: С 52,25; Н 4,97.
c,,H,,
Найдено, %: С 52,33; Н 5,10.
0
5
Пример 8. В 200 мл тетрагид- рофурана растворяют 17 г метил-4-(3- хлорпропил)-7-метокси-3-оксо-3,4- ДИГИДРО-2Н-1,5-бензоксатиепин-4-карб- оксилата, к раствору добавляют 2,8 г комплекса боран-триметиламина и 12 г эфирата трехфтористого бора с после-. дующим перемешиванием при комнатной температуре в течение 20 ч. Реакционный раствор концентрируют при пониженном давлении, к остатку добавляют охлажденную льдом воду и разбавленную соляную кислоту с последующим экстрагированием этилацетатом. Органический слой промывают водой и сушат, растворитель вьшаривают при пониженном давлении. Получающийся в результате остаток очищают с помощью хроматогра- Q фии на колонке из силикагеля (элюент - гексан:этилацетат 1:1).
Получают 13 г бесцветного маслянистого вещества метил-цис-4-(З-хлор- пропил)-3-окси-7-метокси-3,4-дигидро- 5 2Н-1,5-бензоксатиепин-4-карбоксш1а- та.
Вычислено, %: С 51,95; Н 5,52.
С, Н„ CEOjS
Найдено, %: С 52,00; Н 5,48.
Масс-спектр, м/е: 346,348 (М ).
Пример 9. Смесь 30 г метил- 7- метокси-З-оксо-3,4-дигидро-2Н-1,5- бензоксатиепин-4-карбоксилата, 60,0 г 1,3-дибромпропана, 46,0 г безводного карбоната калия, 10,0 г йодистого калия, 1,О г тетрабутиламмоний йодида и 300 мл ацетонитрила нагревают с обратным холодильником в течение 4 ч. После охлаждения смеси неорганическое вещество отфильтровьшают и фильтрат концентрируют при пониженном давлении. Получающийся в результате остаток растворяют в этилацетате, раствор промьшают водой и сушат. Растворитель выпаривают при пониженном давлении и остаток очищают с помощью хроматографии на колонке из силикагеля (элюент - гексан:этилацетат:метилен- хлорид 10:1:10).
Получают метил-7 метокси-4-(3- бромпропил)-7-метокси-З-оксо-З,4- ДИГИДРО-2Н-1,5-бензоксатиепин-4-карб- оксилат. Выход 13 г.
Пример 9. Смесь,содержащзто, г: метил 4-(З-хлорпропил)-7-метокси- З-оксо-З, 4-дигидро-2Н-1 ,5-бензоксатиепин-4 карбоксилат 56; N-фенилпипера- зин 40,0; иодид калия 5,5; карбонат калия 34 и М,М-диметилформамид 250,
0
5
0
5
нагревают при 70°С в течение 7 ч при перемешивании. Реакционную смесь вливают в воду со льдом, экстрагируют этилацетатом. Органический слой промывают водой, сушат и концентрируют при пониженном давлении. Остаток перекристаллизовьшают из 200 мл этанола.
Получают белые кристаллы метил-7- метокси-З-оксо-4- з-(4-фенилпипера- зин-1-ил)пропил -3,4-ДИГИДРО-2Н-1,5- бензоксатиепин-4-карбоксилата. Выход 57 г, т.ил. 110-П2°С.
Рассчитано, %: С 63,81; Н 6,43; N 5,95.
.C,,
Найдено, %: С 63,63; Н 6,31; N 5,88
Найдено, %: С 63,63; Н 6,31; iN 5,88.
Пример 10. По методике примера 9,
Метил-4-(3-бромпропил)-7-метокси- 3-оксо-З,4-ДИГИДРО-2Н-1,5-беНзоксати- епин-4-карбоксилат подвергают взаимодействию с N-фенилпиперазином.
Получают метил-7-метокси-З-оксо- Л 3-(4-фенилпиперазин-1-ил)пропилЗ- 3,4-ДИГИДРО-2Н-1,5-бензоксатиепин-4- карбоксилат.
Пример 11. В смеси 40 мл тетрагидрофурана и 200 мл метанола растворяют 38 г метил-7-метокси-З-ок со-4- з-(4-фенилпиперазин-1-ил)-пропил -3,4-ДИГИДРО-2Н-1,5-бензоксатие- пин-4-карбоксилата и к раствору при охлаждении льдом и перемешивании порциями добавляют 3,7 г боргидрида натрия. После окончания реакции растворитель вьшаривают при пониженном давлении и к остатку добавляют воду с последующим экстрагированием этил- ацетатом. Органические слои объединяют, промывают водой и сушат, растворитель выпаривают при пониженном давлении. Остаток отделяют и очищают с помощью хроматографии на силика- гельной колонке (элюент - гексан; :этилацетат:метанол 20:10:1).Из первого элюата получают 12 г бесцветног маслянистого вещества - метил-транс- 3-окси -7-метокси-4 З- (4-фенилпиперазин-1-ил) пропил -3-4-дигидро-2Н- 1,5-бензоксатиепин-4-карбоксилата.
ИК-спектр (чистый), 3520, 1720.
6
ЯМР-спектр (СОСЕ,)Д : 3,45 (ЗН, синглет, ОСН); 3,60 (ЗН, синглет, ОСН,).
Соединение превращается в белый порошок в виде гидрохлоридной соли.
Вычислено, %: С 54,15; Н 6,36; N 5,05.
С„ Н„ NjO, S 2HCi. 1 /2. Н,0 10 Найдено, %: С 54,27; Н 6,20; N 4,89.
Из последующего злюата получают 18 г бесцветного маслянистого вещества - метил-цис-3-окси-7-метокси-4- 5 З- (4-фенилпиперазин-1 -ил)пропш1 - 3,4-дигидро-2Н-1,5-бензоксатиепин-4- карбоксилата.
ИК-спектр (чистый), см : 3530, 1740.
ЯМР-спектр (CDCe,), : 3,60 (ЗН, синглет, OCHj); 3,62 (ЗН, синглет, OCHj).
Соединение получают в виде гидро- хлоридной соли, т.пл. 165-175 С (раз- лож .)
Вычислено %: С 54,15; Н 6,36; N 5,05.
Cz-rHj NjOyS 2 НС1 1/2
20
25
30
Найдено, %: N 5,00.
Пример на растворяют
35
40
45
Б О
55
HjO с 54,02; Н 6,33;
12. В 20 мл пириди- ,8 г метил-цис-3-гидрокси-7-метокси-4 З-(4-фенилпиперазин- -ил)пропил -3,4-дигидро-2Н-1 ,5- бензоксатиепин-4-карбоксилата и к раствору добавляют 6 мл уксусного ангидрида, после чего выдерживают смесь при комнатной температуре в течение ночи. Реакционный раствор вливают в охлажденную льдом воду с последующей экстракцией этилацетатом. Органический слой промьшают водой, водным раствором бикарбоната натрия и водой, сушат, концентрируют при пониженном давлении.
После перекристаллизации из смеси этилацетат - гексан получают метил- цис-3-ацетокси-7-метокси-4- 3- (4-фе- нилпиперазин-1-ил)пропил -3,4-дигид- ро-2Н-Г,5-бензоксатиепин-4-карбокси- лат в виде бесцветных призм, т.пл. 168-170°С. Структура продукта может быть определена с помощью рентгенана- лиза кристаллов.
Рассчитано, %: С 63,1; Н 6,66; N 5,44.
,,,S
Найдено, %: С 63,01; Н 6,69; N 5,40.
7
Пример 13. 14г метил-цис- 4- (З -хлорпропил) -З-окси-7-метокси- 3,4-ДИГИДРО-2Н-1,5-бензоксатиепин-4- карбоксилата, полученного по примеру 8, ьместе с 9,0 г 4-фенилпиперази- на, 9,0 г безводного карбоната калия, 0,5 г иодида калий и 100 мл ацетонит- рила нагревают с обратным холодильником в течение 20 ч. После охлаждения смеси неорганические вещества отфильтровывают и фильтрат концентрируют при пониженном -давлении. Остаток растворяют в этилацетате, органический слой промъшают водой и сушат. После выпаривания растворителя при пониженном давлении остаток очищают хроматографией на колонке с силика- гелем (элюент - гексангэтилацетат: :метанол 10:10:1).Полученный маслянистый продукт кристаллизуют в воде хлористоводородной соли.
Получают бесцветные кристаллы ди- гидрохлорида метил-цис-З-окси-7-мет- окси-4- З(4-фенилпиперазин-1-ил)про- ,4-дигидро-2Н-1 ,5-бензоксатие- пин-4-карбоксилата, который идентичен соединению, полученному по примеру 11. Выход 8г.
Продукт, перекристаллизованный из 50% этанола, представляет собой бесцветные призмы метил-цис-З-окси-7- метокси-4- З-(4-фенилпиперазйн-1-ил) пропил -3,4-ДИГИДРО-2Н-1,5-бензокса- тиепин-4-карбоксилата моногидрохлори- да, т.пл. 154-155 С (определена на
аппарате микротемпературы плавления lanagincofo, 132 С (разлож.).
Рассчитано, %: С 55,09; Н 6,84; N 5,14.
С45Нэ2М о.,5 нее 2
Найдено, %: С 55,46; Н 6,77; N 5,09.
ИК-спектр, K6tЛ101КС
СМ
36003300 1735; 1720; 1600;,1480; 1250.
ЯМР-спектр (dg - DMSO),5 ;ч/млн 1,3-1,8 (2Н); 2,7-3,8 (12Н); 3,68 (ЗН, синглет); 3,75 (ЗН, синглет); 3,8-4,3 (ЗН); 6,7-7,4 (8Н) .
Примеры 14-18. Способом, описанным в примере 13, получают соединения, указанные в табл.1, реакци ей замещения метил-цис-4-(3-хлорпро- пил)-З-окси-7-метокси-З,4-дигидро-2Н- 1,5-бензоксатиепин-4-карбоксилата различными аминами.
Пример 19. Оптическое расщепление (±) метш1-цис-3-окси-7-метMj., - 102,0 (с 0,54, мета нол) .
Рассчитано. %: С 54,15; Н 6,36; N 5,05 40 ,.N,,05-5 - 2 нее 1/2 Н,0
Найдено,%: С 53,98; Н 6,18; N 4,83.
Пример 20. Способом, описа ным в примере 19, соль (±) метил- цис-3-окси-7-метокси-4- 3-(4-фенил- пиперазин-1-ил)пропил -3,4-дигидро- 2Н-1,5-бензоксатиепин-4-карбоксилат и R -(-)-1,l -бинафтил-2,2 -диил ки лого фосфата перекристаллизовьшают три раза из смеси ацетон - метанол и получают белые кристаллы.
MD - 172° (с 1,03, метанол) .
Полученнзто соль обрабатьшают 1 н раствором гидроокиси натрия с последующей обработкой хлористым водородом и получают (+) метил-цис-3-окси50
55
окси-4- 3-(4-фенилпиперазин-1-ил)про- 7-метокси-4- 3-(4-фенилпиперазин-1
8
,4-ДИГИДРО-2Н-1,5-бенз оксатие- пин-4-карбоксилата.
(i) Метил-цис-3-окси-7-метокси-4- (4-фенилпиперазйн-1 -ил) пропил - 3,4-дигидро-2Н-1,5-бензоксатиепин-4- карбоксилат (1,3 г) иS-/+/-1,Г -бинаф- тил-2,2 -диил кислый фосфат (1,0 г) растворяют в метаноле (50 мл). Раствор выпаривают в вакууме. Остаток растворяют в смеси ацетон - метанол и вьщерживают в холодильнике. Кристаллический осадок отфильтровьшают и перекристаллизовывают три раза из смеси ацетон - метанол, получают белые кристаллы, Ы,д + 175,5 (с 1,01, метанол).
Суспензию полученных кристаллов в метиленхлориде обрабатьшают 1 н. раствором гидроокиси натрия. Органический слой промывают водой, сушат над безводным сульфатом натрия и выпаривают в вакууме. Получают свободное основание в виде бесцветного масла. Полученное основание растворяют в этаноле, обрабатьшают хлористым водородом и выпаривают в вакууме. Остаток растирают со смесью метанол - простой эфир и получают (-) метил- цис-3-окси-7-метокси-4 З-(4-фенил- пиперазин-1-ил)пропил -З,4-дигидро- 2Н-1,5-бенз оксатиепин-4-карбоксилат дигидрохлорид в виде аморфного порошка.
5
Mj., - 102,0 (с 0,54, метанол) .
Рассчитано. %: С 54,15; Н 6,36; N 5,05 0 ,.N,,05-5 - 2 нее 1/2 Н,0
Найдено,%: С 53,98; Н 6,18; N 4,83.
Пример 20. Способом, описанным в примере 19, соль (±) метил- цис-3-окси-7-метокси-4- 3-(4-фенил- пиперазин-1-ил)пропил -3,4-дигидро- 2Н-1,5-бензоксатиепин-4-карбоксилата и R -(-)-1,l -бинафтил-2,2 -диил кислого фосфата перекристаллизовьшают три раза из смеси ацетон - метанол и получают белые кристаллы.
MD - 172° (с 1,03, метанол) .
Полученнзто соль обрабатьшают 1 н. раствором гидроокиси натрия с последующей обработкой хлористым водородом и получают (+) метил-цис-3-окси0
5
7-метокси-4- 3-(4-фенилпиперазин-1ил)пропил -3,4-ДИГИДРО-2Н-1,5-бензок- сатиепин-4- карбоксилат дигидрохлорид в.виде аморфного порошка.
Mjj 110,8° (с 0,48 метанол).
Рассчитано, %: С 54,15; Н 6,36; N 5,05.
C.
2 нее 1/2 С 54,11; Н 5,93;
гв ъг г. Найдено, %:
N 4,80.
Пример 21. Смесь 3,4 г метил-4-(3-хлорпропил)-3-гидрокси 7- метокси-3,4-дигидро-2Н-1,5 бензокеа- тиепин-4-карбоксилата, 4-фенилпипера- зина (1,7 г), иодида калия (0,3 г), безводного карбоната калия (1,4 г) и NJN-диметилформамида (5 мл) перемешивают при 60°С в течение 8 ч. Неорганические материалы удаляют фильтрацией, фильтрат концентрируют при пониженном давлении. Остаток растворяют в этилацетате, промывают водой, сушат над безводным сульфатом натрия и концентрируют в вакууме.Остаток чистят на хроматографической колонке на силикагеле (элюент - гексан:этилаце- тат:метанол 10:10:1), полученное масло превращают в гидрохлорид и пере- кристаллизовьшают из 50% этанола.
этилацетатом. Органический слой про- мьшают водой, сушат и концентрируют при пониженном давлении. Остаток об- рабатьшают по методике примера 21. Получают 1,7 г бесцветньйс призм метил-цис-3-окси-7-метокси-4- 3-(4- фенилпиперазин-1-ил)пропил -3,4-ди- ГИДРО-2Н-1,5-бензоксатиепин-4-карбок1Q силата в форме моногидрохлорида.
Пример 24 Блокирование се- ротонин S -рецепторов (in vitro) соединениями, полученными по предлагаемому способу.
15 Опыт проводят по методу Бевана и Ошера с некоторыми изменениями. Сердце свиньи, только что убитой на бойне, сохраняют путем охлаждения льдом Левую окружающую венечную артерию
20 рассекают не позднее чем через 3ч. Венечную артерию разрезают на кольцевой препарат (приблизительно 3 мм в ширину), который помещают при помощи пары крючков в двухстенный сосуд, со
25 держащий 20 мл раствора Кребса-Гензе- лейта. Один из крючков прикреплен ко дну ванны, а второй подключен к Stra in gauge датчику. Таким образом изовенечной артерии свиньи. Температуру ванны поддерживают на уровне . Раствор Кребса-Гензелейта, насыщенный смешанным газом (97% 0 + 3% СО 2g состоит из 118,7 мг/мол NaCI,
4,7 ммоль КСР, 1,2 ммоль КН,РО, 2,58 мйоль СаС - 2 ,
4 .
1,15 ммоль
MgSO 7 , 25 ммоль НСО, и 11,1 ммоль глюкозы.
40
метрически замеряют и записьшают на Получают 3,9 г метил-цис-3-гидрок- зо полиграф сжатие кольцевого препарата
си-7-метокси-4- З-(4-фенилпиперазин-
1-ил)пропил -3,4-дигидро-2Н-1,5-бензоксатиепин-4-карбоксилата моногидрохлорида в виде бесцветных призм.
Пример 22. Смесь 3,4 метилцис-4-(3-хлорпропил)-З-окси-7-метокси-4-3,4-ДИГИДРО-2Н-1,5-бензоксатиепин-4-карбоксилата, 3,3 г 4-фенилпи-
перазина и 1,0 г иодида калия перемешивают при 90°С в тече.ние 2 ч. Смесь
разбавляют водой с последующей экстракцией этилацетатом. Органический
слой промьшают водой, сушат и концентрируют при пониженном давлении.
Остаток очишают хроматографией на колонке ссиликагелем по методике примера
21 и получают 3,2 г метил-цис-3-окси-7метокси-4- З-(4-фенилпиперазин-1-ил)пропил -3,4-дигидро-2Н-1,5-бензокса-
тиепин-4-карбоксилата в виде хлористов одо родной соли.
Пример 23. Смесь 1,7 г ме-
тил-цис-4-(3-хлорпропил)-3-окси-7метокси-3,4-ДИГИДРО-2Н-1,5-бензоксатиепин-4-карбоксш1ата, 0,8 г 4-фенилпиперазина и 3 мл N,N-диметилацетами- да нагревают при в течение 6 ч.
После охлаждения реакционной смеси к
45
50
55
Через 1-2 ч, когда препарат кровеносного сосуда показывает стабильное натяжение покоя, натяжение покоя доводят до 2 г, в ванну добавляют 10 М серотонина (последняя концентрация) с интервалом приблизительно в 1 ч, чтобы проверить реакцию препарата. Когда реакция кровеносного сосуда на 2-3 добавления серотонина становится стабильной, добавляют в ванну испытуемое соединение за 10 мин до следующего добавления серотонина.. Серотонергический блокирующий эффект испытуемого соединения подсчитьшают по величине сжатия, вызванного серо- тонином до и после добавления испытуемого соединения
Результаты эксперимента приведены в табл.2.
ней добавляют воду и экстрагируют
этилацетатом. Органический слой про- мьшают водой, сушат и концентрируют при пониженном давлении. Остаток об- рабатьшают по методике примера 21. Получают 1,7 г бесцветньйс призм метил-цис-3-окси-7-метокси-4- 3-(4- фенилпиперазин-1-ил)пропил -3,4-ди- ГИДРО-2Н-1,5-бензоксатиепин-4-карбоксилата в форме моногидрохлорида.
Пример 24 Блокирование се- ротонин S -рецепторов (in vitro) соединениями, полученными по предлагаемому способу.
Опыт проводят по методу Бевана и Ошера с некоторыми изменениями. Сердце свиньи, только что убитой на бойне, сохраняют путем охлаждения льдом. Левую окружающую венечную артерию
рассекают не позднее чем через 3ч. Венечную артерию разрезают на кольцевой препарат (приблизительно 3 мм в ширину), который помещают при помощи пары крючков в двухстенный сосуд, со держащий 20 мл раствора Кребса-Гензе- лейта. Один из крючков прикреплен ко дну ванны, а второй подключен к Strain gauge датчику. Таким образом изовенечной артерии свиньи. Температуру ванны поддерживают на уровне . Раствор Кребса-Гензелейта, насыщенный смешанным газом (97% 0 + 3% СО),. g состоит из 118,7 мг/мол NaCI,
4,7 ммоль КСР, 1,2 ммоль КН,РО, 2,58 мйоль СаС - 2 ,
4 .
1,15 ммоль
MgSO 7 , 25 ммоль НСО, и 11,1 ммоль глюкозы.
40
45
50
55
Через 1-2 ч, когда препарат кровеносного сосуда показывает стабильное натяжение покоя, натяжение покоя доводят до 2 г, в ванну добавляют 10 М серотонина (последняя концентрация) с интервалом приблизительно в 1 ч, чтобы проверить реакцию препарата. Когда реакция кровеносного сосуда на 2-3 добавления серотонина становится стабильной, добавляют в ванну испытуемое соединение за 10 мин до следующего добавления серотонина.. Серотонергический блокирующий эффект испытуемого соединения подсчитьшают по величине сжатия, вызванного серо- тонином до и после добавления испытуемого соединения
Результаты эксперимента приведены в табл.2.
Пример 25. Аналогично примеру 24 измеряют серотонергический эффект блокирования.
Результаты приводятся в табл.3.
Пример 26. Опыт проводят на самцах коротконогих гончих собак весом 10-14 кг. Предварительно бьши имплантированы полиэтиленовые трубки в бедренные артерии и вены для измерения систематического кровяного давления и, соответственно,.для внутривенного применения опытного соединения. Имплантация полиэтиленовых трубок была проведена в стерильных условиях под наркозом с использованием пентобарбитала натрия (30 мг/ /кг, внутривенное введение). Другие концы полиэтиленовых трубок были подсоединены подкожно к нормальной части и вьшедены наружу.
Эксперимент проводили через 2-3 дня после операции.
Полиэтиленовая трубка, вставленна в артерию, подключена к датчику давления, и систематическое кровяное давление измеряли и постоянно записывали на полиграфе. После внутривенного введения 3-30 Нг/кг серртонина через полиэтиленовую трубку, вставленную в бедренную вену, наблюдали временную гипертоническую реакцию в зависимости от дозы. После повторного введения 30 Нг/кг серотонина, например, через 30 мин была отмечена восстановительная гипертоническая реакция. Поэтому 30 Нг/кг серотонина применяли для исследования эффекта орального применения соединения, полученного по предлагаемому способу. После того, как 2-3 внутривенных введения 30 Нг/кг серотонина с интервалом около 30 мин дали повышение стабильной гипертонической реакции, было введено соединение по примеру 1I (цис-изомер-дигидрохлорид) орально в дозах 0,1; 0,3 и 1,0 мг/кг. Постоянно проверяли гипертоническую реакцию на 30 Нг/кг серотонина до тех пор, пока уровень гипертонической реакции не станет равным уровню до применения лекарства.
Результаты эксперимента приведены в табл.4.
Соединение по примеру 11 (цис-изо мер, дигидрохлорид) при применении в дозах не менее 0,1 мг/кг показьша- ло зависимое от дозы и устойчивое
0
5
торможение гипертонической реакции на серотонин.
Пример 27. Кальций-антагонистическое действие.
У крысы со спонтанной гипертонией (возраст 14 недель, самец) удалили брыжжейку и ввели через брыжжеечную артерию раствор Кребса-Гензелейта при нагревании до 37°С. Основной ток
равнялся приблизительно 4 мл/мин при давлении перфузии около 40 мм рт.ст. Используемое как индикатор антагонизма кальция торможение роста давле- 5 ния перфузии вызвано инъекцией в
брыжжеечную артерию за 30 мин до инъекции КС 6.
Результаты приведены в табл.5.
В случаях неприменения- соедине- 0 ния, у контрольной группы, увеличение давления перфузии, вызванное КС, было 73-20 (величина для 8 случаев - SEM/MM рт.ст., показана в таблице как 100%). Соединение примера 11 (цис) показьшало в зависимости от дозы значительное торможение вызванного KCt увеличения давления перфузии.
Пример 28. Мочегонное действие.
В эксперименте использовали четыре из пяти групп крыс со спонтанной гипертонией (возраст 13 недель, сам- цы). Испытуемое соединение, суспен- 5 дированное в изотонической соли с
небольшим количеством гуммиарабика и , вводили орально в количестве 25 мл/кг Изотоническая соль, содержащая только гуммиарабик, была дана контрольной 0 группе. После применения каждая крыса была посажена на 5 ч в клетку для сбора мочи. Измеряли количество мочи и количество мочевого Na и К . Кон- центрация Na и К бьша определена 5 при помощи планомерного спектрофотометра (тип Хитачи 205 ДТ).
Результаты показаны в табл.6.
Соединение примера 11 (цис-изомер- дигидрохлорид) при применении орально в дозах 3 мг/кг способствовало
выделению мочи, а также Na и К , а
при применении орально в дозах 10 и 30 мг/кг вызвало значительное увеличение количества мочи и Na и К . c Пример 29. Противотромбозное действие.
Взрослые непородистые собаки были подвергнуты торакотомии под наркозом (пентобарбитал-натрия). Внутри13
к1оронарньш тромбоз был произведен согласно методу Фолтса и др.
. Артериальную канюлю вставляют в левую окружающую венечную артерию, и артериальную кровь пускают из общей сонной артерии через экстракорпоральную цепь для перфузии артериальной крови. Ток коронарной крови замеряют с помощью электромагнитного зонда тока крови, помещенного в экстракорпоральной цепи. Пластиковый констриктор располагают вокруг.окружающей венечной артерии для ее сужения на 70- 80%. Образование внутрикоронарного тромбоза устанавливают по периодически появляющимся уменьшению и увеличению коронарного кровотока, так как известно, что тромбоцитарные тромбозы образуются в суженном участке вследствие турбулентного тока и смываются градиентом повышенного давления. Частое образование и устранение тромбозов приводит к периодическому измерению коронарного кровотока.
Таким образом, in vivo эффективность противотромбозного действия испытуемого соединения определяется по частоте изменения коронарного кровотока.
Испытуемое соединение было введен внутривенно.
Когда был установлен констриктор на окружающующую венечную артерию, т коронарный кровоток постепенно умень шился с начального 20-30 мл/мин, а затем резко увеличился.
Уменьшение и увеличение коронарного кровотока периодически повторялось с частотой 5-15/30 мин.
Результаты эксперимента приведены в табл.7.
Соединение примера 1 (цис-изо- мер-дигидрохлорид) при внутривенном применении приводило к уменьшению частоты периодического изменения коронарного кровотока в зависимости от дозы.
Пример 30. Действие, облегчающее спазм сосудов головного мозга после экспериментального арахнои- дального кровоизлияния.
В эксперименте использовали шесть коротконогих гончих собак весом 10 - 14 кг. Для цереброваскулярной ангиографии предварительно была вставлена полиэтиленовая канюля в правую позво ночную артерию под действием пенто
5
10
15
46044
барбитала (30 мг/кг внутривенно). Це- реброваскулярную ангиографию проводили под действием пентобарбитальной анестезии дважды через каждые 2 с сразу же после инъекции 10 мл контрастного вещества, иодамидового глу- тамина, через вставленную канюлю с использованием рентгенографа Medix- 50 У.Субарахноидальное кровоизлияние было спровоцировано инъекцией 5 мл свежей аутологичной крови, взятой из вены нижней конечности и cistuna magna при помощи спинальной иглы при анестезии пентобарбиталом через 2 дня после имплантации канюли. Церебровас- кулярная ангиография была сделана до. и после 3,6 и 3 дней после субарах- ноидального кровоизлияния, и на рентгеновском снимке был измерен диаметр основной артерии.
Животных разделили на 2 группы по 3 особи в каждой. Одну группу использовали в качестве контрольной, а другой было дано соединение примера 13 (соль моногидрохлорида). Указанную смесь вводили дозами по 30 мг/кг орально в день субарахноидального кровоизлияния, 1 мг/кг внутривенно сразу после субарахноидального кровоизлияния и 30 мг/кг орально - ежедневно в последующие. 13 дней.
Результаты эксперимента приведены в табл„8 (диаметр основной артерии до субарахноидального кровоизлияния и его изменение после субарахноидального кровоизлияния).
В контрольной группе диаметр основной артерии уменьшился примерно на 40-60% через 3-6 дней после кровоиз20
25
30
35
40
5
НИИ церебрального спазма сосудов. У животных, которым вводили соединение по примеру 13,, уменьшение диаметра основной артерии было неболь- уменьшения была значи- сравнению с контрольшим, и степень тельно ниже по ной группой , Пример
0
5
31„ Действие на почечную циркуляцию,
В эксперименте использовали коротконогих гончих собак с нормальным кровяным давлением весом 9-14 кг. Ла- паротомия была сделана вдоль средней брюшной линии под действием пен- тобарбитала. Для измерения тока крови в почках левая почечная артерия была свободно разрезана и вокруг нее был установлен электромагнитный датчик
1513
тока крови. Полиэтиленовая трубка ретроградно была вставлена и зафиксирована в брюшной аорте, концы .провод электромагнитного датчика тока крови и полиэтиленовой трубки были пропущены под кожей и вьшедены наружу на конце шеи.
Через неделю или более после операции животные были подвергнуты эксперименту без действия наркоза. Ток крови почек измерялся электромагнитным датчиком тока крови, а систематическое кровяное давление - при помощи датчика давления. Частота удара сердца измерялась тахометром пульса, включающимся под действием волн пульса.
Соединение по примеру 13 (моногидрохлорид), вводили орально, через 2-3 ч производили измерения.
При контрольном введении лактозы (Ю мг/кг, 7 экспериментов орально) никаких изменений в систематическом кровяном давлении, частоте ударов сердца и почечном токе крови не наблюдалось в течение 7ч.
Применение 3-10 мг/кг испытуемого соединения привело к небольшому снижению систематического давления крови, но не повлияло на частоту ударов сердца. 1Почечньй: ток крови заметно увеличился. Действие продолжалось в течение 7 ч.
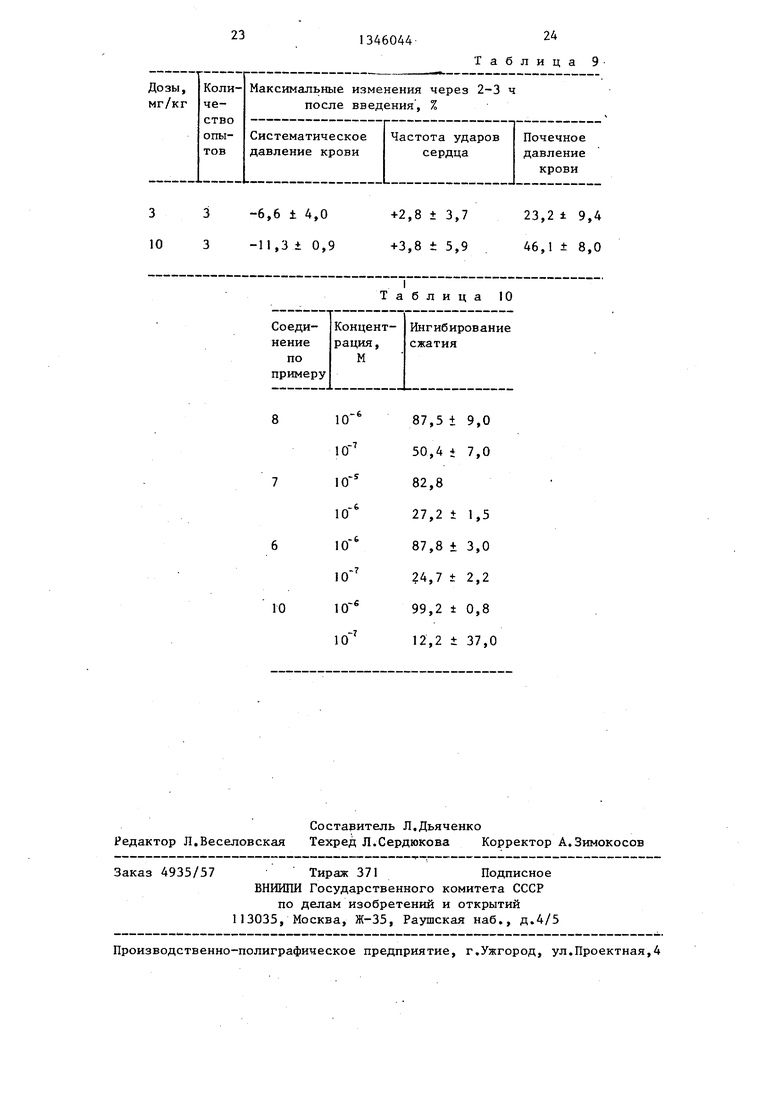
Результаты эксперимента приведены в табл.9..
Пример 32. По методике примера 24 был вычислен серотонергичес- кий блокирующий эффект испытуемых соединений.
Результаты сведены в табл.10.
Пример 33. Соединение, полученное в примере 13 (моногидрохло- рид), вводили подкожно 1Сб:ICR мышам 4-недельного возраста и ICg: Wistar крысам 5-недельного возраста и вычисляли острую токсичность, LD
-50 мг/кг: для мьшей 1000-2000, для крыс 5000.
Соединения формулы (l) могут быть использованы для лечения ишёмиЧеских кардиопатий в виде различных лекарственных форм.
Таблетки (на 1000 шт-), г: метил- цис-3-окси-7-метокси-4- 3-(4-фенил- пиперазии-1-ил)-пропил -3,4-дигидро- 2Н-1,5-бензоксатиепин-4-карбоксилат- гидрохлорид (А) 10; лактоза 90; зерновой крахмал 29; стеарат магния 1.
16
10 г соединения А, 90 г лактозы и 17 г крахмала перемешивают и гранулируют пастой, приготовленной из 7 г крахмала. Добавляют к гранулам 5 г крахмала и 1 г стеарата магния. Смесь сжимается машиной, изготовляющей таблетки. Получают 1000 таблеток диаметром 7 мм. Каждая таблетка содержит 10 мг соединения А.
Капсулы (на 1000 шт), г: метил- цис-3-окси-7-метокси-4- 3-{4-феннл- пиперазин-1-ил)-пропил -3,4-дигидро- 2Н-1,5-бензоксатиепин-4-карбокси- пат-гидрохлорид 10; лактоза 135; тщательно размельченная целлюлоза 70; стеарат магния 5.
Все ингредиенты перемешивают и заполняют 1000 желатиновых капсул № 3.
Каждая капсула содержит 10 мг действующего вещества.
Раствор для инъекции (на 1000 мл), г: метил-цис-З-окси-7- метокси-4- 3-(4-фенш1пиперазин-1- ил)пропил -3,4-ДИГИДРО-2Н-1,5-бензок- сатиепин-4-карбоксилат-тартрат 10; хлорид натрия 9; хлорбитанол 5.
Все ингредиенты-растворяют в 1000 мл дистиллированной воды, полученным раствором заправляют 1000 коричневых ампул. Каждая ампула содержит 1 мл раствора. Воздух вытесняют из ампул азотным газом и ампулы запаиваются. Все стадии приготовления осуществляются в стерильных условиях.
Фо-рмула изобретения
1. Способ получения производных 1,5-бензоксатиепина, формулы I
СООСНз р
RI s-V cH2VKp
, я,
где R, - водород;
R, - низшая алкоксигруппа;
R, и
R
- взятые вместе образуют вместе с атомом азота, с которым они связаны, пиперазиновое кольцо,замещенное фенилом; п - фторфенилом, низший алкил- фенилом, или пиперидиновое кольцо, замещенное фенилом или п-фторфенилкарбонилом,
или Hj низший алкил, а R - диметоксифенилэтил;
HN
171346044 8
У-группа С О или :CH-ORj, подвергают взаимодействию с соедине- где Rj- - водород или низший алканоил; нием формулы III : или их солей, отличающийся тем, что соединение формулы И:
г,
fe::3
где W - галоген;
Y,R,R2. имеют указанные значения,
Р,
где R, и Н имеют указанные значения в среде органического растворителя при температуре от до температуры кипения и вьщеляют целевой продукт в свободном виде или в в|щесоли.
снп « Ж,5-1Г- Х
HN
ействию с
Р,
где R, и Н имеют указанные значения в среде органического растворителя при температуре от до температуры кипения и вьщеляют целевой продукт в свободном виде или в в|щесоли.
Таблица 







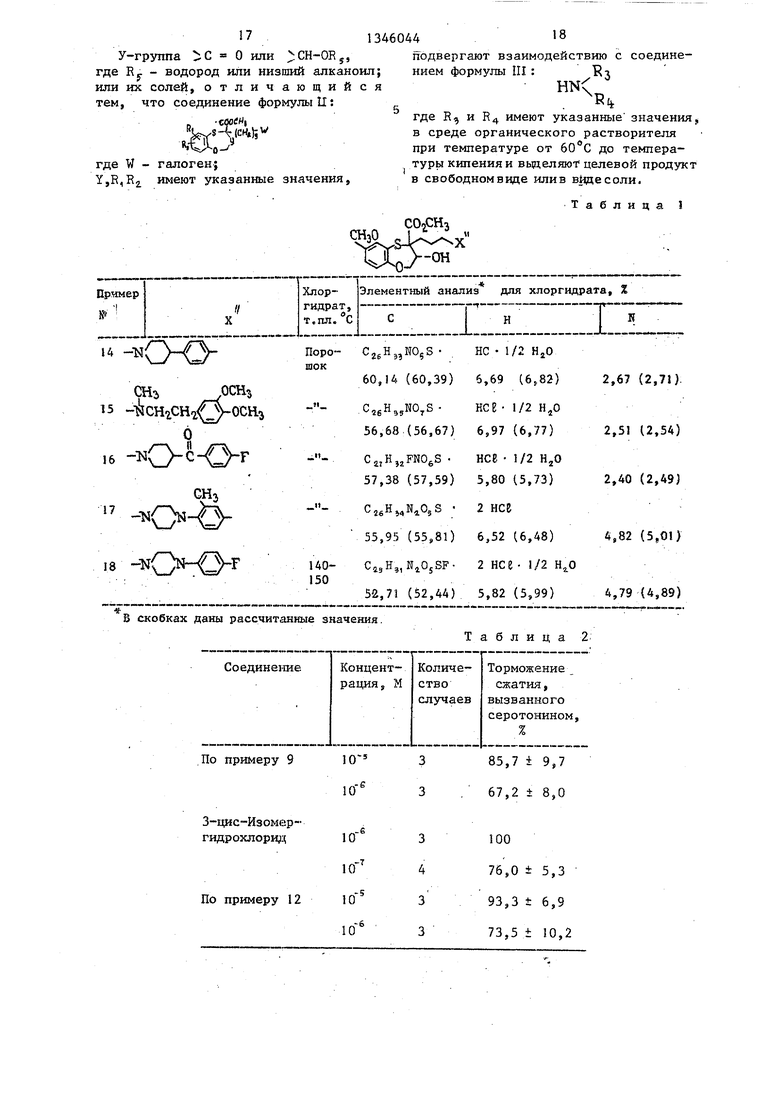


Изобретение касается гетероциклических соединений, в частности новых производных 1,5-беизоксатиепина формулы (I) , CH(RiVCH C-S-(KH)C cmR2l-CH C-0-CH2-Y где - С(0)-0-СН,; К - (СИ Jj-NR, Y - С(0) или CH-ORs.; R, - Н; R - низший алкоксил; R э и R4 вместе с азотом пиперазинил, замещенный фенилом, п-фторфенилом, низшим алкилфенилом или п-фторфенилкарбони- лом; RJ - Н или низший алкил, которые обладают способностью блокировать серотониновые-S рецепторы. Цель - создание активных веществ указанного класса. Получение соединений I ведут из галоидзамещенного соответствующего 1,5-бензоксатиепина и амина в среде органического растворителя при температуре от бО С до точки кипения с последующим выделением целевого продукта в свободном виде или в виде соли. Испытания показывают, что новые соединения проявляют активность, не характерную для известных аналогов, т.е, способны блокировать серотониновые Sj рецепторы,обеспечивают антагонизм действию кальция, вызьшают облегчение спазмов сосудов головного мозга, улучшают ренальную циркуляцию и про- являют диуретическую и противотром- бозную активность. 10 табл. СО со 4 05 4 iU СМ
J4 --N
Порошок
5 -- СНгСНаО-ОСНэ
16 -:«О4- г
,
17
jg -K(
140- 150
НС 1/2 HjO 6,69 (6,82)
нее 1/2 HjO 6,97 (6,77)
нее 1/2 5,80 (5,73)
2 нее
6,52 (6,48)
2 нее 1/2
5,82 (5,99)
2,67 (2,71) 2,51 (2,54) 2,40 (2,49)
4,82 (5,01) 4,79 (4,89)
В скобках даны рассчитгшные значения.
3-цис-Изомер- гидрохлорщ(
10
.
10
По примеру 12
10
10
Таблица 2
3 4 3 3
100
76,0 ±5,3
93,3 ±6,9
73,5 t10,2
Соединение по примеру I1
Доза, М
Изменение давления перфузии при инъекции КСЕ, %
10
г 6
Контроль
100 (8)
Соединение по примеру 11 (цис) 84 ± 3(3)
51 t 14-(5)
30 ± 2(3)
В скобках - количество случаев
Таблица 4
Таблица 5
Контроль
1,02 i 0,10128 1 15
Соединение по примеру 11 (цис)
«
Р 0,05. Р 0,01 .
1,47 ± 0,02
1,07 i 0,07
-38,3±3,7 -59,3±3,8 -12,7±9,9 2,7±2,7 -20,7±12,О -5i5
Р 0,05. 0,01.
59 ± 8
Таблица 7
Таблица
23
Составитель Л.Дьяченко Редактор Л.Веселовская Техред Л.Сердюкова Корректор А.Зимокосов
4935/57
Тираж 371Подписное
ВНИИПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д.4/5
Производственно-полиграфическое предприятие, г.Ужгород, ул.Проектная,4
1346044
24 Таблица 9
Таблица 10
| Вейганд-Хильгетаг | |||
| Методы эксперимента в органической химии | |||
| М.: Химия, 1968, с.413. |
Авторы
Даты
1987-10-15—Публикация
1984-12-12—Подача