11
Изобретение относится к химии нуклеиновых кислот и представляет собой усовершенствованный способ, триэфир- пого синтеза олигонуклеотидов, нахо- дящих широкое применение в молекуляр- 11ОЙ биологии и генной инженерии.
Цель изобретения - ускорение процесса фосфотриэфирного синтеза олиго- луклеотидов за счет повьш1ения скорое- ти реакции конденсации путем применения в качестве катализатора- 4-Н,М-ди- метиламинопиридин-1-оксида.
Нижеследующие примеры илшострир- - ют изобретение, где используют следующие сокращения и условные обозначения :
dbzA - Ы -бензоил-2 -дезоксиаде
нозин;
dT - 2 -дезокситимидин; 20 dbzC - Н -бензоил-2 -дезоксици тидин} dibG - N -изобутирил-2 -дезоксигуанозин;
СЕ - 2-цианоэтил-;
bz - З -О-бензоил-; tbbz - з -О-(п-трет-бутилбензоил)-; + - межнуклеотидная (З -5 )
связь, блокированная 30 п-хлорфенильной группой; TPS - 2,4,6-триизопропилбензолсульфохлорид;PSNT, - 1-(2,4,6-тpиизoпpoпшlбeнтoкcитpизтилкa 498. нм .превращения -ц
Dt
1
где Dt
Dt . D
золсульфонил)3-нитро-1,2j4- 35 мени реакции.
оптич ракта конде Dd - оптич та из ного
(Rf 0
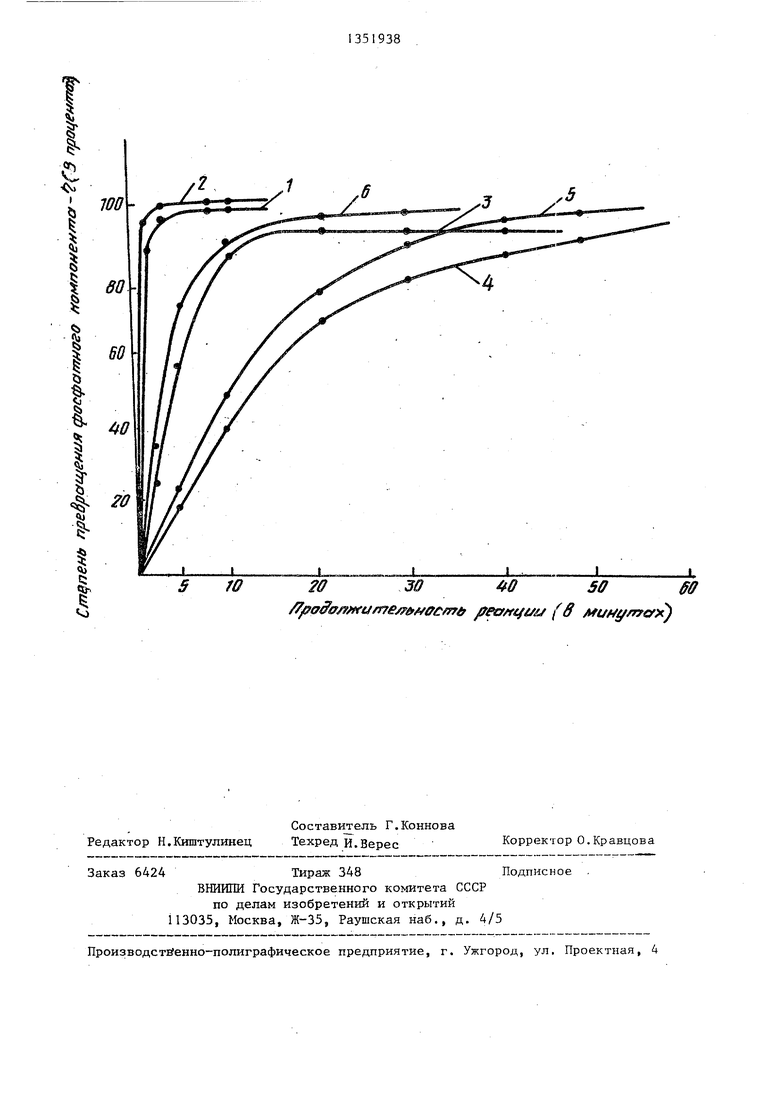
На чертеже симости степен
триазол;
Melm - Н метилимидазол; : DHTr - 4,4 -диметокситрифенилметил;
НМТг - 4-метокситрифенилметил; ВЭЖХ - высокоэффективная жидкостная хроматография; DMAP - 4-М,М-диметиламинопиридин ДМАРО - 4-М,М-диметиламинопиридин-2-оксид.
Пример 1, Сравнение скоростей конденсации в синтезе DMTr-dbrA dbzC-tbbz при использовании различных конденсирующих агентов.
К 2 мл раствора, содержащего 0,025 ммоль триэтиламмониевой соли 3-п-хлорфенилфосфата DMTr-dbzAi; 0,0375 ммоль dbzC-tbbz, 0,225 ммоль катализатора (DMAPO, DMAP, Ме|.т) или без катализатора, добавляют в атмосфере сухого аргона конденсирующий агент (TPS или TPSNT, 0,1 ммоль) и вьщерживают смесь при 20 С. Через определенные промежутки времени с по
мощью шприца отбирают аликвоты по 45 мкл. Аликвоту наносят на пластин- ку 3x8 с.м со слоем сипикагеля (Plagj- tikfolien Kieselgel F. , Merck ФРГ) и хроматографируют в системе хлороформ-этанол (9:1). Пятна с Р. f 0,1 (исходный фосфатный компонент) и RP 0,75 (продукт конденсации), окрашивающиеся в оранжевый цвет парами трифторуксусной кислоты, раздельно снимают с пластинки и помещают в центрифужные пробирки, содержащие 10 мл смеси этанола и 70% хлорной кислоты (2:3 по ) Пробирки интенсивно встряхивают и содержимое центрифугируют. Измеряют спектрофо- тометрически концентрацию 4,4 -диме
тoкcитpизтилкaтиoнa ( 7,700j 498. нм).. Вычисляют степень .превращения -ц по формуле
Dt
1
Dt . D d
100%,
оптическая г лотность экстракта из пятна продукта конденсации (R 0,75); оптическая плотность экстрак та из пятна непрореагирован- ного фосфатного компонента
(Rf 0,1).
ртеже приведены графики завистепени превращения ч от вреПример 2. Синтез динуклеоти- да DMTrd (Т+Т+СЕ) в присутствии 4- N,Н-диметиламинопиридин-1-оксида с применением производных арилсульфокислот как конденсир /ющих агентов,
К раствору 102 мг (Q,12 ммоль) тризтиламмонийной соли DMTr dJ+H, 49 мг (0,1 мoль)dT+CE и 83 мг (0,6 ммоль) DMAPO в 1,5 мл безводного
пиридина добавляют 0,3 ммоль производного арилсульфокислоты и выдерживают 3 мин. Прекращают реакцию добавлением льда и к реакционной смеси приливают 20 мл хлороформа. Органическую
фазу пром }Шают 2x20 ют 0,1 М раствора триэтиламмонийбикарбоната и высушивают безводным Na jSO. Хлороформ упаривают в вакууме и остаток хроматографируют на колонке с силикагелем
- градиенте концентрации этанола и хлороформе. Фракции, содержащие продукт конденсации, собирают, упаривают в вакууме. Определяют выход продукта после высаживания в гексан, высушивают в вакуум-эксикаторе и взвешивания .
Выход динуклеотида DMTrd ) при синтезе в присутствии ДМАРО и ра личных конденсирующих агентов следующий ,. %:
2,4,6-Триизопропилбензол- сульфохлорид (TPS-Cl) 90 Мезитиленсульфохлорид
(MSC1)64
п-Толуолсульфохлорид (TSCI)74
1-(n-Toлyoлcyльфoншl)3- нитpo-l ,2,4-триазол (TSNT) - 84 1-(Мезитиленсульфонил)- тетразол 75 -(2,4,6-TpиизoпpoпшIбeн- зoлcyльфoнил)-3-нитpo- 1,2,4-триазол (TPS-NT) 93 Пример 3. Сравнение скорости межнуклеотидной конденсации На полимерном носителе в присутствии различных нуклеофильных катализато- ров.
В качестве полимерного носителя используют целлюлозные диски хрома- тографической бумаги Whatman 3 ММ, на которых иммобилизован тимидин-3 - 0-сукцинат (I2 мкмоль на диск или 390 мкмоль/г),а непрореагировавшие гидроксильные группы углеводных звенев заблокированы ацетальными остатками.
Упаривают 0,06 ммоль (0,0441 г) DMTr Т+Н и 0,3 ммоль катализатора совместно с целлюлозным диском при добавлении сухого пиридина. Затем добавляют 2 мл сухого пиридина и при перемешивании - 0,12 ммоль (0,0363 г TPS, Через 3 мин каждый диск отмывают пиридином и хлороформом и определяют количество присоединенного нук- леотида по поглощению диметокситри- тилкатиона при 498 нм в растворе хлоная кислота - этанол (3:2).Результаты эксперимента:
Катализатор Процент включения нуклеотида
Megm ОМАР DM АР О
15,3 33,5 84,4
Пример 4. Получение тетра нуклеотида ММТг-d(bzA+ i bG+bzA+CE). К раствору 0,2 ммоль триэтиламмони- евой соли 3 -п-хлорфенилфосфата MMTr-d(bzAHHibG+H) 0,2 ммоль d (i bG+
(-
Q
5 0 5
О
0 g
5
0
bzA+CE), 1,2 ммоль DMAPO в 2,5 мл безводного пиридина добавляют 0,5 ммоль TPS.
Через 3 мин реакционную смесь обрабатывают, как в примере 2, и осаждением эфиром получают 0,192 ммоль (485 мг, 96%) тетрануклеотида.
Пример 5. Синтез олигонукле- отида d (T -C-C-A-G-G-T) на целлюлозном носителе.
Целлюлозный диск бумаги Whatman 3 ММ с иммобилизованным тимидин-З - 0-сукцинатом (5,3 мкмоль) и блокированными ацетилированием остаточными гидроксильными группами целлюлозы помещают в шприц вместимостью 5 мл и промывают безводным ацетонитрилом. Затем в шприц набирают пиридиновый раствор, содержащий 20-кратный избыток 5 -О-диметокситритилнуклеозид- З -О-(4-хлорфенил)-фосфата, 20-кратный избыток TPSNT и 60-кратный избыток DMAPO относительно иммобилизованного первого нуклеозидного звена и выдерживают 5 мин при комнатной температуре. Раствор активированного нуклеотида удаляют и после промывки. диска растворителями в последовательности, указанной в табл. 1, проводят деблокирование 3%-ным раствором три- хлоруксусной кислоты в хлороформе. Далее осуществляют последовательность операций в соответствии с табл.2. После завершения последнего цикла наращивания олигонуклеотидной цепи иммо- билизованньш олигонуклеотид детрити- лируют раствором трихлоруксусной кислоты в хлороформе, целлюлозньШ диск промывают хлороформом и ацетонитрилом, извлекают из шприца и помещают в 10 мл 0,5 М раствора п-нитробензаль- доксимата лития в водном пиридине. Диск выдерживают в деблокирующем растворе 12 ч при комнатной температуре, после чего раствор отделяют фильтрованием и упаривают в вакууме. Остаток растворяют в 10 мл концентрирован ного водного аммиака и раствор нагревают в плотно закрытой колбе 24 ч при 40°С. Аммиак удаляют в вакууме, остаток нейтрализуют 50%-ной уксусной кислотой и разбавляют до 15 мл водой. Водную фазу экстрагируют этил- ацетатом, упаривают в вакууме и обессоливают пропусканием через колонку с био-гелем Р-2. Продукт выделяют с помощью ионообменной ВЭ)СХ в линейном градиенте калийфосфатного буфера
51
(рИ 6,5) на сорбенте, изготовленном на основе силохрома, модифицированном сшитым полиэтиленимином.
Выход, определенный после выделе- ния олигонуклеотида ионообменной хроматографией, составил 34% {или 85% ,на каяодую стадию конденсации).
Пример 6. Синтез олигонуклеотида d CAATTAACAATA).
Навеску полимерного носителя (0,049 г)на .основе CPG-250-Х , на котором известным методом иммобилизовано первое нуклеозидное звено (удельная загрузка 80 мкмоль/г), по- мещают в реактор колоночного типа, снабженный фильтруюпдами пластинками. Через реактор пропускают 3%-ный раствор трихлоруксусной кислоты в хлороформе (о,5 мин). Затем проводят про- мывку растворителями как указано в табл. 2.
Промывают реактор аргоном в течение 1 мин и подают в него смесь нук- леотида (40 мкмоль), TPS и DMAPO в молярном соотношении 1:2:6 в 1-1,5 мл
абс.пиридина. Избыток-нуклеотида относительно первого нуклёотидного звена, иммобилизованного на носителе, составляет 10 экв.
Реактор закрывают и встряхивают 5 мин. Далее операции проводят в соответствии с табл. 2. За степенью протекания межнуклео гидных конденсаций следят посредством измерения поглощения диметокситритилкатиона в элюате после деблокирования при 498 Нм. Вы- ходы на каждой стадии превышают 90%. После завершения последнего цикла наращивания олигонуклеотидйой цепи носитель помещают в 2 мл 0,5 М раствора п-нитробензальдоксимата лития в водном пиридине. Смесь выдерживают в течение ночи при комнатной температуре, после удаления носителя растворитель упаривают в вакууме, остаток обрабатывают аммиаком и далее
386
Очищают целевой проду:кг как описано в примере 5. Выход ол:; гонуклеотида
d(СААТТААСААТА) составляет 99,з ОЕ
при 260 нм или 17% от теоретического. Средний выход на стадию составляет 86%,
Таким образом, предлагаемый способ обеспечивает более высокую скорость конденсации (примерно в 3 раза) чем способ-прототип, в твердофазном варианте триэфирн(эго синтеза оли- гонуклеотидов, так и :лри синтезе оли- гонуклеотидов в растворе. Достигаемые при этом выходы целевых продуктов не ниже, чем при использовании способа-прототипа. В случае твердофазного метода синтеза сокращение времени конденсации позволяет значительно сократить общую длительность наращивания олигонуклеотидной цепи.
Формула изобрет. ения
25
35
1.Способ триэфирного синтеза оли- гонуклаотидов конденсацией 3-п-хлор- фенилфосфата защищенного нуклеозида или олигонуклеотида с защищенным- нук30 леозидом, нуклеотидом или олигонукле- отидом, содержащим свободную 5 -гид- роксильную группу, в пиридине при действии производного арилсульфокси- лоты в качестве конденсирующего агента и в присутствии катализатора, о т- л и чающийся тем, что, с цель ускорения процесса, в качестве катализатора используют 4-Н-К-димитилам- минопиридин-1-оксид, взятый в 2 - 340 кратном молярном избытке по отношению к конденсирующему агенту.
2.Способ по п. 1, о т л и ч а ю- щ.и и с я тем, что Е качестве конденсирующего агента используют 2,4,
45 6-триизопропилбензолсульфохлорид или 1 - (2,4,6-триизопропил:бензолсульфо- нш1)-3-нитро-1,2,4-триазол.
713519388
Таблица
Карта операций для одного цикла наращивания олигонуклеотидной цепи на целлншозном носителе
ГО
2030 050ffff
ff ff/ wa/r7ff effffff:mir / ea e/i/u (в AfUf y/rf&)



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ твердофазного синтеза дезоксиолигонуклеотидов | 1984 |
|
SU1265196A1 |
| МОДИФИЦИРОВАННЫЕ ОЛИГОНУКЛЕОТИДЫ, АКТИВИРУЮЩИЕ РНКазу Н | 2017 |
|
RU2740501C2 |
| Способ получения моноцианэтиловых эфиров защищенных мононуклеотидов | 1979 |
|
SU910649A1 |
| МОДИФИЦИРОВАННЫЕ ОЛИГОНУКЛЕОТИДЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2014 |
|
RU2708237C2 |
| НОВЫЕ АНАЛОГИ 2`, 5`-ОЛИГОАДЕНИЛАТА ИЛИ ИХ ФАРМАКОЛОГИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2311422C2 |
| Способ твердофазного синтеза олигонуклеотидов | 1985 |
|
SU1318600A1 |
| ОЛИГОНУКЛЕОТИДЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2088588C1 |
| СИНТЕЗ ОЛИГОНУКЛЕОТИДОВ | 2006 |
|
RU2465280C2 |
| Способ получения 5 @ -0-диметокситритилтимидин-3 @ -гидрофосфоната | 1990 |
|
SU1759842A1 |
| Способ получения 5 -цианэтиловых эфиров -защищенных дезоксирибоолигонуклеотидных блоков | 1978 |
|
SU717063A1 |
Изобретение относится к химии нуклеиновых кислот, в частности к триэфирному синтезу олигонуклеотидов (ОНТ), которые применяются в биологии и генной инженерии. Цель - ускорение процесса. Синтез ОНТ ведут конденсацией 3-п-хлорфенш1фосфата захдищенно- го нуклеозида или ОНТ с защищенным нуклеозидом, нуклеотидом или олиго- нуклеотидом, содержащим свободную 5 -ОН группу в пиридине при действии конденсирующего агента (КА) и в присутствии катализатора (КТ). В качестве КТ используют 4-М,Н-диметш1амино- пиридин-1-оксид, взятый в-3-кратном мольном избытке по отношению к КА. В качестве последнего используют 2,4,6-триизопропилбензолсульфохлорид или 1-(2,4,6-триизопропипб ензолсуль- фонш1)-3-нитро-1,2,4-триазол. Способ обеспечивает повышение скорости конденсации примерно в 3 раза. 1 з.п. ф-лы, 1 ил., 2 табл. i О) ОО сд со со 00
Редактор Н.Киштуликец
Составитель Г.Коннова Техред и.Верес
Заказ 6424Тираж 348Подписное .
ВНИйПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб,, д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная, 4
Корректор О.Кравцова
| Каюгаин А.Л., БерЛиК ГО.А., Колосов М.И, Нуклеофильный катализ межнуклеотиднЬй конденсации в ф6сфо- триэфирном синтезе олигонуклеотидов | |||
| Биоорганическая химия, 1982, т | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Льновыдергивающая машина | 1923 |
|
SU660A1 |
| Evimov В.А., Pezezdatto С.В | |||
| Ch a-- shmacehieva О.Т | |||
| Hucleic acids rese- ach | |||
| New affect mithod for the Senj- thesis of oligonucleotides, 1982,v.lO, № 21, p | |||
| Гудок | 1923 |
|
SU6675A1 |
Авторы
Даты
1987-11-15—Публикация
1984-08-10—Подача