13564
Изобретение относится к области органической химии к способу полу- п%ния А- КНТропроизводньгх бензо-2, t-jS-- тиадиазола,,, мспо.пьзуемых в качестве фунгицидов, а также служащих исход- ным сырьем дай получения лекарствек- иык зещесттз и красителей из класса 6ензс 2,1,3-тз-шдиазола.
Целью изобретения является упро-, JQ щегше те-хнологий гфоцесса.
Синтез ос т вствляется по следующей скеме
.
{) R,-R,-H,
2)R,-R,,C1,
3)R,C1,
Пример. Способ осуществля- атся следующим образом. ,
Смесь из соответствующего о-фени- лендиамина, хлористого тиснила и концентрированной серной КИСЛОТЫ} взятых в молярном соотношении i;(3, 90&- 8,8): (о5344-0, 7) ., нагревают ч при кипении, охлаждают -и при комнатной тежературе н-: реакционной массе прибавляют снесь, состоящую из концент- рировсшнон серной и азотной кислоты ( г/см ).. Зтаем реакционную массу Воздерживают О ,5 ч при комнатной .теьшературе и выливают на лед. Выпавший осадок отфильтровывают, про водой до нейтральной реакции и высзгвшвают, Выход 70-83%, .
При необходимости целевой продукт перекристалйизовынают из изопропа - нола.
Получение Д-нитробенэо-З,1jS-TKa- диазола В трехгорлую 2-литровую кол бу, снабженную мешалкой, помещают 108 г (1 моль) о-фениленДиамийа и 2.80 №1 (3,906 моль) хлористого тиони лЗо Затег-5 из капельной воронки в течение 5 ыкп приливают 8 мл (0,344 моль) кокцеитрированной серной зкислоты. Смесь кипятят 1 ч. Затем попущенную массу охлаждают до. 35 45 С и к ней прибавляют 2/3 объема концентрированной серной кислоты, входящей в нитрующую смесь, т.е. 280 NUT (3,35 моль). При прибавлении концентрированной серной кислоты тем пература смеси снижается до 2-15 С.
Q
0
5
5
0
g . 55
50
122
Перемешивают реакционную массу 20- 30 мин так, чтобы ее температура поднялась до 20°С и начинают нитровать смесью и 150 мл (2.86 моль) концентрированной серной кислоты и 50 мл (Зз32 моль) азотной кислоты (d i,415 г/см ) поддерживая температуру , Ведение нитрования при О-(7 С приводит к получению смеси из бензо-251,3-тиадиаэола и 4-нит- робензо-25,3-тиадиазола.
Прибавление 300 мл нитрующей смеси занимает 60-100 (тн, По окончании иитрования реакционную массу выдерживают 0,5 ч при комнатной температуре, следя чтобы ее температура
д
не поднялась выше 30 С а затем выливают в ледяную воду. Вьшавший бса- док отфильтровывают, промывают водой до нейтральной реакции, а затем-ме- танолом (300 мл) и сушат. Получают S50 г (82,87%) 4-китробенэо-2, ,3- тиадиазола; т.пл. 05-10 С (в капилляре) согласно ГСТ 18995.4-73 на столике т.пл. }03-Ш5°С; Rj 0,6 (Sllu- fol UV-254, система - хлороформ, проявление в УФ-свете на приборе Хроматоскоп М).
Получение 4-нитро-5,7-дихлорбензо- -2,I З-тиадиазола. Смесь иэ 27 г (0,1525 моль) 2,4-дихлор-6-аминоани- лина, 96,5 мл (1,342 моль хлористого тионгша и 4,65 мл (050873 моль) концентрированной серной кислоты кипятят I ч. Затем реакционную массу охлаждают до 35-45 С и к ней прибавляют примерно 2/3 объема концентрированной серной кислоты, входящей и . нитрующую смесь, а именно 83,5 мл (1,5673 моль), причем температура реакционной массы падает до 12-15 С. После получасового перемешивания реакционной массы при комнатной температуре к ней в течение 20 мин прибавляют нитрующую смесь, состоя1дун из 40,5 мл (0,7604 моль) концентриро- йанной серной кислоты и 27 мл (0,6064 моль) азотной кислоты (d 1, г/см ) так, чтобы температура реакционной массы была в пределах 20-25 С, По окончашш прибавления нитрующей смеси реакционную массу вы- дерзживают 0,5 ч при комнатной температуре, следя за тем, чтобы температура внутри нее не повЕлшалась выше . Затем смесь выливают в ледяную воду, отфильтрозывагот выпавший осадок, про№1вают его водой и метанолом
313
(75 мл) сушат и получают 27г (70,81% А-нитро-5,7-дихлорбензо-2,1,3-тиадиа зола; . в капилляре согласно ГОСТ 18995.4-73, на столике 125-126°С; (Siluf&l UV-254, система хлороформ, проявление в УФ- свете, прибор Хроматоскоп М),
Получение 4-нитро-5-хлорбензо-2, I,3-тиадиазола. Смесь из 14,25 г (0,1 моль) 2-амино-4-хлоранилина, 54 мл (0,751 моль) хлористого тиони- ла, 3,5 мл (0,0657 моль) концентрированной серной кислоты нагревают при кипении 1 ч. Затем реакционную массу охлаждают до 35-45 С и к ней прибавляют 42,75 мл (0,8026 моль) концентрированной серной кислоты, входящей в нитрующую смесь (реакция чрезвычайно эндотермична. Температура пониже- ется до С). Перемешивают реакционную массу при комнатной темпера- т уре в течение получаса, затем при температуре 20-25 С ведут нитрование прибавляя в течение 10 мин смесь из 14,25 мл (0,320 моль) азотной кислоты (d 1,415 г/см ) к 21,4 мл (0,4017 моль) концентрированной серной кислоты. Затем реакционную массу вьщерживают 30 мин при комнатной теьтературе, следя за тем чтобы температура внутри нее не повышалась выше.30 С. Выливают смесь в ледяную воду, вьтавший осадок отфильтровьшают промывают водой и метанолом (40 ш), сушат и получают 16 г (74,24%) 4-нит- ро 5-хлорбензо-2,1,3-тиадиазола, в капилляре т.пл. 145-147 С согласно ГОСТ 18995.4-73, на столике 142- - 144°С; R 0,74 (Silufol UV-254, сие- тема хлороформ, проявление в УФ-све- те, прибор Хроматоскоп М).
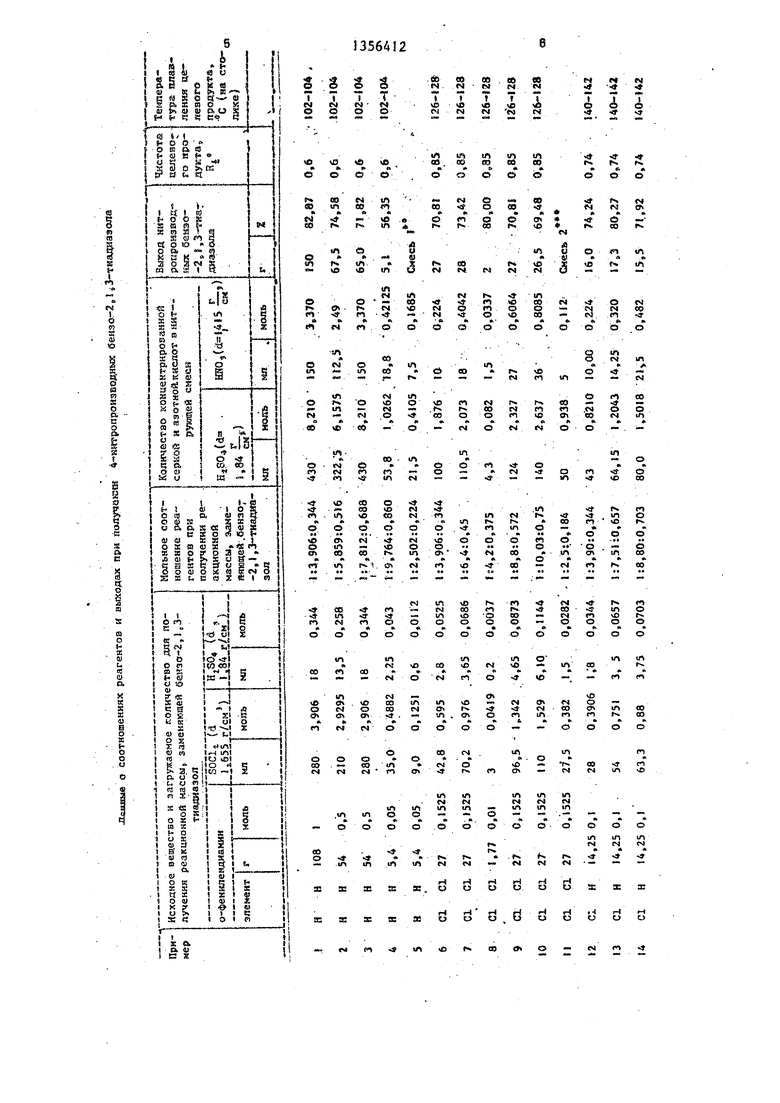
Дополнительные примеры представлены в таблице
Формула изобретения
Способ получения 4-нитропроизвод-г- ньйс бензо-2,1,3-тиадиазола общей
формулы
Wi
Ri-l- «
где R,, или R , или R,C1, ,
включающий нитрование соответствующего бензо-2,I,3-тиадиазола смесью азотной и концентрированной серной кислоты, отличающийся тем, что, с целью упрощения технологии процесса, о-фенилендиакшн общей формулы
где R, и RJ, имеют указанные значения,
подвергают взаимодействию с хлористым тионилом н концентрированной серной кислотой при молярном соотношении о-феннлендиамина - слорнстого тионила - концентрированной серной кислоты, равном 1:3,906-8,8:0,344- 0,7, с последующим нитрованием полученной смеси при 20-25 С с использованием азотной кислоты с удельюым весом 1,А-,5 г/см.

| название | год | авторы | номер документа |
|---|---|---|---|
| 2-[(Бензо-2,1,3-тиадиазол-4-сульфонил)амино] бензойные кислоты в качестве промежуточных продуктов в синтезе N-(4-хлорфенил)- или N-(3,4-дихлорфенил)-2-[(бензо-2,1,3-тиадиазол-4-сульфонил)амино]-5-хлорбензамида, обладающих антигельминтной активностью | 1989 |
|
SU1685935A1 |
| Способ получения бензо-2,1,3-тиадиазола | 1983 |
|
SU1114677A1 |
| Способ лечения мониезиозов овец | 1990 |
|
SU1782593A1 |
| Способ получения смеси динитроизомеров 2-фенилбензимидазола | 1987 |
|
SU1527236A1 |
| N-(Галоидфенил)-2-[(бензо-2,1,3-тиадиазол-4-сульфонил)амино]-5-хлорбензамиды, обладающие активностью при экспериментальном трихоцефалезе | 1989 |
|
SU1685936A1 |
| 2-[(7-Бромбензо-2,1,3-тиадиазол-4-сульфонил) амино]-5-хлорбензойная кислота в качестве промежуточного продукта в синтезе 2-[(7-бромбензо-2,1,3-тиадиапрозол-4-сульфонил) амино]-5-хлор-N-(4-хлорфенил) бензамида, обладающего антигельминтной активностью | 1989 |
|
SU1685937A1 |
| Способ получения производных гидроксиламина | 1984 |
|
SU1428190A3 |
| СПОСОБ ПОЛУЧЕНИЯ 2-(п-АМИНОФЕНИЛ)-6-АМИНО-4H-3,1-БЕНЗОКСАЗИНОНА-4 | 1999 |
|
RU2161611C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИАЗИДО-2-НИТРО-2-АЗАПРОПАНА | 2010 |
|
RU2440974C1 |
| Способ получения 6-метоксиндола | 1958 |
|
SU123531A1 |
Изобретение касается производных тиодиазола, в частности получения 4-нитро6ензо (или 5 ,7-дихлорбе11- 30- или 5 хлорбензо)-2,1,3-тиядиазо- лов - сырья для лекарственных веществ и красителей. Упрощение процесса достигается нредвлрительной обработкой другого сырья о-феш лендиами- на, который хлорируют с помощью хлористого тионила в присутствии конц. HjS04 - при молярном соотношении I:3,906-8,8:О,344-0,7. Дальнейшее нитрование полученного продукта ведут при 20-25 с азотной кислотой с d 1,4-1,5 г/см в смеси с серной кислотой (конц.). Способ обеспечивает выход целевых продуктов 56-83% при меньшем, чем в известном случае, расходе реагентов и более доступного исходного вещества о-фенилендиаь(ина. 1 таб/,. ИЗ

| В.Г | |||
| Лесин, В.А | |||
| Сергеев | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Паровозный поршень, останавливающийся при езде без пара | 1924 |
|
SU839A1 |
| В.Г | |||
| Песин, A.M | |||
| Халецкий | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| V | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| - ЖОХ, 1957, т | |||
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
| Рычажные весы | 1925 |
|
SU2599A1 |
Авторы
Даты
1991-12-15—Публикация
1985-11-27—Подача