135
Изобретение относится к способу получения замещенных тиазоло(3,2-а)- пиримидинов - новых биологически активных соединений, которые могут най ти применение в медицине.
Цель изобретения - новые производные в ряду тиазолоО,2-а)пирими- динов малотоксичных и обладающих
более высокой противоязвенной и про- ю -этенил -5Н-тиазоло(3,2-а)пиримидинтивовоспалительнои активностью.
Пример 1. Проводят взаимодействие 3,06 г 2-аминотиазола с 6,4 г этил-2-метил-ацетоацетата в 15,3 г полифосфорной кислоты (7,1 г . фосфорного ангидрида и 8,2 г 99%-ной ортофосфорной кислоты) с одновременным перемешиванием при 100 С в течение 2 ч. После охлаждения, разбавления смесью воды со льдом и нейтрализации отфильтровывают образовавшийся осадок, промывают его водой и перекристаллизовывают из изопропи- лового эфира, в результате чего получают 5,04 г 6,7-диметил-5Н-тиазоло- (3,2-а)пиримидин-5-она с т.пл. 112- 113 С. Затем проводят реакцию последнего в присутствии 4., 55 г метокси- да натрия с перемешиванием при температуре кипения с обратным холодильником в течение 12 ч с 5,99 г 3-пиридинкарбоксальдегида в 130 мл метанола. После охлаждения осадок отфильтровывают и промывают водой
-5-он с т. пл. 190-191 С,
6-хлор-7-транс- 2-(3-пиридил)-эте- нил -5Н-тиазоло(3,2-а)пиримидин-5- -он, т. пл, 235-237°Ci
15 Пример 2. В 25 г полифосфорной кислоты при перемешивании и при 100 С в течение 8 ч проводят реакцию 5 г 2-аминотиазола с 10,8 г этил-4-хлорацетоацетата.
20 После охлаждения, разбавления « смесью воды со льдом и нейтрализации осадок отфильтровывают и промывают водой. Затем при температуре кипения с обратным холодильником и при одновременном.перемешивании в течение 30- ч.в 130 мл ацетонитрйла проводят взаимодействие 8,8 г полученного 7-хлорметил-5Н-тиазоло(3,2- -а)пиримидина-5-она с 12,8 г трифе30 нилфосфина. После охлаждения осадок отфильтровывают и промывают изопро- пиловым эфиром, в результате чего получают 20,6 г 5Н-тиазоло(3;,2-a)- пиpимидин-5-oн-7-ил l-мeтилтpифeнил-
25
30 нилфосфина. После охлаждения осадок отфильтровывают и промывают изопро- пиловым эфиром, в результате чего получают 20,6 г 5Н-тиазоло(3;,2-a)- пиpимидин-5-oн-7-ил l-мeтилтpифeнил-
до нейтральной реакции. Б результате фосфонийхлорида с т. пл. 295-299°С, кристаллизации из метанола получают 3,2 г 6-метил-7 транс- 2-(3-пири- дил)-этенил -5Н-тиазоло(3,2-а)пири- мидин-5-она с т. пл. 192-194 С. Выход 38,9%.
4b
которьш при перемешивании добавляют в 50%-ную суспензию гидрида натрия (2,61 г) в 300 мл диметилсуль- фоксида и 200 мл дихлорэтана, и при комнатной температуре в течение 6 ч проводят реакцию с 7,15 г 3-пиридин карбоксальдегида. После выпаривания в вакууме дихлорэтана раствор разбавляют смесью воды со льдом, выпав
В ходе проведения аналогичных экспериментов получают следующие соеди- ,нения:
6-метил-7-транс- 2-(4-пиридил)- -этенил -5Н-тиазоло(3,2-а)пиримидин- -5-он с т. пл. 252-253°CV
6-метил-7-транс- 2-(6-метил-2- .-пиридил)-этенил -5Н-тиазоло(3,2-а)- пиримидин-5-он с т. пл. 198-199 0 ,
2,3,6-триметил-7-транс- 2-(3-пи:: ридил)-этенил -5Н-тиазоло(3,2-а) пири МИДИН-5-ОН, т.пл. 193-195°С;
2-хлор-6-метил-7-транс-Г2-(3-пи- рид1ш)-этенил -5Н-тиазоло(3,2-а)пи- римидин-5-он;
3,6 диметил-7-транс- 2-(3-пири- дил)-этенил -611-тиазоло(3, 2-а)пири- МЦЦИН-5-ОН, т.пл. 211-214°Cf
3-(4-аминофенил)-7-транс- 2-(3- пиридил)-этенил -5Н-тиазоло(3,2-а)пири г1идин-5-он, т.пл. 282-284°С (разложение);
о 6-этил-7-транс 2-(3-пиридил)-зте- нил -5Н-тиазоло(3,2-а)пиримидин-5-- он с Т..ПЛ. 176-177°С;
6-пролил-7-транс- 2-(3-пиридил)-этенил -5Н-тиазоло(3,2-а)пиримидин5-он с т. пл. 190-191 С,
6-хлор-7-транс- 2-(3-пиридил)-эте- ил -5Н-тиазоло(3,2-а)пиримидин-5- он, т. пл, 235-237°Ci
Пример 2. В 25 г полифосфорной кислоты при перемешивании и при 100 С в течение 8 ч проводят реакию 5 г 2-аминотиазола с 10,8 г этил-4-хлорацетоацетата.
После охлаждения, разбавления смесью воды со льдом и нейтрализации осадок отфильтровывают и промывают водой. Затем при температуре кипения с обратным холодильником и при одновременном.перемешивании в течение 30- ч.в 130 мл ацетонитрйла проводят взаимодействие 8,8 г полученного 7-хлорметил-5Н-тиазоло(3,2- -а)пиримидина-5-она с 12,8 г трифенилфосфина. После охлаждения осадок отфильтровывают и промывают изопро- пиловым эфиром, в результате чего получают 20,6 г 5Н-тиазоло(3;,2-a)- пиpимидин-5-oн-7-ил l-мeтилтpифeнил-
фосфонийхлорида с т. пл. 295-299°С,
фосфонийхлорида с т. пл. 295-299°С,
4b
которьш при перемешивании добавляют в 50%-ную суспензию гидрида натрия (2,61 г) в 300 мл диметилсуль- фоксида и 200 мл дихлорэтана, и при комнатной температуре в течение 6 ч проводят реакцию с 7,15 г 3-пиридинкарбоксальдегида. После выпаривания в вакууме дихлорэтана раствор разбавляют смесью воды со льдом, выпав45 П1ИЙ осадок отфильтровывают и промывают водой, после чего в результате кристаллизации из изопропилового .спирта получают 6,2 г 7-транс- 2-(3- -пиридш1)-этенил -5Н-тиазоло(3,2-а)50 пиримидин-5-она с т.пл. 206-207 С. Выход 48,6%;
В соответствии с изложенным в ходе проведения процесса с использованием подходящих альдегидов с анало55 гичным выходом получают следующие соединения:
7-транс- 2-(2-пиpидил)-этJeнил - -5Н-тиаз6ло(3,2-а)пиримидин-5-он с т. пл. 231-232 с;
7-транс- 2-(4-пиридил)-этенил - -5Н-тиазоло(3,2-а)пиримидин-5-он с т. пл. 246-247 01
7-транс;- 2-(6-метил-2-пиридил)- этенил -5Н-тиазоло(3,2-а)пиримидинон с т. пд. 213-216°С{
7-транс- 2-(1-метил-2-пирролил)- -этенил -5Н-тиазоло(3,2-а)пиримидин-5-он с т. пл. 211-212°с;
7-транс-Г2-(3-метоксифенил-эте- нил -5Н-тиазоло(3,2-а)пиримидин-5-он с т. пл.
7-транс-р-(4-метилфенил)-этенил -5Н-тиазоло-(3.2-а)пиримидин-5-он с т. пл. 214-216 Ci
3-(4-амино-фенил)-7-транс- 2-(3- -пиридил)-этенил -5Н-тиазоло (3, 2-а)282-284 с
пиримидин-5-он с т.пл. (разложение).
Пример 3. В 40 г полифосфорной кислоты при. 110 С с одновременны перемешиванием в течение 1 ч проводят взаимодействие 8 г 2-амино-5- -хлортиазолигидрохлорида с 15,8 г 4-хлорацетоацетата. После охлаждения разбавления водой и нейтрализах ии 35%-ным раствором гидрата окиси натрия осадок отфильтровывают и промывают водой. В результате кристаллизации из изопропилового эфира получают 7,45 г 2-хлор-7-хлорметил-5Н- -тиазоло(3,2-а) пиримидин-5-она с т. пл. 123-125 с. Затем при перемешивании и вьщержке при температуре кипения с обратным холодильником в течение 10 ч проводят реакцию полученного продукта с 9,42 г трифенил- фосфина в 100 мл ацетонитрила. После охлаждения осадок отфильтровывают и промьшают ацет онитрипом с получением 10 г 2-хлор-5Н-тиазоло(3,2-а)пирими- дин-3-он-7-ш1-метилтрифенилфосфоний- хлорида ст. пл. 300-310°С (с разложением) , который суспендируют далее в 40 мл диметилсульфоксида и обрабатывают 2,48 г трет-бутоксида калия, растворенного в 40 мл диметилсульфоксида. Ьперацию проводят при комнатно температуре с перемешиванием в тече- ние 10 мин. В раствор полученного таким образом илида добавляют 2,45 г 3-пиридинкарбоксальдегида, растворенного в 20 мл диметилсульфоксида, и реакционную смесь с перемешиванием выдерживают при комнатной температур в течение 15 мин. После разбавления воды со льдом и нейтрализации первичным кислым ортофосфатом натрия
20
25
30
50 55
358786
полученный осадок отфильтровывают и кристаллизуют из смеси дихлорметана с изопропиловым спиртом, в результа- 5 те чего получают 4,3 г 2-хлор-7-транс- 2-(3-пиридил)-зтенил)-5Н-тиа- золо(3,2-а)пиримидин-5-она с т.пл. 189-190 С. Выход 31,67.
В ходе проведения процесса анало- 10 гично изложенному получают с аналогичным выходом следующие соединения:
З-метил-7-транс- 2-(3-пиридил)- -этенил) -5Н-тиазоло (3.2-а)пиримидин- -5-он с т. пл. 191-193°С , 15 2,З-диметил-7-транс- 2-(3-пиридил) -этенил -5Н-тиазоло(3,2-а)пири- МИДИН-5-ОН с т. пл. 179-180°С;
З-трифторметил-7-транс- 2-(3-пи- ридил)-этенил -5Н-тиазоло(3,2-а)пи- римидин-5-он с т. пл. 224-226 С ,
2-бром-7-транс- 2-(3-пиридил)-этенил -5Н-тиазоло(3,2-а)пиримидин-5- -он с т. пл. 211-213°С-,
Пример 4. В 250 мл ацетонитрила с перемешиванием при температуре кипения с обратным холодильником в течение 24 ч проводят реакцию 7,8 г 7-хлорметил-3-фенил-5Н-тиазоло(3,2- -а)пиримидин-5-она с т.пл. 194-195 С, полученного в соответствии с примером 5, с 8 г трифенилфосфина. После охлаждения раствор концентрируют в вакууме до небольшого остаточного объема, разбавляют изопропиловым эфи-. ром и выпавший осадок отфильтровывают, в результате чего получают 11 г 3-фенш1-5Н--тиазоло(3,2-а)пиримид ин- -5-он-7-ил -метилтрифенилфосфоний- хлорида, который затем суспендируют в 50 мл диметилсульфоксида и при перемешивании в -условиях комнатной температуры обрабатывают 2,46 г трет-бутоксидом натрия, растворенного в 50 мл диметилсульфоксида. Далее при комнатной температуре в течение 60 мин проводят реакцию раствора полученного таким образом илида с 2.36 г 3-пиридинкарбоксальдегида с последующими разбавлением реакционной смеси смесью воды со льдом и нейтрализацией первичным кислым ортофосфатом натрия. Выпавший осадок отфильт- ровьшают и промывают водой. В результате кристаллизации из смеси дихлорметана с метанолом получают 2,8 г З-фенил-7-транс-f2-(3-пиpидил)- -этениЛ -5Н-тиазоло(3,2-а)пиримидин- -5-она с т. пл. 270-272 С. Выход 30,0 %.
35
40
45
В ходе проведения эксперимента аналогично изложенному получают с аналогичным выходом следующие соединения:
/- 3-(4-фторфенил)-7-транс- Г2-(3- -пиридил)-этенил -5Н-тиазоло(3,2-а)- пиримидин-5-он с т. пл. 241-243 CJ 3-( 4-хлорфенил)-6-транс- -2(3- -пиридил) -э тенил -бН-тиазоло (3,2-а) - пиримидин-5-он с т. пл, 282-283 Cj 3-(4-метилфенил)-7-транс- 2-(3- -пиридил)-этенил -5Н-тиазоло(3,2-а)- пиримидин-5-он с т,пл. 254-255 С , 3-(3-метоксифенил)-7-транс- 2Ш
Выпавший при этом осадок отфильт ровывают и промывают водой. В результате кристаллизации из смеси ди хлорметана с метанолом получают 2,8 г 3-(3-пиридил)-7-транс- 2-(3-пи дил)-этенш1 -5Н-тиазоло (3, 2-а)пирим дин-5-она с т. пл. 270-272°С.Выход
Пример 6. В 375 мл диметил ацетамида, содержащего 71,5 г полифосфорной кислоты (42,5 г фосфорного ангидрида + 29 г ортофосфорной кислоты) в условиях перемешивания п 100 С в течение 24 ч проводят реакцию 10 г 2-аминотиазола с 37,5 г
охлаждения, разбавления водой и нейтрализации добавлением вторичног кислого ортофосфата натрия выпавший осадок экстрагируют этилацетатом.
-(З-пиридил)-этенил -5Н-тиазоло(3,2- t5 этил-2-аЦетоксиацетоацетата. После -а)пиримидин-5-он с т.пл. 209-210 С ,
3-(4-метоксифенил)-6-транс- 2- -(3-пиридил)-этенил -5Н-тиазоло(3.2- -а)пиримидин-5-он с т.пл. 241-242 С
2-метил-3-фенил-7-транс-1 2-(3-пи- 20«0рганический. раствор выпаривают в ридил)-этенил -5Н-тиазоло(3,2-а)пи- римидин-5-он с т. пл. 234-237 С,
3-(4-аминофенил)-7-транс-L2-(3- -пиридил)-этенил -5Н-тиазоло(3.2-а)- 25 пиримидин-5-он с т. пл. 282-284 С (с разложением).
вакууме досуха и остаток чистят в колонке с двуокисью кремния с испол зованием хлороформа в качестве элю- ента.
В результате кристаллизации из изопропилового эфира получают 8 г 6-ацетокси-7-метил-5Н-тиазоло(3,2-а пиримидин-5-она с т.пл. 118-119 С, который подвергают гидролизу путем
Пример 5. 5,30 г 7-хлорме- тил-3-(3-пиридил)-5Н-тиазоло(3,2-а)- пиримидин-5-она с т. пл. 280-290 0 (с разложением). полученного в соответствии с примером 6, используют для проведения реакции в 500 мл аце- тонитрила при одновременных перемешивании и кипячении с обратным холодильником в течение 40 ч с 5 г три- фенилфосфина. После охлаждения раствор концентрируют в вакууме до небольшого остаточного объема, разбавляют изопропиловым эфиром и выпавший осадок отфильтровывают с получением 8 г 3-(3-пиридил)-5Н-тиа- Золо(3,2-а)пиримидин-5-он-7-ил1 -ме- тилтрифенилфосфонийхлорида, который суспендируют в 100 мл диметилсульфок сида, после чего при перемешивании в условиях комнатной температуры сусг пензию обрабатывают 1,66 г трет-бу- токсида калия, растворенного в 50 мл диметилсульфоксида. Далее при комнатной температуре в течение 30 мин проводят реакцию раствора полученного таким образом илида с 1,74 г 3-пиридинкарбоксальдегида, после чего реакционную смесь разбавляют смесью воды со льдом и нейтрализуют добавлением первичного кислого ортофосфата натрия.
Выпавший при этом осадок отфильтровывают и промывают водой. В результате кристаллизации из смеси ди- хлорметана с метанолом получают 2,8 г 3-(3-пиридил)-7-транс- 2-(3-пирй- дил)-этенш1 -5Н-тиазоло (3, 2-а)пирими- дин-5-она с т. пл. 270-272°С.Выход 44%
Пример 6. В 375 мл диметил- ацетамида, содержащего 71,5 г полифосфорной кислоты (42,5 г фосфорного ангидрида + 29 г ортофосфорной кислоты) в условиях перемешивания при 100 С в течение 24 ч проводят реакцию 10 г 2-аминотиазола с 37,5 г
этил-2-аЦетоксиацетоацетата. После
охлаждения, разбавления водой и нейтрализации добавлением вторичного кислого ортофосфата натрия выпавший осадок экстрагируют этилацетатом.
этил-2-аЦетоксиацетоацетата. После
рганический. раствор выпаривают в
вакууме досуха и остаток чистят в колонке с двуокисью кремния с исполь зованием хлороформа в качестве элю- ента.
В результате кристаллизации из изопропилового эфира получают 8 г 6-ацетокси-7-метил-5Н-тиазоло(3,2-а) пиримидин-5-она с т.пл. 118-119 С, который подвергают гидролизу путем
его обработки в 80 мл метанола с перемешиванием при 60°С в течение 4ч 16 г бикарбоната натрия. После охлаждения раствора его упаривают в . вакууме до небольшого остаточного
объема, и этот остаток растворяют в этилацетате с последующей повторной экстракционной обработкой водным раствором гидрата окиси натрия. Водт- ную фазу нейтрализуют добавлением
37%-ной соляной кислоты и выпавший осадок экстрагируют хлороформом. Органический раствор упаривают в вакууме досуха. В результате кристаллизации из этилацетата получают 5,3 г
6-окси-7-метил-6Н-тиазоло(3,2-а)пи- римидин-5-она с т. пл. 225-227°С, который растворяют затем в 50 мл ди- метилформамида. Далее в присутствии 8,1 г безводного карбоната калия в
условиях перемешивания при комнатной температуре в течение 16 ч проводят реакцию раствора продукта с 8,3 г. йодистого метила. Реакционную смесь разбавляют смесью воды со льдом и
подвергают ее экстракционной обработке этилацетатом, после чего органический раствор обрабатыв ают газообразным хлористым водородом. Выпавший осадок отфильтровывают и промывают этилацетатом, в результате чего получают 4,7 г 6-метокси-7-метил- -5Н-тиазоло(3,2-а)пиримидин-5-он гидрохлорида с т. пл. 185-195°С (с разложением). Затем в присутствии 3,3 г мет.оксида натрия при перемешивании и кипячении с обратным холодильником в течение 2Л ч проводят реакцию с 5,4 г 3-пи ридилкарбоксаль- дегида.После концентрирования в вакууме до небольшого остаточного объема и разбавления изопропиловым эфиром выпавший осадок отфильтровывают и промывают изопропиловым эфиром, а затем водой. В результате кристсШлизяции из 50%-ного этанола получают 3,, 2 г 6-метокси-7-Транс- 2- -(3-пиридил)-этенш{ -5Н-тиазоло(3,2- -а)пиримидин-5-она с т. пл. 186 - 187°С (выход 11,2%) и 6-метокси-7- -транс- 2-(3-пиридил)-циклопропип - -5H-тиaзoлo(Зj 2-а)пиримидин-5-он, т. пл. 92-95 С.
В ходе проведения процесса аналогично изложенному с аналогичным выходом получают 6-метокси-7-транс- 2- -(3-1тиридил)-этенил -5Н-тиазоло(3,2- -а)-пиримидин-5-он, т. пл. 163-165 С.
формамида, и в присутствии 15 г карбоната калия при перемешивании и при 60 С в течение 3 ч проводят реак цию раствора продукта с 15,4 г йодис
5 того метила. После охлаждения реакционную смесь разбавляют смесью во- ды со льДом и нейтрализуют добавлением первичного кислого ортофосфата натрия. Выпавший осадок отфильтровыШ вают и водную фазу экстрагируют
этилацетатом с полньм вьщелением про дукта. Б общей сложности получают 5,1 г 2-хлор-6-метокси-7-метил-5Н- (3,2-а)пиримидин-5-она с
f5 т. пл. 138-141 С, а затем в 150 мл бензола при температуре кипения с обратным холодильником в течение 40 ч проводят реакцию продукта с 17 г N-бромсукцинимида, который до20 бавляют отдельными порциями. После охлаждения реакционной смеси его разбавляют этилацетатом и обрабатывают водным раствором бикарбоната натрия, а затем водой. Вьщеленный ор
25 ганический раствор выпаривают в ва- , кууме досуха и остаток кристаллизуют из этилацетата с получением 2,8 г 7- -бромметил-2-хлор-6-метокси-5Н-тиазоло(3,2-а)пиримидин-6-она с т. пл. , Пример 7. В 400 мл диметил- зо 160-162°С, после чего в 50 мл ацето- ацетамида,содержащего 71 г полифосфор- нитрила при температуре кипения с ной кислоты (29 г ортофосфорной кислоты) обратным холодильником в течение 3 ч +42 г фосфорного ангидрида) в условиях
проводят реакцию полученного продукта с 2,6 г трифенилфосфином. После
непрерьшного перемешивания при 100 С в
течение 6 ч проводят реакцию 10 г 2-ами- охлаждения и упаривания в вакууме но- -хлортиазолгидрохлорида с 22 г растворителя остаток чистят с исиоль- этил-2-ацетоксиацетоацетата. После зованием этилацетата, в результате охлаждения, разбавления смесью воды чего получают 3,8 г 2-хлор-6-меток- со льдом и нейтрализации добавлением си-5Н-тиазоло(3.2-а)пиримидин-5-он- 37%-ного раствора гидрата окиси нат- 0 -7-ил -метилтрифенилфосфонийброми- рия выпавший осадок экстрагируют да, который суспендируют в 45 мл
диметилсульфоксида, и при комнатной температуре с перемешиванием в течение 10 мин обрабатьшают 0,75 г 45 трет-бутоксида калия, растворенного в 20 мл диметилсульфоксида.
этилацетатом и органический слои упаривают в вакууме досуха. Полученный остаток подвергают гидролизу путем его обработки в 100 мл диоксана при температуре кипения с обратным холодильником в течение 2 ч 50 мл 35%-ной соляной кислотой. После охлаждения реакционную смесь разбавляют смесью
Затем при комнатной температуре iB течение 1 ч проводят реакцию раст- воды со льдом и нейтрализуют добавле- 50 вора полученного таким образом или- нием 37%-ного раствора гидрата оки- да с 0,9.4 г 3-пиридинкарбоксальдегида. Реакционную смесь разбавляют смесью воды со льдом, нейтрализуют добавлением первичного кислого ор- 2 тофосфата натрия и выпавший осадок отфильтровывают. В результате кристаллизации из этанола получают 0,96 г -а)пйримидин-5-она с т. пл. 214-217 Cj . 2-хлрр-6-метокси-7-транс- 2-(3-пири- который растворяют в 100 мл диметил- ;дил)-этенилЗ-5Н-тиазоло(3,2-а)пиримиси натрия, а выпавший осаДок экстрагируют зтилацетатом. Органический раствор упаривают в вакууме досуха, а полученный остаток кристаллизуют из.метанола с получением 5,85 г 2- -хлор-6-окси-7-метил-5Н-тиазоло(3,2
.
58786 8
формамида, и в присутствии 15 г карбоната калия при перемешивании и при 60 С в течение 3 ч проводят реакцию раствора продукта с 15,4 г йодис5 того метила. После охлаждения реакционную смесь разбавляют смесью во- ды со льДом и нейтрализуют добавлением первичного кислого ортофосфата натрия. Выпавший осадок отфильтровыШ вают и водную фазу экстрагируют
этилацетатом с полньм вьщелением продукта. Б общей сложности получают 5,1 г 2-хлор-6-метокси-7-метил-5Н- (3,2-а)пиримидин-5-она с
f5 т. пл. 138-141 С, а затем в 150 мл бензола при температуре кипения с обратным холодильником в течение 40 ч проводят реакцию продукта с 17 г N-бромсукцинимида, который до20 бавляют отдельными порциями. После охлаждения реакционной смеси его разбавляют этилацетатом и обрабатывают водным раствором бикарбоната натрия, а затем водой. Вьщеленный ор25 ганический раствор выпаривают в ва- , кууме досуха и остаток кристаллизуют из этилацетата с получением 2,8 г 7- -бромметил-2-хлор-6-метокси-5Н-тиазоло(3,2-а)пиримидин-6-она с т. пл. 160-162°С, после чего в 50 мл ацето- нитрила при температуре кипения с обратным холодильником в течение 3 ч
проводят реакцию полученного продукта с 2,6 г трифенилфосфином. После
дин-5-она с т. пл. 205-207°С. Выход 5,4%.
В ходе проведения процесса аналогично изложенному получают 6-метокси- -7-транс- 2-(3-пиридил)-этенил -5Н- -тиазоло(3,2-а)пиримидин-5-он, т. пл. 186-187°С.
Пример 8. В 150 мл дихлорэтана с перемешиванием в условиях комнатной температуры в течение 4 ч проводят реакцию 6,07 г 2-хлор-7- -хлорметил-5Н-тиазоло(3,2-а)пирими- дин-5-она, полученного в соответствии с примером 5, с 3,8 г хлористого сульфурила. Реакционную смесь далее обрабатывают 5%-ным водным раствором бикарбоната натрия, после чего органическую фазу отделяют и упаривают в вакууме досуха. В результате крис- т аллизации из метанола получают 5,6 г 2,6-дихлор-7-хлорметил-5Н-тиа- золо(3,2-а)пиримидин-5-она с т.пл. 117-119 С (с разложением). Затем в 115 мл ацетонитрила при температуре
135878610
-а)пиримидин-5-он с т. пл. 226 - 228°С;
6-хлор-3-фенил-7-транс- 2-(3-пи- ридил)-3 тенил -5Н-тиаэоло(3,2-а)пи- 5 римидин-5-он с т. пл. 203-204 С ,
6-хлор-3-(4-хлорфенил)-7-транс- .
(3-пиридил)-этенил -5Н-тиазодо- (3,2-а)пиримидин-5-он с т. цл. 278- 280°с;
to 6-хлор-3-(4-метоксифенил)-7-транс- . - 2- (3-пиридил) -этеншт -5Н-тиазоло- (3,2-а)пиримидин-5-он с т. пл. 264- 265 С ,
6-хлор-З-(4-фторфенил)-7-транс- 5 - 2-(3-пиридил)-зтенил -5Н-тиазоло- (3,2-а)пиримидин-5-он с т. пл. 268- 269°с;
6-хлор-З-(4-метилфенил)-7-транс- 2-(3-пиридил)-этенил -5Н-тиазоло- 20(3,2-а)пиримидин-5-он с т. пл. 258259°с;
6-хлор-3-трифторметил-7-транс- 2- -(3-Пиридил)-этениот -5Н-тиазоло(3, 2- -а)пир имидин-5-он с т. пл. 247 кипения в течение 20 ч проводят реак- 25 249°С| Цию полученного продукта с 5,95 г 6-хлор-2-метш1-3-фенил-7транс-12- трифенилфосфина. Раствор упаривают ;;-(3-пиридил)-этенил -5Н-тиазоло(3,2- в вакууме досуха и остаток чистят -а)пиримидин-5-он с т. пл. 229-232 С; изопропиловым эфиром, в результате 6-хлор-7-транс- 2-(2-метш1-5-тиа- чего получают 10,4 г 2,6-дихлор-5Н- 30 золил)-этенил1-5Н-тиазоло(3,2-a)пи- -тиaзoлo(3,2-a)пиpимидин-4-oн-7-ИJI)- римидин-5-он, т. пл. 230-233°С;
6-хлор-З-(3-пиридил)-7-транс 2- -(3-пиридил)-этенил -5Н-тиазоло(3,2- -а)пиримидин-5-он с т. пл. 274 - 35 275°С., .
Пример 9. В условиях перемешивания при комнатной температуре в течение 1 ч проводят реакцию 4 г в течение 20 ч проводят реакцию полу- 7-мeтил-5H-тиaзoлo(3,2-a)пиpимидин- чeннoгo таким образом илида с 2,36 г 40 -5-она с т. пл. 127-129 С, получен- 3-пиридинкарбоксальдегида. Реакцион- ного в соответствии с примером 1 с
использованием этилацетоацетата,раство- ренного в 100 мл бензола, с 4,7 г N-бромсукцинимида. Выпавший осадок 45 растворяют добавлением хлороформа и раствор промывают водой, упаривают ,в вакууме досуха и кристаллизуют полученный остаток из метанола, в результате чего получают 5,1 г 6-бром-метилтрифенилфосфонийхлорида, который суспендируют в 50 мл диметилсуль- фоксида и при комнатной температуре обрабатывают 2,41 г трет-бутоксида калия, растворенного в 45 мл диме- тилсульфоксида.
Затем при комнатной температуре
ную смесь разбавляют смесью воды .со льдом, нейтрализуют первичным кислым ортофосфатом натрия и выпавший осадок отфильтровывают. В результате кристаллизации из метанола получают 3,45 г 2,6-диxлop-7-тpaнc- 2-(3-пи- pвдил)-этeнил -5H-тиaзoлo(3,2-a)пи- pI мидин-5-oнa ст. пл. 242-243 С. Выход 41,2%.
В ходе проведения процесса аналогично изложенному получают о аналогичным выходом следующие соединения:
6-хлор-.3-метил-7-транс- 2-(3-пй- pидил)-этeнилЗ-5H-тиaзoлo(3,2-a)пи- pимидин-5-oн с т. пл. 219-220 С1
6-хлор-2,3-диметш1-7-транс- 2- -(3-пиридил)-этенил -5Н-тиазоло(3,250 -7-метил-5Н-тиазоло(3,2-а)пиримидин- г5-она с т. пл. 233-234 0. Затем в 190 мл метанола в присутствии 2,2 т метоксида натрия в условиях перемешивания при температуре кипения с
55 обратным холодильником в течение 2 ч
проводят, реакцию полученного продукта с 3,4 ч 3-пиридинкарбоксаль- дегида. После охлаждения выпавший
50 -7-метил-5Н-тиазоло(3,2-а)пиримидин- г5-она с т. пл. 233-234 0. Затем в 190 мл метанола в присутствии 2,2 т метоксида натрия в условиях перемешивания при температуре кипения с
55 обратным холодильником в течение 2 ч
проводят, реакцию полученного продукта с 3,4 ч 3-пиридинкарбоксаль- дегида. После охлаждения выпавший
111
осадок отфильтровывают и промывают водой до нейтральной реакции. В результате перекристаллизации из ди- хлорметана получают 5,18 г 6-бром- -7-транс- .2-(3-пиридш1)-этенил -5Н- -тиазоло(3,2-а)пиримидин-5-она с т. пл. 208-209 с. Выход 64,3%.
Пример 10. В 50 мл диметил- формамида в условиях перемешивания при комнатной темпераутре в течение 1 ч проводят реакцию 10,4 г триме- тилсульфрксониййодида.с 50%-ным гидридом натрия (2,25 г), а затем в реакционную смесь добавляют раствор 6 г 7-транс- 2-(3-пиридил)-этенил - -5Н-тиазоло(3,2-а)пиримидин-5-она в 50 мл диметилформамида.
В условиях перемешивания при комнатной температуре эту смесь оставляют в спокойном состоянии для т протекания реакции в течение 20 ч, после чего ее разбавляют смесью воды со льдом, нейтрализуют добавлени20
. Пример. 12. 2,4 г 6-метил-7 транс- 2-(3-пиридил)-циклопропил - 5Н-тиазоло(3,2-а)пиримидин-5-он растворяют в этилацетате и обрабаты вают стехиометрическим количеством газообразного НС1 в диэтиловом эфире, осадок отфильтровывают, промывают этилацетатом, получают 2,15 г хлоргидрата 6-метил-7-транс- 2-(3- пиридил)-циклопропил -5Н-тиазоем первичного кислого фосфата натрия ло(3,2-а)пиримидин-5-она, т. пл. и подвергают экстракционной обработке 190 С (с разложением), выход 79,6%. хлороформом. После вьтаривания в вакууме сырой остаток чистят в колонке с двуокисью кремния с использоваПроведены биологические испытания соединений, полученных предлагаемым
Проведены биологические испытания соединений, полученных предлагаемым
нием этилацетата в качестве элюента. 30 способом.
В результате Кристаллизации из этил- Предлагаемые соединения представляют собой агенты, активно воздейст- .вующие на желудочно-кишечный,тракт, в частности они обладают протинояз- 35 венным и / желудочно-антисекреторным действием, кроме того, такие соеди- нения могут быть использованы для ослабления нежелательных побочных эффектов в.желудочно-кишечном трак- 40 те, которые являются следствием
систематического употребления противовоспалительных простагландиновых МИДИН-5-ОН с т. пл. 151-152 С, ингибиторов синтетазы, вследствие
6-метил-7-транс-р-(4-метилфенил)- чего они могут быть использованы с -циклопропил -5Н-тиазоло(3,2-а)пири- 45 этой целью в сочетании с ними. Противоязвенное действие предлагаемых соединений демонстрируется, например, тем фактом что они проявляют активность в ходе проведения испыта- 50 НИИ по подавлению органических язв
у крыс в соответствии с методикой
лопропил -5Н-тиазоло(3,2-а)пиримидин-. Бонфилса и др. В х оде проведения -5-он ст. пл. 159-161 C jэксперимента были использованы шесть
6-хлор-3-фенил-7-транс- 2-(3-пи- . самцов крыс Спрегью-Доули (весом по ридил)-циклопропил .-5Н-тиазоло(3,2- 55 100-120 г), обездвиженных в течение -а)пиримидин-5-он ст. пл. 136-138 С 24 у. Для лишения животных подвиж- 2-хлор-6-метокси-7-транс- 2-(3-пи- ности были использованы квадратные ридил)-циклопропил -5Н-тиазоло(3,2- . сетки из толстой гибко проволоки, -а)пиримидин-,5-он с-т. пл. 92-95 С. причем по «стечении 4 ч после обеэацетата получают 2,35 г 7-транс- 2- -(З-пиридгш)-циклопропил -5Н-тиазо- ло(3,2-а)пиримидин-5-она ст. пл. 115-117°С. Выход 37,3%.
проведения процесса аналогично изложенному получают следующие соединения с аналогичным выхо- дом:
б-метил-7-транс- (3-пиридш1)- -циклопропш11-5Н -тиазоло(3,2-а)пириМИДИН-5-ОН ст. пл. 150-155 С,
2,3,6-триметш1-7-транс- 2- (3-пиридил) -циклопропилТ-5Н-тиазоло(3,2- -а)пиримидин-5-он с т. пл. 120 С (плавится с разложением),
6-хлор-7-транс- 2-(3-пиридил)-ЦИК
12
Пример 11. 2,3 г 6-метокси- 7-транс- 2- (3-пиридил) -этенил -5Н- тиазоло(3,2-а)пиримидин-5-она растворяют в этилацетате и раствор обра- батьшают стехиометрическ| м количест-, вом водного раствора хлористого водорода в среде диэтилового эфира. Выпавший осадок собирают, отфильтро- вьшают и промывают этилацетатом с получением 2,1 г 6-метокси-7- Транс- (3-пиридил)-3 тенилЗ -5Н-тиазоло(3,2-а)пиримидин-5-он-гидрохлорида с т. пл. 2-05-210 С (с разложением). Выход 80,7%.
. Пример. 12. 2,4 г 6-метил-7- транс- 2-(3-пиридил)-циклопропил - 5Н-тиазоло(3,2-а)пиримидин-5-он растворяют в этилацетате и обрабатывают стехиометрическим количеством газообразного НС1 в диэтиловом эфире, осадок отфильтровывают, промывают этилацетатом, получают 2,15 г хлоргидрата 6-метил-7-транс- 2-(3- пиридил)-циклопропил -5Н-тиазоло(3,2-а)пиримидин-5-она, т. пл. 190 С (с разложением), выход 79,6%.
ло(3,2-а)пиримидин-5-она, т. пл. 190 С (с разложением), выход 79,6%.
Проведены биологические испытания соединений, полученных предлагаемым
13 ,1358786
движивания крысы были умерщвлены, у них удалили желудки и подсчитали с помощью препаровальной лупы число повреждений. Испытываемые соединения ввели в организм животных через рот п.о, за 1 ч до .обездвиживания .
Соединение
7-транс- 2-(3-Пиридил)-этенил1 -5Н-тиазоло(3,2- -а)пиримидин-5-он
2-Хлор-7-транс- 2-(3-пиридил)-этенил -5Н-тиа- золо(3,2-а)пиримидин 5-он
Предлагаемые соединения обладают также желудочной антисекреторной активностью, о чем свидетельствует, например, тот факт, что они проявляли активность после введения в организм через двенадцатиперстную кишку, подавляя секрецию желудочного сока у крыс в ходе проведения испытания по методике X. Шея и др. Антисекреторную активность в желудке крыс оценивали с использованием пилорусно-лигатурной техники. В каждой группе подопытных животных использовали по шести .самцов крыс Спрегью-Доули (весом по 110-130 г). За 24 ч до начала испытаний крыс ли- пшли пищи, однако воду продолжали давать. В.день операции под легкой эфирной анестезией перевязали пило- рус. Каждое испытываемое соединение вводили внутрь двенадцатиперстной кишки (в.д.) во время перевязки. По истечении 4 ч после перевязки крыс умертвили, выделенный в желудке сок собрали и подвергли центрифугированию со скоростью вращения 3500 об/мин в течение 10 мин, после чего определению подвергали весь объем жидкости без осадка. Количество свободной соляной кислоты в желудочном соке определяли ;титрованием 0,01 н. раствором гидрата оки14
В табл. 1 приведены приблизительные величины EDyg (эффективной дот зы) противоязвенной активности, достигнутой в ходе прове;д;ения описанного испытания на крысах после введения в их организм двух предлагаемых соединений.
Таблица 1
Противоязвенная активность при введении через рот EDyp, мг/кг.
10
си натрия до рН 7,0 с помощью элект- роматического рН-метра. -Одно из
предпочтительных предлагаемых соедиг нений, которое обладает желудочным антисекреторньм действием, представляет, собой, например, 6-метокси-7- . -транс- 2-(3-пиридил)-этенил -5Н-тиазоло(3,2-а)пиримидин-5-он, величина которого составила 30 мг/кг, как это определили в ходе проведения описанных испытаний на крысах после введения в организм через двенадцатиперстную кишку.
Предлагаемые соединения обладают также противовоспалительным действием, так как они проявляют активность после введения в организм через рот
при подавлении образования отека на задней лапе крыс в ответ на подподошвен- ную инъекцию каррагенина в соответствии с методикой К.А. Уинтера и др. и обратной пассивной реакции Артуса
(ОПРА) на лапах крыс, которая вызы- .вается взаимодействием антигена с антителом, в результате чего происходит образование осаждающего иммунного комплекса с последующими фикса-Цией комплемента и накоплением поли- морфонуклеарных лейкоцитов в фокальной точке. Предлагаемые соединения обладают также анальгетической активностью. Аиальгетиче скую активность
1513
определяли, например, с помощью фе- нилхинона, вызывающего болевые корчи у .мышей.в соответствии с методикой Зигмунда. Таким образом, предлагаемые соединения могут быть использованы в те рапии для лечения болезненных и воспалительных процессов, например ревматоидных артритов и остео артрозов.
Соединение
7-:транс- 2- (3-Пиридил)-этенил -5Н-тиазоло (3, 2-а)- пиримидин-5-он
4-Хлор 7-транс- 2-(З-пиридил)-этенагП-ъЗН-тиазоло- (3,2-а)пиримидин-5-он
6-Метокси-7-транс-| 2-(3-пиридш1)-этенил -5Н- -тиазоло(3,) пиримидин-5-он
.Соединение
6-Метил-7-транс- 2г-(3-пиридш1)-этенилТ -5Н- -тиазоло(3,2-а)пиримидин-5-он.
2-Хлор-7-транс- 2-(3-пиридил)этенил -5Н- -тиазоло(3,2-а)пиримидин-5-он
Что касается анальгетического действия, то для одного из предпочтительных предлагаемых соединений, например для 2-хлор-7-транс- 2-(3- -пиридил)-этенил -5Н-тназоло(3,2-а)- пиримидин-5-она, приблизительная величина составляла 25 мг/кг, как это определили в ходе проведения испытаний с болевыми корчами, вызы6
16
В табл. 2 и 3 указаны приблизительные величины ED полученные при определении противовоспалитель ного действия в ходе проведения ука- занньпс испытаний на крысах, в организм KOTOjibDC через рот вводили некоторые предлагаемые соедине ния.
Та.блица 2
Противовоспалительное действие на отек, вызванный введением карра- генина, ED , мг/кг
16
15
ТаблицаЗ
Противовоспалительное действие по реакции ОПРА , мг/кг
22
25
55.
ваемыми у крыс посредством фенил- хинона, после введения в организм животных испытьшаемого соединения герез рот.
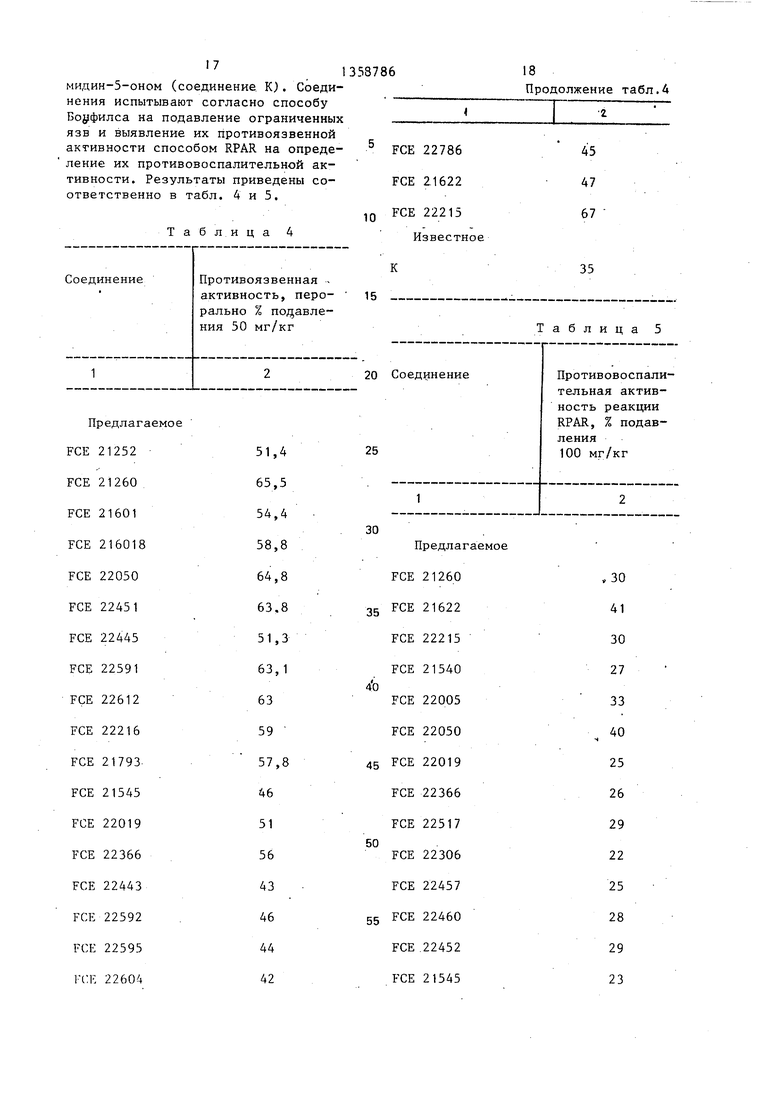
Для сравнительных целей предла- raeNfije соединения испытывают вместе с известным соединением - 2,3-дигид- ро-7-(3-пиридил)тиазолое(3,2-а)пири19Продолжение табл.5
FCE 21601
23
FCE 22451
Известное
20
Коды FCE, приведенные в табл. 4 и 5, относятся к следующим соединениям:
21252 - 7-транс-(2-(3-метоксифе- нил)-ВИНШ1 -5Н-тиазоло(3,2-а)пирими- дин-5-oHt
21601 - 7-транс- 2-(4-пиpидшI)- -виншI -5Н-тиазоло ( 3,2-.а) пиримидин- -5-он ,
21618 - 7-транс- 2-(6-метш1-2-пи- римидш1)-винил - 5Н-тиазоло(3,2-а)пи- 25 римидин -5-он;
22451 - 2,3-диметил-7-транс- 2- - (З-пиридил) -винил -5Н.-тиазоло- (3,2-; -а) пиримидин-5-он ,
22445 - 3-(З-пиридил)-7-транс- 2- -(З-пиридил)-винилЗ-5Н-тиазоло(3, 2- -а)пиримидин-5-oHi
22591 - 3-(4-метилфенил)-7-транс-{2-(З-пиридил)-винилЗ-5Н-тиазоло- (3,2-а)пиримидин-5-он,
2261.2 .- 2-метил-3-фенил-7-транс- 2- (З-пиридил) -винил -5Н-тиазоло- (3,.2-а) пиримидин-5-он J
22216 - 6-этокси-7-транс- 2-(3-22005 - 7-транс- 2-(4-пиридил)- 15 -винял -5Н-тиазоло(3,2-а)пиримидин-5-он,
22457 - 6-метил-7-транс- 2-(З-пи ридил )-циклопропил -5Н-тиазоло(3,2- -а)пиримидин-5-он
22460 - 6-хлоро-7-транс- 2(З-пири дил) -циклопропил -5Н-тиазоло(3, 2-а) пиримидин-5-он,
22452 - 7-транс- 2-(4-метилфенил -винил -5Н-тиазоло(3,2-а)пиримидин- -5-oHj
21545 - 7-транс- 2-(2-пиридил)- -этенил -5Н-тиазоло(3,2-а)пиримидин -5-OHV
22019 - 3-метил-7-транс- 2-(3-пи- ридил) -этенил -5Н-тиазоло (3 ,.2-а) пи- римидин-5-OHi
22366 - З-фенил-7-транс- 2-(З-пиридил)-этенил -5Н-тиазоло(3,2-а)пи- римидин-5-он;
22443 - З-трифторметил-7-транс- (3-пиридил)-этенил -5Н-тиазоло(3,2-а) пиримидин-5-он ,
22592 - 3-(4-фторфенил)-7-транс- - 2-(3-пиридш1 5-этенил -5Н-тиазоло30
-пиридил)-винил -5Н-тцазоло (3,2-а) (3,2-а)пиримидин-5-он , рИМИдин-5-он;22595 - 3-(4-хдорфенил)-7-транс22793 - 7-транс- 2-(З-пиридил)-- з-(3-пиридил)-зтенил -5Н-тиазоло-цикяопропил -5Н-тиазоло(3,2-а)пири- мидин-5-oHj
(3, 2-а)пиримидин-5-он ,
22604 - 3-(3-метоксифенил)-721260 - 7-транс- 2-(3-пиридил)-ви-45 -транс- 2-(З-пиридил)-этенил -5Ннил -5Н-тиазоло(3,2-а)пиримидин-5- -он,.
21622 - 6-метил-7-транс- 2-(3-пи- ридил)-винил -5Н-тиазоло(3,2-а)пири- мидин-5-рн,
222.15 - 6-метокси-7-транс - 2-(3- -пиридил)-винил -5Н-тиазЬло(3,2-а)- пирймидин-5-онJ
21540 - 6-хлор-7-транс-- 2-(З-пиридил) -винил -5Н-тиазоло(3,2-а)пи- римидин-5-он ,
22050 - 2-хлор-7-транс- 2-(3-пи- ридш1)-винил -5Н-тиазоло(3, 2-а)-пи- римидин-5-он,
-тиазоло(3,2-а)пиримидин-5-он
22786 - 3-(4-аминофенил)-7-транс- (З-пиридил)-этенил -5Н-тиазо- ло (3,2-а) пиримидин-5-он; 5021622 - 6-метил-7-транс- 2-(3-пиридил)-зтенил -5Н-тиазоло(3,2-а)пи- римидин-5-oHj
22215 - 6-метокси-7-транс- 2-(3- 55 -пиридил)-этенил -5Н-тиазоло(3,2-а)- в пиримидин-5-он;
2160-1 - 7-транс- 2-(4-пиридил)- -этенил -5Н-тиазоло(3,2-а)-пирими- - дин-5-oHJ
20
25
;
35878620
22019 - 3-нетил-7-транс- 2-(3-пиридил)-винил -5Н-тиазоло(3,2-a)- пиpимидин-5-oн;
22366 - З-фенил-7-транс- 2-(З-пиридил) -винил -5Н-тиазоло(3,2-а)пири- МИДИН-5-ОН}
225)7 - 2-хлор-6-метокси-7-транс- -2 (З-пиридил)-винил -5П-тиазоло- Q (3,2-а)пиримидин-5-он
22306 - 2-бром-7-транс- 2-(3-пи- ридил)-винил -5Н-тиазоло(3,2-а)пири- МИДИН-5-ОН;
22005 - 7-транс- 2-(4-пиридил)- 15 -винял -5Н-тиазоло(3,2-а)пиримидин-5-он,
22457 - 6-метил-7-транс- 2-(З-пиридил )-циклопропил -5Н-тиазоло(3,2- -а)пиримидин-5-он
22460 - 6-хлоро-7-транс- 2(З-пиридил) -циклопропил -5Н-тиазоло(3, 2-а)- пиримидин-5-он,
22452 - 7-транс- 2-(4-метилфенил)- -винил -5Н-тиазоло(3,2-а)пиримидин- -5-oHj
21545 - 7-транс- 2-(2-пиридил)- -этенил -5Н-тиазоло(3,2-а)пиримидин- -5-OHV
22019 - 3-метил-7-транс- 2-(3-пи- ридил) -этенил -5Н-тиазоло (3 ,.2-а) пи- римидин-5-OHi
22366 - З-фенил-7-транс- 2-(З-пиридил)-этенил -5Н-тиазоло(3,2-а)пи- римидин-5-он;
22443 - З-трифторметил-7-транс- (3-пиридил)-этенил -5Н-тиазоло(3,2-а) пиримидин-5-он ,
22592 - 3-(4-фторфенил)-7-транс- - 2-(3-пиридш1 5-этенил -5Н-тиазоло30
4о (3,2-а)пиримидин-5-он , 22595 - 3-(4-хдорфенил)-7-транс- з-(3-пиридил)-зтенил -5Н-тиазол
(3, 2-а)пиримидин-5-он ,
22604 - 3-(3-метоксифенил)-745 -транс- 2-(З-пиридил)-этенил -5Н-тиазоло(3,2-а)пиримидин-5-он
22786 - 3-(4-аминофенил)-7-транс- (З-пиридил)-этенил -5Н-тиазо- ло (3,2-а) пиримидин-5-он; 5021622 - 6-метил-7-транс- 2-(3-пиридил)-зтенил -5Н-тиазоло(3,2-а)пи- римидин-5-oHj
22215 - 6-метокси-7-транс- 2-(3- 55 -пиридил)-этенил -5Н-тиазоло(3,2-а)- в пиримидин-5-он;
2160-1 - 7-транс- 2-(4-пиридил)- -этенил -5Н-тиазоло(3,2-а)-пирими- - дин-5-oHJ
211358786
22451 - 2,3-диметил-7-транс- 2- -(3-пиридил)-этенил -5Н-тиазоло(3,2- -а)пиримидин 5-он,
Принимая во внимание высокие терапевтические показатели предлагаемых г соединений, их Можно без риска использовать в медицине. Так, например,, приблизительная величина остротоксиА - связь, обеспечивающая двойную связь между рс и ft углеродными ато- мами .или -СН -группа,, образующая цикщ и и с я формулы
тем, что соединение общей
О
15
Ri-TT- -V
ЛлЛр,
ческой дозировки (L5o) соединений
7-транс- 2-(3-пиридил)-этени -5Н-тиа- ю лопропановое кольцо, включающее л золо(3,2-а)пиримидин-5-он и 2-хлор- и / атомы углерода, о тличаю- -7-транс- 2-(3-пиридш1)-этени Г -5Н- -тиазолоСЗ,2-а)пиримидин-5-он, определенная в ходе проведения испытаний на мьшах при введении в виде одной порции в постоянно возрастающей дозировке с измерениями на седьмой день после введения в организм, составляла свыше 800 мг/кг (для введе- йия через рот) . Аналогичные токсико- 2( логические данные бьши получены и для других предлагаемых соединений.
Полученные результаты показывают, что соединения, полученные в условиях предлагаемого способа, малотоксичны, проявляют более высокую противоязвенную и противовоспалительную активность, чем известные соедине- : ния - 2,3-дигидро-7-СЗ-пиридил)-тиа- золо(3,2-а)пиридимин-5-он.
25
S -N
где R, - R-5 имеют указанные значения
Rj - сн,-,
X - хлор или бром,
вводят во взаимодействие с альдегидом формулы
R -СНО
30
где R имеет указанные значения, процесс ведут в органическом растворителе в присутствии алкоголята щелочного металла и полученные при этом соединения выделяют или вводят во взаимодействие с диметилсульфок- сонийметилидидом.
Фо.рмула изобретения
Приоритет по призСпособ получения замещенных тиазоло(3,2-а)пиримидинов общей формулы35
Г)15.07.81 при R - водород, (,1 -алкил, фенил; незамещенный или
Тх
.-i АЛг.я-снКг
S 15
CH-CH-RH
/
40
замещенный в положении 3 (, ).- -алкокси группой или в положении 4 галоидом или алксилом (С,-С,), R, - водород, галоид, (,)-алкил. .
де R, - водород, галоид, С,-С,-алкил;RJ, - водород, С,-Сз-алкил, трифторметил, 3-пиридил, фенил, 45 незамещенный или замещенньй в положении 3 (Cj-Сэ)-алкок- си или в положении 4 галоидом, амином или алкилом (C,-C3)i-50
R, - водород, галоид, С,-С -алкил,
(,)-алкокси R - незамещенный 2,3- или 4-пиВНИИПИ Заказ 6012/59
Тираж 372 Подписное
Произв.-полигр. пр-тие, г. Ужгород, ул. Проектная, 4
2.
ридил или 2-пиридил, замещенный в положении 6 (С,-С,)- -алкилом, или фенил, замещенный в положении 3 (C,-Cj)- -алкокси или в положении 4. (с,-С)-алкилом,
А - связь, обеспечивающая двойную связь между рс и ft углеродными ато- мами .или -СН -группа,, образующая циклопропановое кольцо, включающее л и / атомы углерода, о тличаю-
щ и и с я формулы
тем, что соединение общей
О
Ri-TT- -V
ЛлЛр,
лопропановое кольцо, включающее л и / атомы углерода, о тличаю-
S -N
лопропановое кольцо, включающее л и / атомы углерода, о тличаю-
где R, - R-5 имеют указанные значенияj
Rj - сн,-,
X - хлор или бром,
вводят во взаимодействие с альдегидом формулы
25
R -СНО
где R имеет указанные значения, процесс ведут в органическом растворителе в присутствии алкоголята щелочного металла и полученные при этом соединения выделяют или вводят во взаимодействие с диметилсульфок- сонийметилидидом.
Приоритет по приз
замещенный в положении 3 (, ).- -алкокси группой или в положении 4 галоидом или алксилом (С,-С,), R, - водород, галоид, (,)-алкил. .
20.01.82 при R - водород, ( С)-алкил-фенил,незамещенньй или замещенный вположении 4 галоидом или (С4-С,)-алкит1ом, R, - (С,-С,)-ал- кокси.
29.04.82 при .R - водород, ( -С.)-алкил, трифторметил, 3-пири- дил или фенил, незамещенньй или замещенный в положении 3 ()- -алкокси или в положении 4 галоидом или (С4-Сj)-алкилом.
Тираж 372 Подписное









Изобретение касается производ- . ных- полициклических азотсодержащих гетероциклических систем, в частности замещенных тиазоло-(3,2-а)пирими- динов (ТП) формулы t -GN-C(0)-C--R3 t -C-S-C N-С-СИ-CHRit-A где R, - Н, галоид, С,-Сз-алкил, RJ - Н, С,-С,-алкил, CF,, 3-пиридил, фенил, не- или замещенный в положении 3 С-1-С5-алкоксилом идив положении 4 галоидом, амином или С,-Сэ-ал- килом, Р-э - Н, галоид. С, кил. С,-Сэ-алкокси, R - 2,3- или 4-пири- дил, 2-пиридил, замещенный в положении 6 С,-С -алкилом, или фенил, 3- или 4-С,-С,-алкоксифенил; А - двойная связь между об - и i -углеродными атомами или СН -группа, образующая циклопропановое кольцо с включением Ы-- и (5 -атомов углерода, которые обладают биологической активностью и могут найти применение в медицине. Для выявления активности среди соединений указанного класса были получены новые ТП. Их синтез ведут из- альдегида формулы. R - СИ . О и производного тиазоло(3,2-а)пиримидина формулы . г-С-:N-aoVC-K Ri-C-S-C N -С-КБ где К,-R указаны выше; R - СН, -СН,2,Р -(CgH5),X, Х - хлор или бром, в среде органического растворителя в присутствии алкоголята щелочного металла с вьщелением ТП или обработкой диметилсульфоксонийметилиоди дом. Испытания показьшают, что ТП малотоксичны (, 800 мг/кг) и проявляют более высокую противояз- в енную и противовоспалительную активность, чем: известный 2,3-дигид- ро-7-(3-пиридш1)тиаз оло(3,2-а)пири- МИДИН-5-ОН. 5 табл. g (У) со О1 00 00 О5 см

| Серрей А | |||
| Справочник по органическим реакциям | |||
| - М.: Химия, 1962, с | |||
| Нефтяной конвертер | 1922 |
|
SU64A1 |
Авторы
Даты
1987-12-07—Публикация
1982-07-13—Подача