1
(21)4000047/04 (22)301г85 (46)30.12.93 Бюа№ 47-48
(71)Харьковский фармацевтический институт; Новосибирский медицинский инаитут
(72)Гайдукевич АН; Микитенко ЕЕ; Левитин ЕЯ; Яворовская В.Е; Евстропов АН. (54)БЕНЗИЛИДЕНГИДРАЗИДЬ 2-ХЛОР- 4-НИТРОБЕНЗОЙНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ АКТИВНОСТЬ В ОТНОШЕНИИ ВИРУСА ВЕЗИКУЛЯРНОГО СТОМАТИТА
(57) Изобретение касается гидразидов кислот, в чааноаи R-бензипиденгидразидов 2-хлор4-нитробензойной кислоты, где R-n или о-СН 0-.
3
или п - С И О- (ГБ). которые проявляют активность в отношении вируса везикулярного стоматита и могут быть использованы в медицине. Цель - создание новых активных и малотоксичных веществ указанного класса Синтез ГБ ведут из гидразида 2-хлор-4-нитробензойной кислоты и соответа- вующего алкоксибензальдегида в феде этанола фи кипении. Выход %: тлл.°С; брутто ф-ла: а)97.190 - 192; С Н GIN О ; б) 98. 193 - 195;
° Новые ГБ имеют низкую токсичность (максимапы о
переносимая доза от 125 до 250 мг/кг, против 100 мг/кг для рибамедила). Зтабл.
ИзоЗретение относится k новым хими- ески.1 соединениям формулы
С1
о
.R
)C-NHN GH-/6)
где R-n-СНзО, 0-СНзО или П-С2Н50, которые проявляют активность в отношении вируса везикулярного стоматита.
Цель изобретения - изыскание в ряду производных ароматических карбоновых ноеых соединений, обладающих ан- тивирусиыгл действием s отношении вируса везикулярного стоматита и имеющих меньшую токсичность.
П р и м е р 1. Пара-метоксибензилиден- гидразмд 2-хлор-4-нитробензойной кислоты. 3,0 г (0,0139 моль) гидразида 2-.хЯор-4-нитробензойной кислоты и 1,9 г (0,0139 моль) п.-метоксибензальдегида растворяют в 60 мл. этанола и нагревают на водяной бане при кипении в течение 15 мин. По охлаждении разбавляют реакционную србду водой. Выпадают желтые кристаллы. Кристаллизуют из этанола.
Выход 4.5 г (97%), Т.пл. 190-192 - С.
Найдено, %;:с 54,12; N 13.08; Н 3,66.
Ci5Hi2G(N30/
Вычислено, %: С 53,98; М 12,59; Н 3,62.
.bS (л /1лацетат - хлороформ 4; 1);
,S2 (пропаиол - хлороформ t:1).,
Хромзтографирование осуществлено на пластиме Si ufol-uv-254.
Структура полученного соединения подтверждена данными ИК-спектроа в таблетках калия бромида: у NH 3268, v о-снз 2885, 2935,2985, 1 со 1665, 1600, «5wH 1500, у М02 1350, V c-d 765(см ).
Спектр соединения снят на спектрофотометре Specord.
Пример. Орто-метоксибензилиден- гидразид 2-х/ Ор-4-нитробензойной кислоты. 2,5 г (0,0116 моль) гидразида 2-хлор-4-иитро6ензойной кислоты и 1,6 г (0,0116 моль) о метоксибензальдегида растворяют в 50 мл этанола и нагревают на водяной бане а течение 1 мин. По охлажде- ни5л раствор разбавляют водой и выпавшие кристаллы фильтруют. Кристаллизуют из .этанола. Выход 3.27 г (98%). Т.пл. 193- S
Найдено. %: С 53.78; N 12,46; Н 3,50.
Cl5Hi2CIN304.
Вычислено. %: С 53,98; N 12.59; .Н 3,62. ,49 (этилацетат -хлороформ ;1); .72 (пропанол - хлороформ 1;1).
Условия хроматографирования аналогичны приведенным в примере 1.
Структура полученного соединения
подтверждена данными ИК-спектров в таблетках калия бромида VNH 3195. оснз
2845, 2945, 3050, гс-о 1665, 1595.
5мн 1505, 1345. V с-а 745 (см 5.
П р и м е р 3. Пара-этоксибензилиден- гидразид 2-хлор-4-нитробензойной кисло- ты. 5,0 г (0,023 моль) гидразида 2-хлор-4-нитробензойной кислоты; 3,5 г (0,023 моль) п-этоксибензальдегида растворяют в 100 мл этанола и нагревают на водяной бане в течение 30 мин. По охлаждении разбавляют водой, образовавшиеся кристаллы кремового цвета фильтруют, сушат и перекристаллизовыаают из этанола. Выход 6,5г(81,3%);Т.пл. 189-19ГС.
Найдено, %: С 55,71; N12,01; Н4,01. Ci6Hi4CiN304
Вычислено, %; С55,26; N 12,08; Н 4,06.
Rf ,54 (этилацетат - хлороформ 4;1);
,84 (пропанол - хлороформ 1:1).
Хроматографирование осуществлялось на пластинах Si ufol-uv-254 Проявление хроматограмм проводилось УФ-облучени- ем,
Структура полученного соединения
подтверждена данными И.К-спектров в таблетках калия бромида VNH 3250. voc2H5
2845, 2935, 2965, 1665, VW 1600;
1350; (5ын 1500;г с-а 765(см 0.
Полученные соединения представляют собой кремово-желтые мелкокристалличе- ские вещества, растворимые а спирте, ацетоне, диоксане, ДМФА и не растворимые в воде.
Изучение физиологической активности осуществлялось следующим образом. Определение токсичности испытуемых химических соединений (ХС) проводили в культуре фибробластов эмбриона человека (ФЭЧ), для чего к питательной среде 199 добавляли различные количества ХС, начиная с 5000 мкг и менее на 1 мл среды. Наблюдение за культурой клеток вели на протяжении 4 сут с ежедневным просмотром. За максимальную переносимую дозу (МПД) испытуемого ХС принимали его наибольшее количество, которое не вызывало дегенерации клеток. Рабочая доза (РД) составляла 1 /2 МПД. .
Данные по определению МПД испытуемых соединений в культуре ФЭЧ приведены в табл.1.
Определение противовирусной активности к РНК-содержащим вирусам Коксаки А13 (Flores), Коксаки В4 (Power) ECHO 11 (Upsala). везикулярного стомэтитэ (Indiana) и ДНК-содержащему вирусу простого герпе
са 1 типа (штамм Л-2) проводили в культурах клеток ФЭЧ и Нер-2 в условиях одноцикло- вого опыта. При смене среды в культуре клеток к 0,8 мл среды 199 добавляли РД исследуемого ХС в обьеме 0,1 мл и 100 ТЦД50/о,1 мл соответствующего тест-вируса. Каждый опыт сопровождался контролем тест-вируса, взятого в той же дозе. Все пробирки с культурой клеток инкубировали прм 37°С в течение одного цикла репродукции каждого тест-вируса. Затем после промораживания при -10°С проводили титрование проб общепринятым методом. Снижение титра вируса под влиянием ХС на 2,0 Ig и более по сравнению с контролем оценивали как проявление активности испытуемого ХС. Исследование прот вогриппозной активности ХС проводили в развивающихся куриных эмбрионах с использованием вируса гриппа А (Виктория) 35/72 НЗ N2.
Противовирусная активность бензили- денгидразидов 2-хлор-4-нитробензойной кислоты приведена в табл.2.
Определение величины химиотерапев- тического индекса (ХТИ)(см. табл.3) по отношению к вирусу везикулярного стоматита проводили следующим методом.Тест-вирус в дозе 100 ТЦД50/о,1 мл вносился в культуру клеток и инкубировался 1 ч при 37°С. Непосредственно после адссфбции вирус Сливался, клетки отмывались средой 199 и в пробирки вносилась среда поддержки, содержащая различные концентрации исследуемого препарата. Наблюдение велось на протяжении 72 ч с ежедневным просмотром. Отсутствие цитопатического действия вируса в опыте при срабатывании его в контроле, позволяло считать препарат в указанной концентрации активным.
В культуре ФЭЧ соединения имели следующие МПД: п-метоксибензилиденгидра- зид 2-хлор-4-нитробензойной кислоты 250 мкг/мл. о-метоксибензилиденгидразид 2- хлор-4-нитробензойной кислоты 125 мкг/мл, п-этоксибензилиденгидразид 2- хлор-4-нитробензойной кислоты 125 мкг/мл.
Из данных, приведенных в табл.2, следует, что все 3 соединения снижали уровень
репродукци 1 вируса только везикулйриого стоматита на 3,5 ig; 5,5 Ig; 3,0 Ig соответственно. Для всех трех соединений ХТИ-2,
Аналог предлагаемых соединений по структуре Кутиэон, являющийся производным гидразина, в 4-5 раз более токсичен (LD50 54 мг/кг), чем п-метоксибензилиден- гидразид 2-хлор-4-нитробензойной кислоты (LDso 250 мг/кг) и о-метокси- или п-этоксибензилиденгидразиды 2-хлор-4-нитробен- зойной кислоты (LDso для обоих 200 мг/кг). Токсические дозы установлены на беспородных белых мышах массой 16-18 г. Кроме того, кутизон и проявляет активность
против вируса гриппа, он не активен по отношению к вирусу везикулярного стоматита.
Другой противовирусный препарат широкого спектра действия - рибамидил - имеет МПД 100 мкг/мл. Преимуществом
предлагаемых соединений является их
меньшая токсичность (МПД от 125 до 250
мкг/мл). К тому же рибамидил, как и кутизон, не оказывает влияния на репродукцию
вируса везикулярного стоматита.
Как следует из полученных данных (см. табл. 1-3), лредлагаемые соединения менее токсичны, чем известный противовирусный препарат рибамид-ил. В отличие от последнего они обла.г-.ают выраженной активностью () против вируса везикулярного стоматита;(сбмейство рабдовирусов). Подобная активность обнаружена впервые. Учи- тывая отсутствие химиопрепаратов,
эффективных в отношении рабдовирусов
(куда входит, в частности, вирус бешенства),
данные еоединения могут применяться в
экспериментальной терапии рабдовирусных инфекций, а также быть модельными
для направленного синтеза более активных соединений.
(56) Колла В.З. и Бердинский М.С. Фармакология и химия производных гидразина. Йошкар-Ола. 1976, с.169-170.
Линицкая Г.Л. и др. Вопросы вирусологии, 1983, № 6. с.673-675,
3 б л и ц а 1


п-Метоксибензилиденгидразид 2-хлор4-нитробемзойной
1 /|СЛОТЫ
+ + + -f + +
4-1 дегенерация 100 % клеток, 4-4-4- дегенерация 75 % клеток, + + дегенерация 50 % клеток, + дегенерация 26 % клеток. - отсутствие дегенерации.
Примечай и е. Вещество считается проявляющим активность при снижении уровня репродукции вируса на 2,0 ig и более.
п-Этоксибензилиденгидразид 2-хлор- 1нитробензойной
кислоты
4- + + 4+ + + +
4- 4Таблица 2
Н.и, - не исследовали.
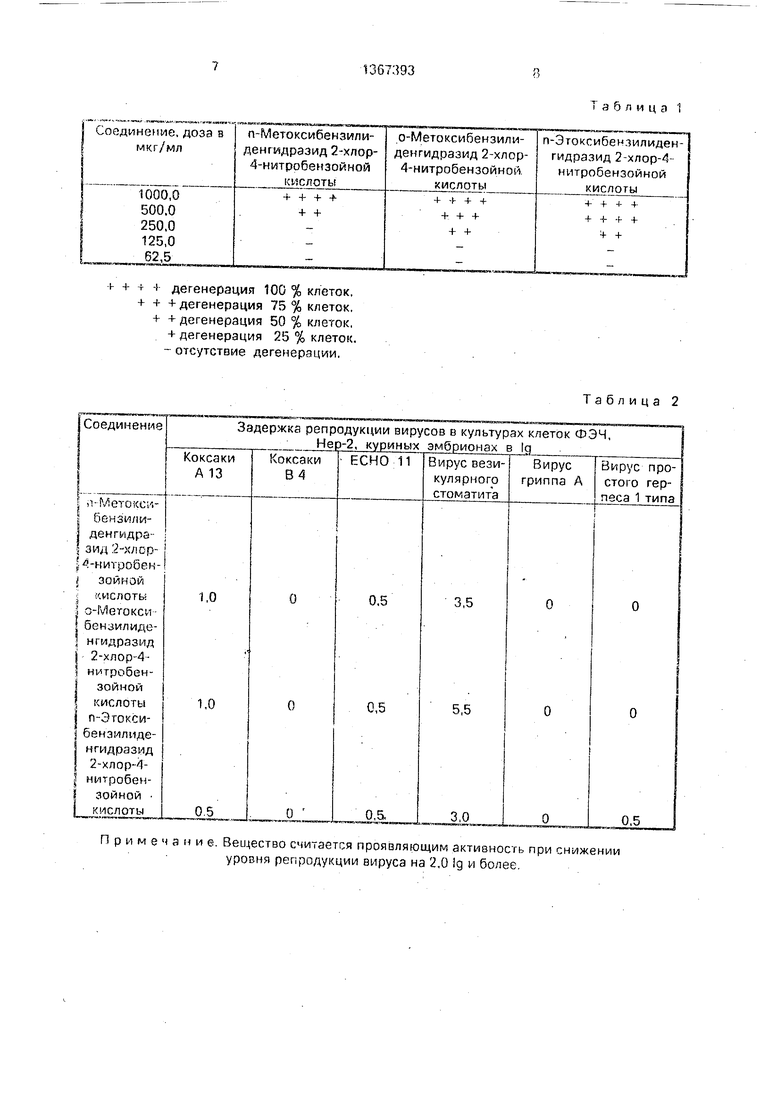
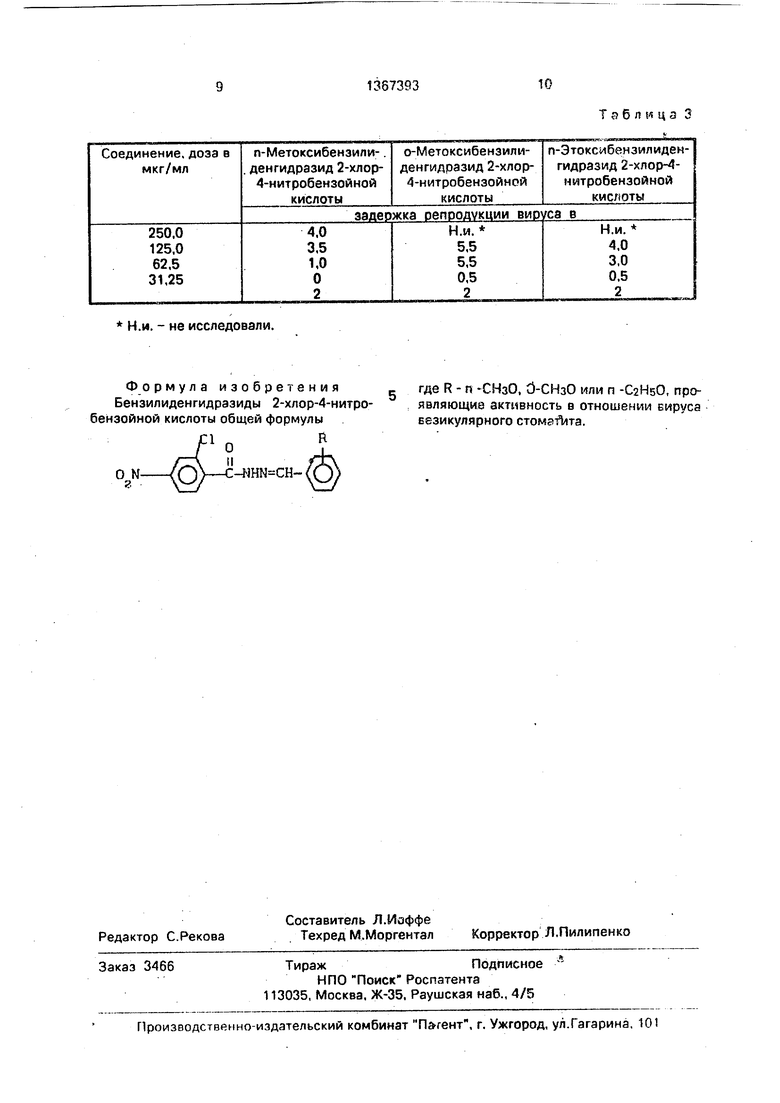
Ф о рмула изобретения Бензилиденгидразиды 2-хлор-4-нитро- бензойной кислоты общей формулы
C-4JHN CH-
Таблица 3
где R - п СНзО, d-СНзО или п -CaHsO. проявляющие активность в отношении вируса везикулярного стоматита.
Авторы
Даты
1993-12-30—Публикация
1985-12-30—Подача