Иэстбретение относится к способу получения новых биологически активных соединений - пептидов иди их содей, обладающих способностью стимулировать рост животных, которые могу найти применение в ветеринарии.
Цель изобретения - новые пептиды, обладающие низкой токсичностью и более высокой способностью стимудиро- вать pt)CT животных.
Значения Rf определяют на пласти нах, предварительно покрытых слоем силикагеля 60 Р у/Мерк) , толщиной
0,25 мм, длиной 20 см с исподьзова-
нием следующих проявляющих систем:
Система А. Бензол:бензин (60:80) (этилацетат 70:10:40 по объему;
Система В. Бензол:триацетат:уксусная кислота:вода 100:100:20:10 по объему (верхняя фаза);
Система С. Бензол:этилацетат:уксусная кислота:вода 100:100:40:15 по объему (верхняя фаза);
Система D. н-Бутанол:уксусная кис лота:вода 4:1:1 по объему;
Система Е. Метиленхлорид:метило- вый с лтирт 98:2 по объему;
Система F. Meтиденхлорид:метиловый спирт 95:5 по объему (Е.Мерк является торговым названием).
Анализ с помощью тонкослойной хроматографии проводится при температуре и интервале от 18 до 25 С; поэтому значения R изменяются на ±5%. Температуры плавления определяют в открытьк капиллярах с помощью аппарата системы Тоттоли и они не были откорректированы. Большинство производных размягчаются и разлагаются до до тижсния температуры плавления. Высоковольтный электрофорез на бумаге проводят в аппарате системы ферогра- фориджинал-Франкфурт типа 64 на бумаге фирмы Ылейхер и Шюл № 2317 при показателе рН 1,2 (муравьиная кисло- та:уксусная кислота:вода 123:100: 777) и напряжения 1600 в (40 В/см) и при показателе рН 5,8 (пиридин:уксусная кислота:вода 450:50:4500) и напряжении 1400 В (32,5 В/см). Эти продукт характеризуются подвижность относительно Glu при показателе рН 1, (Е , 2) ч при показателе рН 5, & (Е ) .
В изобретении используют символы и сокращения, обычно применяемые в химии пептидов. Другими используемыми симнолами и сокращениями являются AcOEt - этилапстат; - диметил
0
5
0
5
О
0
5
формамид; EtjO - простой диэтиловый эфир; МеОН - метиловый спирт; NMM-N- метилморфолин; РЕ - петролейный эфир; Phe(Cl) - пара-хлор-Ъ-фенилаланни; Pip-L - пипеколиновая кислота; iPrjO - простой диизопропиловый эфир; iРгОН- изопропиловый спирт; THF - тетрагидро- фуран.
Пример 1. Получение НС1 и H-Leu-Gly-Trp-OMe (IV).
Стадия I. Boc-Leu-Gly-Obrl (I).
К раствору 4,63 г (20 ммоль) Вос- Leu-OH в 60 мл безводного татрагид- рофурана последовательно добавляют 2,2 мл (20 ммоль) N-метилморфолина и 1,98 мл (20 ммоль) этилхлорформата при -12 С.
После перемешивания при этой температуре в течение 2 мин добавляют холодный раствор (-30°С) 6,75 г
(20 ммоль) тозилата H-Gly-OBrl и 2,2 мл N-метилморфолина (20 ммоль) в 60 мл диметилформамида.
Реакционную смесь перемеишвают в течение 45 мин при -12 С и в течение 90 мин при , затем отфильтровывают от солей и упаривают в условиях вакуума. Остаток растворяют в этилаце- тате и несколько раз промывают насыщенными растворами хлористого натрия, содержащими 1М раствор лимонной к;ис- лоты, 1М раствором бикарбоната натрия и воду. Органический слой высушивают над безводным сульфатом натрия и растворитель удаляют в условиях вакуума.
Было получено 6,81 г (выход 90%) соединения (I) в виде масла. ,59.
Стадия 2. Boc-Leu-Gly-OK (II).
6,6 г (17,44 ммоль) Boc-Leu-Gly- -OBrl (I), растворенного в 50 мл метанола, гидрируют при комнатной температуре и атмосферном давлении в присутствии 1,65 г 10%-ного паллади- рованного угля. Катализатор удаляют фильтрованием и раствор концентрируют в условиях вакуума.
4,17 г (выход 83%) соединения (II) получают из смеси этилацетата и пет- ролейного эфира, температура плавления 115-121°С, / 29,0° (с 1, МеОН); Rtg 0,50; Е 5,8 0,75.
Стадия 3. Boc-Leu-Gly-Trp-OMe (III).
Используя в качестве исходных материалов 3,95 г (13,70 ммоль) Вос- Leu-Gly-OH (И) и 3,49 г (13,70 ммоль)
HCl-Н-Тгр-ОМе и действуя так, как описано в стадии 1, получают г (выход 90%) частично очищенного соединения (III) в виде пены, используя для его получения простой диэтиловый эфир (Rf 0, Rfj 0,69), после . чего это соединение применяют в следующей стадии.
Стадия 4. HCl-H-Leu-Gly-Trp-OMe Q (IV).
5,75 г (11,77 ммоль) Boc-Leu-Gly- Тгр-ОМе (III) растворяют в 60 мл насыщенного раствора хлористого водорода в ледяной уксусной кислоте, после чего в этот раствор добавляют 6 мл анизола и 3 мл 2-меркаптоэтанола. Через 30 мин нахождения этого раствора при комнатной температуре завершается удаление элемента Вое, а раство-2п ритель удаляют в условиях вакуума при ЗО С.. Сырой продукт очищают с помощью хроматографии на колонках из силика- геля (Мерк) 0,040-0,063 мм, используя в качестве .элюента смесь этилацетата 5 и метанола 9:1.
Из смесь этилацетата и простого диэтилового эфира было получено 3,05 г (выход 61%) соединения. (IV): температура плавления 180-185 С (пена); , t:l +16,9 (с 1, МеОН); Rf , 0,67; Е 1 0,80.
Пример 2. Получение НС1 « H-Ahx-Gly-Trp-OMe (VIII). Стадия 1. Boc-Ahx-Gly-OBrl (V).
Используя в качестве исходных ма- ериалов 4,63 г (20 ммоль) Boc-Ahx-OH . 6,75 г (20 ммоль) тозилата H-Gly- OBrl и действуя так, как описано в примере 1 (стадия 1), из смеси этил- ацетата и петролейного эфира получают 6,66 г (выход 88%) соединения (V); емпература плавления 84-86°С; (/1 -22,0° (с 1, МеОН); Rf 0,58.
Стадия 2. Boc-Ahx-Gly-OH (VI).
Используя в качестве исходного ма- териала 6,35 г (16,78 ммоль) Boc-Ahx- Gly-OBrl (VI )и действуя так, как описано в примере 1 (стадия 2), поучают 4,31 г (выход 89%) соединения (VI) в виде масла: Rp 0,54; Е у 50 0,74. .
Стадия 3. Boc-Ahx-Gly-Trp-OMe (VIII).
Используя в качестве исходных материалов 4,12 г (14,28 ммоль) Boc-Ahx55 -Gly-OH (VI) и 3,64 г (14,28 ммоль) НС1 Н-Тгр-ОМе и действуя так, как описано в примере 1 (стадия 1), получают
40
п
0
5,93 г (выход 85%) соединения (VII) в виде масла: R f. 0,81.
Стадия 4. НС1H-Ahx-Glу-Тгр-ОМе (VIII).
Используя в качестве исходного материала 5,60 г (11,46 ммоль) Boc-Ahx- -Gly-Trp-OMe (VII) и действуя так, как описано в примере 1 (стадия 4), но применяя на стадии очистки метилен- хлорид, содержащий возрастающее количество метилового спирта .(до 5%), в качестве элюента, из смеси этилацетата (простого диэтилового эфира получают 3,61 г (65% выход) соединения (VIII): температура плавления 114- 117 С (пена); J1 % +25,8 (с 1, МеОН); Rf JJ 0,64; Е ,, 0,79.
Пример 3. Получение НС1 (H-Ahx-Gly-Trp-Mec-OMe (X).
Стадия 1. Boc-Ahx-Gly-Trp-Met-OMe (X).
Используя в качестве исходных материалов 1,66 г (5,41 ммоль) Boc-Ahx- -Gly-OH (VI, пример 2) и 2,09 г (5,41 ммоль) HCl-H-Trp-Met-OMe и действуя так, как описано в примере 1 (стадия 1), но применяя метиленхлорид на стадии очистки, из смеси этилацетата и простого диэтилового эфира получают 2,85 г (выход 87%), соединения (IX); Rf g 0,74.
Стадия 2. HCl-H-Ahx-Gly-Trp-Met- -ОМе (X).
Используя в качестве исходного материала 2,60 г (4,19 ммоль) соединения (IX) и действуя так, как описано в примере 1 (стадия 4), но применяя на стадии очистки в качестве элюента этилацетат, содержащий возрастающее количество метилового спирта (от 10 до 15%), из смеси изопропилового спирта и простого диэтилового эфира получают 1,40 г (выход 60%) соединения (X), температура плавления bb-l(fc (пена), о/7 д 5,9 (с 1, МеОН), Rfj, 0,70; Е 5 0,60.
Пример 4. Получение НС1 H-Ahx-Gly-Trp-Phe-OMa (XIV).
Стадия 1. Boc-Trp-Phe-OMe (XI).
Используя в качестве исходных материалов 6,09 г (20 ммоль) Вос-Тгр-ОН и 4,31 г (20 ммоль) HCl-H-Phe-OMe и действуя так, как описано в примере 1 (стадия 1), из смеси этилацетата и простого диизопропилового эфира получают 7,73 (выход 83%) соединения (XI) температура плавления 117-120 С;
513
Jj / 20,2° (с 1, feOH); R 0,79; Rf , 0,56.
Стадия 2, HCl H-Trp-Phe-OMe (XII)
Используя в качестве исходного ма- териала 7,47 г (16,05 ммоль) соединения (XI) и действуя так, как описано в примере 1 (стадия 2), из смеси этилацетата и простого диэтилового эфира получают 5,55 г (выход 86%) соединения (XII): R. 0,75; Е 0,83.
Ctaдия 3. Boc-Ahx-Gly-Trp-Phe-OMe (XIII).
Используя в качестве исходных материалов 1,83 г (6,35 ммоль) Boc-Ahx- -Gly-OH (VI) и 2,55 г (6,35 ммоль) НС1-H-TRp-Phe-OMe (XII) и действуя так, как описано в примере 3 (стадия О, получают 3,19 г (выход 79%) соединения (XIII) в виде масла: R г 0,76.
Стадия А. НС1-H-Ahx-Gly-Trp-Phe- -ОМе (XIV).
Используя в качестве исходного ма- териала 2,85 г (4,48 ммоль) Boc-Ahx- Gly-Trp-Phe-OMe (XIII) и действуя так, как описано в примере 1 (стадия 4), но очищая сырое маслянистое де- бл окированное соединение (XIV) путем нескольких промывок простым диэтило- вым эфиром, в конечном счете из смеси изопропилового спирта и простого диэтилового эфира выделяют соединение (XIV) (1,54 г, выход 60%). Rn 0,75 Е,, 0,68.
Пример 5. Получение НС1 li-Leu-GI-y-Trp-Phe-OMe (XVI).
Стадия 1. Boc-Leu-Gly-Trp-Phe-OMe (XV).
Используя в качестве исходных материалов 1,75 г (6,10 ммоль) Boc-Leu- -Gly-OH (II) и 2,45 г (6,10 ммоль) НС1-H-Trp-Phe-OMe (XII) и действуя так, как описано в примере 3 (стадия 1) получают 3,10 г (выход 80%) соединения (XV) в виде масла: Rn 0,73
Стадия 2. НС1-H-Leu-Gly-Trp -Phe- -ОМе (XVI).
Используя в качестве исходного материала 2,75 г (4,30 ммоль) Boc-Leu- -Gly-Trp-Phe-OMe (XV) и действуя так как описано в примере 1 (с тадия 7), из смеси изопропилового спирта и простого диэтилового эфира получают 2,09 г (выход 85%) соединения (XVI): температура плавления 103-108°С (пена); , 9,4 (с 1, МеОН); Rj 0,73; Е ,, 0,67.
0
5
0
06
с
5 g 5
5
iO
5
156
Пример 6. Boc-Trp-Leu-NHJ.
Действуя так, как описано в предыдущих примерах, получают указанный в заголовке пептид с 80%-ным выходом.
R 0,79, температура плавления 158°С (изопропиловый спирт - простой диизопропиловый эфир) , в -18,4° (с 1, МеОН).
Пример 7. HCI H-Trp-Leu-NHj,.
Используя в качестве исходного материала Boc-Trp-Leu-NHj,полученный в предыдущем примере, и действуя так, как описано в примере 1 (стадия 4), получают указанное в заголовке соединение с 94%-ным выходом, температура плавления 135°С (этилацетат и простой диизопропиловый эфир), of д +9,6° (с 1, МеОН), RJ 0,76; ,84.
Пример 8. НС1-H-Trp-Val-OMe.
Стадия 1. Boc-Trp-Val-OMe.
К раствору 12,17 г (40 ммоль) Вос-Тгр-ОН в 100 мл безводного тетра- гидрофурана последовательно добавляют 4,5 мл (40 ммоль) N-метилморфолина и 3,96 г (40 ммоль) зтилхлорформиата при температуре -12°С. После перемешивания в течение 2 мин к реакционной смеси добавляют холодный раствор 6,70 г (40 ммоль) HCl-H-Val-OMe и 4,5 мл N-метилморфолина (40 ммоль) в 50 мл диметилформамида. Реакционную смесь перемешивают в течение 1 ч при -12°С и 2 ч при температуре 0-15°С, отфильтро ываиот соли и выпаривают в условиях вакуума. Остаток растворяют в этилацетате и последовательно несколько раз. промывают насыщенными растворами хлористого натрия, содержащими 1 М раствор лимонной кислоты, 1 М раствор бикарбоната натрия и воду. Органический слой высушивают над безводным сульфатом натрия, а растворитель удаляют в условиях вакуума.Из смеси изопропилового спирта и простого диизопропилового эфира получают 12,1 г (выход 84,4%) указанного в заголовке соединения. К. 0,81; Rj 0,87.
Стадия 2. НС1-H-Trp-Val-OMe.
12,52 г (30 ммоль) Boc-Trp-Val-OMe растворяют в 15 мл муравьиной кислоты при комнатной температуре.
После завершения удаления элемента Бос (контролируемого с помощью тонкослойной хроматографии) растворитель упаривают в условиях вакуума при 30 С. Остаток растворяют в метаноле, охлажденном до О С, после чего к этому ра713
створу добавляют 11 мл (33 ммоль) ЗМ раствора хлористого водорода в безводном тетрагидрофуране. Растворител удаляют в условиях вакуума, в результате чего из смеси изопропилового спирта и простого диизопропилового эфира получают 9,55 г (выход 90%) указанного в заголовке соединения, Rf 0,69; Е о 0,98 Glu.
Пример 9.НС1.Н-Рго-Тгр- Met-NHo.
Стадия 1. Boc-Pro-Trp-Met-NH.
Используя в качестве исходных материалов 1,722 г (8 ммоль) Вос-Рго О и 2,967 г (8 ммоль) HCl-H-Trp-Met-NHj и действуя так, как описано в стадии 1 примера 8, из изопропилового спир- ,та получают 3,828 г (выход 90%) указанного в заголовке соединения: ) -70,2 (с 1, МеОН); R 0,38; R{ 0,73.
стадия 2. НС1- K-Pro-Trp-Met-NH,.
3,722 г (7 ммоль) Boc-Pro-Trp-Met -NHjрастворяют в 40 мл муравьиной кислоты при комнатной температуре. После завершения удаления элемента Вое (контролируемого с помощью тонкослойной хроматографии) растворитель упаривают в условиях вакууме при . Остаток растворяют в метаноле, охлажденном до 0°С, после чего к этому раствору добавляют 3,6 мл (10,8 ммоль) ЗМ раствор хлористого водорода в безводном тетрагвдрофура- не. Растворители удаляют в условиях вакуума, в результате чего из абсолютного этилового спирта получают 2.621 г (выход 80%) указанного в заголовке соединения; 0 -23,0° (с
1, МеОН); Rp 0,4l;ETj 0,76. Пример Ю. H-Leu-Gly-Trp
-Met-NH,-HCl.
Действуя так, как описано в предыдущих примерах, получают указанное в заголовке соединение с 79%-ным выходом: температура плавления 180- (изопропиловый спирт - простой
ДИИЗОПРОПИЛОВЬЙ эфир , Се/7)- +1,0°(с 1, МеОН), R 0,63; Е 0,66 Glu.
Проведены биологические испытания пептидов, полученных в условиях предлагаемого способа.
Испытание на синтез белка в живом организме и в лабораторных условиях проводится в течение 7 дней с использованием группы из шести самцов крыс (Вистар, Хагеман, Экстерталь), раз8
0
5
0
5
0
5
деленных на подгруппы по три животных, которые содержатся в клетках из макролона, где в качестве подстилки применяется древесная стружка.
Воду и пищу (стандартный рацион Альтромин 1321, содержащий 19% сырого белка) дают животным по потребности.
Пептиды вводят подкожно в виде раствора, ежедневные дозы Которого составляют от 0,1 до 100 нг/кг.
Измерение препарата производится в жидкостном сцинтштляиионном счетчике PL (1,0 мл 5 мл сцинтилляцион- ной жидкости) ПРИАС.
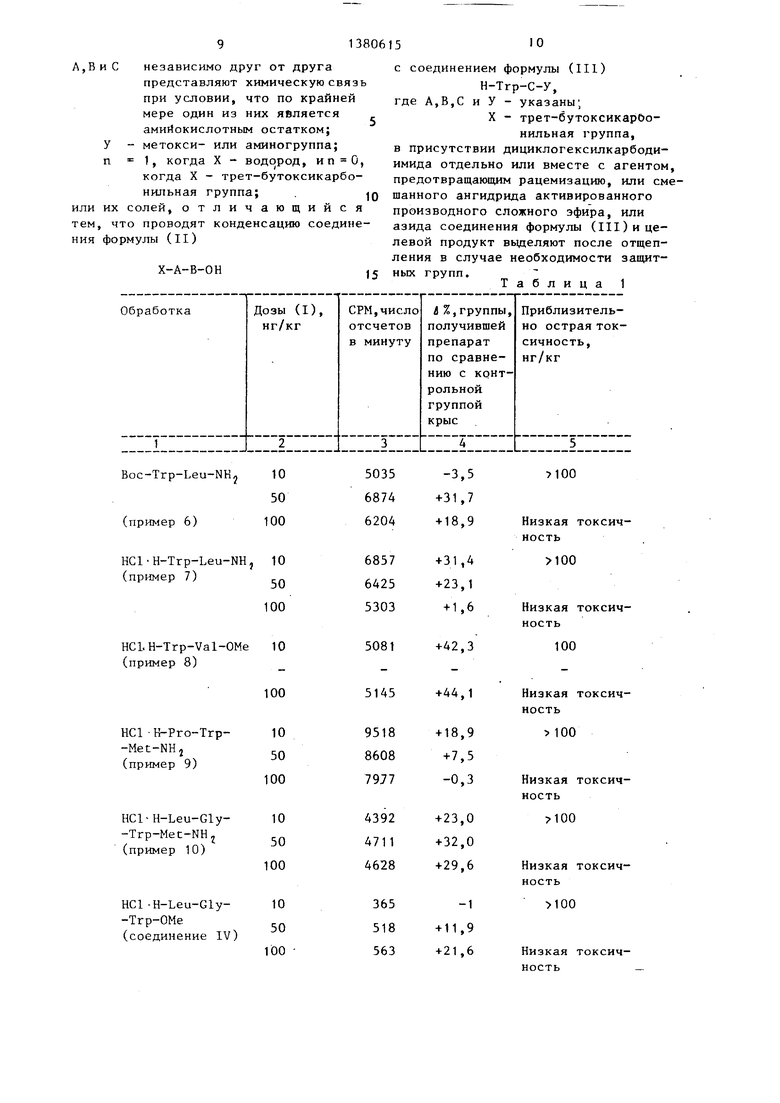
Б табл. 1 приведены результаты измерений скорости синтеза протеинов тканью печени самцов крысы после обработки в течение 7 дней (ежедневные подкожные инъекции).
Измерение скорости синтеза белка соединений, перечисленных в табл. 1, существенно отличается от результатов, полученных в контрольной группе, состоящей из крыс, которь м ежедневно вводили физиологический раствор хлористого натрия ввиде подкожных инъекций.
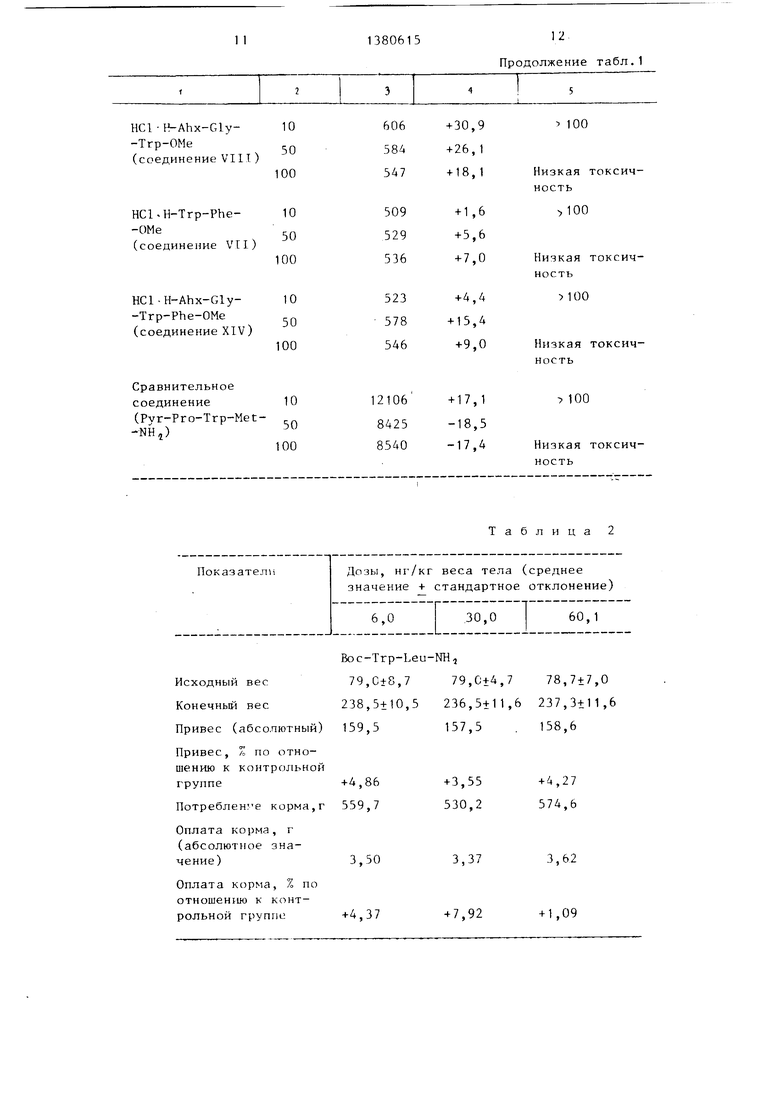
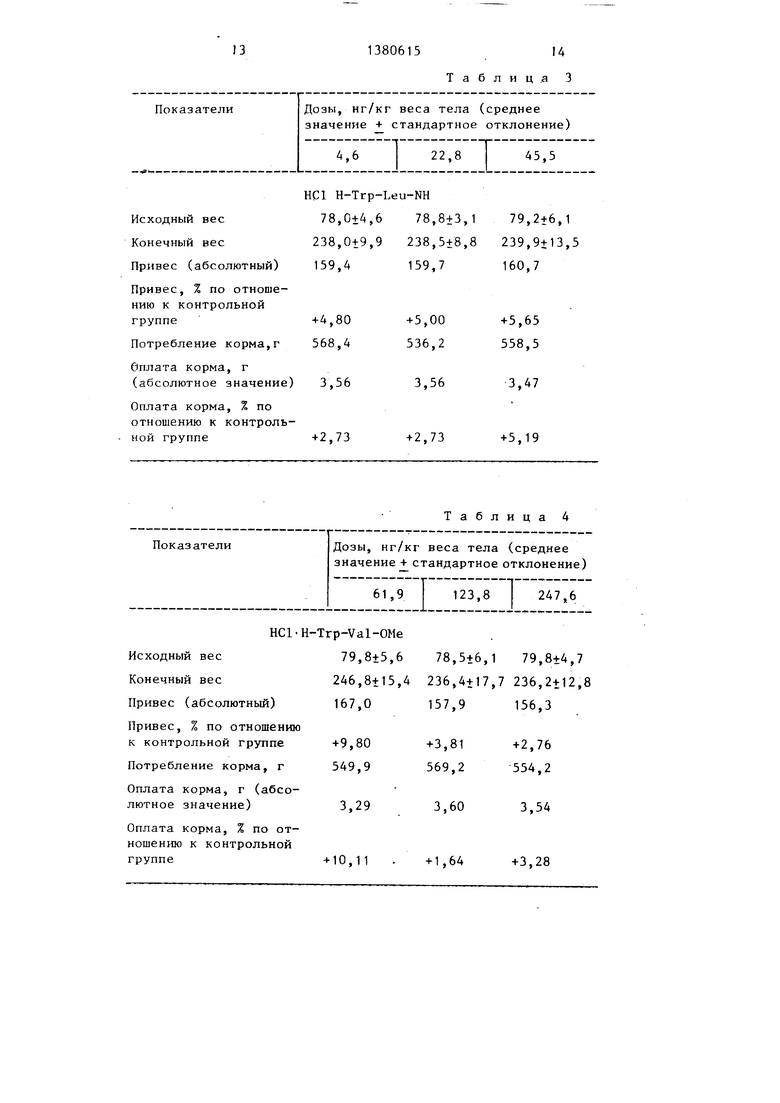
При определении стимулирующей рост активности в живом организме крысам с исходным весом, примерно равным 79 г, препарат вводят через рот во время кормления (стандартный рацион Альтромин 1320) в дозах, составляющих от. 4 до 250 мг/кг веса тела. Еженедельно регистрируют привес и потребление корма. Результаты показаны в табл. 2 (дозы превращенных в соль пептидов относятся к свободным основаниям) .
Проведенные испытания показали, что пептиды, полученные в условиях предлагаемого способа, малотоксичны и значительно увеличивают скорость синтеза протеинов тканью печени.
Формула изобретения
Способ получения пептидов формулы (I)
X-A-B-trp-C-y - HCllp,
где X - водород или трет-бутоксикарбонильная группа; А - Leu или Ahx; В - Pro или Gly; С - Val, Leu, Met или Phe, или
независимо друг от друга
представляют химическую связь при условии, что по крайней мере один из них является амийокислотным остатком; метокси- или аминогруппа; 1, когда X - водород, , когда X - трет-бутоксикарбо- нильная группа; , Q
солей, отличающийся о проводят конденсацию соедине
НИН формулы (II)
Х-А-В-ОН
Q
5
с соединением формулы (III)
Н-Тгр-С-У, где А,В,С и У - указаны;
X - трет-бутоксикарОонильная группа,
в присутствии дициклогексилкарбоди- имида отдельно или вместе с агентом, предотвращающим рацемизацию, или смешанного ангидрида активированного производного сложного эфира, или азида соединения формулы (III)и целевой продукт выделяют после отщепления в случае необходимости защитных групп.
Таблица 1




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных хлоргидрата гептапептида | 1984 |
|
SU1342424A3 |
| Способ получения пептидов | 1980 |
|
SU1316565A3 |
| Способ получения антрациклиновых гликозидов | 1986 |
|
SU1553015A3 |
| Способ получения пептидов | 1976 |
|
SU639446A3 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИПСИХОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2411248C2 |
| ПЕПТИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2067000C1 |
| Способ получения производных дигидробензопирана или дигидробензотиопирана или их фармацевтически приемлемых солей | 1983 |
|
SU1321375A3 |
| СПОСОБ ПОЛУЧЕНИЯ БИЦИКЛИЧЕСКИХ ПЕПТИДНЫХ СОЕДИНЕНИЙ | 2003 |
|
RU2330045C9 |
| Способ ферментативного получения пептидов | 1980 |
|
SU1378785A3 |
| ПРОИЗВОДНЫЕ НОНАПЕПТИДОВ ИЛИ ИХ СОЛЕЙ С ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫМИ КИСЛОТАМИ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2115659C1 |
Изобретение относится к пептидам в частности к получению пептидов формулы (I): Х-А-В-Тгр-С-У- НС1 , где X - водород или трет-бутоксикарбо- нильная группа, A-Leu или Ahx, В-РгО или Gly, C-Val, Leu, Met или Phe, или A, В и С независимо друг от друга представляют химическую связь при условии, что по крайней мере один из них является аминокислотным остатком, У - метокси или аминогруппа, п равно 1, когда X - водород, и п равно О, когда X трет-бутоксикарбонкпьная группа, или их солей, обладающих способностью стимулировать рост животных, и могут найти применение в ветеринарии. Цель - получение новых более активных веществ указанного класса.Получение соединений (I) ведут конденсацией соединения формулы (II): Х-А- В-ОН с соединением формулы (III) Н-Тгр-С-У, где А, В, С и У - указаны вьш1е, X -трет-бутоксикарбонильная группа, в присутствии дициклогексил- карбодиимида отдельно или вместе с агентом, предотвращающим рацемизацию, или смешанного ангидрида, активированного производного сложного эфира, или азида соединения формулы (III), Целевой продукт выделяют после отщепления в случае необходимости защитных групп. Испытания показывают, что соединения (I) малотоксичны и значительно увеличивают скорость синтеза протеинов тканью печени. 6 табл. СО со 00 о о ел
Boc-Trp-Leu-NKj 10
50 (пример 6) 100
HCl-H-Trp-Leu-NH, 10 (пример 7) Q
HCl.H-Trp-Val(пример 8)
НС1-К-Рго-Тгр- -Met-NHj (пример 9)
HCl-H-Leu-Gly- -Trp-Met-NHj (пример 10)
НС1-H-Leu-Gly- -Trp-ОМе (соединение IV
-3,5 +31,7 -t-18,9
+ 31,4
+23,1
+ 1,6
+42,3
+44,1
+ 18,9 + 7,5 -0,3
+ 23,0 + 32,0 +29,6
-1
+ 11,9 + 21,6
100
Низкая токсичность
100
Низкая токсичность
100
Низкая токсичность
100
Низкая токсичность
100
Низкая токсичность
100
Низкая токсичность
11
159,5
+4,86
559,7
3,50
+4,37
Boc-Trp-Leu-NH,,
79,0+8,7 79,0+4,7 238,5+10,5
236,5+11,
157,5
+ 3,55 530,2
3,37 + 7,92
1380615
12 Продолжение табл.1
Таблица 2
79,0+4,7
78,7+7,0 236,5+11,6 237,3±11,6
158,6
+ 4,27 574,6
3,62 + 1,09
HCl H-Trp-Leu-NH
78,0+4,6 78,8+3,1
238,0+9,9 238,5+8,8
159,4 159,7
+4,80 +5,00
568,4 536,2
3,56 3,56
+2,73 +2,73
НС1 Н
Исходный вес Конечный вес Привес (абсолютный)
Привес, % по отношению к контрольной группе
Потребление корма, г
Оплата корма, г (абсолютное значение)
Оплата корма, % по отношению к контрольной группе
-Trp-Val-OMe
79,8+5,6 78,5+6,179,8+4,7
246,8+15,4236,4+17,7236,2+12,8
167,0157,9156,3
+9,80 549,9
3,29 +10,11
+3,81 569,2
3,60 + 1,64
+2,76 554,2
3,54 +3,28
Таблиц.a 3
79,2+6,1 239,9+13,5 160,7
+5,65 558,5
3,47 +5,19
Таблица 4
+2,76 554,2
3,54 +3,28
151380615
Таблнца5
Показатели
НСЬ. Leu-Gly-Trp-Met-NH,
Исходный вес79,9+4,478,0+3,879,4+5,5
Конечный вес243,8+21,1 255,7+6,5227,5+11,5
Привес (абсолютный)163,9177,7148,1
Привес, % по отношен1Ж1
к контрольной группе +7,76 +16,83 -2,63
Потребление корма, г 564,8 563,4 564,2
Оплата корма, г (абсолютное значение) 3,45 3,17 3,69
Оплата корма, % по отношению к контрольной группе+5,74 +13,39 -0,28
V
Таблица 6
Показатели
Исходный вес 78,0+5,5 Конечный вес 230,0+14,3 Привес (абсолютный) 152,1 Потребление корма,г 556,9
Оплата корма, г (абсолютное значение) 3,66
Дозы,нг/кг веса тела (среднее значение + стандартное отклонение)
31,6 63,3 126,6
Контрольная группа (среднее иначе ние + стандартное отклонение)
| Шредер Э., Любке К | |||
| Пептиды | |||
| М.: Мир, 1967, Ч.1, с | |||
| Способ получения бензидиновых оснований | 1921 |
|
SU116A1 |
| УСТРОЙСТВО ДЛЯ ИЗМЕРЕНИЯ РАСХОДА ЖИДКИХ СРЕД | 1997 |
|
RU2130590C1 |
| Колосниковая решетка с чередующимися неподвижными и движущимися возвратно-поступательно колосниками | 1917 |
|
SU1984A1 |
Авторы
Даты
1988-03-07—Публикация
1985-11-26—Подача