(Л
с

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения жирных карбоновых кислот @ - @ | 1981 |
|
SU1019299A1 |
| Способ определения цинка | 1981 |
|
SU960124A1 |
| Титрант для осадительного потенциометрического титрования анионов | 1983 |
|
SU1142782A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ β-ИНДОЛИЛУКСУСНОЙ КИСЛОТЫ | 1992 |
|
RU2024867C1 |
| Потенциометрический способ определения дитиокарбаматов | 1984 |
|
SU1276980A1 |
| Способ определения аммонийной соли 5,5,6-триметилбицикло(2,2,1)гептан-2-он-3-экзосульфокислоты | 1987 |
|
SU1437750A1 |
| Способ определения цинка | 1990 |
|
SU1758550A1 |
| Способ определения концентраций фторид-ионов в электролитах | 2023 |
|
RU2812827C1 |
| Мембрана ионоселективного электро-дА | 1979 |
|
SU842546A1 |
| Способ определения удельной поверхности тонкодисперсного материала | 1981 |
|
SU940051A1 |
Изобретение относится к аналитической химии. Целью изобретения является расширение области определения и повышение селективности. Титрование водных растворов перхлорат- ионов осуществляют раствором соли четвертичного алюминиевого основания с числом атомов углерода в молекуле более 24 в хлорированном углеводороде. Значение перхлоратселективного электрода измеряют в водной фазе ре-- акционной смеси. 3 табл. с «S
00
СХ) 00 Ч СП
10
I1388775
Изобретение относится к аналитической химии и может быть использовано в лабораторной и заводской практике для контроля за содержанием перхлорат-ионов в растворах.
Целью изобретения является расширение области определения и повьппение селективности,
Пример, Анализируемый водный раствор помещают в стакан с магнитной мешалкой, добавляют из бюретки аликвоту титранта и смесь перемешивают в течение 1 мин. После расслоения фаз электроды помещают в водную ере- j ду и измеряют значение потенциала перклоратселективного электрода. Указанную последовательность операций повторяют до завершения регистрации всей кривой титрования, по которой с использованием известной концентрации титранта и стандартной процедуры определения точки эквивалентности рас- чить(вают концентрацию перхлорат-ионов в анализируемом растворе.
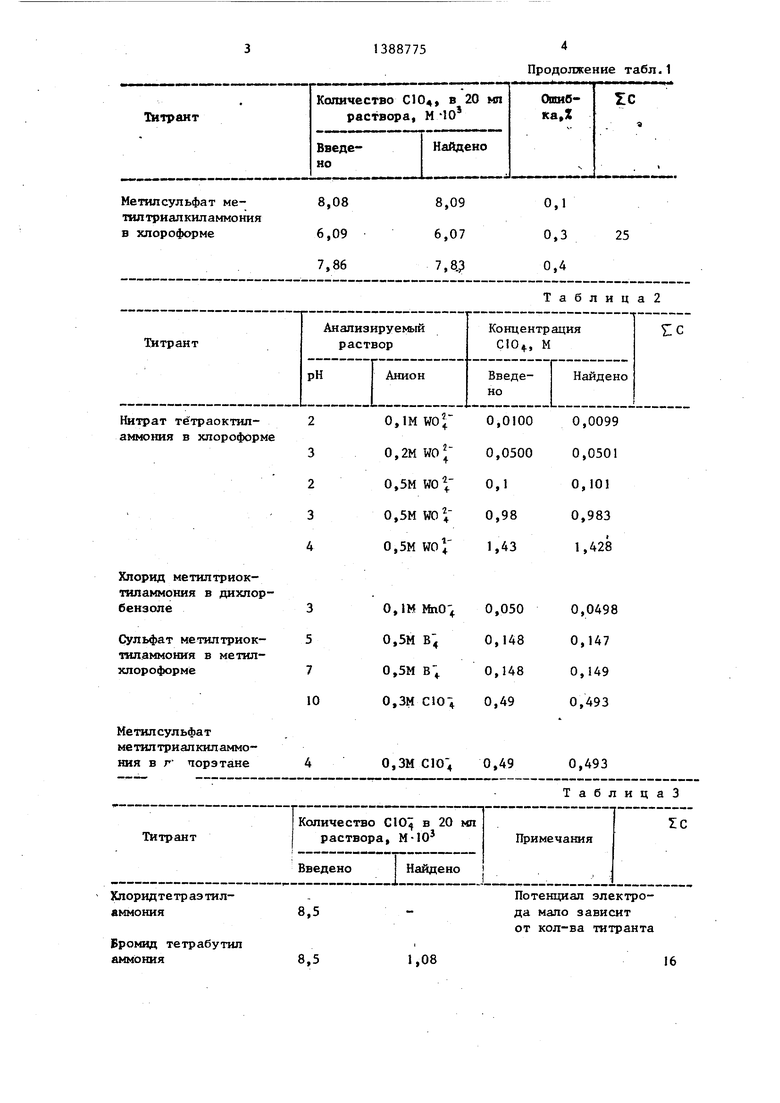
Результаты представлены в табл,1.
Из табл,1 видно, что способ позволяет проводить определение содержания перхлорат-ионов в растворах сложного
20
Раствор, используемый при титров нии, представляет собой органическу фазу с высокой плотностью, позволяющую после добавления титранта к анализируемому раствору получить двухфазную систему, в которой водна фаза легче органической. После быст го перемешивания и расслаивания вод ный раствор, в который погружены злeктpoдЫj не содержит капель тяжелой органической фазы, в связи с чем органическая жидкость не налипает на мембрану электрода.
Концентрацию соли четвертичного аммониевого основания в разбавителе подбирают таким образом, чтобы при титровании объемы титранта и водного раствора в конце определения бы ли близки, В связи с тем, что емкость солей четвертичных аммониевых оснований (без разбавителя по перх лорат-ионам составляет около двух молей, данный титрант расширяет об25
ласть определения перхлорат-ионов в водных растворах.
Для определения пригодны соли четвертичного аммониевого основания с числом атомов углерода в молекуле солевого состава с высокой точнЬстью, JQ более 24, это подтверждается данныВ условиях описанного примера проводят анализ водных растворов, содержащих перхлорат-ионы и примеси ряда неорганических анионов. Полученные
Способ потенциометрического определения концентрации перхлорат- Из экспериментальных данных, представленных в табл,2, следует, что эффективность способа з аключает- ся в повьшгении избирательности и расширении области определения перхрезультаты приведены в табл,2,
35
40
ми, приведенными в табл,3. Формула изобретения
ионов в водных растворах с использованием перхлоратселективного электрода, отличающийся тем, что, с целью расширения области определения повьш1ения селективности, титрование ведут раствором соли чет вертичного аммониевого основания с числом атомов углерода в молекуле более 24 в хлорированном углеводоро де.
лорат-ионов в водных растворах сложного солевого состава. Определение можно проводить в широком диапазоне изменения рН анализируемого раствора от 2 до 10,
Хлорид метилтриал- киламмония в хлороформе
0
j
0
Раствор, используемый при титровании, представляет собой органическую фазу с высокой плотностью, позволяющую после добавления титранта к анализируемому раствору получить двухфазную систему, в которой водная фаза легче органической. После быстрого перемешивания и расслаивания водный раствор, в который погружены злeктpoдЫj не содержит капель тяжелой органической фазы, в связи с чем органическая жидкость не налипает на мембрану электрода.
Концентрацию соли четвертичного аммониевого основания в разбавителе подбирают таким образом, чтобы при титровании объемы титранта и водного раствора в конце определения были близки, В связи с тем, что емкость солей четвертичных аммониевых оснований (без разбавителя по перхлорат-ионам составляет около двух молей, данный титрант расширяет обДля определения пригодны соли четвертичного аммониевого основания с числом атомов углерода в молекуле более 24, это подтверждается данными, приведенными в табл,3. Формула изобретения
Способ потенциометрического определения концентрации перхлорат-
0
ионов в водных растворах с использованием перхлоратселективного электрода, отличающийся тем, что, с целью расширения области оп5
ределения повьш1ения селективности, титрование ведут раствором соли четвертичного аммониевого основания с числом атомов углерода в молекуле более 24 в хлорированном углеводороде.
Таблица 1
0,1 0,7 0,1
25
Титр ант
Количество С104, в 20 мл раствора, М/ш
Введено
Хлорид метилтриок- тиламмония в дихлор- бенэоле
Сульфат метилтриок- тиламмоння в метил- хлороформе
Метилсульфат ме тил триал кил аммония в Г пор этане
Хлорид тетр аэ тиламмония8,5
Бромид тетрабутил
аммония8,5
Продолжение табл.1
Ошибка,Z
1C
Найдено
Таблица2
МпО- В В
сю0,050 0,148 0,148 0,49
ю; 0,49
0,0498 0,147 0,149 0,493
0,493
Потенциал электрода мало зависит от кол-ва титранта
1,08
16
Титрант
Количество С10 в 20 мп раствора. М-10
Введено
Хлорид цетилтриме- тиламмония
8,5
Бромид цетилин- ридиния
85
Иодид тетрагек- силаммония
85
Продолжение табл.3 Щ инечаю1я
1C
Найдено
Наблюдается образование устойчивых эмульсийНаблюдаетсяобразование коллоидного раствора
123
24
| Selig W | |||
| Fresenius Z | |||
| Analyt, Chem | |||
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
| Устройство для биологического очищения сточных вод | 1924 |
|
SU419A1 |
| Baczuk R.Z | |||
| Analyt. | |||
| Chem | |||
| Приспособление для контроля движения | 1921 |
|
SU1968A1 |
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
| Катодный усилитель с питанием усилительной лампы переменным током | 1923 |
|
SU685A1 |
Авторы
Даты
1988-04-15—Публикация
1984-11-13—Подача