Изобретение относится к новым производным THeHo 2,3-d nHpHMHAMHa, обладающим биологической активностью, которые могут найти применение в медицине.
Цель изобретения - создание новых производных тиено(2,3-й)пиримидина, обладающих более высокой противогерпети- ческой активностью в сочетании с противотуберкулезной активностью.
Пример 1. Получение 4-метокси-5-ме- тил-6-нитpoтиeнo{2,3-d пиpимидииa (1 а).
Получение исходного соединения - 4- xлop-5-мeтил-6-нитpoтиeнo 2.3-d}пиpимидинa (2а).
Смесь 1,7 г {0,008-моль) 5-метил-6-нит- po-3.4-диrидpoтиeнoi2,3 d пиpимид-4-oнa, 1 мл (0,01 моль) хлорокиси фосфора, 0.84 мл (0,01 моль) диметилформамида (ДМФА) в 30 мл сухого дихлорэтана (ДХЭ)кипйТ1ВТ при перемешивании в течение 30 мин. Реакционный раствор промывают водой, ДХЭ упаривают в вакууме, остаток кристаллизуют из смеси гексана и хлористого метилена (1:1).
Получают 1,5 г (82%) 4-хлор-5-метил-б- нvlтpoтиeнo 2,3-d пиpимидинa в виде кристаллического порошка желтого цвета; т.пл. 134-135°С, Найдено, %; С 36,5; Н 1,9; С1 15,2; N 18,2; S 14,1.
C7H4CIN302S
Вычислено, %; С 36.6; Н 1,8; С1 15,4; N 18.3; S 14,0.
Спектр ЯМР (СНС1з, внутр.ст.ТМС). 6 , М.Д.; 9,15 (с, 2Н). 2,52 (с, 5СНэ).
Получение целевого продукта - 4-меток- cи-5-мeтил-6-нитpoтиtнo{2,3-d пиpимидинa (1а).
Кипятят раствор 2,29 г (0,01 моль)соединения 2а в 40 мл метанола в течение 30 мин. Раствор охлаждают, выпавший осадок отфильтровывают,
Получают 1,12. г (50%) 4-метокси-5-ме- тил-6-нитpoтиeнo 2,3-d пиpимидинa в виде кристаллического порошка желтого цвета, растворимого в хлоруглеводородах, спиртах, т.пл, 119-120°С,
Найдено, %: С42,4; Н 3,0; N 18.7; S 14,1.
СвНуЫзОзЗ
Вычислено. %; С 42.6; Н 3,1; N 18,6; S 14,2.
Пример 2. Получение 4-метокси-5- нитpo-6-мeтилтиeнo 2,3-d пиpимидинa (16).
Получение исходного соединения - 4- xлop-5-нитpo-6-мeтилтиeнc 2,3-d пиpимидинa (26) - проводят в условиях примера 1.
Из 3,8 г (0,018 моль) 5-нитро-6-метилти- ,3-d nиpимид-4-oнa. 1,65 мл РОС1з, 1,39 мл ДФМА в 100 мл сухого ДХЭ получают 2 г (70%) 4-хлор-5-нитро-6-метилтие- .3-d пиpимидинa в виде порошка
кремового цвета, растворимого в спиртах, хлоруглеводородах, диоксане, кетонах. т.пл. 84-85°С (хлористый метилен;гексан 1;1).
Найдено; %; С 36,6; Н 1,8; С 15,6; N 18,4; 514,1,
C7H4CIN302S
Вычислено, %; С 36,6; Н 1,8; С1 15,4; N t8,3; S 14,0.
Спектр ЯМР (СНС1з, внутр.ст. ТМС), б . м,д.; 8,93 (с, 2Н), 275 (с. 6-СНз).
Получение целевого продукта - 4-метокcи-5-нитpo-6-мeтилтиeнo{2,3-d пиpимидинa
(15) - проводят аналогично примеру 1 из
1,12 г (0.005 моль) соединения 2а в 30 мл
метанола.
Получают 0,65 г (55%) 4-метокси-5-нит- pp-6-мeтилтиeнo 2,3-d пиpимидинa в виде порошка белого цвета с кремовым оттенком, т.пл. 95-96°С.
Найдено, %; С42,7; Н 3,2; N 18,9; S 14.3. СаН уМзОзЗ
Вычислено, %; С 42,6; Н 3,1; N 18,6; S 14,2.
Описываемые соединения изучены в опытах на культурах клеток по подавлению размножения вирусов простого герпеса I и II антигенных типов.
Для изучения противогерпетической активности соединений использовали первич- но трилсинизированную культуру клеток фибробластов эмбриона курицы (ФЭК), которую получали путем трипсинизации 9- дневных куриных эмбрионов. В качестве тест-вирусов использовали вирусы простого герпеса I и II антигенных типов (штаммы Л2 иТр).
Двухдневный монослой культуры клеток инфицировали разведениями вируса, содержащими от 10 до 1000 ТЦДбо в 0,4 мл. После адсорбции и удаления неадсорбировавшегося вируса (через 1 ч после инокуляции вируса) вносили изучаемые соединения в концентрациях, составляющих 1/2 от максимально переносимой для культуры клеток
концентрации, и в меньших концентрациях.
Результаты учитывали через 48 ч по способности изучаемых соединений предотвращать цитопатическое действие вируса на клетки и выражали количеством ингибируемых 50% тканевых цитопатических доз вируса (ТЦДбо).
Изучение вирусингибирующей активности соединений по изобретению в отношении вирусов простого герпеса проведено на
1600 пробирках с монослоем клеточной культуры ФЭК; результаты обработки статистические.
Противотуберкулезную активность соединений по изобретению изучали в опытах In vitro, определяя минимальную подавляющую концентрацию (МПК) методом серийных разведений на среде Сотона. В качестве тест-культуры использовали микобактерии туберкулеза человеческого типа (М.tuberculosis H37Rv). Сроки культиви- рования испытуемых концентраций соединений с тест-культурами составляли 14 дней при37°С..
Токсичность соединений по изобретению изучали в опытах на культуре клеток ФЭК (96 пробирок) и белых нелинейных мышах с массой тела 18-20 г (120 мышей). На монослой 48-часовой культуры клеток ФЭК наносили питательную среду № 199, содержащую испытуемое соединение в различ- ных концентрациях, и в течение 5 дней проводили микроскопию клеточных культур для выявления цитотоксического действия соединений и определения максимально переносимой клетками концентрации,
Мышам испытуемые соединения вводили внутрь в виде взвеси в 1 %-ном крахмальном геле в объеме 0,5 мл 1 раз в день в течение 5 дней. Наблюдение за выживаемостью животных проводили в течение 14 дней и определяли максимально переносимую дозу (МПД) соединения.
Результаты изучения противогерпети- ческой активности соединений приведены в табл. 1 и 2.
Сравнение проводили с известным соединением формулы А
Н
обладающим вирусингибирующим действием в отношении вируса простого герпеса в клеточной культуре ФЭК,
Результаты изучения соединений по изобретению свидетельствуют о том, что эти соединения обладают выраженной ви- русингибирующей активностью в отношении вируса простого герпеса. Соединение 1а в концентрациях 2,5 и 2,0 мкг/мл подав5
0 5 0
5
0
5
0
5
ляет репродукцию вируса герпеса I типа на 1,0-2,0 Ig ТЦДйо. а II типа на 1.0-1.5 Ig ТЦДк). Соединение 16 эффективно только в отношении вируса герпеса I типа: в концентрации 10 и 5 мкг/мл подавляет его репродукцию на 2,0-1,0 Ig ТЦДм по сравнению с контролем. Соединение А уступает по про- тивогерпетической активности соединениям по изобретению в отношении вируса простого герпеса I типа и неактивно в отношении вируса герпеса II типа.
Результаты изучения противотуберкулезной активности соединений приведены в табл. 3.
Как следует из табл. 3, соединения по изобретению кроме противовирусной активности обладают высокой противотуберкулезной активностью в отношении микобактерии туберкулеза человеческого типа, близкой по активности к известному противотуберкулезному антибиотику стрептомицину.
Результаты изучения токсичности соединений по изобретению свидетельствуют о том, что они хорошо переносятся животными: при введении per os 1 раз в день в течение 5 дней МПД для мышей соединений 1а и 1 б составляют 500 мг/кг, что выше МПД соединения А в 4 раза и свидетельствует о меньшем токсичности соединений по изобретению.
Анализ полученных результатов показывает, что соединения по изобретению обладают более выраженным действием и меньшей токсичностью по сравнению с соединением формулы А, Кроме того, соединения по изобретению обладают высокой противотуберкулезной активностью, сравнимой с активностью известного антибиотика стрептомицина.
(66) Харизоменова И.А, и др. Синтез и противовирусная активность производных 3- аминотиеио 2.3-Ь пиримидина, Хим.фарм.журнал. 1981, N 9, с 40,
Машковский М,Д. Лекарственные средства. М.: Медицина, 1984, т. 2. с.230.
Таблица 1

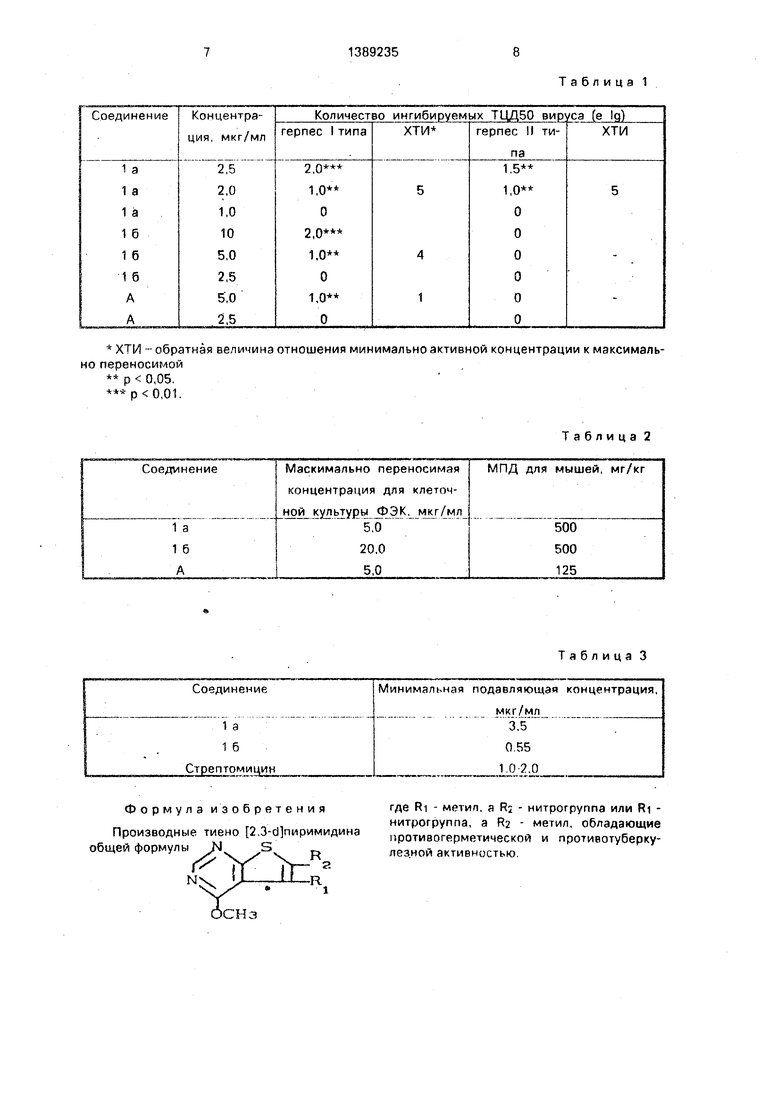
Изобретение касается замещенных пиримидина, в частности тиено I2,3-d пиpимидинo8 общей ф-лы СН -О- C N-CH N-C C-S-CR CR где э 1I1 2 а) R -СН, и R-NO . б) R-NO, и R-СН, обпа13221223 дающих лротивогерпетической и противотурберку- лезной активносгьк), что может быть использовано в медщине. Цель изобретения - создание новых более активнь1х веществ с расширенным спектром действия Их синтез ведут из соответствующего 3,4-дигидротиено 2,3-d| пиримид - 4 - она и РОС в присутавии дйметилформамида с последующим кипячением в метаноле. Выход %: тля, С брутто-ф-ля; а) 50, 119 - 120; б) 55; 95 -96. С Н N О S. Новые вещеава активны против герлеса f и 11 типов при концентрации 1 мкг/мл против 5 мкг/мл для известного (химиоте- рапбвтический индекс 5); минимально подавляющая концентрация для туберкулеза 3 и 0,55 мкг/мл против 1-2 МЮ-/МЛ для арептомицина. 3 табп
ХТИ - обратная величина отношения минимально активной концентрации к максимально переносимой р 0,05, ,01.
Соединение
1 а
1 б
Стрептомицин
Таблица 2
Таблица 3
подавляющая концентрация, мкг/мл
3:5
0.55 1.0-2,0
Авторы
Даты
1993-11-15—Публикация
1986-08-25—Подача