А «
ы ч©
)
о
Ol
ы
Изобретение касается новых химических, соединений ряда Ti/ieHo 2,3-d nHpHMH- дииа, а именно производных 5-формилтиено 2,3-Ь пиримидина общей формулы г
1 N-;.....,.CHO
JCIL.,,
N S гдеП1«ы(0 R2°H(1a):
I , R2 H (16);
обладающих протиаогерпетической актив ОСТЬЮ.., .
Цель изобретения - производные тие- ,3d пиpимидинa, .обладающие более выраженной противогерпетической активностью а отношении вирусов простого герпеса и меньшей токсичностью.
Приме р 1. Получение 4-морфолино-5- формилтиено 2,3-Ь пири1Мидина (la. I А, Получение исходного соединения :(Па)-4-хлор-5-дибромметилтиено 2 ,3-й пиримидина,
Смесь 3,68 г (0,02 моль) 5-метил-4-хлор- тйeмo 2,3-d пмpимидинa, 7,12 г (0,04 моль) N-бромсукцинимида, 0,01 г перекиси бензо- ила в 30 мл четыреххлористого углерода кипятят 30 мин. Реакционную массу промывают водой, растворитель упаривают в вакууме досуха, остаток кристаллизуют из хлористого метилена.
Получают 5,13 г (75%) 4-хлор-5-дибром- мeтилтиeнo 2,3-d пиpимидинa в виде кри- Ьталлического порошка белого цвета с желтоаатым оттенком, т.пл. 81-82°С
l(CH2Cl2).
Вычислено, %: С 24,5; Н 0,8; Вг 46,7; С 10,3;-М 8,2; 59,4,
C7H4Br2CIN2S
Найдено, %: С 24.5; Н 0,9; Вг 46,7; CI 10,2; N 8,2; S 9,4.....
Б. Получение целевого продукта (1а}-4-мор- фoлинo-5-фopмилтиeнo 2,3-d пиpиммдинa.
Смесь 6,84 г (0,02 моль) 4-хлор-5-диб- :ромметилтиено 2,3-Ь пиримидина в бензола и 21 мл морфолина выдерживают npi; в течение 30 мин. Реакционную массу промывают водой, бензол отгоняют. Костатку при перемешивании добавляют 18 МП воды и 20 мл 20%-ной l-t2S04. Образовавшийся раствор оставляют на .12ч при ком- нгчтной температуре, экстрагируют хлороформом, последний упаривают в вакуме. Остаток кристаллизуют из водного спирта (1;1.).
Получают 3,68 г (75%) 4-морфолино-5- opмилтиeнo 2iЗ-d пиpимидинa в виде кри- сталлического порошка белого цвета с кремовым оттенком, т.пл, 156-157 С.
Вычислено, %: С 52,99; Н 4,44; N 16.85; S 12,86
CiiHiiN302:S
Найдено, %: С 53,0; Н 4,46; N 16,81; S 12,9,:
ИК-спектр. v,CM Vl680(CO). П р и м е р 2, Получение 4-метокси-5- фopмилтиeнo 2,3-d пиpимидинa (15). А. Получение исходного соединения (Иб) - 4-метокси-5-дибромметилтиено 2, римидина-проводят в условиях, описанных в примере 1а, из3.6 г(0.02 моль)4-метокси- 5-мeтилтиeнo 2.3-d пиpимидинa, 7.12 г N- бромсукцинимида, OjOT г перекиси бензоила в ЗО мл четыреххлористого углерода.
Получают 5J4 (85%) 4-метокси-6-дибpoммётилтиeнo 2iЗ-d пиpимидинa в виде
кристаллического порошка кремового цвета, растворимого в хлоруглеводородах,
спиртах диоксане, т.пл. 7б-77°С.
Вычислено, %: G 28,4; Н 1,8; Вг 47,3; N 8.3; 59,5.
С8НбВГ2Н203
Найдено, %; С 28,6; Н 1,8; Вг47,3; N8.2; 59,6,
6, Получение целевого продукта (16) 4- мeтoкcи-5-фopмилтиeнo 2,3-d пиpимидинa проводят в условиях примера 16 из 6,76 г
(0,02 моль) 4-метокси -5-дибромметилтие- )иримидина. 21 мл морфолина. 18 мл воДы и 20 мл 20%-ной H2S04. После кислотного гидролиза продукт выпадает в осадок, , .: -
Получают 2,75 г (71 %) 4-метокси-5-формилтиeнo 2.3-d пиpимидинa в виде кристаллического порошка кремового цвета, растворимого в спиртах, диоксане, хлоруглеводородах, т.пл. 158-159°С.
Вычислено, %: С 49,5; Н 3,1; N 14,4; S
16,5.
C8H6N2025
Найдено, %; С49,6; И3,3; N 14,5; 5 16,6.
-1.
ИК-спектр, V,CM : 1680 (СО).
П р и м е р 3. Получение 4-МОРФОЛИНО-5- фopмил-6-бpoмтиeнo 2,3-dlпиpимидинa
(1в)К раствору2 г(0,008мoлb)4-мopфoлинo- 55 5-фopмилтиeнo 2,3-d пйpимидинa в 20 мл ДМФА при перемешивании прикапывают 0,41 мл (0,008 моль) брома, Реакционную массу выдерживают при комнатной температуре 1 ч, выливают в воду. Выпавший осадок отфильтровывают, сушат и кристаллизуют из спирта.
Получают 1.3 г (50%) 4-морфолино-б формил-6-бромтиено 2,3- пиримидина в виде кристаллического порошка белого та с желтоватым оттенком, растворимого в спиртах, диоксане, т.пл. 178-179°С.
Вычислено, %: С 40,3; Н 3.7: N 12,8; S 9,8: Вг24,4.
CiiHioN302SBr
Найдено. %: С 40.4; Н 3.5: N 12.8; S 9.7: Вг24.4.;
ИК-спектр, V. см -: 1710 (СО).
П р и м е р 4. Полученные соединения обладают противогерпетической активно- стью 8 отношении вирусов простого герпеса f и (I антигенных типов.
Изучение активности соединений рб- щей формулы I проводят на культурах клеток по подавлению размножения вирусов.
Для изучения противогерпетической активности соединений используют первич- но-трансинизированную культуру клеток фибробластов эмбриона курицы (сЬэК). которую получают путем трипсиНизации 9- дневных куриных эмбрионов. В качестве тест-вирусов используют вирусы герпеса простого I и 11 антиг енных типов (штаммы Л2 иТр).
Двухдневный монослой культуры кле-. ток инфицируют разведениями вируса, содержащими 10 1000 ТЦД50 в 0.4 мл. После адсорбции и удаления неадоорбировавще- гося вируса (через 1 ч после инокуляции вируса) вносят изучаемые соединения в кон- центрациях, составляющих 1/2 максимально переносимой для культуры клётОК концентрации, и в меньших концентрациях. Результаты учитывают через 48 ч по cndt6b6- ности изучаемых соединений предотвра- щать цитопатическое действие вируса на клетки и выражают количеством ингибируемых 50% тканевых цитопатических доз вируса (ТЦДйо).
Изучение вирусингибирующейактивности предлагаемых соединений в отношении вируса простого герпеса проведено на 15.00 пробирках с монослоем клеточной культуры ФЭК.
Токсичность полученных соединений изучают в опытах на культуре клеток ФЭК (96 пробирок) и на 120 белых нелинейных мышах массой тела 18-20 г.
На монослой 48-часовой культуры клеток ФЭК наносят питательную среду № 199, срдержащую испытуемое соединение в различных концентрациях. В течение 5 дней проводят мифоскопию клеточных культур для выявления цитотоксйческого действия
соединений и определения максимально переносимой клетками концентрации (МИК).
Мышам испытуемые соединения вводят внутрь в виде взвеси в 1 %-ном крахмальном геле в объеме 0.5 мл 1 раз в день в течение 5 дней. Наблюдение за выживаемостью животных проводят в течение 14 дней и определяют максимально переносимую дозу (МПД) соединения.
Результаты изучения полученных соединений приведены в табл.1 и 2. Сравнение проводят с известным 3-(п-оксифенилами- но)-4-9ксо-5,б-диметил-3.4-дигидротиено 2 ,3-б пиримидином (соединение А), обладающим вирусингибирующим действием в отношении вируса простого герпеса в клеточной культуре ФЭК.
Результаты изучения полученных соединений свидетельствуют о том. что эти соединенияобладаютвысокойвирусингибирующей активностью а отношении вируса герпеса простого I антигенного типа, выращенного в клеточной культуре ФЭК. В концентрациях от 5 до 2 мкг/мл они подавляют репродукцию 2,0-2,25 Ig ТЦДво вируса. ,
Соединение А. уступает по активности . предлагаемым соединениям : в максимально переносимой для клеток концентрации 5 мкг/мл оно снижает инфекционный титр вируса на 1,0 Ig ТЦДбо, предлагаемое соединение 16 - на 2,25 дТЦП50.
Кроме того, соединения а и 16 активны в отноше1-1ии вируса герпеса простого И антигенного типа, соединение А такой активностью не обладает (см.табл.1).
Результаты изучения токсичности предлагаемых соединений свидетельствуют о том, что они хорошо переносятся животными - при введении 1 раз в день в течение 5 дней МПД для мышей составляют 250 мг/кг (соединение 1а) и 500 мг/кг (соединения 16,в), менее токсичны, чем соединение А. МИД которого составляет 125 мг/кг.
Для клеточной культуры ФЭК. МПК для всех трех указанных соединений примерно 5-10 мкг/мл.
Предлагаемые соединения обладают более вырзжент1ым противогерпетическим дейстеием и меньшей токсичностью по сравнению с соединением А.
(56) Харизомемова И.А. и др. Функциональные производные тйофела XX. Синтез и про- тивовируснэя активность производных 3-aMiiHOTneHo 2.3-d nMpMM nKa. Хим. фарм. журнал, 198}. т.15, № 9, с: .
713910528
Табли ца 1 Результаты изучения противовирусной активност предлагаемых соединений 1а, 16, 1в.

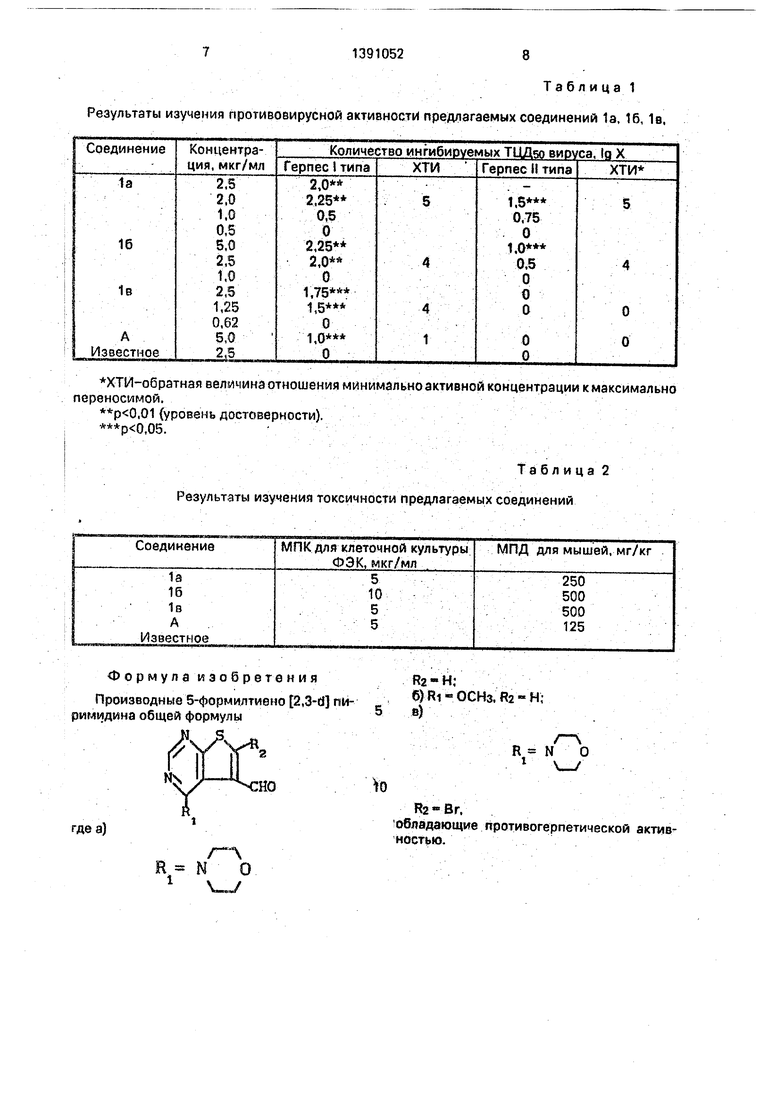
Изобретение касается замещеннь х пиримидина, в. частности производных З-фтормилтиено 2,3-d пиримидина (ПМ) общей формулы -C CM-S-CR -СН-СН 0, где а) 1 I2, R -морфолииил: R Н; б) R ОСН ; R Н; в) R - морфолинил; R Вг, которые обладают противогер- петической активностью и могут быть использованы в медицине. Цель - создание более активных веществ указанного класса. Синтез ПМ ведут броми- , рованием 4-мopфoлинo-5-фopмилтиeнo 2,3-d пиримидина бромом в среде диметилформамида при комнатной темлерат ре. Выход %, т.пл. °С; брутто ф-ла: а) 75,156 - 157. С Н N О S: б) 71, 158 - 159, С в) 179, С Н N О SBr. Мака1мально переносимая кон11 10 3 2 центрация для переично-трипсиннзированных культур клеток фиброблааов эмбриона курицы составляет для ПМ 5 мкг/мл лри токсичности 250 - 500 иг/кг. 2 табл.
ХТИ-обратная величина отношения минимально активной концентрации к максимально переносимой.
,01 (уровень достоверности). ,05.
Та б л и ца 2 Результаты изучения токсичности предлагаемых соединений
Формулаизобретения
Производные 5-формилтиено 2,3-dримидина общей формулы
/Г
N4 J-1Ц,у
где а)
X
R N О -„У
R2-H.б)Н1«оенз.«2-н,8)
/
R N о -/
.
обладающие противогерпетической активностью.
Авторы
Даты
1993-11-30—Публикация
1986-08-25—Подача