со
;О 








| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения азотсодержащих полисахаридов, обладающих противоопухолевым действием | 1977 |
|
SU730277A3 |
| Способ получения полисахаридов, обладающих противоопухолевым действием | 1977 |
|
SU704431A3 |
| Способ получения азотсодержащего полисахарида, промотирующего чувствительность к лекарствам у бактерий, устойчивых к антибиотикам | 1978 |
|
SU793408A3 |
| Способ получения полисахаридов, обладающих противоопухолевым действием | 1976 |
|
SU786855A3 |
| Способ получения мукополисахаридов | 1977 |
|
SU961565A3 |
| Способ получения полисахарида, обладающего противоопухолевым действием | 1977 |
|
SU740156A3 |
| Способ получения антибиотика 2188 и штамм плесневого гриба РеNIсILLIUм RUGULоSUм FERM ВР-142,используемый для получения антибиотика 2188 | 1983 |
|
SU1419521A3 |
| Способ получения биомассы базидиомицетов | 1977 |
|
SU1090261A3 |
| Способ получения монокариотического мицелия гриба coRIoLUS VeRSIcoLoR (FR) QUeL | 1977 |
|
SU991954A3 |
| Способ получения углеводородного топлива и пека | 1983 |
|
SU1545946A3 |
Изобретение относится к химии высокомолекулярных полисахаридов, конкретно к получению полисахаридов на основе грибов рода Coriolus, обладающих высокой противоопухолевой активностью при пероральном применении, и может быть использовано при производстве лекарственных средств. Изобретение позволяет расширить арсенал биологически активных средств за счет того, что мицелий грибов рода Coriolus экстрагируют 0,1-0,4 н. водным раствором едкого натра при 93-97 С, полученный экстракт под- ёергают ультрафильтрации при давлении 0,5-5,0 кг/см или обратному осмосу при давлении 20-35 кг/см, затем вводят 84-90 об.% сульфата аммония и полученный осадок растворяют в воде до образования 3-10%-ного раствора с последующей его очисткой сначала ультрафильтрацией при давлении 0,5-5,0 кг/см и затем в ионообменной диэтиламиноэтилцеллюлозной колонке концентрированием: раствора и сушкой целевого продукта. 3 табл. § О) с
СМ
Изобретение относится к химии высокомолекулярных полисахаридов, а именно к получению полисарахидов на основе грибов рода Coriolus, обла- дающих высокой противоопухолевой активностью при пероральном применении и может быть использовано при производстве лекарственных средств.
Цель изобретения - расширение арсенала биологически активных средств,
,Пример1.
1-1. Культура грибкового штамма.
Штамм (именуемый СМ-103 и офици- ально выращиваемый в Японском Государственном исследовательском институте ферментации под номером осаждения FERM-P2414) б азидиомицетного грибка Coriolus versicolor (Fr) Quel вводят в виде затравки в.двадцать 200-миллилитровь11х конических колб, каждая из которых содержала 30 мл водного раствора среды культуры, содержащей, мае. %: глокоза 5; дрожже- вой экстракт 0,3; , 0,1; MgSO, 0,1, и затравочный (прививочный) материал оставляют для выращивания на 10 дней при 25-27°С. Выросшие слои грибка на поверхности среды культуры в колбах собирают и гомогенизируют при помощи 20 л физиологического соляного раствора для приготовления рассады культуры грибкового штамма в виде суспензии.
20 л полученной таким образсм рассады культу вводят в ввде затравки в 1,600 л водного раствора среды культуры, содержащей, мас.%: глюкоза 10; дрожжевой экстракт 1,5; 0,1; MgSO 7H, 0,1, содержащихся в вертикальис ферменторе объемом 2м , и затравочный материал оставляют для выращивания в тече- ние 7 дней при . При зтом в среду культуры продувают воздух со скоростью 0,5 л мин на 1 л среды культуры и осуществляют перемешивание среды культуры со скоростью 150 об/мин.
Полученный таким образом выращенный материал сушат в сушильном аппарате с двойным барабаном, чтобы получить около 30 кг сухого материала, содержащего в основном распространяющиеся грибницы грибкового штамма.
Q
5 Q 5 О
д
0
5
Каждые 100 г сухого материала подвергают следующему процессу для извлечения полисахарида.
1-2. Извлечение полисахарида из сухого материала.
100 г полученного таким образом сухого материала подвергают экстрагированию сначала 3 л горячей воды при 95i2°C в течение 3 ч в 5-литровой колбе с мешалкой для перемешивания, и затем содержимое колбы фильтруют для разделения его на грибковый остаток и раствор экстракта. Грибковый остаток промывают при помощи 1 л воды, промывку сочетают с раствором экстракта, что приводит к общему количеству 3,5л.
Грибковый остаток подвергают экстрагированию при помощи 2 л водных растворов едкого натра с соответствующими нормальностями 0,1, 0,2, 0,3 и 0,4 при 95±2 С в том же порядке и в той же самой колбе, что и ранее, и после каждой операции экстрагирования грибковый остаток отделяют от раствора экстракта и промывают 5л воды. Промывку комбинируют с раствором экстракта, приводя к общему количеству 2,2 л. Получают 12,3 л водного раствора, содержащего экстракт грибкового штамма. Этот водный раствор, называемый далее водным раствором экстракта, подвергают очистке. I
1-3. Очистка водного раствора экстракта.
Очистку упомянутого выше водного раствора экстракта, содержащего полисахарид, осуществляют или при помощи ультрафильтрации, далее обозиа- чаемой как 1-3-г1, или при помощи обратного осмоса,далее обозначаемого как 1-3-2.
1-3-1. Очистка при помощи уль- тра4 1льтрации.
Часть (7,2 л) водного раствора экстракта (12,3 л), приготовленного из 100 г сухого материала,упомянутого вьше, подвергают ультрафипьтрациИ( при 10 С при помощи введенного водного раствора экстракта в ультрафильтр (типа фильтра Amicous 2000 Beneh, снабженного мембраной М-5, которая позволяет проходить молекулам только с молекулярным весом менее чем 5000, чтобы оставлять водный экст-г ракт, содержащий только молекулы с
31403990
весом не менее чем 5000,
го на ни чт ул ле к
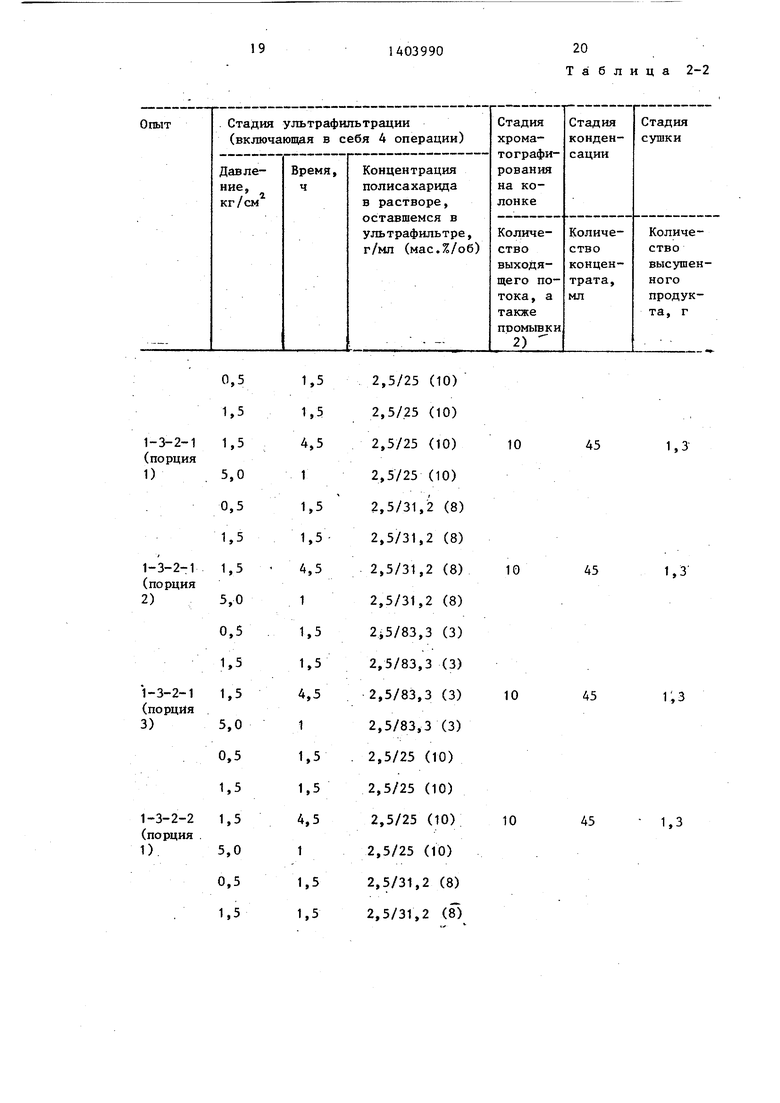
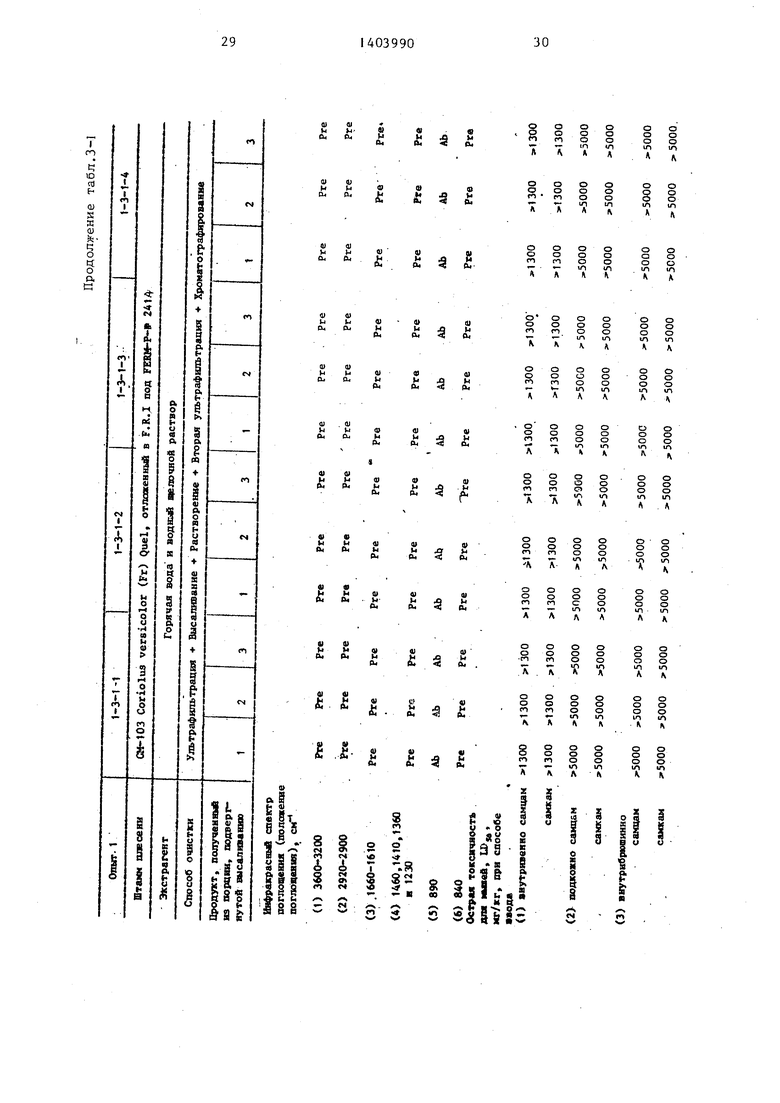
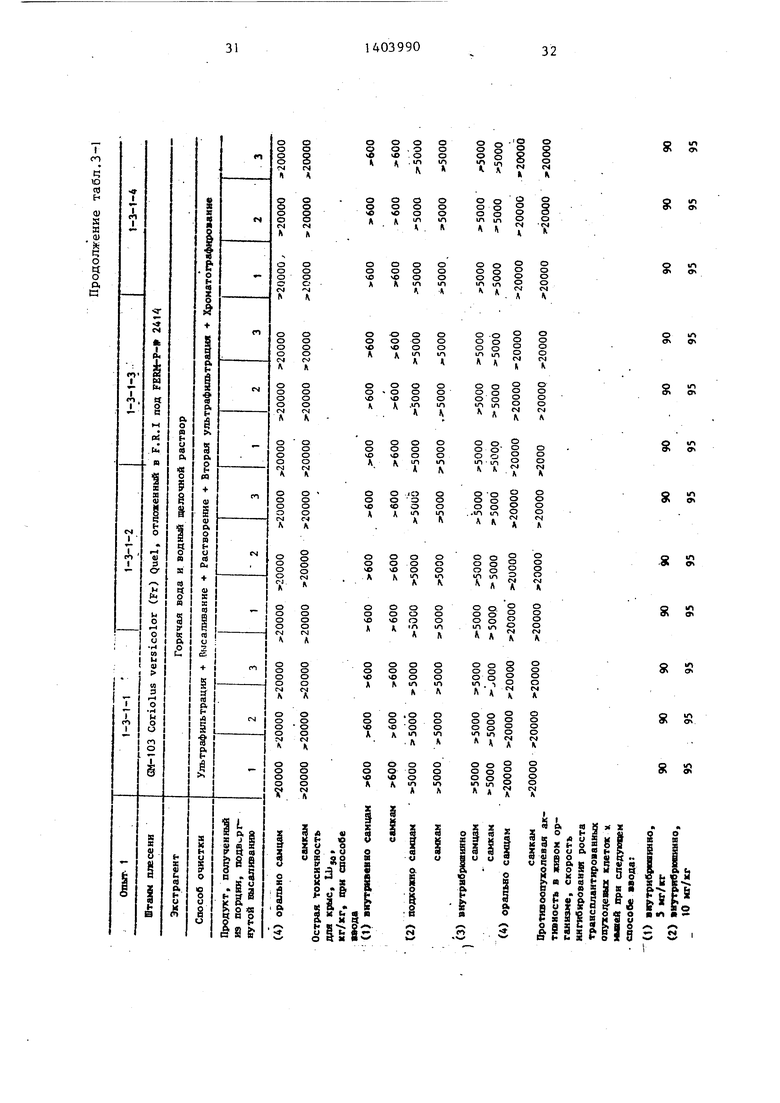
и при помощи подачи в него давления. Операцию ультрафильтрации осуществляют 4 раза при давлении 0,5 кг/см и времени операции 1,5 часа в серии 1-3-1-1; давлении 0,5 кг/см й времени операции 2,5 ч в серии 1-3-1-2; давлении 3,0 кг/см и времени операции 2 ч в серии 1-3-1-3 и давлении 5,0 кг/см и времени операции ,2,5 ч в серии 1-3-1-4.
Количество водного раствора экстракта, оставшегося в ультрафильтре, составляет 840 мл (серия 1-3-1- 1), 380 МП : (серия 1-3-1-2), 150мл (серия 1-3-1-3) и 110 мл (серия 1- 3-1-3).
Водный экстракт, оставленньш в ультрафильтре в каждом опыте указанной выше первой ультрафильтрации, делят на три равные части (порция 1, порция 2 и порция 3) и добавляют кристаллический сульфат аммония в кажПосле приложения давления, равного 0,5 кг/см , к водному раствору, находящегося в ультрафильтре в течение периода времени, равного 1,5 ч, что является первой операцией второй ультрафильтрации, производят добавление определенного количества воды к .водному раствору, оставшемуся в уль
10 трафильтре, а вторая операция на этой второй ультрафильтрации заключается в создании Давления, равного 1,5 кг/см , на ультрафильтре и поддержании этого давления в тече15 ние 1,5 ч. После добавления определенного количества воды к водному раствору, оставшемуся в ультрафильтре, давление, равное 1,5 кг/см, сно ва прикладывают к ультрафильтру, и
20 это давление сохраняют в течение
4,5 ч,что является третьей операцией Определенное количество воды снова добавляют к водному раствору, оставшемуся в ультрафильтре, и давледую из порций,тем самым производится 25 ние, равное 5 кг/см, снова приклавысаливание полисахарида, присутствующего в водном экстракте, и самого экстракта. Количество сульфата аммо- ,ния, добавляемого в каждую из- порций водного экстракта, оставшегося в ультрафильтре при проведении каждого из onbiTOB в указанной выше ультрафильтрации, показано в табл.1-1, и эти данные соответствуют 90 мас.% от объема водного экстракта в порции 1; 87 мас.% от объема водного экст- ракта в порции 2 и 84 мас.% от объема водного экстракта в порции 3 в каждом из опытов по ультрафильтрации.- Полисахарид, полученный в результате проведения стадии высаливания, далее собирают фильтрацией и. подвергают растворению в дистиллированной воде.
Каждый из полученных таким образом водных растворов полисахарида подвергают второй ультрафильтрации в том же самом ультрафильтре, оснащенном той же самой мембраной, как было указано вьш1е, для удаления сульфата аммония, оставшегося в полисахариде, полученном высаливанием. При проведении второй ультрафильтрации one- рацию проводят четыре раза подряд с тем, чтобы удалить сульфат аммония так тщательно, как только это возможно, из полисахарида, полученного выщелачиванием (табл.1-2).
4
После приложения давления, равного 0,5 кг/см , к водному раствору, находящегося в ультрафильтре в течение периода времени, равного 1,5 ч, что является первой операцией второй ультрафильтрации, производят добавление определенного количества воды к .водному раствору, оставшемуся в ультрафильтре, а вторая операция на этой второй ультрафильтрации заключается в создании Давления, равного 1,5 кг/см , на ультрафильтре и поддержании этого давления в течение 1,5 ч. После добавления определенного количества воды к водному раствору, оставшемуся в ультрафильтре, давление, равное 1,5 кг/см, снова прикладывают к ультрафильтру, и
это давление сохраняют в течение
4,5 ч,что является третьей операцией. Определенное количество воды снова добавляют к водному раствору, оставшемуся в ультрафильтре, и давление, равное 5 кг/см, снова прикла5
дывают к ультрафильтру в течение 1 ч, и это является четвертбй операцией, завершающей вторую ультрафиль- ,трацшо.
0 Концентрация полисахарида в водном растворе, оставшемся в ультрафильтре после завершения стадии второй ультрафильтрации, составляет 10 г/100 мл в том случае, когда ёто- рую ультрафильтрацию проводят на порции 1 каждого опыта; 8 г/100 мл в том случае, когда это касается порции 2 каждого опыта и 3 г/100 мл в том случае, когда это касается пор-
0 ции 3 каждого опыта.
Далее каждый из полученных таким образом водных растворов, соответственно остающийся в ультрафильтре после завершения второй ультраg фипьтрации, на соответствующих порциях каждого из опытов, подвергают хроматографированию, и эту операцию осуществляют путем выливания водного раствора в колонку, заполненную диэтиламиноэтилцеллюлозой с целью адсорбции азотсодержащих материалов, которые являются примесями в водном .растворе.
Выходной раствор, который пропу- 5 екают через колонку и из которого отделяют азотсодержащие материалы с помощью адсорбента в колонке, собирают, затем его подвергают конденсации при пониженном давлении и далее су0
шат с получением в результате очищенного полисахарида.
1-3-2. Очистка при помощи фаз, представленных обратным осмосом.
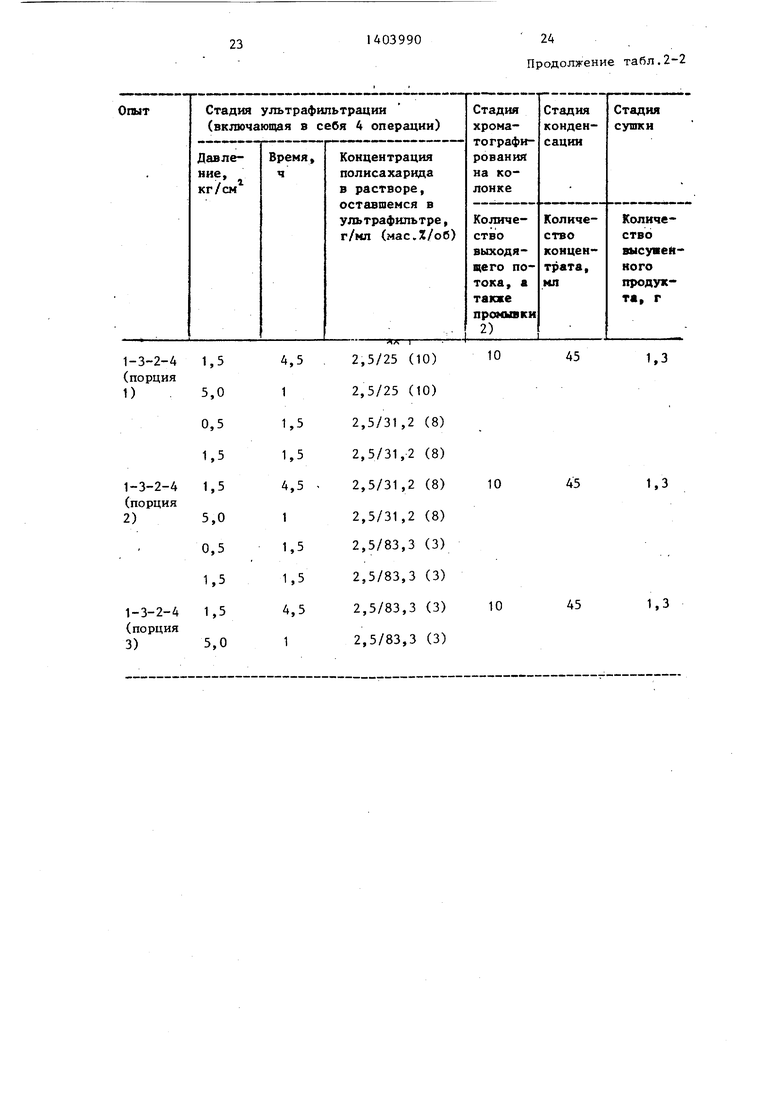
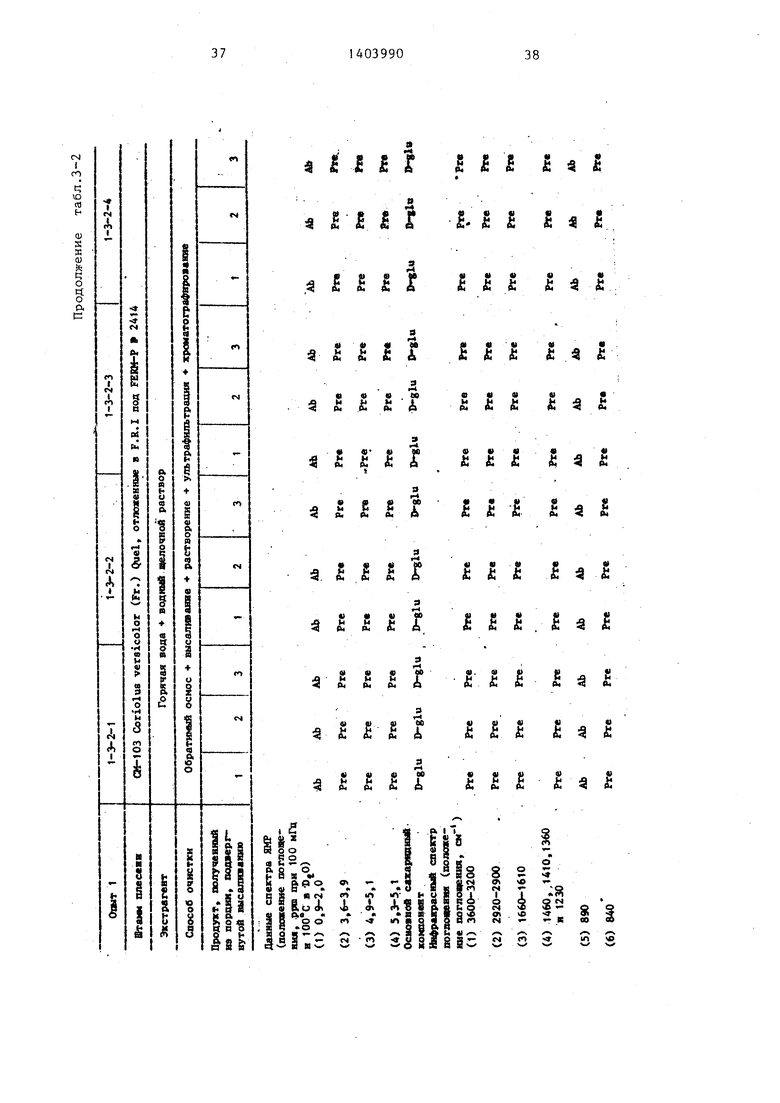
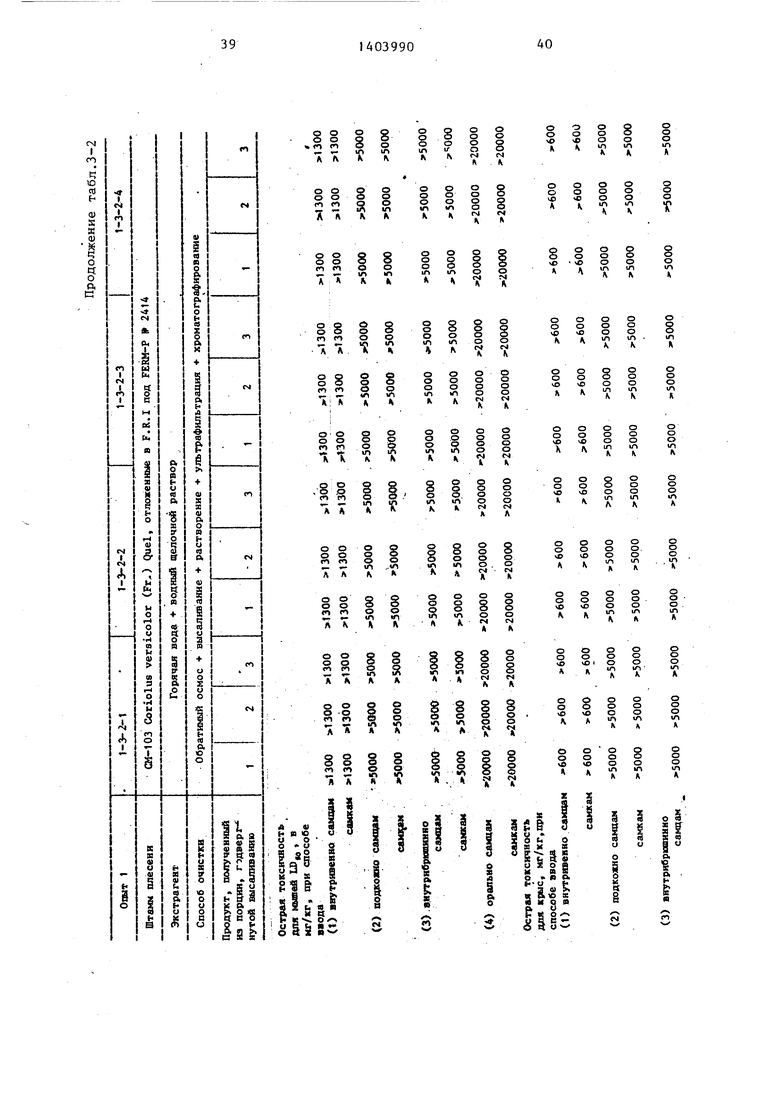
Часть (7,2 л) водного раствора экстракта (12,3 л), приготовленного из 100 г очищенного материала, упЬ- мянутого вьше, подвергают обратному осмосу. Операцию обратного осмоса осуществляют 4 раза при соответствующих условиях, т.е. давлении 20 кг/см и времени операции 3 ч в серии 1-3- 2-1; давлении 20 кг/см и времени операции 4,5 ч в серии 1-3-2-2; давлении 29 кг/см и времени операции .5 ч в серии 1-3-2-2 и давлении 35 кг/см и времени .операции 5 ч в серии 1-3-2-4 и при общих и фиксированных условиях температуры 10 С в аппарате для обратного осмоса, снабженного мембраной, которая позволяет проходить только молекулам с молекулярным весом меньше 5000. Эти данные составляют 90 мас.% от объема .раствора порции 1,87 мас.% от объема раствора порции 2 и 84 мас.% от объема раствора порции 3 стадии высаливания по примеру 1. Полисахарид, по25 лического сульфата аммония; добав ние проводят к каждой порции при комнатной температуре и тем самым осуществляют высаливание полисаха да из водного раствора. Количеств
лученный в результате проведения ста- зо сульфата аммония, добавляемого в
дии высаливания, собирают фильтрацией и затем подвергают растворению в дистиллированной воде.
Каждый из полученных таким образом водных растворов полисахарида из порции соответствующих .опытов подвергают ультрафильтрации в ультрафильтре, оснащенном мембраной,как и в опыте 1-3-1 для удаления сульфата аммония, присутствующего в вод- ном растворе с использованием той же i методики, которая была указана для
второй ультрафильтрации в опыте 1- 3-1.
35
40
каждую из порций раствора, оставш ся в аппаратуре для обратимого ос моса при проведении каждого из оп тов, представлено в табл.2-1.
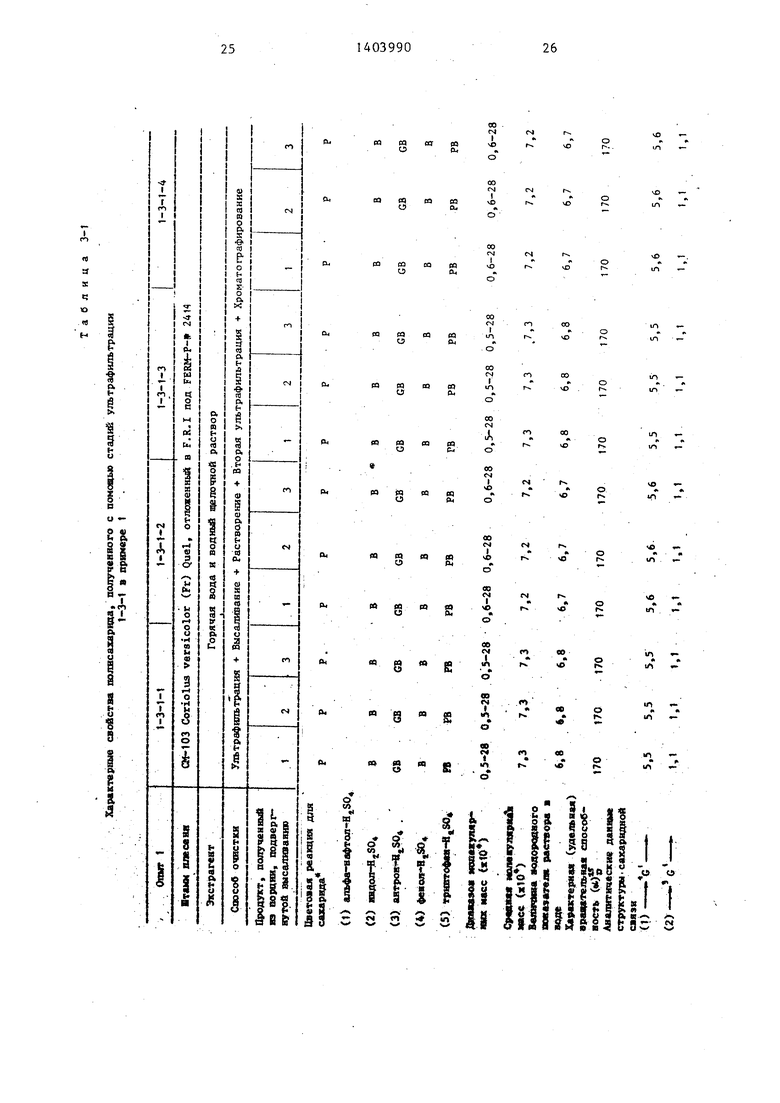
1-4. Измерение характеристик п лагаемого полисахарида.
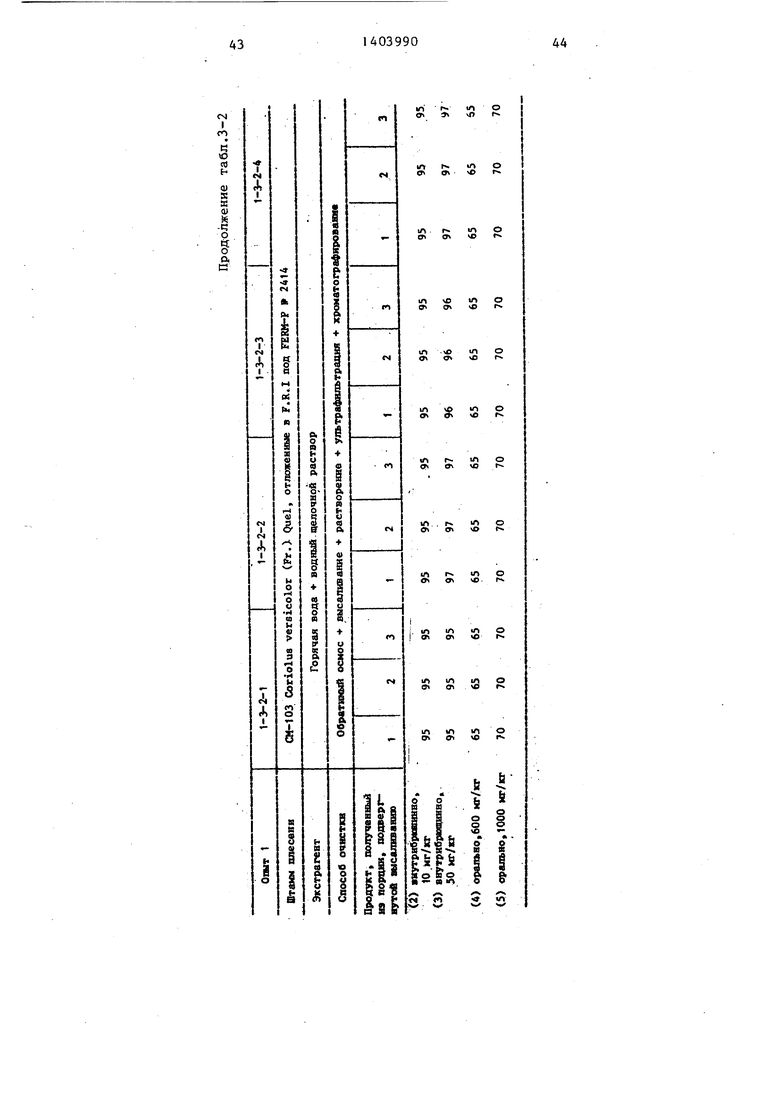
Характеристики, включающие стр турные характеристики и противооп холевые активности, полисахаридов полученные при помощи представлен ного выше процесса, показаны табл.3-1 и 3-2.
1-4-1. Спектр поглощения инфра
Водный раствор, оставшийся в уль- трафильтре после завершения операций ультрафильтрации, подвергают хромато графированию на колонке с использованием той же методики, которая бьша указана при проведении хроматографи- рования на колонке в опыте Т-3-1 для удаления азотсодержащих материалов, содержащихся в качестве примесей в водном растворе; концентрация полисахарида в водном растворе, оставшемся в ультрафильтре после завершения операции ультрафильтрации, является равной 1 г/100 мл для порции 1;равно
8 г/100 мл для порции 2 и равной
3 г/100 мл для порции 3 по каждому из опытов обратимого осмоса (т.е. опытов 1-3-2-1, 1-3-2-2, 1- 3-2-3 и
1-3-2-4).
Выходящий раствор, который пропускают через колонку и очищают от азотсодержащего материала с помощью адсорбента в колонке, собирают,
конденсируют при пониженном давлении и сушат с получением в результате очищенного полисахарида.
Условия и результаты, полученные при проведении указанной очистки водного экстракта, содержащего полисахарид, проведенной в соответствии со способом 1-3-2, представлены в табл.2-1 и 2-2. Раствор, оставленный в аппарате для обратного осмоса
после завершения каждого из опытов по обратному осмосу, разделен на 3 равные части (порция 1, порция 2 и порция 3) и затем проводят добавление определенного количества кристаллического сульфата аммония; добавление проводят к каждой порции при комнатной температуре и тем самым осуществляют высаливание полисахарида из водного раствора. Количество
сульфата аммония, добавляемого в
5
0
каждую из порций раствора, оставшегося в аппаратуре для обратимого осмоса при проведении каждого из опытов, представлено в табл.2-1.
1-4. Измерение характеристик предлагаемого полисахарида.
Характеристики, включающие структурные характеристики и противоопухолевые активности, полисахаридов, полученные при помощи представленного выше процесса, показаны в табл.3-1 и 3-2.
1-4-1. Спектр поглощения инфра
красных лучей,
Спектр поглощения инфракрасных лучей образца полисахарида измеряют в соответствии со спобом использования таблетки бромида калия. Таблетка, используемгш в этом способе приготовлена при помощи смешивания 1 г КВг с количеством около 1/3 до 1/2 мерной лопаточки образца в соответствии с общим способом. Поглощение отмечено при диапазонах, см : 3600- 3200; 2920-2900; 1660-1610; 1460.; 1410; 1360; 1230; 1150; 1080; 1060 - 990; 925; 840; 755; 705. Поглощение
при 840 см характерно для ot- -соединений сахаридов. Это свидетельствует о том, что данное вещество состоит из глюкозита о(. -соединения.
1-4-2. Удельное вращение.
Оптическое вращение измерено при помощи D-лучей (589 мкм) натрия при использовании 0,25%-ного водного . раствора образца и 5 см элемента и удельное вращение вычислено (о)р из вращения Ь .
1-4-3. Молекулярный вес.
Молекулярный вес полученного таким образом полисахарида измерен при помощи использования способа ультрацентрифугирования. Результаты показывают,что молекулярный вес всех измеренных образцов находится внутри диапазона от 5000 до 300000. Для измерений использовалось условие равновесия осаждения и синтетической граничной структуры с применением оптической системы интерференции. Экспериментальные условия следующие: концентрация образца, 0,3% растворителя, М/10М КС1; температура 25 С, столб жидкости 1,7 мм; скорость 22000 об/мин, время измерения 5 ч.
1-4-4. Составляющая сахарида в по лисахариде.
Составляющую моносахарида в полученном таким образом полисахариде анализируют следующим образом. В стеклянную ампулу вводят 3 мг образца с добавлением 10 мл 3%-ного раствора метанола хлористого водорода,метано- лиз осуществляют в течение 16 ч при 100 С и затем нейтрализуют хлористоводородную кислоту при помощи карбоната серебра, прореагированную смесь отфильтровывают при комнатной температуре. Фильтрат конденсируют, выпаривают до сухого состояния, остаток растворяют вО,5мя сухого пиридина.
Раствор смешивают с 0,2 мл гекса- метилдисилазона и 0,3 мл триметил- хлорсилана, и смесь оставляют при комнатной температуре на 30 мин для осуществления триметилсиляции. После ее окончания смесь растворяют в хлороформе, и после удаления избытка реагента при помощи промьюочной во- ды полученный раствор выпаривают до . сухого состояния t Остаток растворяют в тетрахлориде углерода и производят анализ при помощи газовой хроматографии. Результаты анализа показывают, что глюкоза составляет более 90% сос0
тавляющих сахарида данного вещества (полисахарида), а другие сахариды, такие как манноза, галактоза, ксилоза, фукоза и др. составляют очень малое количество.
Для того, чтобы определить конфигурацию (D-форма или ei -форма) глюкозы, как основной составляющей предлагаемого полисахарида, полисахарид подвергают гидролизу, глюкозу, изолированную от гидролизата при помощи хроматографической колонки, подвергают анализу понижения точки плав5 ления после смеси с подлинным образцом D-глюкозы. В соответствии с результатами, что точка плавления смеси была той же самой, что и подлинного образца и образца гидролизата, найдено, что глюкоза предлагаемого полисахарида имеет D-форму.
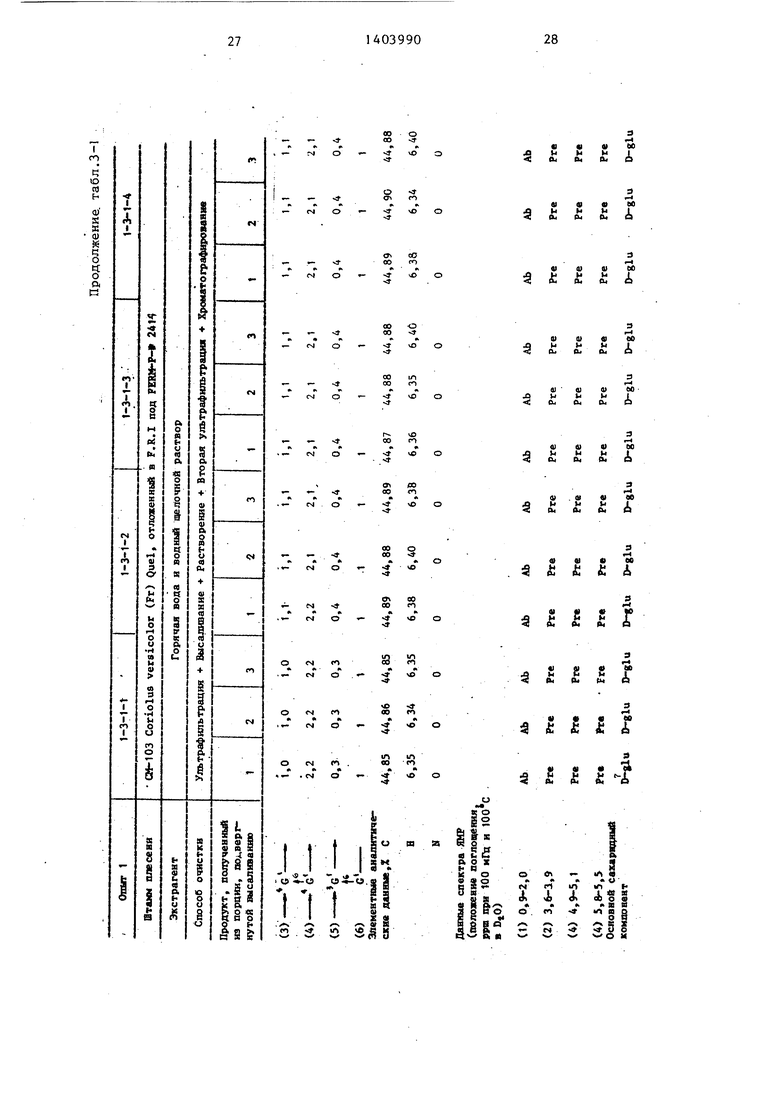
1-4-5. Структура соединения сахарида. I
5 Структура соединения сахарида в данном веществе определялась в соответствии со способом Howorth.
В 10 мл раствора 1 н. гидроокиси /натрия растворяют 2 г образца и при этом раствор поддерживают при 40-50°С в потоке азота и строгом перемешивании, по каплям в раствор в течение нескольких часов добавляют 20 мл диметилсульфата и 40 мл 30%-ного водного раствора гидроокиси натрия и оставляют смесь на ночь. После чего смесь была подвергнута обработке при помощи метилирования с использованием такого же количества агентов метилирования, После нейтрализации реакционной смеси ее.диализи- руют проточной водой и диализат конденсируют при пониженном давлении и затем подвергают такой же обработс ке метилированием, как ранее, три раза.
После завершения окончательной нейтрализации и диализа полученный диализат выпаривают до сухого состояния при пониженном давлении и остаток растворяют в 20 мл смеси с соотношением 10:1 хлороформа и метанола. К полученному таким образом раствору добавляют смесь с соотношением 1:1 петролейного эфира и простого эфира, чтобы осадить метили рованное вещество. Затем 20 мг метилированного вещества подвергают гидролизу с водным раствором 1 н.серной
0
5
0
0
5
9
кислоты в течение 16 ч при , и гидролизат превращают в алдитолаце- тат в соответствии со способом для измерения его молярного отношения при помощи сравнения зон пиков его хроматограммы. Для определения разницы между 2,3,6-три-О-метилглюко- зой и 2,3,4-три-О-метилглюкозой, 20 кг метилированной глюкозы подвергают метанолизу при 100 С в течение 16 ч в герметичной ампуле при использовании 3%-ного спиртового раствора хлористого водорода. В результате хроматографического анализа продукта метанолиза не обнаружено 2,3,4- три-0-метилглюкозы.. Для подтверждения каждьй из разлагаемых продуктов подвергают идентификации с газовой хроматограммой подлинного вещества, при этом каждый гидролизат изолирован при помсяци хроматографической колонки и кристаллизовался или превращался в кристаллические производные вещества.
Условия проведения процесса, параметры процесса и некоторые результаты, полученные при проведении стадии ультрафильтрации для очистки водного экстракта штамма СМ-103 Coriolua versiolor (Fr) Quel
0,5
U5840280 (порция 1)
280 (порция 2) 280 (порция 3)
2,5380126 (порция 1)
126 (порция 2) 126,6 (порция 3)
403990
Формула
10 изобретения
Способ получения полисахаридов, включающий экстракцию растительного материала, отличающийся тем, что, с целью раапирения арсенала биологически активных средств, в качестве растительного материала используют мицелий грибов рода Corio- lus, экстракцию проводят 0,1-0,4 н. водным раствором едкого натра при 93-97 С, полученный экстракт подвергают ультрафильтрации при давлеНИИ 0,5-5,0 кг/см или обратному осмосу при давлении 20-35 кг/см , затем вводят 84-90 об.% сульфата аммония и полученный осадок растворяют в воде до образования 3-10%-ного раствора с последующей его очисткой сначала ультрафильтрацией при давлении 0,5-5,0 кг/см и затем в ионообменной диэтиламиноэтилцеллюлозной колонке концентрированием раствора
и сушкой целевого продукта.
Таблица 1-1
(90) (87) (84)
2,8/280 2,8/280 2,8/280
113,9/126,9 (90) 2,8/280 110,1/126,6 (87) 2,8/280 106,3/126,6 (84) 2,8/280
1-3-1-3 3,0
150
1-3-1-4 5,0
2,5110
5,0 0,5
12,5/25 (10)
1,5 2,5/31,2 (8)
Стадия растворения
Концентрация полученноговысаливанием полисахарида в дистиллированной воде, г/мл
45/50 (90)2,8/280
43,5/50 (87)2,8/280
42/50 (84)2,8/280
32,9/36,6 (90)2,8/280
32/36,6 (87)2,8/280
30,8/36,6 (83)2,8/280
Таблица 1-2
2,5/31,2 (8)
2,5/83,3 (3)
2,5/83,3 (3)
2,5/83,3 (3)10
2,5/83,3 (3)
2,5/25 (10)
2,5/25 (10)
2,5/25 (10)10
2,5/25 (10)
2,5/31,2 (8)
2,5/31,2. (8)
2,5/31,2 (8)10
2,5/31,2 (8)
2,5/83,3 (3)
2,5/83,3 (3)
2,5/83,3 (3)10
2,5/83,3 (3)
2,5/25 (10)
2,5/25 (10)
45
1,3
45
1,3
45
45
1,3
15
2,5/25 (10)
2,5/25 (10) 2,5/31,2 (8) 2,5/31,2 (8) 2,5/31,2 (8)
2,5/31,2.(8) .2,5/83,3 (3)
2,5/83,3 (3) 2,5/83,3 (3)
2,5/83,3 (3) 2,5/25 (10) .2,5/25 (10) 2,5/25 (10) 2,5/25 (10) 2,5/31,2 (8)
2,5/31,2 (8) 2,5/31,2 (8)
2,5/31,2(8)
2,5/83,3(3)
2,5/83.3(3)
2,5/83,3(3)
2,5/83,3(3)
Т403990
16 Продолжение табл,1-2
45
1,3
45
1,3
45
1,3
45
1,3
45
1,3
45
Условия проведения процесса, параметры процесса и некоторые результаты, полученные при проведении стадии обратного осмоса для очистки водного экстракта штамма СМ-103 Coriolus versicolor (Fr) Quel
20 3 300 100 (порция 1)
100 (порция 2) 100 (порция 3)
20 4,5 180 60 (порция 1)
60 (порция 2) 60 (порция 3)
29 5 150 50 (порция 1)
50 (порция 2) 50 (порция 3)
35 5 110 36,6 (порция 1)
36,6 (порция 2) 36,6 (порция 3)
90/100 (90) 7/100 (87) 84/100 (84) 4/60 (90) 52,2/60 (87) 0,4/60 (83) 45/50 (90) 43,5/50 (87) 42/50 (84) 32,9/26,6 (90) 32/36,6 (87) 30,8/36,6 (84)
2,8/280
2,8/280
2,8/280
2,8/280
2,8/280
2,8/280
2,8/280
2,8/280
2,8/280
2,8/280
2,8/280
2,8/280
10 10 10 10
45
45
45
45
1,3
1,3
1,3
21
1403990
Продолжение табл.2-2
4 я
1,5
5,0 0,5 1,5 1,5 5,0 0,5 1,5 1,5 5,0
4,5
1
1,5
1,5
4,5 1
1,5
4,5
1
Продолжение табл.2-2
10
10
10
45
45
45
1,3
1,3
1,3
II I г III
III г I- I I I I
Ilir III
I I I I I II I I
« . M
4 (k я
l-l « «) M
Й i: г
a
t-i
0 о w
I I i
. I ,1 I r 9 s s Й Г
} Й4 1 Й
К s г
SQ 04 04
« я
Ii
«U
Q 0.4 Q
I s s
,318 8
о
2 5
л- Я& G
9 я tt.f О NO
« -; -ЗЛязт V т «и
J, 4vA 8|is| 8 S 82
.n- r-« Slils
9 в e H
- N ajXet «)/-4
«4- n-«ЭйЖйв oSSBB a
o -Ф
(M CO sr
III
I I I I I
A P4- A
« V tt9tf
i: I
I I I.I € I
i I I I I 5 I
04 -cQ
I 111 I
I s s
8
о
2 5
G
О NO
S 82
o -Ф
s;
00
(M CO srlO O
о о о
1Л
о о о
1Л
л
о о о in к
о о о .
1Л А
о о о
U-I
g
о «л
К:
SI
ж «1
§
13,
|.
&
Ч
Cvf
А
-
CSI
о
я
м
о
А
гч
°
см
п
А
о
м
I
о
о
«.
сч
ГЛ
О
«41
к «
- i
о
А
го
о
а
ч
ts
ел
А
О
О
«
(S
1Г
о
о
А
м
о
- «- м
см
1ч
- о
s
41 1
о
о ш
ч -о
о
А М
in
«
о
см «л
«
- о
о «л
к « о о
g
S
g
S
g
S S
9
S( 9(
S
.ge|i:|
л a W о Bl о я
iriflirJ I 8 i IS S
|в|8|а|
/-. о рьЕ|Е|о.-ч
sli&a&lisc
Авторы
Даты
1988-06-15—Публикация
1978-01-26—Подача