00
ел
Изобретение относится к новым соединениям, а именно к диаминовым комплексам платины (II), проявляющим противоопухолевую активность.
Цель изобретения - изыскание но-, вых соединений, проявляюдах более высокую противоопухолевую активность по сравнению с известными.
Пример 1. цис-Циклопента- метиленмалонат-1,1-ди(аминометил)цик- логексанплатина (II).
20,65 г цис-дийод-151 ди(амино- метш1(циклопентанплатины (II) добавляют к раствору 11,55 г AgNOj в 85 мп воды. Затем раствор перемешивают в течение 10 мин при 95 100°С, Agl отфильтровывают и промывают водой. Пока фильтрат горячий, к нему добавляют раствор 5J 0323 г циклопентаметилен малоновой кислоты в i 14,34 мл 0,511 25 и. NaOH и полученную смесь нагревают s течение 12 мин при 95-100 С. Затем смесь охлаждают, остаток отфильтровывают с подсосом и промывают водой. После сушки при пониженном давлении, полученньш продукт экстрагируют 4 л метанола, метанольный раствор обрабатывают активированным углем, отфильтровывают до прозрачности и полученньш фильтрат выпаривают досуха при пониженном давлении. Остаток суспендируют в 500 мл спирта; отфильт- ровывают с подсосом и промывают ме- танолом. Выход 4,75 г.
Результаты элементарного анализа (вес.%):
Вычислено, %: С 37,86; Н 5,56; ;N 5,52; Pt 38,46.
Найдено,%: С 37,50; Н 5,50; N 5,60; Pt 38,19.
СН2 (кольцо): 1,3 уширенный син- глет; CH.J (у азота): 2,3 широкий пик Ж-г.: три пика 5,3; 4,7 и 5,9,
Все полученные соединения крис-- таллы очень бледного желтого цвета,,
Пример 2. цис-Д1ихлор-(2- -метил-2-этил) -1 .,3-пропандиаминпла- тину (II)формулы
СНз С1
:/ /Ч
),рХ )
СНз-СН2 СН2-КН2 С1
псшучают, исходя из (2 метил--2-этил)- -1,3-пропандиамина.
К раствору 8,05 г K PtCl4 в 80 мл воды добавляют раствор 13,2 г KI в
10 мл воды,и смесь нагревают в течение 5 мин на водяной бане при . После этого добавляют 2,5 г 2-метил- -2-ЭТИЛ-1,3-диаминопропана и после перемешивания полученной- смеси в течение 5 мин при 95°С осадок отсасывают и промывают водой (Зх) холодным этанолом (2х) и эфиром (2х) с образованием 9,5 г (84 мас.%) цис- дийод-(2-метил-2-этил)-1,3-пропанди- аминплатины (II).
5,65 г дийодопроизводного добавляют к раствору 3,23 г AgNC в 25 мл воды. После перемешивания раствора в течение 10 мин при 95°С (защищенного от воздействия света) Agl отфильтровывают и промывают водой.
К-прозрачному фильтрату добавляют 1,64 г КС и смесь перемешивают в течение 12 мин при 95 С. После охлаждения смеси осадок отсасывают и промывают водой. Выход 2,1 г (55 мас.%).
Вычислено, %: С 18,86; Н 4,22; N 7,33; PC 51,04; С1 18,85.
Найдено, %: С 18,73; Н 4,14, N 7,26; Pt 51,33; С1 18,69.
0,8 синглет + триплет; СН2(этш1): 1,2 квартет; СН2(у азота) 2,, 1 триплет; NH : три пика 4,9;, 5,5 и 4,2.
Пример 3, цис-дихлор-2,2- диэтил-1 З-пропандиаминплатину (TI) формулы
СН2 CHo-NH Ci
/ /
Г Рг
Л
СН2 CH2-NH2 С1
СИ
0
5
0
получают, исходя, из 2, 2-диэтил-1,3- -пропандиамина.
К раствору 4,45 г KjPtCL в 45 мп воды добавляют раствор 7,11 г KI в 5 мл ВОДЫ и смесь нагревают при в течение 5 мин на водяной бане. После этого добавляют 1,55 г бис-2- -этил- 1, 3-диамииопропана и после перемешивания полученной смеси в течение 5 мин при 95 С осадок отсасывают, и промывают водой (Зх), холодным этанолом (2х) и эфиром (2х) с образованием 4,2 г (72 Maci%) цис-дийод-2,2- -диэтил-1,3-диаминопропанплатины (II).
3 г дийодного производного добавляют к раствору 1,53 г AgNOj в 12 мл воды. После перемешивания в течение 10 мин при 95 С (при защите от воз31414850
действия света) Agl фильтровывают и :
промывают водой.
К прозрачному фильтрату добавляют 0,745 г КС1 и полученную смесь перемешивают в течение 12 мин при 95°С. После охлаждения смеси осадок отсасывают и промывают водой.
Выход 1,4 г. (70 мас.%).
Вьиислено, %: С 21,22; Н 4,58; N 7,07; Pt 49,24; С1 17,89.
Найдено, %: С 21,04; Н 4,50; N 7,02;/Рс 49,43; С1 17,83.
2 СНз : 0,8 мультиплет; СН2(этш1): 1,8 мультиплет; азота) 2,2 триплет; три пика 4,9; 5,5 и 4,3.
Пример 4. цис-Дихлор-1,1- -ди(аминометил)циклопентанплатину (II) формулы
Q(
ОН2-/Н2
(ИП
получают, исходя из 1,(аминометил ) цикпопентана .
К раствору 3,6 г KyPtCl в 35 мл воды добавляют раствор 5,7 г KI в 8,5 мл воды и смесь нагревают в течение 5 мин при 95 с на водяной бане.
После этого добавляют 1,1 г 1,1- -ди(аминоэтил)циклопентана и после перемешивания смеси в течение 5 мин при 95°С осадок отсасывают и промывают водой (Зх), холодным этанолом (2х) и эфиром (2х) с образованием 3,5 г (70 мас.%) цис-дийод-1 ,-1-ди (аминоэтил)циклопентанплатины.
3,2 г дийодопроизводного добавляют к раствору 1,83 г AgNO в 15 мп воды. После перемешивания раствора в течение 10 мин при (при защите от действия света) Agl отфильтровывают и промьшают водой. К прозрачному фильтрату добавляют 0,9 г КС1 и смесь перемешивают в течение 12 мин при 95°С.
После охлаждения смеси осадок отсасывают и промьшают водой. Выход 1,6 г (76 мас.%).
Вычислено, %: С 21,33; Н 4,09; N 7,11; Pt 49,49; С1 17,98.
Найдено,- %: С 21,36; Н 4,10; N 7,14; Pt 49,27; С1 17,91.
СНл(кольцо): 1,5 мультиплет; азота): 2,2 триплет; NHj: три пика 4,9; 4,3 и 5,5.
П р и м е р 5, цис-1, 1-Ди (аминометил) циклогексанплатина (II) сульфат формулы
(|у;
,yCH2-NH2
(л Ptso.
- CH2-NH2
2 г дийодопроизводного
-4/CH2-NH2X./J W CH2-NH2 3
суспендируют в 150 мл воды.
После перемешивания в течение 20 ч с 1,0 г AgjSO Agl отфильтровывают и промывают HjO. Прозрачный фильтрат, выпаривают.
Выход 1,1 г (80 мас.%).
Вычислено, %: С 22,17; Н 4,19; N 6,46.
Найдено, %: С 22,02; Н 4,62; N 6,31.
СН2(кольцо): 1,4 широкий синглет; СИ2 (у азота): 2,2 широкий пик; КНг: 4,5-6,5 широкий сигнал.
Пример 6. цис-Дихлор-1,1- -ди(аминометнл)циклобутанплатина (II) формулы
/. CH2-NH2 С1
х. р
/ СНо-NH С1
(V)
2,8 г 1,1-ди(аминометил)циклобу- тана, 2 г НС1 и 6,2 г растворяют в 50 мл воды, нагревают до 95-100°С и к раствору добавляют по каплям 1,2 г NaOH в 25 мл воды настолько быстро, чтобы поддерживать рН при t 6. Полученный при этом осадок -отфильтровывают с подсосом, промы50
55
вают водой и высушивают. Полученный продукт помещают в 250-300 мл раствора NH и отфильтровьшают. После выпаривания NH, продукт промывают 2 Н. НС1, водой и высушивают.
Выход 3,7 г (65 мас.%).
Вычислено, %: С 18,96; Н 3,71; N 7,37; Pt 51,31; С1 18,65.
Найдено, %: С 18,95; Н 3,67; N 7,37; Pt 51,02; С1 18,47.
5141А850
СН(кольца): 1,4 широкий синглет; CHj (у азота): 2,4 триплет; NHj: три пика 4,9; 4,3 и 5,5.
Пример 7. 1 ис-Дихлор-2,2- g -дибензил-1,3-пропандиаминплатину (II) формулы
ду во
N
N
NH, С1 рУ
/ NHo Ci
(VI)
получают, исходя из 2,2-дибензил-1,3- -пропандиамина.
1,4 г бис(2-бензил)-1,3-диамино- пропана, 0,4 г НС1 и 2,28 г KjPtCl 20 МП воды, нагретой до
растворяют в 95 С, и к полученной смеси по каплям добавляют раствор 0,5 г NaOH в 15 мл воды так быстро, чтобы поддерживать рН на значении t6.
После охлаждения осадок отсасывают, промывают водой и сушат. Продукт
растворяют в 200-250 мл жид- 1 и фильтруют. После вьшаривареакциикого NH,
НИН NHj продукт промывают 2 N раствором НС1, водой и сушат.
Выход 1,3 г (45 мас.%).
Вычислено, %: С 39,24; Н 4,26; N 5,38.
Найдено, %: С 39,81; Н 4,38; N 5,73.
СНг (у азота): 2,3 широкий пик; CHj (бензил): перекрыт ДМСО; NH,: тр пика 5,1; 4,5 и 5,7.
Пример В. цис-Дихлор-2,2- -дии 3 опр опил-1,3 пр оп андиаминпл атина (II) формулы
СНз
СН CH2-NH2 С1 CHs
СНз / /
снр-кно С1
СН5
(VII)
Найдено, %: N 5,55.
Пример
1,1-Ди(аминоГ
1,6 г бис(2-изопропил)1,3-диаминопропана, 0,73 г НС1 и 4,15 г KiPcCLf go метил)циклогексанмалонато1шатина (II),
имеющая формулу
О
растворяют в
, и к этому раствору по
50 ми воды, нагретой до
каплям
добавляют раствор 0,9 г NaOH в 10 мл воды настолько быстро, чтобы поддерживать рН на значении ±6. Образовавшийся осадок отсасывают и промывают водой. После сушки продукт растворяют в 250-300 МП жидкого аммиака и фильтруют. После вьтаривания Ш про5S
0(,
СН2NH2pV /
ОCH2-NH2 0-С О
g
%: С 25,48; Н 5,23; : С 26,31; Н 5,39;
0
15
0
дукт промывали 2 N раствором НС1, водой и сушат.
Выход 1,0 г (24 мас.%).
Вычислено, N 6,60.
Найдено, 5 N 6,90.
Пример 9. цис-Дихлор-2,2- -диизопропил-1,3-пропандиаминплатину (II) формулы (VIII) получают, исходя из 2,2-диизопропил-1,3-пропандиамина, аналогично примеру 6.
Вычислено, %: С 25,48; Н 5,23; N 6,60.
Найдено, %: С 26,31; Н 5,39; N 6,90..
CHj: 0,9 дублет; NH сигнал..
Пример 10. 1,1-Ди(аминоме тил)циклогексан-бис(хлорацетато)платина (II),имеющая формулу
ji 4,6 широкий
-СНо
о
nu.NH2 о
CH2-NH2 0
О
II
C-CHgCl . (Vlir) C-ChbCl
II о
1,6 г дихлорпроизводного, полученного согласно примеру 2 (формула IV), добавляют к раствору 1,28 г AgNGj в 25 МП воды. После перемешивания смеси в течение 1 ч при AgCl отфильтровывают и промывают водой. К прозрачному фильтрату добавляют раствор 0,73 г монохлоруксусной кислоты и 0,45 г КОН в 25 мл воды и полученную смесь перемешивают в течение 2 ч при комнатной температуре. Осадок отсасывают и промывают водой. Выход 1,3 г (65 мас.%).
Вычислено, %: С 27,49; Н 4,23;
N
5,34,
Найдено, %: N 5,55.
Пример
С 27,43; Н 4,21;
1,1-Ди(аминоГ
метил)циклогексанмалонато1шатина
0(,
СН2NH2pV /
ОCH2-NH2 0-С О
1,6 г дихлорпроизводного
../
7
CH2-NH2
р
С1
С1
добавляют к раствору 1,28 г AgNC з 25 мл. воды. После перемешивания смеси в течение 1 ч при 40 С AgCl отфильтровывают и промывают водой. К прозрачному фильтрату добавляют раствор 0,4 г малоновой кислоты и 0,455 г КОН в 10 мл воды. После перемешивания в течение 2 ч при комнатной температуре осадок отфильтровывают И сушат. Выход 1,0 г (59 мас.%).
Вычислено, %: С 30,07; Н 4,59; N 6,38; Pt 44,40; О 14,57.
Найдено, %: С 29,98; Н 4,54; N 6,32; PC 44,32; О 14,57.
В таблице приведено также соединение формулы
О
11
NH2 О-С
Р
NH2 0-С
О
)о
:(х)
414850°
наиболее опасной и ограничивает дозировку, которую можно, применять на практике.
Предлагаемые соединения не оказывают каких-либо вредных побочных эффектов на почки. Это установлено путем гистологического исследования крыс после воздействия на них токси10 ческих доз новых соединений, тогда как при аналогичном изучении с помощью ЩЩ установлены серьезные поражения почек.
Новые комплексы не оказывают также
15 и вредного влияния на деятельность почек,- Основной метод определения почечной токсичности заключается в оценке тгроцентного количества моче- винного азота в крови (мочевинньй
20 азот крови, BUN), который также определяется как непротеиновый азот NPN.
Формула изобретения
25 Диаминовые комплексы платины (II) общей формулы
R, CH.-NH. А
СНг- NH, /
/
R,
/Ч
CHj-NH
Pi / Ч



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения платино-диаминовых комплексов | 1979 |
|
SU1160937A3 |
| Платино ( @ )-диаминовые комплексы,проявляющие противоопухолевую активность | 1981 |
|
SU1186617A1 |
| Способ получения платино (1у)-диаминовых комплексов | 1980 |
|
SU1083911A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИС-ДИХЛОРОДИИЗОПРОПИЛАМИНПЛАТИНЫ(II) | 2007 |
|
RU2360866C1 |
| Способ получения производных - 7- -аминодезацетоксицефалоспорановой кислоты в виде смеси цис и трансизомеров или в виде одного из них | 1972 |
|
SU466662A3 |
| СПОСОБ ПОЛУЧЕНИЯ ТРАНС-ДИХЛОРОМЕТИЛАМИНИЗОПРОПИЛАМИНПЛАТИНЫ (II) | 2011 |
|
RU2464231C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТРАНС-ДИХЛОРОМЕТИЛАМИНЭТИЛАМИНПЛАТИНЫ (II) | 2011 |
|
RU2464232C1 |
| Способ получения замещенных аминодикислот,их рацематов или оптических изомеров,или их фармацевтически приемлемых солей | 1981 |
|
SU1153827A3 |
| В П Т Б | 1973 |
|
SU404233A1 |
| ТРЕХПЛАТИНОВЫЕ КОМПЛЕКСЫ PT(II), СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2140422C1 |
Изобретение касается металлоор- ганических веществ, в частности диаминных комплексов платины (2+) (КП) общей ф-лы -CH.;-NH,j-Pt(X),, R, R, - R, R, R R, - CHj где, когда R, - CH ; Rj Rf R - , TO 2X H3o-CjH,, TO X - Cl; когда SOj ; когда (R ( + Rj) - С4-С -циклоалкил, то X - Cl или 2X - S0|; или ,(0), или CH7C1-C(0)0- , которые способны проявлять противоопухолевую активность, что может быть использовано в медицине. Цель - создание новых более активных веществ указанного класса. Их синтез ведут обработкой соединения платины соответствующим диамином. Новые комплексы платины обладают высокой терапевтической активностью против различных форм рака без проявления токсикоза к почкам и других нежелательных побочных эффектов. Степень ингибирования в сравнении с контролем составляет при дозе 2 мг/кг (внутрибрюшинно) 197%. 1 табл.а (Л
Исследования показывают, что предлагаемые соединения обладают высокой терапевтической активностью против рака. В отличие от платиновых комплексов, применяемых для борьбы с раком, таких как цис-платинадиаминди- хлорид (ПДЦ), также обнаружено, что предлагаемые соединения проявляют лишь незначительную токсичность по отношению к почкам или не проявляют ее совсем.
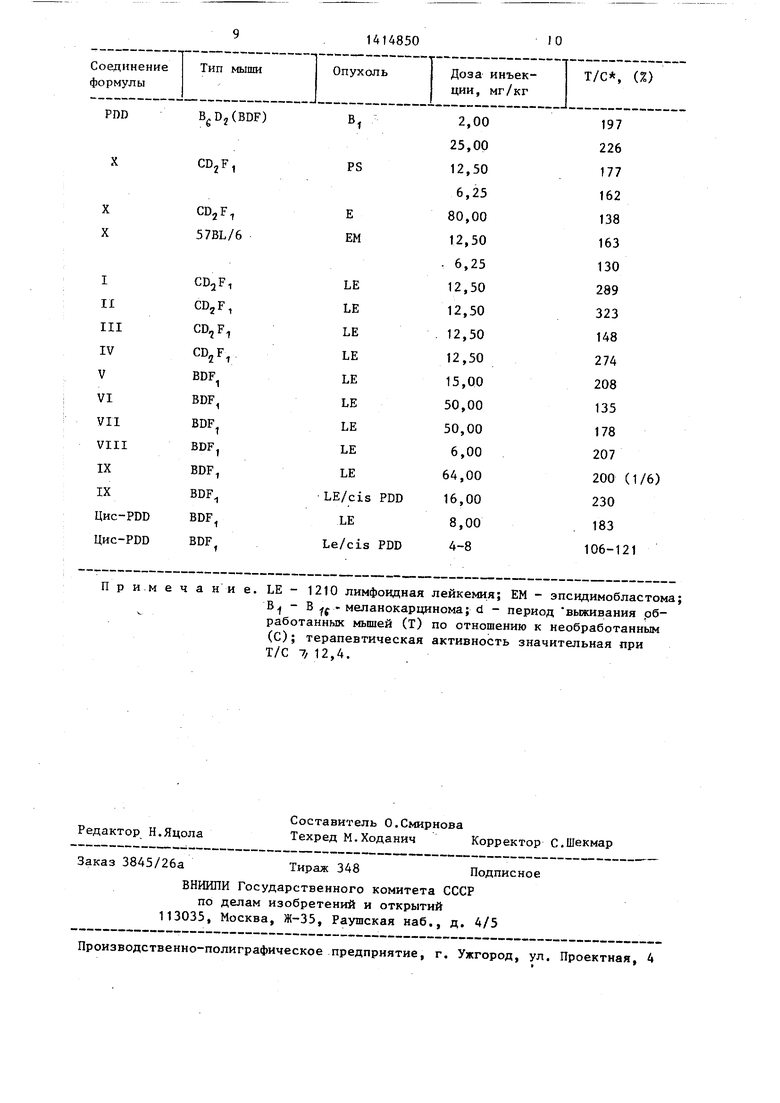
Новые соединения проявляют противоопухолевую активность против большого числа различных типов опухолей, таких как Р-388 лимфоцитная лейкемия, L 1210 лимфоидная лейкемия, эпедимо- бластома и В 16 меланокарцинома. Терапевтическая активность новых соединений выше, чем у ПДЦ, который используют .в качестве экспериментального клинического хемотерапевтическо- го средства (табл.).
Недостатком применяемого на практике ПДЦ, как и всех других известных противоопухолевых платиновых комплексов, является высокая токсичность, причем почечная токсичность является
где R - RI -
R Rj - - 5R R2 - изо CjH,, тогда X хлор, или когда R, R - CjHj, тогда 2X
или когда R и R вместе образуют 4-б-членнре циклическое кольцо, тогда X - хлор, 2Х - SO/ , или
О -0-С-СН2С1
о
5 -О-С
-о-с
) или
о
-О-С-СНгСГ
о
проявляющие противоопухолевую активность.
Приоритет по признакам: 06.07,78 2х SO или
О
55
-О-С
сХЗ
п о
FDD
BgDjCBDF)
I
PDD
PDD
,
, 57BL/6
, CDjF, CD,F, CDjFy BDF,
BDF, BDF BDF,
BDF, BDF BDF BDF,
PS
E EM
LE
LE
LE
LE
LE
LE
LE
LE
LE LE/cis PDD
LE Le/cis PDD
n p И.М e ч a ни e. LE - 1210 лимфоидная лейкемия; EM - эпсидимобластома;
Б - В j. - меланокарцинома; d - период выживания .обработанных мьшей (т) по отношению к необработанным (С); терапевтическая активность значительная при Т/С 7/ 12,4.
2,00 5,00 12,50
6,25 0,00 12,50 6,25 12,50 12,50 12,50 12,50 15,00 0,00 0,00
6,00 4,00 16,00
8,00
4-8
197 226 177 162 138 163 130 289 323 148 274 208 135 178 207
200 (1/6) 230 183 106-121
| Chem arid Eng News | |||
| Шеститрубный элемент пароперегревателя в жаровых трубках | 1918 |
|
SU1977A1 |
| Солесос | 1922 |
|
SU29A1 |
| Cancer | |||
| Chemotherapy Reports | |||
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
| I, T | |||
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| МАШИНА ДЛЯ ПЕРЕРАБОТКИ ТОРФЯНОЙ МАССЫ | 1923 |
|
SU629A1 |
Авторы
Даты
1988-08-07—Публикация
1983-05-04—Подача