Изобретение относится к новым производным бициклооксифенипмочевины фор- НУЛЫ
(I)
де при М- СН- Х.Х, - Н, С1,
F;
V «.
Y Н, Н. Н,
С1, GH,,;
СН,; С1, СН
3
CF,
при условии, что R - Н, С1, OCHj, Н(СНз)2.
при условии, что
R
- С1, F, Н; Y - Н, С1, Yj - Н, С1, СНз, ОСИ
СН
S
R Н, С1, N(CH3)j, . -х Х. при
Р101„
Brt
э
Y Н,
- Н, F, С1; Y
ри М - N; X - С1; Хц - Н; Y - С1;
Jf, Y - Н,
проявляющим пест йцидную активность.
Цель изобретения - изыскание новых соединений общей формулы (I), Проявляющих более высокую по сравнению с известными соединениями Пестицидную активность.
Соединения согласно изобретению можно получить двумя различными способами. В первом способе бициклоокси анилин обрабатывают арилизоцианатом ,цля получения 1-(бициклооксифенил)-3 бензоилмочевины:
О
HzN ,Y -f
М, В,
ов
R имеют указанные
где.Х, Y, значения.
Предлагаемые соединения можно получить реакцией бициклооксифенилизо- цианата с амидом согласно следующей реакционной схемы;
У R.
О
25
R имеют указанные
0
5
0
5
0
5
Реакции в обоих способах протекают без необходимости использовать дополнительные реагенты. Однако предпочтительно использовать органический растворитель. Обычно пригоден любой растворитель, который инертен по отношению к реагентам, а именно ароматические углеводородные и галоид- замещенные углеводородные растворители (толуол и 1,2-дихлорэтан),Эти ре- акции, как правило, протекают в широком интервале температур.
Бициклооксианилин получают реакцией бициклического фенола с 4-хлор- олнитробензолом в присутствии основания в инертном растворителе при повышенной температуре, чтобы можно было получить нитрозфир. Подходящие основания включают гидрид натрия, гидрат окиси калия и карбонат калия. Подходящие растворители включают толуол, диметилформамид и диметилсульфоксид. Если реакция является гетерогенной, то можно добавить фазопревращающйй реагент (галоид четвертичного аммония или комплекс краунзфиров).
Восстановление нитроэфиров в анилин можно осуществить в атмосфере водорода, используя гетерогенный катализатор гидрогенизации. Такие катализаторы включают платину или палладий на инертном носителе, или никелевый катализатор Рэнея. Эти реакции восстановления можно проводить в широком
14
интервале температур и давлений. Однако предпочтительно использовать интервал давлений 5,6-8-,4 атм при комнатной температуре. Выбираемые растворители включают ароматические углеводороды (толуол) или спирты (этанол) . Восстановление можно также осуществить химическим восстановителем (переходный металл или его соли), в растворе неорганической кислоты, олово или железо, либо их соли в соляной кислоте. Совместный растворитель (диоксан или спирты) можно добавить, чтобы улучшить растворимость реаген- тов в реакционной среде. Анилин можно превратить в изоцианат посредством реакций с фосгеном.
Пример 1. Получение 2,6-ди- фторобензоилизоцианата.
Смесь, содержащую 30,26 г (0,193 моль) 2,6-дифторобензамида в 250 мл 1,2-дихлорэтана, помещают в атмосферу азота и охлаждают до 5 С. Затем к ней добавляют по каплям раствор 25,0 МП (34,8 г, 0,27 моль) хлористого оксалила в 50 мл 1,2-дихлорэтана. Во время этого добавления температуру поддерживают ниже 10 С. Полученную реакционную смесь затем перемешивают в течение 1/2 ч в ледяной бане. Последнюю удаляют, реакционную смесь, нагревают до комнатной температуры. После перемешивания при комнатной температуре в течение 1-1,5 ч реакционную смесь медленно нагревают с обратным холодильником. После нагревания с обратным холодильником в течение 5 ч реакционную смесь охлаждают до комнатной температуры . После удаления растворителя под вакуумом получают 31,77 г оранжевого масла. ЯМР (CDCl--,) ,6 : 6,6-7,7 (m) .
ИК (СНС1з), см : 3370, 2990, 2220, 1770, 1747, 1685, 1605, 1450.
Пример 2. Получение 1-( хлоро-1-нафтокси -З,5-дихлорофенил)- 3-(2,6-дифторобензоил)мочевины.
Для получения 4-(4-хлоро-1-нафто- кси)-3,5-дихлоро-1-нитробензола к смеси, содержащей 28,02 г (0,203 моль безводного карбоната калия и 30,26 г (0,134 моль) 3,4,5-трихлоро-1-нитробензола в 300 МП безводного диметил формамида в атмосфере азота при комнатной температуре добавляют 30,04 г (0,168 моль) 4-хлоро-1-нафтола. Колбу затем помещают в нагреваемую масляную баню. Температуру реакции 105°С
д
0
5Q
0 5
0
90,
поддерживают в течение 20 ч. После охлаждения реакционной смеси до комнатной температуры диметилформамид удаляют под вакуумом. Остаток поглощают в 1,5 л смеси 1:1 этилацетата:ди- этилового эфира и 300 мл Hi20. Слои разделяют и промывают дважды 5%-ным- NaOH, дважды HjO и один раз насьщен- ным водным раствором NaCl.После сущ- ки над безводным N33804 и удаления растворителей получают 48,73 г темно-коричневого твердого вещества.Это вещество перекристаллизовывают дважды из смесигвксана -этилацетата, чтобы полз чить 15,84 г бледно-желтых игл, т.пл. 121,5-123°С.1
ЯМР (CDClj),: 6,18 (d, Гц,1Н) 7,25 (d, Гц, 1Н); 8,4-8,7 (т, 2Н); 8,0-8,5 (т, 4Н, содержит 8,25 Sl).
Для каталитического восстановления 4-(4-хлоро-1-нафтокси)-3,5-дихлоро-1- нитробензола в качающийся гидрогени- затор емкостью 0,56 л загружают раствором 15,84 г 4-(4-хлоро-1-нафтокси)- 3,5-дихлоро-1-нитробензола в 250 мл толуола. К этой смеси добавляют 0,5 г 5%-ной платины на угле, затем автоклав закрывают, Водород подают до давления 7 атм. Давление водорода поддерживают от 5,6 до 7,0 атм до тех пор, пока не прекратилось поглощение водорода. Продукт удаляют из автоклава и фильтруют через целит. После удаления растворителей от фильтрата получают 13,99 г белого твердого вещества, т.пл. 145-147°С.
ЯМР (ДMCO-dб),(5: 5,72 (щирокий син- глет, 2Н), 6,38 (d, Гц, 1Н), 6,82 (S, 2Н), 7,3-8,7 (га, 5Н).
Для химического восстановления 4-(4-хлоро-1-нафтокси)-3,5-дихлоро- 1-нитробензола 37,47 г (0,1 моль) 3,5-дихлоро-4-(4-хлоро-1-нафтокси)- нитробензола осторожно добарляют к раствору 75,6 г (0,335 моль) хлорида олова (2), 67 МП НС1 и 50 мл диокса- на при 80 с. (Необходима механическая мешалка по причине вязкости полученной суспензии). Суспензию перемешивают еще в течение 30 мин при кипячении с обратным холодильником. Продукт охлаждают, а затем выливают в химический стакан, содержащий 134 г (3,3 моль) NaOH в 340 мл HgO с равным количеством льда. Белое твердое вещество отфильтровывают, поглощают в CHgClg и сушат. После удаления растверителей получают 32,21 г белого Твердого вещества.
Для получения 1-(4-.4-хлоро-1-наф- toKCH -3,5-дихлорфенил)-3-(2,6-ди- фторобензоил)мочевины раствор, содер- ащий 2,25 г (6,6 ммоль) 4-{4-хлоро- i -нафтокси) -3,5-дихлор.оанилина в 5 МП толуола, помещают в атмосферу 13ота и нагревают до , затем через дополнительную воронку добавляют 1,82 г (9,9 ммоль) 2,6-дифторобензо- 1|шизоцианата в 5 мл толуола. Получен- Йую смесь затем перемешивают при 70 С в течение 45 мин, а затем охлаждают До комнатной температуры. Затем ее с| хлаждают ниже О С и фильтруют. Собранное белое твердое вещество сушат под вакуумом, получив 1,86 г целевого Продукта, т.tin. 237-239 с.
ЯМР (ДМСО-а), : 6,47 (d, Гц,
Н); 7,0-8,6 (т, ЮН); 10,40, (широкий (|1инглет, 1Н); 11,60 (широкий синглет,
Н).
14251906
использовании обесцвечивающего угля, дает 22,04 г бледно-желтого твердого вещества, т.пл. 176-179°С,
ЯМР (СВС1э),сГ: 1,7-2,0 (га, 4Н); - 2,20 (S, 6Н); 2,7-3,0 (т, 4Н); 5,95
. (d, Гц, 1Н); 6,95 (d, Гц, 1Н); 8,02 (S, 2Н).
Для получения 4-(4-хлоро-5,6,7,81О тетрагидро-1-нафтокси)-3,5-диметил- анилина в однолитровый качающийся гидрогенизатор Парра помещают раствор, содержащий 19,11 г (4-(4-хлоро- 5,6,7,8-тетрагидро-1-нафтокси)-3,515 диметил-1-нитробензола в 600 мл толуола. К этой смеси добавляют затем 1,0 г 5%-ной платины на угле. Затем эту смесь помещают в атмосферу водорода под давлением примерно 7 атм.
20 Внутреннее давление поддерживают до тех ПОР, пока продолжалось поглощение водорода. Когда поглощение водорода прекратилось, выливают содержимое из гидрогенизатора и реакционный со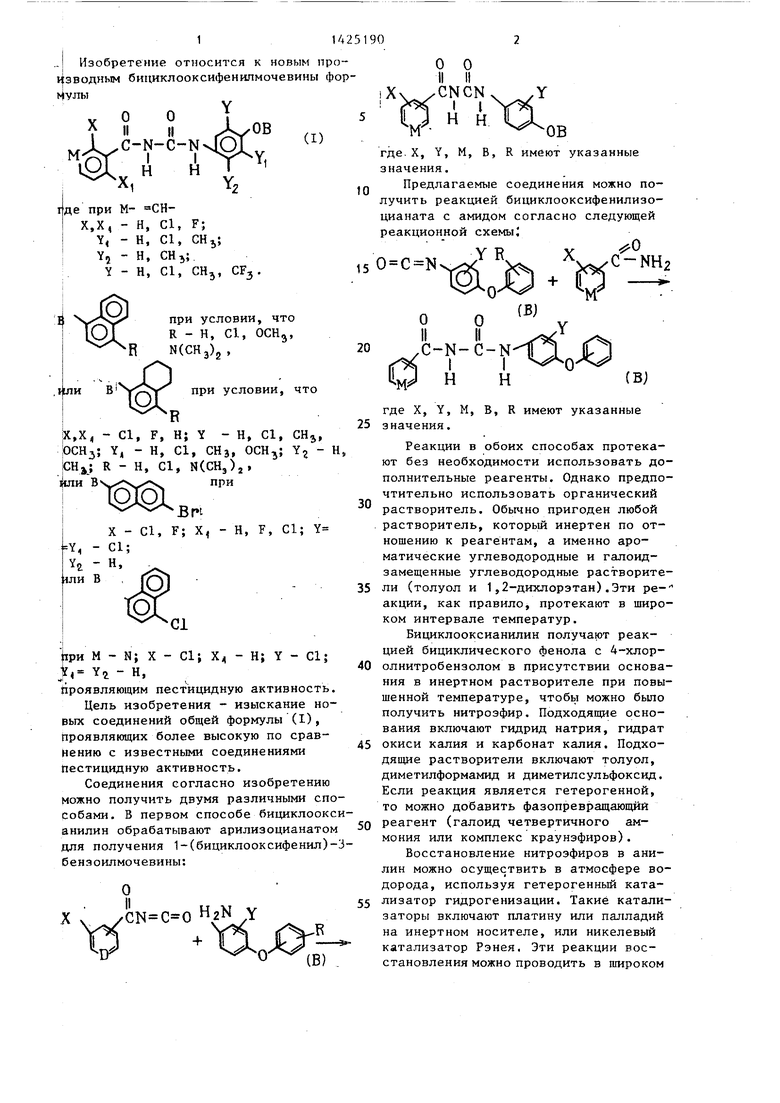







Изобретение касается замещенных мочевин, в частности производных би- циклооксифенилмочевины (ИМ) общей формулы x,o-cH-CH-M-cx«e-c№)-irt«-(omtt-c-cY,-CY,-ci(m)-cr-cH где а) МСН-; X и Xi - Н, С1, F; Y - Н, С1, СНэ, , СН,; X - Н, С1, СН, CF,, В-группы (II) (III) Bhiv) (V) при этом, когда В - группа (II), то R - Н, 01, ОСИ,,, N(CH5)e; когда В - группа (ill), то X и X, - С1, F, Н; - Н, С1, ОН,,, ОСК,; Y,j - Н, СНд; R - Н, С1, N(CH,)5; когп.а В - группа (IV), то X - С1, F; X, - Н, F, С1; - С1; Y, - Н; б) М - N; В - rpynna(V)5 X, - К; X - 01; Y - С1; Y Yi - Н, которые проявляют пести- цидную активность, что может быть использовано в сельском хозяйстве. - создание новых, более активных веществ указанного класса. Синтез ПК ведут либо обработкой бициклооксиани- лина арилизоцианатом, либо реакгщей бициклооксифенилизоцианата с амидом, преимущественно в среде растворителя. Новые ПМ обладают инсектицидной актив ностью против клещей, личинок южных ратньЕх червей на капусте, бо;кьей коровки при концентрации 8-10 г/мл со 100%-ной эффективностью. 9 табл. (Л 4iak сл со
ПримерЗ. По способу, описан- 25 суд промывают толуолом. Промывки в примере 2, получают также дру- смешивают с реакционной смесью. За- 1| ие бензоилмочевины.тем отфильтровывают через целит. По: Пример4. Получение 3-( еле удаления растворителей получают флоро-5,6,7,8-тетрагидро,-1-нафтоксиJ- 17,30 г бледно-желтого твердого веще30
3,5-диметилфенил)-1-(2-хлоробензоил) мочевины.
Для получения 4-(4-хлоро-5,6,7,8- етрагидро-1-нафтокси)-3,5-диметил- i-нитробензола к раствору 35,62 г (0,19 моль) 4-хлоро-3,5-диметил-1- итробензола и 38,54 г (0,21 моль) 4-ХЛОРО-5,6,7,8-тетрагидро-1-нафтола В 300 МП безводного диметилформамида В атмосфере азота и при комнатной Температуре добавляют 29,16 г (0,21 моль) безводного карбоната ка- . Полученную реакционную смесь на- 1 ревают до 140°С. Реакционную смесь аатем нагревают при температуре от 140 до 150°С в течение 40 ч. Затем реакционную смесь охлаждают до комнатной температуры. Диметилформамид удаляют на роторном испарителе под ва- куумом.. Оставшееся темно-коричневое Полутвердое вещество растворяют в 500 мл горячего .толуола и фильтруют. Собранное твердое вещество тщательно промывают горячим толуолом. Толуоловые промывки смешивают с толуоловым фильтратом, и после удаления растворителей получают 34,8 г темно-коричневого твердого вещества. Перекрис- Таллизация из горячего гексана, содержащего немного этилацетата, при
ства,
35
40
45
50
55
t, т.пл. 126-135°С.
ЯМР (CDClj),: 1,6-1,8 (m, 4Н); 2,0 (S, 6Н); 2,6-2,9 (т, 4Н); 3,45 (S, 2Н); 6,13 (d, Гц, 1Н); 6,37 (S, 4Н); 6,93 (d, Гц, 1Н).
Для получения 3-(4- Л-хлоро-5,6, 7,8-тетрагидро-1-нафтокси -3,5-диме- тилфенил)-1-(2-хлоробензоил)мочевины к раствору, содержащему 3,0 г 4-(4- хлоро-5,6,7,8-тетрагидро-1-нафтокси)- 3,5-диметиланилина в 40 мл толуола, в атмосфере азота и при нагревании до медленно добавляют раствор, содержащий 2,7 г 2-хлоробензоилизо- цианата в 5 мл толуола. Полученную смесь нагревают при в течение 1/2 ч. Реакционную смесь охлаждают до О С и отфильтровывают. Собранное твердое вещество промывают толуолом, а затем гексаном. Его сушат под вакуумом, получив 3,58 г белого твердого вещества, т.пл. 224-226 0.
ЯМР (ДМСО-dg),: 1,7-2,2 (т, ЮН, содержит синглет при 2,03); 2,7-3,0 . (т, Чн); 6,07 (d, Гц, 1Н); 7,07 (d, Гц, 1Н); 7,07 (d, 1 9 Гц, 1Н); 7,4-7,7 (т, 4Н); 10,38 (S, 1Н); 11,20 (S, 1Н).
Пример 5. .Получение 3-(3-хло- рЬ-4- 2,3-дигидро-2,2-диметил-7-бенеле удаления растворителей получают 17,30 г бледно-желтого твердого веще
ства,
t, т.пл. 126-135°С.
ЯМР (CDClj),: 1,6-1,8 (m, 4Н); 2,0 (S, 6Н); 2,6-2,9 (т, 4Н); 3,45 (S, 2Н); 6,13 (d, Гц, 1Н); 6,37 (S, 4Н); 6,93 (d, Гц, 1Н).
Для получения 3-(4- Л-хлоро-5,6, 7,8-тетрагидро-1-нафтокси -3,5-диме- тилфенил)-1-(2-хлоробензоил)мочевины к раствору, содержащему 3,0 г 4-(4- хлоро-5,6,7,8-тетрагидро-1-нафтокси)- 3,5-диметиланилина в 40 мл толуола, в атмосфере азота и при нагревании до медленно добавляют раствор, содержащий 2,7 г 2-хлоробензоилизо- цианата в 5 мл толуола. Полученную смесь нагревают при в течение 1/2 ч. Реакционную смесь охлаждают до О С и отфильтровывают. Собранное твердое вещество промывают толуолом, а затем гексаном. Его сушат под вакуумом, получив 3,58 г белого твердого вещества, т.пл. 224-226 0.
ЯМР (ДМСО-dg),: 1,7-2,2 (т, ЮН, содержит синглет при 2,03); 2,7-3,0 . (т, Чн); 6,07 (d, Гц, 1Н); 7,07 (d, Гц, 1Н); 7,07 (d, 1 9 Гц, 1Н); 7,4-7,7 (т, 4Н); 10,38 (S, 1Н); 11,20 (S, 1Н).
Пример 5. .Получение 3-(3-хло- рЬ-4- 2,3-дигидро-2,2-диметил-7-бензофуранилоксиЗфенил)-1-(2,6-дифторо- бензоил)мочевины.
Для получения 3-хлоро-4-(2,3-ди- гидро-2,2-диметил-7-бензофуранилок- си-1)-нитробензола к смеси, содержа- щей 32,63 г (0,236 моль) безводного карбоната калия и 30,41 г (0,158 моль) 3,4-дихлоро-1-нитробензола в 250 мл
безводного диметилформамида, при ком- IQ Далее смесь охлаждают ниже в мо- натной температуре и в атмосфере азо- розильнике, а затем отфильтровывают.
та добавляют 30,88 г (0,188 моль) 2,3-дигидро-2,2-диметил-7-оксибензо- фурана. Затем реакционную смесь по мещают в масляную баню и нагревают до 110 С в течение 20 ч. Затем реакционную смесь охлаждают до комнатной температуры. Диметил- формамид удаляют под вакуумом. Остаток растворяют в 1,5 л смеси 1:1 этилацетата:эфира ив 300 мл воды. Слои разделяют. Органический слой дважды промывают 5%-ным NaDH, дважды . KqO и один раз насьщенным водным
Собранное твердое вещество промывают холодным толуолом. Сушат под вакуумом, получив 5,43 г целевого продук15 та в виде белого твердого вещества, т.пл. 171°С.
ЯМР (ДМСО-аб),д: 1,40 (S, 6Н); 3,05 (S, 2Н); 6,3-8,0 (т, ЮН); 10-20 (широкий синглет, 1И); 11,47 (широкий
20 синглет, 1Н).
Аналогичным способом получают 4- (4-бензотиенилокси-З-хлоранилин посредством конденсации 5-оксибензотио- фена с 3,4-дихлоро-1-нитробензолом
раствором NaCl. После высущивания над 25 в присутствии безводного карбоната безводным и удаления раствори- калия в горячем диметилформамиде.
телей получают 48,42 г светло-рыжего твердого вещества. Его перекристал- лизовывают из смеси гексан - этил- ацетат, получив 44,19 г белых кристаллов, т.пл. .
ЯМР (CDCb),5 : 1,42 (S, 6Н); 3,05 (S, 2Н); 6,5-7,2 (m, 4Н); 7,95 (doft, ,2 Гц, 1Н); 8,28 (d, Гц, 1Н).
Для получения 3-хлоро-4-(2,3-дигид- ро-2,2-диметил-7-бензофуранилокси)анилина к раствору, содержащему 42,5 г З-хлоро-4-(2,З-дигидро-2,2-диметил- 7-бензофуранилокси)-1-нитробензола в 600 МП толуола добавляют 1,5 г 5%-ной платины на угле. Эту смесь за-, тем помещают в однолитровый качающийся гидрогенезатор. .В автоклав подают водород давление примерно 7 атм. Давление поддерживают в пределах от 7 до 5,6 атм. Содержимое извлекают из автоклава и отфильтровывают через целит. После удаления растворителей получают 34,91 г белого твердого вещества, т.пл.102-104 с.
ЯМР (CDClj),: 1,45 (S, 6Н); 3,0 (S, 2Н); 3,55 (широкий синглет, 2Н); 6,2-6,9 (т, 6Н).
Для получения 1-(3-xлopo- t,-L2,3Этот продукт восстанавливают либо химически хлористым оловом (2) в соляной кислоте, используя диоксан в ка- 30 честве совместного растворителя, либо путем каталитической гидрогенизации, чтобы получить целевой анилин. Аналогичным способом получают 4-(4- бензотиенилокси)-3,5-дихлоранилин из 1,2,З-трихлоро-5-нитробензола.
35
40
45
50
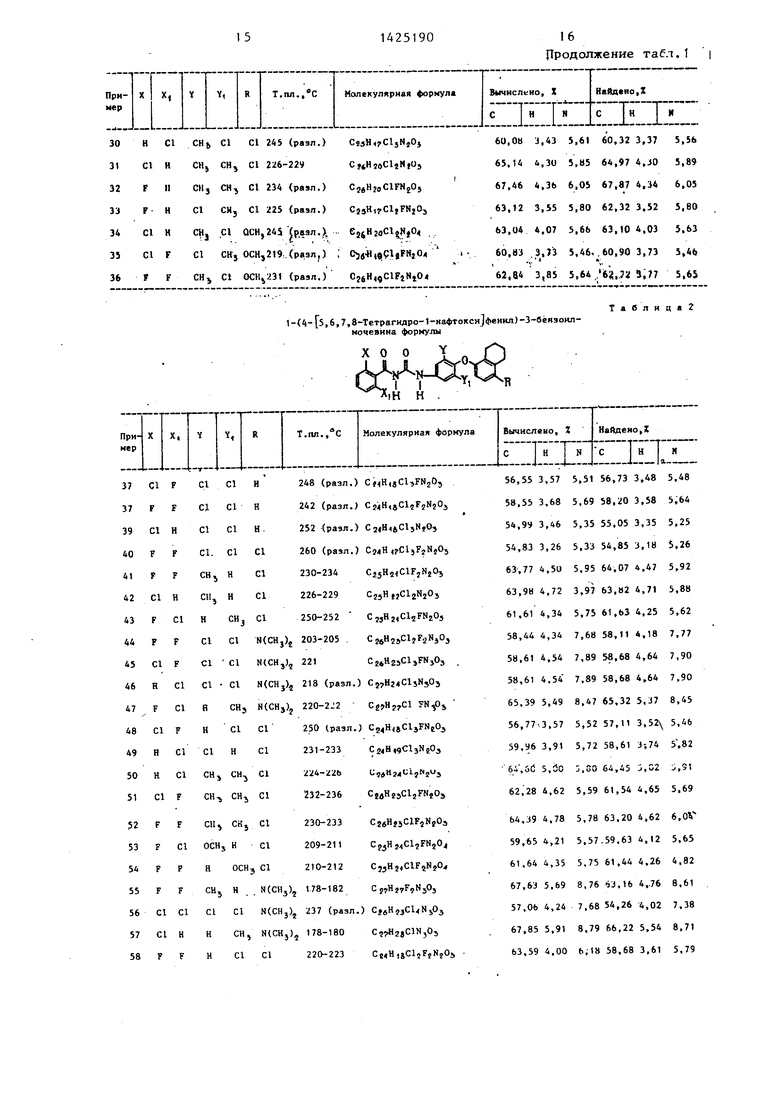
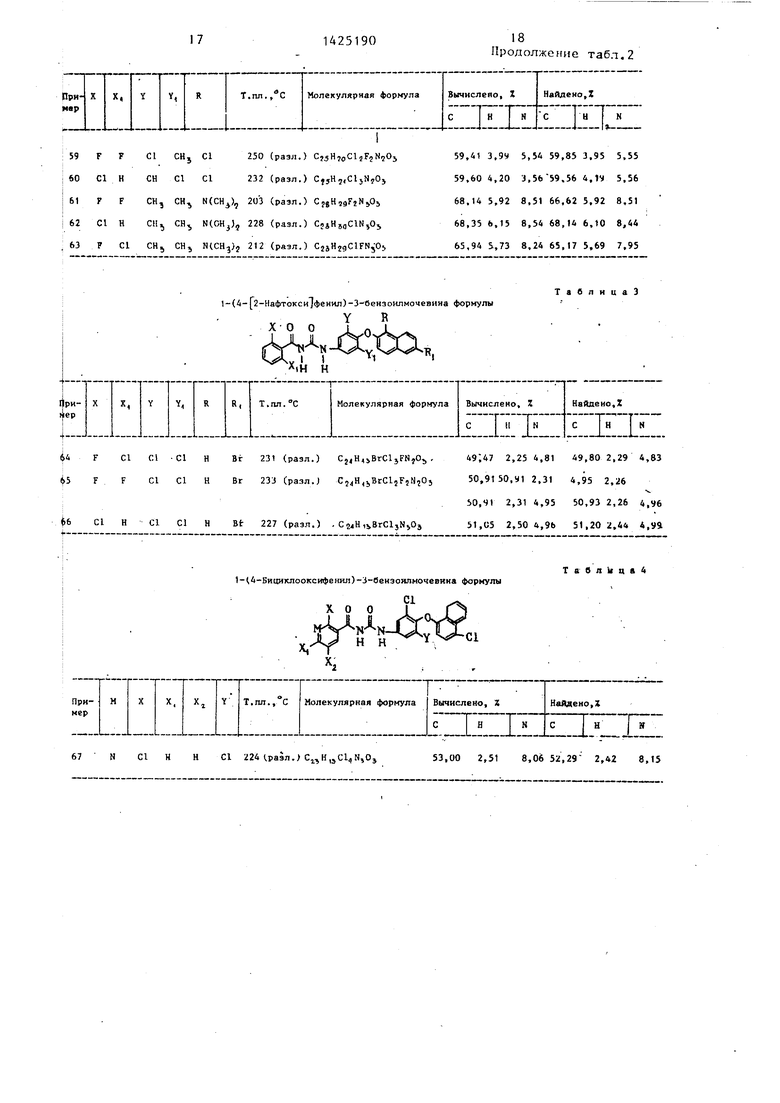
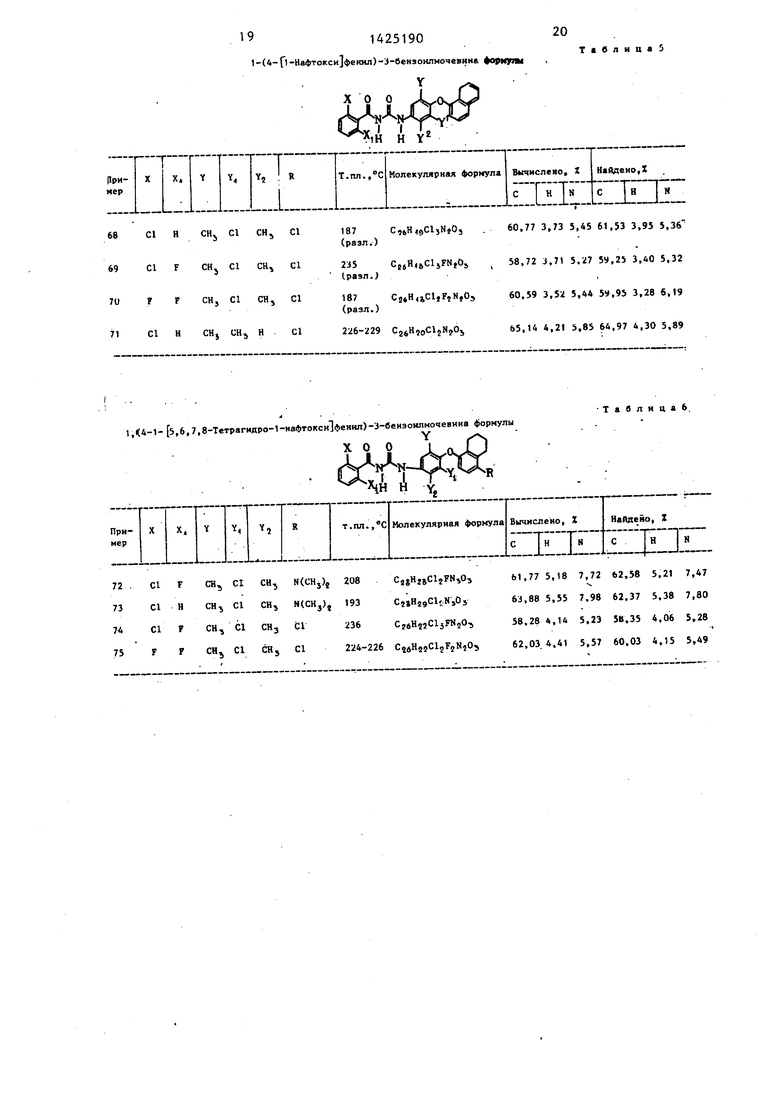
В табл. 1-6 указаны физические свойства бензоилмочевин, полученных предлагаемым способом.
Проводят испытания отобранных би- циклооксифенилмочевин для их инсектицидной и противоклещевой активности.
Готовят суспензии исследуемых соединений путем растворения одного гамма-соединения в 50 мл ацетона, в котором перед этим растворено О,V г (10% от веса соединения) алкилфено- кси-этанольного поверхностно-активного реагента, используемого в качестве эмульгирующего или диспергирующего реагента. Полученный раствор смешивают путем выливания в 160 мл воды, получив примерно 200 мл суспензии, содержащей соединение в виде мелких частиц. Полученная таким образом исГотовят суспензии исследуемых сое динений путем растворения одного гам ма-соединения в 50 мл ацетона, в котором перед этим растворено О,V г (10% от веса соединения) алкилфено- кси-этанольного поверхностно-активно го реагента, используемого в качеств эмульгирующего или диспергирующего реагента. Полученный раствор смешивают путем выливания в 160 мл воды, получив примерно 200 мл суспензии, содержащей соединение в виде мелких частиц. Полученная таким образом исдигидро-2,3-диметш1-7-бензофуранйлокси1фенил)-3-(2,6-дифторобензоил)моче- ходная суспензия содержит 0,5 мас.%
вины раствор, содержащий 4,0 г соединения. Исследуемые концентрации
(13,8 ммоль) З-хлоро-4-(2,3-дигидро- 2,2-диметил-7-бензофуранилокси)анштиполучают путем разбавления исходной суспензии водой.
на в 45 мл толуола, помещают в атмосферу азота и нагревают до . К этой смеси добавляют 3,79 г (20 ммоль) 2,6-дифторобензоилозоциа-- ната в 5 мл толуола через дополнительную воронку. Полученную смесь нагревают в течение 45 мин, а затем охлаждают до комнатной температуры.
Собранное твердое вещество промывают холодным толуолом. Сушат под вакуумом, получив 5,43 г целевого продукта в виде белого твердого вещества, т.пл. 171°С.
ЯМР (ДМСО-аб),д: 1,40 (S, 6Н); 3,05 (S, 2Н); 6,3-8,0 (т, ЮН); 10-20 (широкий синглет, 1И); 11,47 (широкий
синглет, 1Н).
Аналогичным способом получают 4- (4-бензотиенилокси-З-хлоранилин посредством конденсации 5-оксибензотио- фена с 3,4-дихлоро-1-нитробензолом
в присутствии безводного карбоната калия в горячем диметилформамиде.
Этот продукт восстанавливают либо химически хлористым оловом (2) в соляной кислоте, используя диоксан в ка- честве совместного растворителя, либо путем каталитической гидрогенизации, чтобы получить целевой анилин. налогичным способом получают 4-(4- бензотиенилокси)-3,5-дихлоранилин из 1,2,З-трихлоро-5-нитробензола.
В табл. 1-6 указаны физические свойства бензоилмочевин, полученных предлагаемым способом.
Проводят испытания отобранных би- циклооксифенилмочевин для их инсектицидной и противоклещевой активности.
Готовят суспензии исследуемых соединений путем растворения одного гамма-соединения в 50 мл ацетона, в котором перед этим растворено О,V г (10% от веса соединения) алкилфено- кси-этанольного поверхностно-активного реагента, используемого в качестве эмульгирующего или диспергирующего реагента. Полученный раствор смешивают путем выливания в 160 мл воды, получив примерно 200 мл суспензии, содержащей соединение в виде мелких частиц. Полученная таким образом исходная суспензия содержит 0,5 мас.%
получают путем разбавления исходной суспензии водой.
Испытания на южных ратных червях.
Подопытными насекомыми являются личинки южных ратных червей (Spodop- teraeridania, (Cram)), которых выращивают на растениях зеленой капусты при 26,7±2,8 С и при относительной влажности .
Препараты исследуемых соединений 1|отовят путем разбавления исходной с|успензии водой, чтобы получить сус- ензию, содержащую 500 ч.исследуемо- ifo соединения на ррт ч. конечного ijipenapaTa. Выращенные в горшках растения зелёной капусты стандартной фысоты и возраста помещают на вра- 1|1ающийся поворотный стол и опрыскивают 100-110 мл препарата исследуемого соединения, используя установку для опрыскивания Девилбисс при давлении воздуха примерно 0,7 атм. Та- сой обработки, продолжительностью с, достаточно для увлажнения )астений до стекания с них влаги. $ качестве контроля на зараженные растения также наносят 100-110 мл иодоацетонового эмульсионного раст- ора, не содержащего исследуемого Ьоединения. После высушивания пар- 1ые листья отделяют и по одному помещают в 9-сантиметровые чашки Петри, застеленные увлажненной фильтровальной бумагой. По Пять случайно выбранных личинок кладут в каждую чашку и чашки закрывают. Закрытие чашки hoдпиcывaют и выдерживают при 26,7- р9, в течение пяти дней. Несмотря Na то, что личинки могут легко съест Целый лист за 24 ч, больше пищи не робавляют. Личинок, которые не могут )изменять длину своего тела, даже при стимуляции путем покалывания, считают мертвыми.
Испытания на божьих коровках Epilachna varivestis.
Подопытными насекомыми являются личинки божьей коровки в четвертой возрастной стадии вида Epilachna varivestis (Muls), которых выращивают на растениях зеленой капусты пр 26, 712,8 с и ПРИ относительной влажности .
Препараты исследуемых соединений готовят путем разбавления исходной суспензии водой, чтобы получить суспензию, содержащую 500 ч , исследуемого соединения на ррт конечного препарата. Выращенные в горщках растения зеленой капусты стандартной вы
5
0
соты и возраста помещают на вращающийся поворотный стол и опрыскивают 100-110 мл препарата исследуемого соединения с помощью распылительной установки Девилбисс при давлении воздуха О, 7 атм. Этого нанесения, продолжительностью 25 с,достаточно, чтобы увлажнить растения до стекания с них влаги. В качестве контроля на зараженные растения также наносят 100-110 мл водоацетонового эмульсионного раствора, не содержащего исследуемого соединения. После высушивания парные листья отделяют и по одному помещают в 9-сантиметровые чашки Петри, застеленные увлажненной фильтровальной бумагой. По пять случайно выбранных личинок помещают в каждую чашку, и чашки закрывают. Закрытие . чашки надписывают и выдерживают при 26,,8 С в течение пяти дней. Несмотря на то, что личинки могут легко съесть цельй лист за 24 часа,
5 больше пищи им не дают. Личинок, которые не могут изменять длину своего .тела, даже при раздражении, считают мертвыми.
Испытание противоклещевого опрыс0 кивания листвы.
Двупятнистого клещика (Tetranychus urtical koch) во взрослом состоянии и в стадии нимфы выращивали на зеленой капусте при контролируемых услоg ВИЯХ 8015 Ф (примерно 26,7t2,8 c) и при относительной влажности . Зараженные листья от исходной культуры поместили на первичные листья двух растений высотой 6-8 дюймов.
jQ Со срезанных листьев на свежие растения переходит достаточное число клещиков (150-200). Зараженные растения зеленой капусты стандартной высоты и возраста помещают на вращающийся
.g поворотный стол. Приготовленную водную смесь химикатов (100 мл) наносят на растения с помощью распьшительной установки Девилбисс при давлении воздуха 2,8 атм. Нанесение такого объема препарата соединения занимает 25 с. Этого объема опрыскивания достаточно для того, чтобы увлажнить растения до стекания с них влаги.
Препараты исследуемых соединений готовят обычным способом путем растворения в ацетоне, добавления эмульгатора и разбавления водой. Первичную обработку проводят при концентрации 500 ррт.
0
55
Любой индивид, который может двигать- ю приведенные в таблице, наглядно пока20
зывают преимущество соединений по настоящему изобретению по сравнению с известным инсектицидом.
При концентрации 8 ррга процент 15 смертности димилина после пяти дней воздействия на южного ратного червя составляет 20%, а на божью коровку составляет 60%. Для следующих соединений процент смертности для контрольных тестов при 8 ррт составляет 100% при воздействии как на южного ратного червя, так и на божью коровку (пример 2,10,15 -20,23,24,26,28,2 31,33 - 36, 40,41,43,44,46,48,50 - 52,55,5.6,58 - 63,65,67- 75).
Соединения по примерам 11,12,14, 1,64 и 66 при 8 ррт имеют 100%-ную смертность после 5 дней воздействия на южного ратного червя.
Соединения по примерам 6-8, 30 и 38 при 8 ррт имеют 100%-ную смертность после 5 дней воздействия на божью коровку.
25
30
ся при раздражении, считается живым.
Испытание действия на яйца клещей.
Яйца двупятнистого клещика(Тейга- nychus. urtical (Koch)) получают от взрослых клещиков, вьфащиваемых на зеленой капусте в контролируемых условиях 26,7-2, при относительной влажности 50±5%. Сильнозараженные листья из исходной культуры помещают на незараженные растения. Самок оставляют на 24 ч для кладки яиц, а затем листья растений погружают в раствор тетраэтилпирофосфата в концентрации 1000 ррт для того, чтобы убить подвижные формы и предотвратить дополнительную кладку яиц. Тет- раэтилпирофосфат не влияет на выживаемость яиц.
Растения помещают на вращающийся поворотный стол. Приготовленную водную смесь химиката (100 мп) подают на растения с помощью распыпительной установки Девилбисс при давлении воздуха 2,8 атм. Нанесение этого объема приготовленного соединения занимает 25 с. Этого объема опрыскивания достаточно, чтобы смочить растения до стекания с них влаги. На зараженные растения для проверки или для контроля также распыляют эквивалентное количество водоацетонового раствора, содержащего эмульгатор и ацетон в тех же ca№ix концентрациях, как и в инсектицидной смеси, но без испытываемого инсектицида.
Препараты исследуемых соединений готовят обычными способами путем растворения, в ацетоне, добавления эмульгатора и разбавления водой. Первичные отборочные испытания проводят при концентрации 500 ррт.
Обработанные растения выдерживают при 26,7 2, и при относительной влажности 5015% в течение 7 дней, после чего производят подсчеты.
Микроскопическое исследование.про- или В водят на листья растений, отмечают число невьшупленных яиц (которых считают мертвыми) и оболочек пустых яиц Н, F,Cl; Y-H,Cl, СН, , OCHj-; Y4 - Н,
35
40
Формула изобретения
Производные бициклооксифенилмоче- вины общей формулы
О о IIи
C-N-C-N
Н
Н
45
где при М- СН- Х,Х, - Н, С1, F; Y - Н,-С1, СН, Y, - Н, СН,
г
Y - Н, С1, СН,, СРз
50 В
при условии,- что R - Н, С1, ОСН,, N(CH)t,
при условии - что Х,Х|.
0
зывают преимущество соединений по настоящему изобретению по сравнению с известным инсектицидом.
При концентрации 8 ррга процент 5 смертности димилина после пяти дней воздействия на южного ратного червя составляет 20%, а на божью коровку составляет 60%. Для следующих соединений процент смертности для контрольных тестов при 8 ррт составляет 100% при воздействии как на южного ратного червя, так и на божью коровку (пример 2,10,15 -20,23,24,26,28,29, 31,33 - 36, 40,41,43,44,46,48,50 - 52,55,5.6,58 - 63,65,67- 75).
Соединения по примерам 11,12,14, 1,64 и 66 при 8 ррт имеют 100%-ную смертность после 5 дней воздействия на южного ратного червя.
Соединения по примерам 6-8, 30 и 38 при 8 ррт имеют 100%-ную смертность после 5 дней воздействия на божью коровку.
5
0
35
40
Формула изобретения
Производные бициклооксифенилмоче- вины общей формулы
О о IIи
C-N-C-N
Н
Н
где при М- СН- Х,Х, - Н, С1, F; Y - Н,-С1, СН, Y, - Н, СН,
г
Y - Н, С1, СН,, СРз
50 В
при условии,- что R - Н, С1, ОСН,, N(CH)t,
,Cl, СН, , OCHj-; Y4 - Н,
при условии - что Х,Х|.
13
CHs, OCHft; Y - H, R NCCH,), в
- H,
ил
X - Cl, F; X - H, F, Cll; Y - Y, - Cl; Ya - H,
1(4-Г1-иафтокск феииЛ)-3-о«нэоилмочевина формулы X 00
С1 С1 - 37-234
С1 Н 231,5-232,5
Cl H 2: 7-229
Cl H 231,5-232,5
Cl H 227-229
Cl H 237-2J7,5
Cl H246-248
Cl Cl 252-253,5
Cl Cl 2045-245
H , Cl 215-217
H H 233-236
Cl OCH 232 (раэл,
Cl OCHj 229 (раэл,
Cl OCHj 237 (раэл,
И Cl 233 (раэл,
H Cl 211 (раэл,
H Cl 247(рвял,)
Я N( (pasn.)
H N(.CH,,5
Cl Cl 2t3 (paan.)
H Cl 176-179
CHj Cl 244-2 6
CHj Cl 226-229
H OCHj 228 (разп.)
H . OCHj 225
H OCHj 193 (раал.)
CHjOCHj 115 (раэл.)
Hj, Cl 229 (разл.)
C,H,,,Cl,FjN,0, C5,H,5CljN50, Ct HnCijF HjO, Cy HisClsN-jOr, C24H,4CljF5NtO, C54H,,,CljFN,0,, Cj HiiCl NjOj Cj HijCJ FMjOj C54H,4Cl4N,Oj CjiHMClFjNjOj Cj5H,,,03 ) C,jH,6CljFN,04 ) CjjH,Cl,F,N30 ) С,5Н,7С1зНгО ) CssHfTClFjNjOj ) CzeH,sCl2NsOj CjaHiyCljNiOu
С; ншС1гРЫ,о,
CeeHzeClFjNjO, C«H CljFN,Oj Cj,H,6CirN,Oj
. CaeHjgCijK.o,
CjeH,eClF,N,Oj
Cs5HuCljNj04
C «Hj9FjN{0
CjeH ClHjO,,
C«H(,F,N,0
CajHfeCijFjHjOs
14
или в
при М - N; X - Cl;
X, - H;Y - Cl; Y4 YB - J, проявляющие пестицидную активность.
т а а л и ц а 1
55,26 2,465,36
59,623,155,78
59,57 2,B55,57
59,62 3,155,78
59,37 2,855,57
57,78 2,885,57
55,37 2,59-5,38
53,60 2,415,17
55,53 2,715,54
57,46 2,695,30
59;82 2,865,54
56,41 2,865,19
57,92 3,045,13
58,31 3,355,55
64,03 3,495,92
464,0700
2,06 3,473,70
51I,OS71
63,15 4,038,48
57,09 2,595,35
66,74 4,016,20
62,97 3,883,67
63,37 3,926,14
62,20 3,925,84
67,69 4,296,07
67,66 4,376,26
62,01 3,735,81
60,33 3,355,5t
НС1СНьС1 С1 245 (разл.)CsaH,CljN,Oj
ciНСИ,сн, С1 гг(-2гчc,4Hjoci4H,Oj
гIICHjСН, С1 234 (реял.)CjjHjoClFNjO,
РНсгCHj С1 :г25 (раэл.)CjjHiyCljFNjOj
С1НqijCl QCH,245 (р.аэл.).ejjHjoCl jO«
ClFClCHj OCHj2l9, (разл,) , (,4«,c|gijFNj04
FFCH Cl (pasn.)CjjH,,ClFiNiO«
1-(,6,7,8-Тетрагидро-1-нафтоксн фенил)-3-бёнэоил- ночевнна формулы
60,Ob3,435,61 60,32 3,37
65,144,305,H5 64,97 4,30
67,464,366,05 67,87 4,34
63,123,555,80 62,32 3,52
63,044,075,66 63,104,03
60,аз3.735,46,.60,90 3,73
..
62,843,855,64 ,
Таблица
X О О
А,н Н .
Пример
X,
F F
С1 Н
С1 CHj С1
250(раэл.) C,5H,oCljF5N70j
СН С1 С 232(разл.) CjjHj.CljNjOj
F F СН, СН, N(CH), 203(раэл.) CjgHjflFzNjOj
Cl Н СН,, СН N(GHj), 228(раэл.) CjiHsaClNjOj
F Cl СН, СН, N(CHj)2 212(раэл.) CjjHjgClFNjOj
1-(4- 2-Нафтоксн1фенил)-3-бензоилмочев11на формулы
Y В X О о
iH Н
1-(4-Вициклооксифенил)-3-вензоилмочевина формулы X О О °
67N С1 Н Н С1 224 (.разл.) ,,Oj
59,41 3,9У3,5А 59,85 3,955,55
59,604,203,5659.56 4,1У5,56
68,14 5,928,51 66,62 5,928,51
68,35 6,158,54 68,14 6,108,44
65,94 S,738,24 65,17 3,697,93
ТаблицаЗ
ТаОлЬца4
33,00 2,51 8,06 3i,29 2,2 8,15
1-(-Г1-Нафтокси фенип)-3-Севэоклмочввина фощудм
Y
X О О
68Cl Н CHj Cl СН, Cl
69Cl F CHj Cl CH Cl
70F F CHj Cl CH, Cl
71Cl H CHj UH, HCl
1, 4-1- 5,6,7,8-Тетрагидро-1 -на4ртокси фенил) -3-бенэонлмочевина (формулы
X О О
(M-fi
4 A V
73ClHСН,ClCHjN(CHj)j193CjiHjjCljNsOs63,88 5,557,9862,375,387,80
74ClFCH,ClСНзCl236CjeHjjCljFNjO,58,284,145,235b,354,065,28
75FFCHjClCH,Cl224-226CteHjjCl FjNjO,62,03,4.415.5760,034,155,49
Таблица
Ы А Y
187С,Н,вС1)ЫгОэ
(раэл.)
60,77 3,73 5,45 61,53 3,95 5,36
235Cjjtt,bCljFN,Oj 58,72 3,71 5.27 5У,25 3,40 5,32
(раэл.)
187CjiHtiCliF NjO,60,59 3,52 5,44 5,95 3,28 6,19
(разл.)
226-229 C24H7(,Cl2NyO,,
65,U 4,21 5,85 64,97 4,30 5,89
Таблица 6.
-fi
4 A V
инение
J
Концентрация, ррт
Божья коровка(Kpilachna varives- tis), X смертности Q через 5 дней
р о о
ЛЖ
Известное |о единение милин)8
примеру
28
108
178
248
388
508
528
i 68-8
i 708
718
60 100 100 100 100 100 100 100 100 100 ТОО
Таблица8
90
100
70
26 32 37 42 45
47 49
53
54
57 Димилин
8 8 8 8 8 8 8 8 8 8 8
100
100
60
УО
100
100
80
30
50
100
20
Таблица9
5
9
13
26 32 37
42 45 47 53 54 57 Димилин
8 8 8 8 8 8 8 8 8 8 8 8 8
90
100
90
80
80
90
100
90
90
90
100
90
60
| Патент США-№ 3933908, кл | |||
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| опублик | |||
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
Авторы
Даты
1988-09-23—Публикация
1983-01-10—Подача