Изобретение относится к способу получения амидов 1,2,3,4,6,7,12,12Ь- -октагидроиндоло(2,3-а)хинолизин-1- -ил-алканкарбоновых кислот.
Полученные амидные производные 1,2,3,4,6,7,12,12 сг-октагидроиндоло (2,3-а)хинолизин-1-ил-алканкарбоновых кислот и их соли присоединения кислот обладают спазмолитическим,сосудорас- ;
ширяющим,антиаритмическим и гастроци-, тозащитным действием (особенно зна|чительным).
Цель изобретения - синтез новых соединений, обладающих активностью, не характерной для данного ряда соединений .
Пример 1. (-)-(1S:12bS)- -этш1-1,2,3,4,6,7,12,12Ь-октагидроин
ы
доло-(2,3-а)хинолизин-1-ил-пропионо- вая кислота-(К)-1-фенилэтиламид.
3,26 г (0,01 моль) (-)-(1S:12bS)- -1-ЭТИЛ-1,2,3,4,6,7,12,12Ь-октагидро- индоло(2,3-а)хинолизин-1-ил-пропионо- вой кислоты в атмосфере азота и при постоянном перемешивании добавляют к приготовленному с 20 мл- безводного тетрагидрофурана раствору 2,04 г (0,02 моль) перегнанного над натрием N-метилморфолина. Раствор охлаждают до -5°С, и затем при сильном перемешивании по каплям однако непрерывно, смешивают с 1,10 г (0,01 моль) этилового эфира хлормуравьиной кислоты, причем внутренняя температура не должна превышать 0°С. Реакционную смесь перемешивают при 0°С в течение 30мин.
т.пл.
185-192 С (и
Гидробромид: пропанол),
Соль этансульфокислоты: т.пл. 143-150 С (из смеси изопропанола и диизопропилового эфира).
Соль метансульфокислоты: т.пл. (из смеси изопропанола и диизопропилового эфира. 0 Гидрохлорид: т.пл. 195-200°С (изопропанол), о( -2,6° (с 2,0, этанол).
Рассчитано, 7.: С 72,16; Н 7,79; N 9,02; С1„он ,61.
(М 466,04)
Найдено, %: С 72,01; Н 7,57; 87; С1„он 7,53.
Пример 2. (-)-Бензиламид (18:12Ь5)-1-этил-1,2,3,4,6,7,12,12
N
Затем при (-5)°С - в течение при- 20 -октагидроиндоло(2,3-а)хинолизин0193
4
т.пл.
185-192 С (изоГидробромид:пропанол),
Соль этансульфокислоты: т.пл. 143-150 С (из смеси изопропанола и диизопропилового эфира).
Соль метансульфокислоты: т.пл. (из смеси изопропанола и диизопропилового эфира. 0 Гидрохлорид: т.пл. 195-200°С (изопропанол), о( -2,6° (с 2,0, этанол).
Рассчитано, 7.: С 72,16; Н 7,79; N 9,02; С1„он ,61.
(М 466,04)
Найдено, %: С 72,01; Н 7,57; 87; С1„он 7,53.
Пример 2. (-)-Бензиламид (18:12Ь5)-1-этил-1,2,3,4,6,7,12,1 2ЬN





















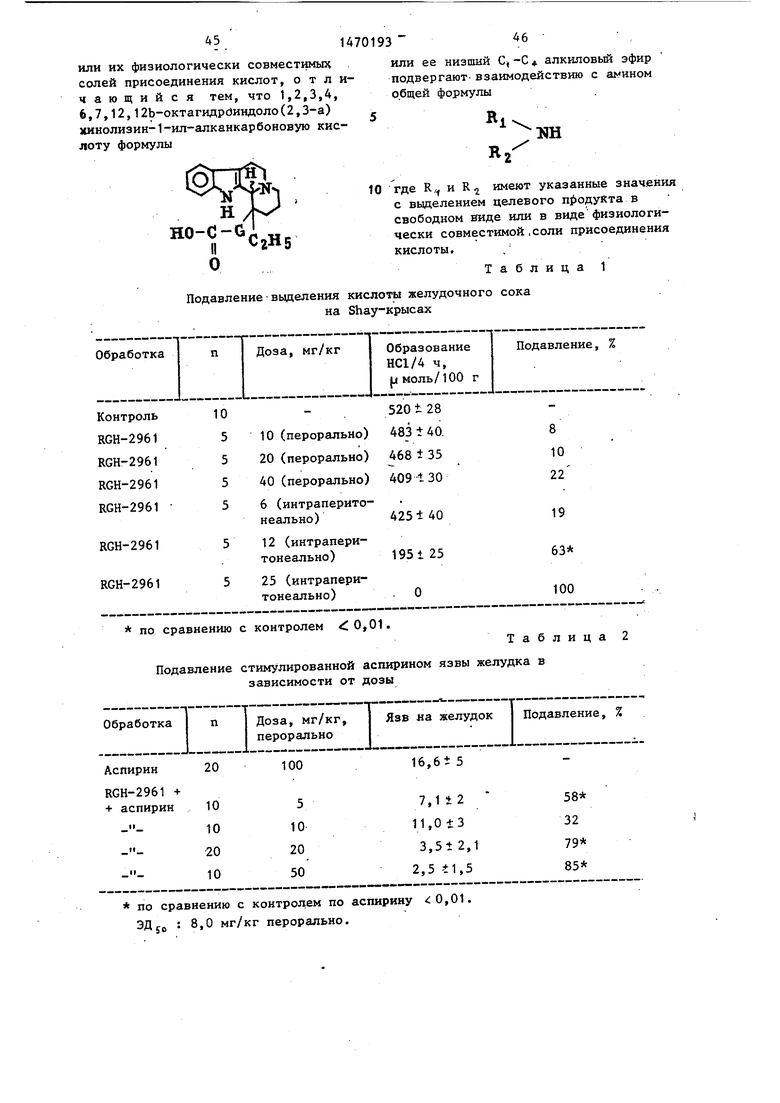
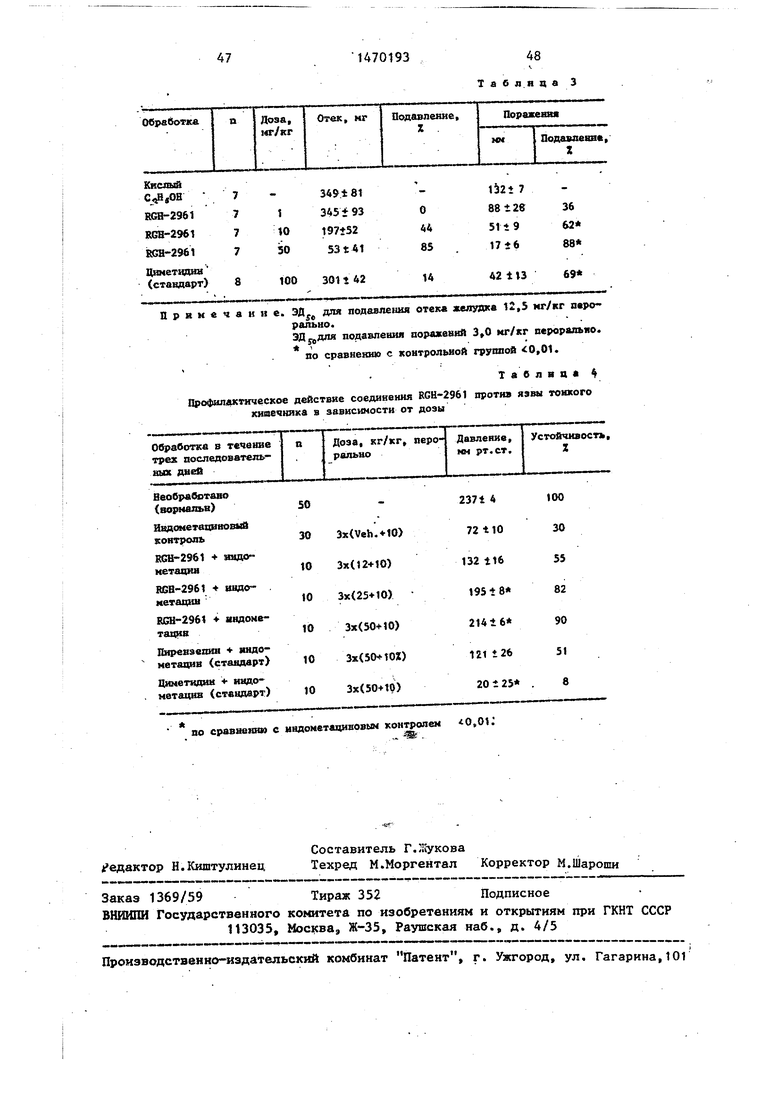
Изобретение относится к гетероциклическим соединениям, в частности к получению амидов 1,2,3,4,6,7,12, -октагидроиндоло(2,3-а)хинолизин-1- -ил-алканкарбоновых кислот фор-лы С2Н5 где R., - С -С4-алкил; RI. - фенил; G - линейная С ,-С -алкиленовая группа, или их физиологически совмести- мьк солей присоединения кислот, которые обладают спазмолитическим, сосудорасширяющим, антиаритмическим и гастроцитозащитным действием. Цель - вьшвление новых соединений указанного класса, обладающих указанной активностью. Получение их ведут взаимодействием 1,2,3,4,6,7,12,12t-OK- тагидроиндоло(2,3-а)хинолизин-1-ил- -алканкарбоновой кислоты или ее низшего С -С4-алкилового эфира с амином фор-лы R R-iNH, где R, и R-i-указаны выше. Процесс ведут с выделением це--., левогсз продукта в свободном виде или в виде физиологически совместимой соли присоединения кислоты. 4 табл. § СП | со со
мерно 10 мин прикапывают приготовленный с 10 мл безводного тетрагидрофурана раствор 1,33 г (0,011 моль) (R)- -1-фенилэтиламина при сохранении внутренней температуры ниже . Реакционную смесь перемешивают в течение 30 мин при и затем еще следующие 4ч, причем температуре дают подняться до комнатной. Смесь выпаривают на ротационном испарителе, остаток смешивают с 50 мл дихлорметане и 20 мл воды и после тщательного встряхивания осуществляют разделение фаз. Органическую фазу промьшают 20 мл 5%-ного раствора соды, затем трехкратно по 20 мл водой, сушат над. сульфатом магния и после этого выпаривают. Сырой продукт очищают перекристаллизацией из изопропанола. ВыгО
ход 2,92 г (68%), т.пл. 154-156 С, СогЗв° -50,4°(с 2,0, этанол).
Рассчитано; %: С 78,28; Н 8,21; N 9,78.
(М 429,58)
Найдено, %: С 78,05; Н 8,40; N 9,77.
Н -ЯМР (CDCli) f 1,05 (ЗН, триплет, J 7 Гц, Cl-CH -CHi); 1,37 (ЗН, дублет,J с«.с:нэ 7 Гц, . Ш-СН-СНз); 3,33 (1Н, С1 2Ь-н); 5,00 (1Н, -CH.-CHj); 5,40 (1Н, шир. дублет J мн, си 7 Гц СО-Ш); 7,0-7,50 (9Н, мультиплет, ароматические протоны); 8,0 (1Н, шир. синглет, индол-Ш) м.д.
Соль фосфорной кислоты: т.пл. 198-204°С (из изопропаиола),. -32,4° (с 1,0, вода)
5
5
-1-ил-пропионовой кислоты.
3,26 г (0,01 моль) (-)-(1S,12bS)- -12-этил-1,2,3,4,6,7,12,12Ь-октагид- роиндоло(2,3-а)хинолизин-1-ил-пропионовой кислоты в атмосфере азота и при постоянном перемешивании добавляют к приготовленному с 20 мл безводного тетрагидрофурана раствору 2,04 г (0,02 моль) перегнанного 30 над натрием N-метилморфолина . Раствор охлаждают до -5 С и затем при сильном перемешивании, однако непрерывно, по каплям смешивают с 1,10 г (0,01 моль) этилового эфира хлормуравьиной кислоты, причем внутренняя температура не должна превышать 0°С. Реакционную смесь перемешивают при в течение 30 мин, заг тем при (-5 - 0°С в течение примерно 10 мин прикапывают приготовленный с 10 мл безводного тетрагидрофурана раствор 1,18 г (0,011 моль) бензил- амина при сохранении внутренней температуры ниже 0°С. Реакционную смесь перемешивают в течение 30 мин при и затем еще следующие 4 ч, причем температуре позволяют подняться до комнатной. Смесь выпаривают на ротационном испарителе, остаток смешивают с 50 мл дихлорметана и 20 мл воды и после тщательного встряхивания осуществляют разделение фаз. Органическую фазу промывают 20 мл 5%-ного раствора соды, затем трехкратно по 20 мл водой, сушат наСд сульфатом магния и после этого вьша- ривают.,Сырой продукт очищают с помощью колоночной хроматографии (с помощью содержащего 10% диэтиламина то0
5
0
5
Б14
луола на силикагеле). Выход 2,35 г (57%); можно очищать далее путем перекристаллизации из толуола, Т.пл, 95-99 С, Wl J -128,8° (с 2,0, хлороформ).
Рассчитано, %: С 78,03; Н 8,00;;
N 10,11.
CL jJSjO (М 415,56) . Найдено, % : С 77,90; Н 8,49; N 9,68.
1Н-ЯМР (CdCl,,): f 1,10 (ЗН, триплет,. J 7 Гц, С1-СН -СНз); 3,35 (1Н, С1 26-Н); 4,30 (2Н, дублет, Jt«,N Гц, фенил-СН.,), 5,53 (1Н, уширенный триплет, CO-NH); 7,0-7,47 (9Н, мультиплет, ароматические протоны); 7,96 (1Н, уширенный синглет, индол-Ш) М.Д.), м.д.
Этансульфоновокислая соль (этан- сульфонат): т.пл. 169-171°С (из смеси изопропанола с этилацетатом),
. -71.1° /с 2,0, вода).
Рассчитано, 7,: С 66,25; Н 7,48; N 7,99; S 6,10.
CjjHj NjO.S (М 525,69)
Найдено, %: С 66,39; Н 6,99; N 7,91; S 6,69.
Осуществляют аналогично примеру 1, в качестве ацилируемого амина, -одна- .ко, применяют 1,10 г (0,011 моль) н-гексиламина, сырой продукт очищают , 25 с Помощью колоночной хроматографии при применении содержащего 5% диэтил- амина толуола на силикагеле. Выход 1,88 г (46%) пенообразного вещества. 1Н-ЯМР (CDClj): 1,08 (ЗН,
20
Л р-„ „: р 3. -,-а-,-Фе,„„,™- 30 -:--„ ;. /: б ;;%--(й:)
амид(15, 12Ь5)-1-этил-1,2,3,4,6,7, С12Ь-Н)- 5 20 (1Н 12,12Ь-октагидроиндоло(2,3-а)хиноли- . С0-Ш); 7 о-Л;0 зин-1-ил-пропионовой кислоты.„yльtиплeт, ароматические проОсуществляют аналогично примеру 1, уширенньй синглет,
в качестве ацилируемого амина приме- 35 „ „ ын м п
няют 1,33 г (0,011 моль)(К)-1-фенил- «««°Гансульф; ;вокислая соль: т.пл. Ьтиламина и очищают сырой продукт пу- 47-150°С (из смеси изопроПанола с
диизопропиловым эфиром) ,WJ-ц -63,4 (с 2,0, вода).
Рассчитано, %: С 64,70; Н 8,72; N 8,09; S 6,17.
S (молекулярный вес ,73).
Найдено, %: С 64,39; Н 8,51; N 7,76; S 6,31.
Пример 5. (-)-Н-Метилбензш1- амид(15: 12ЬЗ)-1-этил-1,2,3,4,6,7,12, 12Ь-октагидрош13оло(2,3-а)хинолизинЙА.;, -«„.-CJ-CB., ;-5 .0 (,„ у.ир. 50 - -Г™ . -пример, .. дублет, JNH.CH- / в качестве ацилируемого амина, однако, применяют 1,34 г (0,011 моль) К-метилбензиламина. Сырой продукт очищают с помощью колоночной хрома- тографии на силикагеле при использовании содержащего 5% диэтиламина толуола. Выход 2,40 г (56%) пенооб- .разного вещества.
тгем перекристаллизации из изопропанола. Выход 2,92 г (68%), т.пл. 154- 155°С, Сс -50,4° (с 2,0, этанол) .
Рассчитано, %: С 78,28; Н 8,21;
N 9,78.
С H.NjO (М 429,58)
Найдено, %: С 78,05, Н 8,40; 9,77.
1Н-ЯМР ( сг 1,05 (ЗН, триплет, J 7 Гц, Cl-CH -CH j); 1,37 (ЗН, дублет, Лси,снГ 7 Гц, NH-CH-CHj) 3,33 (1Н, С12Ь-Н); 5,00 (1Н, мульти45
7,50 (9Н, мультиплет, ароматические протоны); 8,0 (1Н, уширенный синглет, индол-NH), м.д.
Фосфорнокислая соль: т.пл. 198- 204°С (из изопропанола); (фосфат) dr4 -32,4° (с 1,0, вода)
Гидробромид: т.пл. 185-192 С (изопропанол),
93
Этансульфоновокислая соль: т.пл. 143-150°С (из смеси изопропанола с - диизопропиловым эфиром).
Метансульфоновокислая соль: т.пл. 155-165 С (из(смеси изопропанола с диизопропиловым эфиром).
Гидрохлорид: т.пл. 195-200 0 (изо- пропанол) -2,6° (с 2,0, f, этанол) .
Рассчитано, %: С 72,16; Н 7,79; N 9,02; С1«с,„ 7,61.
C JljjClNjO (молекулярный вес 466,04)
Найдено. %: С 72.01; Н 7-,57; N 8,87; С1„он 7,53.
Пример 4. (-)-н-Гексиламид (IS, 12Ь5)-1-этил-1,2,3,4,6,7,12, 12Ъ-октагидроиндоло(2,3-а)хинолизин- -1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1, в качестве ацилируемого амина, -одна- .ко, применяют 1,10 г (0,011 моль) н-гексиламина, сырой продукт очищают , 25 с Помощью колоночной хроматографии при применении содержащего 5% диэтил- амина толуола на силикагеле. Выход 1,88 г (46%) пенообразного вещества. 1Н-ЯМР (CDClj): 1,08 (ЗН,
5
0
30 -:--„ ;. /: б ;;%--(й:)
1Н-ЯМР (CDClj): di 1,08 (3H, триплет, J 7 Гц, С1СН,-СНэ); 2,01 (ЗН, синглет, N-CH); 3,32 (1Н, С12Ъ- -Н); 4,32 (2Н, уширенные, фенил-СН.) 6,9-7,4 (АН, мультиплет, ароматические протоны); 7,96 (1Н, уширенный синглет, индол-Ш), м.д.
Этансульфоновокислая соль: т.пл, 200-207 С (из смеси изопропанола с диизопропиловым эфиром), WЛи - -84,2° (с 2,0,, вода).
Рассчитано, %: С 66,76; Н 7,66; N 7,79; S 5,94.
(молекулярный вес
539,71).
Найдено, %: С 66,11; Н 7,96;
т.пл. 200-220 С
т.пл.
175-197°С (ацеN 7,32; S 6,21.
Гидробромид: (ацетон).
Гидрохлорид
тон).
Пример 6. (-)-Фурфуриламид (IS, 12ЬЗ)-1-этил-1,,2,3,4,6,7,12, 12Ь-октагидроиндоло(2,3-а)хинолизин -1-ил-пропионовой кислоты.
Осуществля{9Т аналогично примеру с тем различием, что в качестве аци лирующего амииа применяют t,08 г (0,011 моль) фурфуриламина. Сырой продукт очищают с помощью колоночной хроматографии при использовании содержащего 5% диэтиламина толуола на силикагеле.
Выход 2,18 г (54%) пенообразного вещества.
1Н-ЯМР (CDCl,): f 1.08 (ЗН, триплет, J 7 Гц, Cl-CH -CHj); 3,33 (Ш, С12Ь-Н); 4,27 (2Н, дублет JcHo ыц 5 Гц, Ш-СНг); .34 (1Н, уширенный триплет, СО-Ш); 6,tO (tH
мультиплет, J } ,4 - 5, 5
t Гц, С З -Н); 6,26 (1Н, мультиплет, Jj , 4 3 Гц, ,s 2 Гц, С4 -Н); 7,0-7,47 (5Н мультиплет, ароматические протоны с 5 -Н), м.д.
Этансульфоновокислая соль: т.пл. 142-146 С (из смеси изопропансла с диизопропиловым эфиром) , Со -65,9(с 2,0, вода).
Рассчитано, %: С 62,89; Н 7,23; N 8,.15.
(молекулярный вес
-515,65).
Найд ено, %: С 63,40; Н 7,35;
N 7,93.
Пример 7. (-)-2-(3,4-Димет оксифенил)этиламид (IS:12Ь8)-этил-Г 2,3,4,6,7,12,12Ь-октагидроиндоло
5
0
5
(2,3-а)хинолизин-1-ил-пропионовой
кислоты.
Осуществляют аналогично примеру 1, в качестве ацилируемого амина, однако, применяют 2,00 г (0,011 моль) 2-(3,4-диметоксифенил) -гэтиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при использовании содержащего 5% ди- этиламина толуола. Выход 2,64 г (54%) пенообразного вещества.
1Н-ЯШ (CDClj): 1,09 (ЗН, триплет; J 7 Гц, Cl-CH -CHj); 3,34 (2Н, мультиплет, NH-CH,); 3,33 (1Н, С12Ь-Н); 3,78 + 3,80 (6Н, синглет ОСН}); 5,27 (1Н, уширенный триплет, СО-МН); 6,52-6,78 (ЗН, мультиплет, С/-Н, С5 -Н, Сб -Н); 7,0-7,51 (4Н, мультиплет, ароматические протоны); 8,02 (1Н, уширенный синглет, индол-NH), м.д.
Этансульфоновокислая соль: т.пл.
144-147°С (ацетон) -60,7° (с 2,1, вода).
С 64,08; Н 7,56;
N
Рассчитано, 7,01
7,:
r jNjOjS (молекулярный вес
0
%: С 63,75; Н 8,00;
т.пл. 160-165 С
5
0
5
50
55
599,77)
Найдено, N 6,78.
Гидробромид (изопропанол).
Пример 8. (-)-2-Фениламид (ТВ,12ЬБ)-1-этил-1,2,3,4,6,7,12,12Ь- -октагидроиндоло(2,3-а)хинолизин-1- ,-ил-пропионовой кислоты.
.Осуществляют аналогично примеру 1 с тем различием, что в качестве ацилируемого амина применяют 1,34 г (О,ОИ Моль) 2-фенилзтиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола.
Выход 2,41 г (56%) пенообразного вещества.
; 1Н-ЯМР (СОС1з) 1,08 (ЗН, триплет, J 7 Гц, Cl-CHi-СНэ); 3,32 (1Н, С12Ь-Н); 3,36 (2Н, мультиплет, Ш-СН), 5,20 (1Н, уширенный триплет, СО-Ш); 7,0-7,50 (9Н, мультиплет, ароматические протоны); 7,96 (1Н, уширенный синглет, индол-Ш), м.д.
Этансульфоновокислая соль: т.пл. 186-191 0 (из смеси изопропанола с диизопропиловым эфиром) , Ы JJ -47,5 (с 2,0, вода).
Рассчитано, %: С 66,76; Н 7,66; N 7,79; S 5,94.
(молекулярный вес 539,71) J Найдено, %: С 66,81; Н 8,05;
т.пл. 180-190 с
N 7,78; S 6,07.
Гидррбромид: (изопропанол).
Пример 9. (-)-Ы-Метил-2- Q -оксиэтиламидСТS,12Ь5)-1-этил-1,2,3, 4,6,7,12,12Ь-октагидроиндоло(2,3-а) хинолизин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве аци- 15 лируемого амина используют 1,50 г (0,02 моль) Ы-метил-2-оксиэтиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагвле при использовании содержащего 15% 20 метанола толуола.
Выход 2,20 г (57%) пенообразного
147019310
-СН-); 5-27 (1Н, ущиренный дублет, CO--NH); 7,0-7,5 (4Н, мультиплет, ароматические протоны); 8,05 (1Н, уширенный синглет, индол-Ш), .м.д.
Гидрохлорид: т.пл. 225-245°С (разложение) (изопропанол) ,о( -80,0° (с 2,1, вода).
Рассчитано, %: С 66,41; Н 8,36; N 9,68; С1цон 8,17.
I ClNjOj (молекудярньй вес
434,00).
Найдено, %: С 65,96; Н 8,45; N 9,29; С1„ок7,78.
Пример 11. (-)-Пирид-2-ил- -метиламид(15;12Ь8)-1-зтил-1,2,3,4, 6,7,12,12Ь-октагидроиндоло(2,3-а) хинолизин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1, однако в качестве ацилируемого амина используют 1,20 г (0,011 моль) пирид- -2-ил-метиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении соОсуществляют аналогично примеру 1, однако в качестве ацилируемого амина используют 1,20 г (0,011 моль) пирид- -2-ил-метиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении совещества.
1Н-ЯМР (CDClj): с 1,10 (ЗН, триплет, J 7 Гц, Cl-CH -CHj), 2,66 25 держащего 5% диэтиламина толуола. (ЗН, синглет, N-CHj); 3,32 (1Н, С12Ь- Выход 2,52 г (62%) пенообразного -Н); 3,36 + 3,63 (2Н, мультиплетCHjOH); 6,95-7,48 (4Н, мультиплет, ароматические протоны); 8,02 (1Н, уширенный синглет, индол-NH), м.д.
Гидрохлорид: т.пл. 163-169 С (из смеси изопропанола с диизопропиловым эфиром), 11 -81,2 (с 1,0, вода).
Рассчитано, %: С 65,77; Н 8,16; N 10,00; Сг„он 8,44.
Ci,H,ClNjO (молекулярный вес 419-98).
Найдено, %: С 65,65; Н 8,07; N 9,87, Cli,,64.
Пример 10. (-)-(5)-Бутан- -1-ол-2-амид(1S,12bS)-1-зтил-1,2,3,4, 6,7,12,12Ь-окта гидроиндоло(2,3-а)хи- нолизин-1-ил-пропионовой кислоты.
вещества.
ЧН-ЯМР (CDClj): of 1,06 (ЗН, триплет, J 7 Гц, СЬ-СН -СН ; 3,35 30 (Ш, С12Ь-Н), 4,31 (2Н, дублет,
JCK,.NH 5 Гц, Ш-СНг); 6,44 (1Н, уширенный триплет, CO-NH); 7,0-8,46 (6Н, мультиплет, ароматические протоны + СЗ -Н + С5 -Н); 7,56 (1Н. муль- « типлет, С4 -Н); 8,16 (уширенный синглет, индол-Ш); 8,45 (1Н, мультиплет, €6 -Н), м.д.
Этанолсульфоновокислая соль: т.пл. 207-211°С (из смеси изопропанола с 40 диизопропиловым эфиром) , о/ JJ -78,7 (с 2,0, вода).
Гидрохлорид: т.пл. 168-178 с (изопропанол) .
Пример 12- (-)-4-Фенш1бутилОсуществляют аналогично примеру 1 45 амид(15-12Ь5)-1-этил-1,2,3,4,6,7,12, однако в качестве ацилируемого амина 12Ь-октагидроиндоло()хинолизин50
применяют 1,79 г (0,02 моль) (З)-бу- тан-1-ол-2-амина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при использовании содержащего 10% диэтиламина толуола .
Выход 2,36 г (59%) кристаллизующего масла.
1Н-ЯМР (CDClj): f 1,10 (ЗН, триплет, J 7 Гц, С1-СН -СНз); 0,82 (ЗН, триплет, J 7Гц,ЫН-СН-СНд-СНз); - 3,34 (1Н,С12Ь-Н); 3,47 (2Н,мультиплет, -CH.); 3,68 (1Н, мультиплет. Щ-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1, с тем различием, что в качестве ади- лируемого амина используют 1,64 г (0,11 моль) 4-фенилбутиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при использовании содержащего 5% диэтиламина толуола.
Выход 2,38 г (52%) пенообразного вещества.
1Н-ЯМР (CDClj): f 1,07 (ЗН, триплет, J 7 Гц, С1-СНа-СНр; 3 33
I ClNjOj (молекудярньй вес
434,00).
Найдено, %: С 65,96; Н 8,45; N 9,29; С1„ок7,78.
Пример 11. (-)-Пирид-2-ил- -метиламид(15;12Ь8)-1-зтил-1,2,3,4, 6,7,12,12Ь-октагидроиндоло(2,3-а) хинолизин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1, однако в качестве ацилируемого амина используют 1,20 г (0,011 моль) пирид- -2-ил-метиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола. Выход 2,52 г (62%) пенообразного
держащего 5% диэтиламина толуола. Выход 2,52 г (62%) пенообразного
вещества.
ЧН-ЯМР (CDClj): of 1,06 (ЗН, триплет, J 7 Гц, СЬ-СН -СН ; 3,35 (Ш, С12Ь-Н), 4,31 (2Н, дублет,
JCK,.NH 5 Гц, Ш-СНг); 6,44 (1Н, уширенный триплет, CO-NH); 7,0-8,46 (6Н, мультиплет, ароматические протоны + СЗ -Н + С5 -Н); 7,56 (1Н. муль- типлет, С4 -Н); 8,16 (уширенный синглет, индол-Ш); 8,45 (1Н, мультиплет, €6 -Н), м.д.
Этанолсульфоновокислая соль: т.пл. 207-211°С (из смеси изопропанола с диизопропиловым эфиром) , о/ JJ -78,7 (с 2,0, вода).
Гидрохлорид: т.пл. 168-178 с (изопропанол) .
Пример 12- (-)-4-Фенш1бутил
-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1, с тем различием, что в качестве ади- лируемого амина используют 1,64 г (0,11 моль) 4-фенилбутиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при использовании содержащего 5% диэтиламина толуола.
Выход 2,38 г (52%) пенообразного вещества.
1Н-ЯМР (CDClj): f 1,07 (ЗН, триплет, J 7 Гц, С1-СНа-СНр; 3 33
1114
(1Н, C12b-H); 5,20 (1Н, уширенный триплет, CO-NH); 6,,48 (9Н, муль типлет, ароматические протоны), м.д.
Этансульфоновокислая соль: т.пл. 146-148°С (из смеси изопропанола с диизопропиловым эфиром) , о/3 ;) -58,3 (с 2,0, вода).
Рассчитано, %: С 67,69; Н 7,99; N7,40.
Хмолекулярный вес
567,77)
Найдено, %: С 67,40; Н 8,00; 7,19.
т.пл. 150-159 С
N
Гидрохлорид: (изопропанол).
Пример 13. (-)-Гептаметилен имид(18, 12Ь8)-1-этил-1,2,3,4,6,7,12 12Ь-х)Ктагидроиндоло( 2, 3-а) хинолизин- -1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве аци- лируемого амина используют 1,24 г (0,011 моль) гептаметиленимина. Сырой продукт очшдают с помощью колоночной хроматографии на силикагеле при использова нии содержащего 5% диэтиламина толуола.
Выход 1,78 г (42%) пенообразного вещества.
1Н-ЯМР (CDClg): / 1,09 (ЗН, триплет, J 7 Гц, Cl-CH -CH,); 3,3 (Ш, С12Ь-Н); 6,95-7,47 (4Н, мульти плет, ароматические протоны); 8,10 (1Н, уширенный синглет, индол-МН),
м.д.
.Ш1. 201-238 с -85,4° (с 1,0,
вода).
Рассчитано, %: С 70,79; Н 8,80; N 9,17, CtuoH 7,74.
GjiH ClNjO (молекулярный вес 458,06).
Найдено, %: С 70,53; Н 9,01, N 9,05; С1„„„7,56.
Фосфорнокислая соль: т.пл. 105 - 135 С (разложение) (изопропанол).
Пример 14. (-)-Диэтанола ш (18:12Ь5)-1-этил-1,2,3,4,6,7,12,12Ь -октагидроиндоло(2,3-а)хинолизин-1- -ил-пропионовой кислоты.
Осуществляют аналогично примеру с тем различием, что в качестве аци лируемого амина используют 2,10 г (0,02 моль) диэтаноламина. Сырой продукт очищают с помощью колоночно хроматографии на силикагеле при использовании содержащего 30% диэтиламина толуола.
Гидрохлорид:
25 П
(ацетон).
193
12 (42%)
пенообразного
O
Выход 1,74 г вещества.
1Н-ЯМР (CDClj): 1,08 (ЗН, триплет, J 7 Гц, Cl-CH -CHj); 3,29 (1Н, С12Ъ-Н); 3,25 + 3,60 (4Н, муль- типлет, два ); 6,95-7,48 (4Н, мультиплет, ароматические протоны); 8,08 (1Н, уширенный синглет-индол- HNH), м.д.
13С-ЯМР (CDClgJ: 7,95 (С1- CH -CHj;; 21,81 (С7); 21,81 (СЗ); 27,70 (С13); 29,03 (С12), 30,30. (Cl-CHi-CHj); 34,60 (С2); 39,72 5 (C1)F 50,48 и 52,12 (два N-CH);
54,26 (С6); 56,87 (С4); 60,37 и 61,09 (два СН,-ОН); 66,87 (С12Ь); 111,02 (СП), 111,07 (С7а); 117,72 (С8) ; 119,48 (С9); 121,65 (СЮ); 126,71 с (С7); 134,12 (С12а); 136,09 (С11а); 176,16 (ПСО), м.д.
А обмениваемые друг с другом.
Гидробромид: т.пл. 135°С (разложение) (этилацетат) , -62,9° 25 (с 2,0, вода).
Рассчитано, %: С 58,29; Н 7,34; N 8,50; Вг„,„16,16.
C,,HjiBrN,,Oj (молекулярный вес 494,46).
30 Найдено, %: С 57,72; Н 7,42; N 8,29; Вг„„„16,06.
Пример 15. (-)-2-Оксиэтил- амид(15,12Ь5)-1-этил-1,2,3,4,6,7,12, 12Ь-октагидроиндоло(2,3-а)хинолизин- -1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 однако в качестве ацилируемого амина используют 0,67 г (0,011 моль) эта-, ноламина. Сырой продукт очищают с
лл помощью колоночной хроматографии на до
силикагеле при применении содержащего
30% диэтиламина толуола. Выход 1,47 г (40%) пенообразного вещества.
1Н-ЯМР (СВС1з): «f 1,10 (ЗН, триплет, J 7 Гц, С1-СН7-СН,); 3,34
(1Н, С12Ь-Н); 3,55 (2Н, триплет, J 5 Гц, ), 5,68 (1Н, уширенный триплет, CO-NH); 7,0-7,49 (4Н, ароматические протоны); 7,88 (1Н, уширенный сиНглет, индол-NH), м.д.
50 Гидробромид: т.пл. 169-179 С при разложении (изопропанол), -67,7° (с 1,0, вода).
Рассчитано, %: С 58,66; Н 7,16;
35
55
N 9,33; Вг,о„17,74.
С l BrNjO, (молекулярный вес 450, 41).
Найдено, %: С 58,42; Н 9,45; N 9,45; Вг„е„1б,82.
13
1470193
Гидрохлорид: (изопропанол). Пример
т.пл. 164-178 С
.. I, .... - г 16. (-)-З-Метоксипро- пиламид(18:12Ъ5-1-этил-1j2,3,4,6,7, 12,12Ь-октагидроиндоло(2,3-а)хино- лизин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве аци- лируемого амина используют 0,98 г (0,001 моль) 3-метоксипропиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 20% ди- этиламина толуола. Выход 2,39 г (60%) пенообразного вещества.
1Н-ЯМР (CDClj): с/ 1,08 (ЗН, J 7 Гц, С1-СН -СНз); 3,35 (1Н, С12Ь-Н); 3,12 (2Н, триплет, J - 6 Гц, СН,-ОСНэ); 3,17 (ЗН, синглет ОСНз); 5,76 (1Н, уширенный триплет, CG-NH); 7,0-7,47 (4Н, мультиплет, ароматические протоны); 8,07 (1Н, уширенный синглет, индол-Н), м..
Гидрохлорид: т.пл. 144-149 С (изопропанол), ЫJ if 72,5 (с 1,0
Рассчитано, %: С 66,41; Н 8,36; 9,68; 8,17.
(молекулярный вес 434,00)
Найдено, 7.: С 66,47; Н 8,71; 9,52; С1«ои8,17.
Пример 17. (-)-й1-2-Оксипр пиламид(.15;12Ь5-1-этил-1 ,2,3,4,6,7, 12,12Ь-октагидроиндоло(2,3-а)хино- лизин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру с тем различием, что в качестве аци лируемого амина используют 0,83 г (0,011 моль) cil-2-оксипропиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагел при применении содержащего 30% ДИ- эталамина толуола. Выход 1,60 г (42 пенообразного вещества. 1Н-ЯМР (CDClj): с 1,08 (ЗН,. трплет, J 7 Гц, Cl-CHi-QHj); 1,02 (ЗН, дублет, J 7 Гц, OH-CH-CH); 3 33 (1Н, С12Ь-Н); 3,71 (1Н, мулЬти плет, СН-ОН); 5,82 (1Н, уширенный триплет, CO-NH); 6,95-7,49 (4Н, мултиплет, ароматические протоны); 8,0 (1Н, уширенный синглет, индол-Ш),
гидрохлорид: т.пл. 175-181 С (ипропанол), -75,4 (с 1,0., вода).
N
N
N
0
15
20
25
35
N
14
Рассчитано, %: С 65,77; Н 8,16; 10,01; ,44.
q ClNjO (молекулярный вес - 419,98).
Найдено, %: С 65,48; Н 8,12; 9,86; С1,он8,22.
Гидробромид: т.пл. 184-191 С (изопропанол) .
Этансульфоновокислая соль: т.пл.
185-200°С (ацетон).
Пример 18. (-)-Циклопропш1- амид(15:12Ь8)-1-зтил- 1,2,3,4,6,7,12, 12Ь-октагиДроиндоло(2,3-а)хинолизин- -1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве аци- лируемого амина используют 0,63 г (0,t1 моль) циклопропил амина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при использовании содержащего 20% диэтил- амина толуола.
Выход 2,15 г (59%) пенообразного вещества.
1Н-ЯМР (CDClj): rf 1,10 (ЗН, триплет, J 7 Гц, С1-СНа-СНз); 3,34 (1Н, С12Ь-Н); 0,15-0,8 (4Н, мультиплет, С2 -Hj и СЗ -Н,); 1,85 (1Н, 30 мультиплет, Cl -H); 5,30 (1Н, уши- ренный синглет, CO-NH); 7,0-7,5 (4Н, мультиплет, ароматические протоны); 8,0 (1Н, уширенный синглет, индол/ -Ш), м.д.
Этансульфонат (этансульфоновокислая соль): т.пл. 160-167 0 (ацетон), (с 2,0, вода).
С 63,13; Н 7,84;
40
-65,7
Рассчитано, N 8,83; S 6,74.
. (молекулярный вес
475,63).
С 62,72; Н 8,15;
т.пл. 193-200 С
Найдено, %: N 8,74; S 6,73. Гидробромид: ., (изопропанол).
пример 19. (-)-N-ЭтшI-2- -oкcиэтилaмид(1S,12ЪS)-1-зтил-1,2, 3,4,6,7,12,12Ь-октагидроиндоло(2,3- -а)хинолизин-1-ил-пропионовой кис-
лоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве ацили- руемого амина используют 0,98 г (0,011 моль) К-этш1-2-оксиэтиламина. Сырой продукт очищают путем перекристаллизации из изопропанола. Выход .2,44 г (61%), т.пл. 199-202°С.
1Н-ЯМР (CDClj): cf 1,09 (ЗН, триплет, J 7 Гц, Cl-CHi-СНр; 0,71 +
55
+ 0,98 (ЗН, триплет, J 7 Гц, N- ); 3,30 (1Н, С12Ь-Н); 3,6 (2Н, мультйплет, ); 6,95-7,48 (4Н, мультйплет, ароматические про- тоны); 8,02 и 8,10 (1Н, уширенный синглет, индол-NH), м.д.
Гидробро ид: т.пл. 235-239°С (разложение) ( изопропанола с диизопропиловым эфиром). « 1д -77,9 (с 2,0, вода).
Рассчитано, %: С 60,24; Н 7,58; М 8,78; Br;,J6,70.
Cj lj BrNjO/i (молекулярный вес 478,46).
Найдено, %: С 60,29; Н 7,35; N 8,59; Вг„,„1б,52.
Пример 20. (-)-Аллиламид (13,12ЬЗ)-1-этил-1,2,3,4,6,7,12,12Ь -октагидроиндоло(2,3-а)хинолизии-1- -ил-пропионовой кислоты.
Осуществляют аналогично примеру однако в качестве ацилируемого амин используют 0,63 г (0,011 моль) ал- лиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 10% диэтиламина толуола. Выход 1,50 г (41%) пенообразного вещества 1Н-ЯМР (CDClj): 1,09 (ЗН, триплет, J ; 7 Гц, Cl-CH/i-CHj); 3,3 (1.Н, C12b-H); 3,71 (2Н, мультиплект Ш-СНа); 5,03 и 5,06 (2Н, мультйплет, СН), 5,20 (1Н, уширенный тр .плет, NH-CH);,5,71 (1Н, мультйплет, -СН) ; 6,95-7,49 (4Н, мультйплет, ароматические протоны(; 7,94 (1Н, уширенный синглет, индол-NH), м.д.
Метансульфонат (метансульфоново- кислая соль): т.пл. 257-261 С (изо- пропанол), -74,2° (с 2,0, вода).
Рассчитано, %: С 62,44; Н 7,64; N 9,10; S 6,95.
Cj E jN304S (молекулярный вес 461,61).
Найдено, %: С 62,39; Н 7,99; N 8,70; S 6,65.
Пример 21. (-)-2-Метокси- этш1амид(13:12Ь8)-1 этил-1,2,3,4, 6,7,12,12Ь-октагидроиндоло(2,3-а) хинолизин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру с тем различием, что в качестве аци- лируемого амина используют 0,83 г (0,011 моль) 2-метоксиэтиламина. Сы рой продукт очищают с. помощью коло
0
5
5
0
5
N
N
0
5
0
ночной хроматографии на силикагеле при использовании содержащего 10% диэтиламина толуола.
Выход 2,22 г (58%) пенообразного вещества.
1Н-ЯМР (CDClj): 1,10 (ЗН, триплет, J 7 Гц, Cl-CH-CHg); 3,25 (ЗН, синглет, OCHj); 3,32 (1Н, С12Ь-Н); 3,3 (4Н, мультйплет, NH-CH+ +CH«,-OCHj); 5,48 (1Н, уширенный триплет, СО-Ш); 6,95-7,50 (4Н, мультйплет, ароматические протоны); 7,99 (1Н, уширенный синглет, индол-NH), м.д.
Гидробромид: т.пл. 159-1бЗ°С при разложении (изопропанол) ,о( -65,0° (с 2,0, вода).
Рассчитано, %: С 59,48; Н 7,38; 9,05;:Вг„о„17,21.
.: (молекулярный вес 464,43).
Найдено, %: С 59,29; Н 7,82; 8,97; Вг,„1б,88.
Этансульфонат: т.пл. 206-214°С (изопропанол).
Гидрохлорид: т.пл. 148-155 0 (изопропанол).
Пример 22. (-)-Дибензил- амид(1S-12Ь S)-1-этил-1,2,3,4,6,7,12, 12Ь-октагидроиндоло(2,3-а)хинолизин- -1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве ацилируемого амина используют 2,17 г (0,011 моль) дибензиламина. Сырой продукт очищают путем перекристалли - зации из изопропанола.
Выход 2,48 г (49%), т.пл. 140 - 142°С.
Рассчитано, %: С 80,75; Н 7,77.; N 8,31.
C j ijgNjO (молекулярный вес 505,67)
Найдено, %: С 80,66; Н 7,80; N 8,17..
1Н-ЯМР (CDClj)t f 1,05 (ЗН, триплет, J Гц, Cl-CH -CHj), 3,28 (Ш, С12Ь-Н ; 3,95-4,35 (4Н, уширенный синглет, две N-CH,); 6,8-7,45 (14Н, мультйплет, ароматические протоны); 7,92 (1Н, уширенный синглет, индрл-Ш), м.д.
Метансульфонат: т.пл. 205-215 С
смеси изопропанола с диизопропиловым эфиром) , o/J -71,3° (с
(из
-71,3 2,0, вода).
Рассчитано, %: С 69,85; Н 7,20; N 6,98; S 5,33.
17
jO S (молекулярный вес 601,78). Найдено,
1470193
Ь
N
N
С 69,61; Н 7,40;
N 6,83; S 5,43. 5
Этйнсульфонат: т.пл. 188-205 С (изопропанол).
Пример 23. (-)-З-Оксипропил- амид(13,12Ь5)-1-этил-1,2,3,4,6,7,12, 12Ь-октагидроиндоло(2,)хинолизин- i о -1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что дв качестве аци- лируемого амина используют 0,83 г (0,011 моль) 3-оксипропиламина. Сырой 15 продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 10% диэтиламина
zii iT:::.
li-S (cSci,): / 1,09 (ЗН, три-пионовой кислоты при перемешивании плет, J 7 Гц, С1-СН,-СН,); 3,36 (1Н, С12Ь-Н); 3,59 (2Н, триплет, J
- S Гч ГН -он) 6 08 (1Н, уширенный a рипле; СО-Ш 6 9.5- ,49 (4Н, нуль-25(0,02 моль) перегнанного над натритриплет, ои 1чп, , , . „ „т„„ ,„.пч.пЛ1г,т1ння. PacTBOD охлаж.(1Н, уширенный синглет, индол, Ш),
м.д.р
Этансульфонат: т.пл. 215-219 С (из смеси изопропанола с диизопропи- ловым эфиром), D -53,1 (с 2,0, вода).
Рассчитано, %: С 63,56; Н 7,40; 7,17; S 5,47. q H jNjOgS (молекулярный вес 585,74).
Найдено, %: С 63,32; Н 7,22; 7,23; S 5,60.
Пример 25. (-)-Анилид(15: :12ЬЗ)-1-этил-1;2,3,4,6,7,12,12Ь- октагидроиндоло(2,3-а)хинолизин-1- -ил-пропионовой кислоты.
3,26 г (0,01 моль) (-)-(1S:12bS)- -1-этил-1,2,3,4,6,7,12,12Ь-октагнди в атмосфере азота добавляют к приготовленному с 20 мл безводного тет- рагидрофурана раствору 2,04 г
1 ШиХЪ А ) ,-Х -Т 7
типлет, ароматические протоны); 8,23 (1Н, уширенный синглет, индол-NH),
Гидрохлорид: т.пл. 219-229°С (изопропанол), t -76,4° (с 2,0,
вода).
Рассчитано, %: С 65,77; Н 8,16;
N 10,.01; 8,44.
C,Jl,,ClN,Oi (молекулярный вес - 419,98).
Найдено, %:
ем N-метилморфолина. Раствор охлаждают до -5°С. При интенсивном перемешивании прикапывают непрерывно 1,10 г (0,01 моль) этилового эфира 30 хлормуравьиной кислоты, причем внут ренняя температура не должна превышать . Смесь перемешивают в те35
С 65,92; Н 8,24;
N 9,92; С1„ои 8,61.
Этансульфонат: т.пл. 200-218 С
(изопропанол).
Пример 24. (-)-2,4-Диметок- дО сибензиламид(15:12Ь5)-1-этил-1,2,3,4, 6,7,12,12Ь-октагидроиндоло-(2,3-а) хинолизин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что используют 45 1,84 г (0,011 моль) 2,4-диметокси- бензиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 10% диэтиламина толуола. Вькод Q 2 81 г (59%) пенообразного вещества. 1Н-ЯМР (CDCl,): cf 1,08 (ЗН, триплет, J 7 Гц, С1-СН -СНз); 3,34 (1Н С12Ь-Н); 3,,73 (6Н, синглет, два OCHj); 4,23 (2Н, дублет, JCH.NIT 55 5 Гц); 5,61 (1Н, уширенный триплет,, CO-NH); 6,39 (2Н, мультиплет, СЗ -Н ч С5 -Н); 6,95-7,48 (5Н, мультиплет, ароматические протоны С6 -Н), 7,99
чение 30 мин при , затем при (5) - в течение примерно 10 ми прикапывают приготовленный с 10 мл безводного тетрагидрофурана раствор 1,86 г (0,02 моль) анилина при сохранении внутренней температуры ниже 0°С. Смесь перемешивают в течение 30 мин и затем еще следующие 4ч причем позволяют температуре поднят ся до комнатной. Реакционную смесь выпаривают на ротационном испарител и остаток смешивают с 50 мл дихлор- метана, а также 50 мл воды. Смесь встряхивают. Нерастворившееся в воде и дихлорметане вещество (которое представляет собой гидрохлорид обра зовавшегося соединения) отфильтровы вают, хорошо промывают дихлорметано и затем водой, суспендируют в смеси 25 мл воды с 25 мл дихлорметана и суспензию при энергичном перемешивании осторожно подщелачивают с пом щью 4,24 г (0,04 моль) карбоната н рия. После того, как все растворил органическую фазу отделяют, промыв трижды по 10 мл водой, сушат над с фатом магния и затем выпаривают. П
N
N
(1Н, уширенный синглет, индол, Ш),
.д.р
Этансульфонат: т.пл. 215-219 С (из смеси изопропанола с диизопропи- овым эфиром), D -53,1 (с 2,0, вода).
Рассчитано, %: С 63,56; Н 7,40; 7,17; S 5,47. q H jNjOgS (молекулярный вес 585,74).
Найдено, %: С 63,32; Н 7,22; 7,23; S 5,60.
Пример 25. (-)-Анилид(15: :12ЬЗ)-1-этил-1;2,3,4,6,7,12,12Ь- октагидроиндоло(2,3-а)хинолизин-1- -ил-пропионовой кислоты.
3,26 г (0,01 моль) (-)-(1S:12bS)- -1-этил-1,2,3,4,6,7,12,12Ь-октагндпионовой кислоты при перемешивании
a (0,02 моль) перегнанного над натрии в атмосфере азота добавляют к приготовленному с 20 мл безводного тет- рагидрофурана раствору 2,04 г
5(0,02 моль) перегнанного над натри„„ ,„.пч.пЛ1г,т1ння. PacTBOD охлажем N-метилморфолина. Раствор охлаждают до -5°С. При интенсивном перемешивании прикапывают непрерывно 1,10 г (0,01 моль) этилового эфира 0 хлормуравьиной кислоты, причем внутренняя температура не должна превышать . Смесь перемешивают в те5
дО
45 Q 55 ,
чение 30 мин при , затем при (5) - в течение примерно 10 мин прикапывают приготовленный с 10 мл безводного тетрагидрофурана раствор 1,86 г (0,02 моль) анилина при сохранении внутренней температуры ниже 0°С. Смесь перемешивают в течение 30 мин и затем еще следующие 4ч, причем позволяют температуре подняться до комнатной. Реакционную смесь выпаривают на ротационном испарителе и остаток смешивают с 50 мл дихлор- метана, а также 50 мл воды. Смесь встряхивают. Нерастворившееся в воде и дихлорметане вещество (которое представляет собой гидрохлорид образовавшегося соединения) отфильтровывают, хорошо промывают дихлорметаном и затем водой, суспендируют в смеси 25 мл воды с 25 мл дихлорметана и суспензию при энергичном перемешивании осторожно подщелачивают с помощью 4,24 г (0,04 моль) карбоната натрия. После того, как все растворилось, органическую фазу отделяют, промывают трижды по 10 мл водой, сушат над сульфатом магния и затем выпаривают. Получают 2,69 г (67%) соединения, которое можно очищать путем перекристаллизации из толуола, Т.ил. 159-163 С.
1Н-ЯМР (CDCl,,): 1,08 (ЗН, гриплет, J 7 Гц, Cl-CH -CHj; .3,33 4lH, C12b-H), 6,92 (1Н, уширенный синглет, CO-NH); 7,0-7,51 (9Н, муль- типдет, ароматические протоны); 7,92 (1Н, уширенный синглет, индол-NH), м.д; .
Метансульфонат: т.пл. 167-170 С (вода), Ce Dj -86, (с 2,0, этанол).
Рассчитано, %: С.65,16; Н 7,09; N 8,44; S 6,44.
С JJIjO S (молекулярный вес 497,64).
Найдено, %: С 64,90; Н 6,89; N 8,60; S 6,44.
Гидрохлорид: т.пл. 200-250 С с постепенным плавлением (этанол).
1Н-ЯМР (CDCljt ДМСО): сГ 1,07 (ЗН, триплет, J 7 Гц, Cl-CH -CHj); 4,46 (1Н, С12Ь-Н); 6,86-7,70 (9Н, мультиплет, ароматические протоны); 9,6 (1Н, уширенный синглет, СО-Ш); 9,78 (1Н, уширенный синглет, индол- -NH), м.д.
13С-ЯМР (CDClj + ДМСО): f 7,97 (Cl-CH-j-CHj); 18,67 (03); 18,67 (С7); 28,79 (С13); 30,03 (С14); 30,71° (Cl-CHa-CHj); 31,65 (С2); 39,85 (С12); 54,70 (С6); 55,53 (С4); 67,46 (С13Ь); 108,71 (С7а); 112,54 (СП); 117,78 (С8); 119,63 (С9); 122,46 (СЮ); 125,46 (С12а); 126,56 (С7Ь); 137,33 (Cl la); 119,63 + 128,34 + 123,21 + 139,05 (фенил- -С-атомы); 171,81 (NCO), м.д.
о - обмениваемы друг с другом.
Этансульфонат: т.пл. 157-161°С (вода).
Лимоннокислая соль (цитрат): т.пл. Г36-140°С (вода).
D-Гидротартрат: т.пл. 135-140°С (вода).
Гидробромид: т.пл. 203-212°С (изопропанол).
Фосфорнокислая соль (фосфат): т.пл. 16р-167°С (изопропанол).
Пример 26. (-)-4-Хлорбен- зиламид(15:12bS)-1-этил-1,2,3,4,6,7, 12,12Ь-о.ктагидроиндоло(2,3-а)хино- лизин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве аци- лируемого амина применяют 1,56 г (0,011 моль) 4-хлорбенаиламина.
Выход 2,56 г (57%) кристаллизующегося при стоянии масла.
1Н-ЯМР (CDClj): :f 1,10 (ЗН, триплет, J 7 Гц, Cl-CHi-CHj); 3,33 (1Н, С12Ь-Н); 4,20 (2Н, дублет.
0
5
СН, NW
5 Гц, Ш-СН); 5,51 (1Н, уши- рен ный триплет, CO-NH); 7,0-7,48 (8Н, мультиплет, ароматические про- тоны); 7,94 (1Н, уширенный синглет, индол-NH), м.д.
Фосфат: т.пл. 155-158°С (изопропанол), Ы1 65,9° (с 2,0, вода).
Этансульфонат: т.пл. 141-145 С (из смеси изопропанола с диизопропи- ловым эфиром).
Гидрохлорид: т.пл. 227-240 С (изопропанол) .
0 Пример 27. (-)-4-Метилбензил- амид(13:12Ь5)-1-этил-1,2,3,4,6,7,12, 12Ь-октагидроиндоло(2,3-а)хинолизин- -1-ил- пропионовой кислоты.
Осуществляют аналогично примеру 25 5 с тем различием, что в качестве аци- лируемого амина используют 1,34 г (0,015 моль) 4-метилбензиламина. Выход 2,61 г (61%) медленно кристаллизующегося при стоянии масла. 0 1Н-ЯМР (CDClj): с/ 1,08 (ЗН, триплет, J 7 Гц, Cl-CH,-CHj); 2,27 (ЗН, синглет, фенил-СНJ; 3,33 (1Н, С12Ь-Н); 4,22 (2Н, дублет, J снг.мк 5 Гц, Ш-СН,); 5,52 (1Н, уширенный 5 триплет, CO-NH); 6,95-7,47 (8И, мультиплет, ароматические протоны), 8,0 (1Н, уширенный синглет, индол-NH), м.д.
Фосфат: плавится начиная с 85 С Q постепенно при разложении (изопропанол), Ы ц -65,3° (с 2,0 йода). Гидрохлорид: т.пл. 220-242 С (изопропанол) .
Метансульфонат: т.пл. 140-148 С с (из смеси изопропанола с диизопропи- ловым эфиром).
Пример 28. (-)-4-Метилани- лид(15:12Ь8)-1-этил-1,2,3,,7,12, 12Ь-октагидроиндоло(2,3-а)хинолизин- -1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 25,- однако в качестве ацилируемого амина используют 1,18 г (0,011 моль) 4-метиланилина.
Выход 2,54 г (61%) соединения, которое можно очищать далее путем перекристаллизации из изопропанола.
1Н-ЯМР (CDClj): У 1,09 (ЗН, триплет, J 7 Гц, Cl-CH -CHj); Ь78
21
(2Н, квинтет, J 7 Гц, С1-СНг-СНj); 2,23 (ЗН, синглет, фенил-СНз); 3,35 (1Н С12Ь-Н); 6,80 (1Н, уширенный синглет, СО-р); 7,0-7,50 (4Н, муль- типлет, ароматические протоны); 7,0 (2Н, мультиплет, СЗ -Н + С5 -Н); 7,20 (2Н, мультиплет, С2 -Н + С6 -Н); (1Н, уширенный синглет, индол-NH), м.д.
Метансульфонат: т.пл. 196-199 С (изопропанол) , Co J д -92,3 (с 1, этанол).
Рассчитано, %: С 65,72; Н 7,29; N 8,21; S 6,27.
(молекулярный вес 511,66).
Найдено, %: С 65,36; Н 6,95; N 8,15; 6,28.р
Гидрохлорид: т.пл. 147-159 С. Пример 29. (-)-З-Трифтор- метиланилид(13:12ЪЗ)т1-этил-1,2,3,4, 6,7,12,12Ь-октагидроиндоло(2,3-а) хинолизин-1-ил-пропионовой кислоты. Осуществляют аналогично примеру 25, однако в качестве ацилируемого амина используют 1,77 г (0,011 моль) 3-трифторметиланилина. Выход 3,2 г (68%) соединения, которое можно перекристаллизовать из смеси толуола с н-гексаном. Т.пл. 154-155,5 С. to -135,5° (с 2,0 этиловый спирт).
Рассчитано, %: С 69,06; Н 6,44;
N-8,95.
,N,0 (молекулярный вес
469, з з).
Найдено, %: С 69,04; Н 6,56;
.N 8,95.
1Н-ЯМР (CDCb): rf 1,10 (ЗН, триплет, J 7 Гц. С1-С1Ц-СНз); 1,76 (2Н, квинтет, 7 Гц, Cl-CH -CHj); 3 34 (1Н, С12Ь-Н); 6,90 (1Н, уширен- льш синглет, CO-NH); 7,0-7,60 (8Н, мультиплет, ароматические протоны +С2 -Н -Н С4 Н С5 -Н + С6 -Н); 7,8 (1Н, уширенный синглет, индол-NH),
м-Д.о
Гидрохлорид: т.пл. /14-zzt ь.
Метансульфонат: т.пл. 220-228 С (изопропанол).
Пример 30. (-)-4-Метокси- анилид(15:12Ь5)-1-этил-1,2,3,4,6,7, 12,12Ь-октагидроиндоло(2,3-а)хиноли зин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 25, однако в качестве ацилируемого амина используют 1,35 г (0,011 моль 4-метоксианилина.
;
10
0193 22
Выход 2,66 г (62%) пенообразного вещества.
1Н-ЯМР (CDClj): «Г 1,08 (ЗН, триплет, J 7 Гц, Cl-CHj-CHj); 1,75 (211, квинтет, J 7 Гц, С1-СН --СН j) ; 3,33 (1Н, С12Ь-Н); 3,70 (ЗН, синглет, OCHj); 6,74 (2Н, мультиплет, СЗ -Н н- + С5 -Н); 6,91 (1Н, уширенный синглет, CO-NH); 7,20 (2Н, мультиплет, С2--Н + С6 -Н); 6,91 (1Н, уширенный . синглет, CO-NH), 7,20 (2Н, мультиплет, С2 -Н С6 -Н); 7,0-7,51 (4Н, мультиплет, ароматические протоны), 7,97 (1Н, уширенный синглет, индол-NH), м.д.
Метансульфонат: т.пл. 190-197 С (изопропанол), -88,9° (с 1, этанол).
Рассчитано, %: С 63,73; Н 7,07; N 7,96; S 6,08.
С „Hj,N jOj S (молекулярный вес - 527,66).
Найдено, %: С 53,57; Н 6,98; N 7,89; S 6,10.
Пример 31. (-)-4-Фенилани- лид(15:12ЬЗ)-1-этил-1,2,3,4,6,7,12, 12Ь-октагидроиндоло(2,3-а)хинолизин-1-ил-пропионовой кислоты.
Осуществля19т аналогично примеру 25 с тем различием, что в качестве ацилируемого амина используют 1,86 г (0,011 моль) 4-аминобифенила. Выход 2 93 г (61%) соединения, которое можно очищать путем перекристаллизации из толуола. Т.пл. 97-105 С,
20
25
30
35
ЦПГ1 JTJ-Jiv--
(«.-152,3 (с 2, этанол).
Рассчитано, %: С 80,47; Н 7,39;
8,80. Cj-jH gNjO (молекулярный вес 477,62).
Найдено, %: С 81,06; Н 7,65; N 8,90.1
1Н-ЯМР (CDClj): 1,08 (ЗН, триплет, J 7 Гц, Cl-CH -CHj); 1 76 (2Н, квинтет, J 7 Гц, Cl-CH- - -CHj); 3,33 (Ш, C12b-H); 6,91 (1Н, уширенньш с,инглет, CO-NH) , 6,95 7,55 (13Н, мультиплет, ароматические протоны); 7,89 (1Н, уширенный синглет, индол-NH), м.д. Гидрохлорид: т.пл. 257-271 С. Метансульфонат: т.пл. 220-244 С (изопропанол).
Пример 32. (-)-4-Ацетш1ани- лид(1S:12bS)-1-этил- 1,2,3,4,6,7,12, 12Ь-октагидроиндоло(2,3-а)хинолизин- -1-ил-пропионовой кислоты..
Осуществляют аналогично примеру 25 с тем различием, что в качестве ацилируемого амина используют 1,49 г (0,011 моль) 4-аминоацетофенона. Выход 1,45 г (33%) пенообразного вещества,
(CDCl): 1,11 (ЗН, триплет, J 7 Гц, Cl-CHj-CH,); 1,79 (2Н, квинтет, J 7 Гц, С1-СН СНз); 2,47 (ЗН, синглет, СО-СНз); 3,36 (1Н, С12Ь-Н); 7,03 (1Н, уширенный синглет, CO-NH); 7,0-7,52 (4Н, муль- типлет, ароматические протоны); 7,39 (2Н, мультиплет, С2 -Н + Сб -Н) 7,82 (2Н, мультиплет, СЗ -Н + С5 -Н) 7,88 (1Н, уширенный синглет, индол- -NH), м.д.
Гидрохлорид: т.пл. 164-173 0.
Пример 33. (-)- 4-Оксибен- зиламид(13:12ЬЗ)-1-этил--1,2,3,4,6,7, 12,12Ь-октагидроиндоло(2,3-а)хиноли- зин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 25 с тем различием, что в качестве ацилируемого амина используют 1,35 г (0,011 моль) 47оксибензиламина.
Выход 2,41 г (56%) пенообразного вещества. .
1Н-ЯМР (CDClj): f 1,06 (ЗН, три плет, J 7 Гц, Cl-CHt-CHj); 3,32 (1Н, С12Ь-Н); 4,14 (2Н, дублет, JcHa,«H 5 Гц, NH-CHa);, i5 (1Н, уширенный синглет, ОН); 5,63 (1Н, уширенный триплет, CO-NH); 6,65 (2Н, мультиплет, + С5 --Н), 6,90 (2Н, мультиплет, С2 -Н + Сб -Н); 7,0-7,47 (4Н, ароматические протоны) 7,96 (1Н, уширенный сннглет, индол- -NH), м.д.
Этансульфонат:, т.пл. 152-160 с при разложении (изопропанол), j, -59,б (с t,0, вода).
Рассчитано, %: С 64,33; Н 7,26; N7,76; S 5,92.
Cj HjjNjOyS (молекулярный вес So 541,69)
Найдено, % ,С 64,59; И 7,50; N 7,69; S 5,82.
Метансульфонатг т.пл. 157-164 С
(изопропанол).
Пример 34. (-)-Бензиламид (18:12Ь5)-1-этил-1,2,3,4,6,7,12,12Ь- -октагидроиндоло)2,3-а)хинолизин-1- -ил-уксусной кислоты.
3,12 г (0,01 моль) (-)-(1S;12bS)- -1-этил-1,2,--3,4,6,7,12,12Ь-октагид- роиндоло ( 2,3- а ). хинолизин-1 -ил-уксусной кислоты при перемешивании ив ат
0
5
0 0
5
5
0
мосфере азота добавляют к приготовленному с 20 мл безводного тетрагид- рофурана раствору 2,04 г (0,02 моль) перегнанного над натрием N-метилмор- фолина. Раствор охлаждают до -5 С и при интенсивном перемешивании по каплям, однако непрерьшно, смешивают- с 1,10 г (0,01 моль) зтилового эфира хлормуравьиной кислоты, причем внутренняя температура не должна превьш1ать . Реакционную смесь перемешивают в течение 30 мин при , затем при (-5) - 0°С в течение примерно 10 мин прикапывают приготовленный с 10 мл безводного тетрагидро- фурана раствор 1,18 г (0,011 моль) бензиламина при сохранении внутренней температуры ниже 0°С. Реакционную смесь перемешивают при в течение 30 мин и затем еще следуюЕ1Ие 4 ч, причем позволяют температуре подняться до. комнатной. Реакционную смесь выпаривают на ротационном ис- |парителе, остаток смешивают с 50 мл цихлорметана и 20 мл воды и хорошо встряхивают. Органическую фазу отде- пяют, промывают 20 мл 5%-ного рас тво- ра соды и затем 20 мл воды, сушат над сульфатом магния и выпаривают. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 10% диэтиламина толуола. Выход 1,89 г (44%) соединения, которое можно очищать далее путем перекристаллизации из бензола, .т.пл. 179-180 с.
1Н-ЯМР (СВС1з): с 1,13 (ЗН, триплет, J 7 Гц, Cl-CH/i-CHj); 3,70 и 4,24 (2Н, каждый - дублет; J р„ 15 Гц, JCMI,NH 5 + 7 Гц, фе- нил-СН); 3,34 (1Н, С12Ь-Н); 5,80 (1Н, уширенный триплет, CO-NH); 7,0-7,49 (9Н, мультиплет, ароматические протоны); 7,92 (1Н, уширенный триплет, индол-NH); 2,20 и 2,62 (2Н, дублет, J гр„ 14,5 Гц CO-CH-j), м.д.
П-Гйдротартрат: т.пл. 112-116 С (изопропанол), -55 (с 1, зтанол).
Рассчитано, %: С 65,32; Н 6,76; N7,62.
jO (молекулярный вес 551,62).
Найдено, %; С 64,92; И 6,71; N 7,61.
П р и м е р. 35. (-)-Анилид(13:
:12ЬЗ)-1-этил-1,2,3,4,6,7,12,12Ь25 1470193
-октагидроиндоло(2,3-а)хинолизин- -1-ил-уксусной кислоты.,
Осуществляют аналогично примеру 34, однако в качестве ацилируемого амина используют 1,02 г (0,011 моль) анилина. Сырой -продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола. Выход 1,47 г (38%) пенообразного вeщecтвai
1Н-ЯМР (CDC1): 1,16 (ЗН, триплет, J 7 Гц, Cl-CHj-CH); 2,34 +
,14.5 Гц,
10
26
Пример 37. (-)-(3)-1-Фенил зтиламид(13:12ЬЗ)-1-этил-1,2,3,4,(5, 7,12,12Ь-октагидроиндоло(2,.3-а)хино- лизин-1-ил-уксусной кислоты.
Осуществляют аналогично примеру 34, однако в качестве ацилируемого ,амина используют 1,33 г (0,011 моль) (3)-1-фенилэтш1амина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола. Выход 1,66 г (40%) соединения, которое может быть Ь 1ищено далее пус 1,10 (ЗН, Гц, Cl-CH-z- CH); 1,34 7 Гц, NH-CH -CH);
+ 2,68 (2Н, дублет, Jrt«
СО-СНл); 3 40 (1Н, С12Ь-Н); 6,93-7,47 .с .тем перекристаллизации из этанола.
- - ч- - -г з -s.nsi. 188-192 с.
1Н-ЯМР (CDCl):. триплет, J 7 (ЗН, дублет, J
3,35 (1Н, С12Ь-Н); 4,91 (1Н, мульти- плет, NH-CH); 5,87 (1Н, дублет, JNHCH 7 Ц CO-NH); 7,0-7,48 (9Н, мул ьтиплет, ароматические протоны); 7,65 (1Н, уширенный синглет, индол25
(9Н, ароматические протоны); 7,75 (1Н, уширенный синглет, CO-NH); 7,88 (1Н, уширенный синглет, индол-NH),
м.д.
Метансульфонат: т.пл. (изопропанол) , т -164
172-180 С ° (с
20
1,0, метанол).
Рассчитано, %: С 64,57; Н 6,28; N 8,69; S 6,63.
, (молекулярный вес 483,61).
Найдано, %: С 64,44; Н 6,64; N 8,62; S 6,82.
Пример 36. (-)-(3)-1-Фенил- этиламид()-1-этил-1,2,3,4,6, 7,12,12Ь-октагидроиндоло)2,3-а)хино- лизин-1-ил-уксусной кислоты.
Осуществляют аналогично примеру 34, однако в качестве ацилируемого амина используют 1,33 г (0,011 моль) (3)-1-фенилэтиламина. Сьфой продукт, очищается с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола.
Выход 1,47 г (38%) пенообразного вещества.
1Н-ЯМР (CDClj): 1,16 (ЗН, триплет, J 7 Гц, С1-СН2-СНз); 2,34 + + 2,68 (2Н, дублет, Лгем 1,5 Гц, СО-СНг); 3,40 (1Н, С12Ь-Н); 6,95 - 7,47 (9Н, мультиплет, ароматические протоны); 7,75 (1Н, ущиренный синглет, CO-NH); 7,88 (1Н, уширенный синглет, индол-Ш) , м.д.
Метансульфонат: T.jxn. 172-18{ГС (изопропанол), -1644 (с « 1,0, метанол).
Рассчитано,, %: С 64,57; Н 6,28; N 8,69; S 6,63.
CLH (молекулярный вес « 48,61).
Найдено, %: С 64,44; Н 6,64; N 8,62; 3 6,82.
ге
3d
35
40
45
50
55
-NH), 2,58 и 2,83 (2Н, дублет, 15 Гц, СО-СН), м.д.
Фосфат: Т.пл. 130°С при разложе- нии (изопропанол),Г(1 .и -125 (с 1, метанол).
Пример 38. (-)-(Ю-1-Фенил- этиламид(18:12ЬЗ)-1-зтил-1,2,3,4,6, 7,12,12Ь-октагидроиндоло(2,.3-а)хино- лизин-1-ил-уксусной кислоты.
Осуществляют аналогично примеру 34, однако в качестве ацилируемого амина используют 1,,33 г (0,011. моль) (Ю-1-фенилэтиламина. Сьфой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола. Выход 1,67 г (40%) соединения, которое может быть очищено далее путем перекристаллизации из этанола. Т.пл. 138-142 С.
1Н.ЯМР (CDClj): (f 1,08 (ЗН, дублет, J 7 Гц, NH-CH-СНз); 1,12 (ЗН, триплет, J 7 Гц, Cl-CHj-CHj); 2,27 и 2,61 (2Н, дублет, Jre« 15 Гц, СО.-СН); 3,32 (1Н, С12Ь-Н); 4,78 (1Н, мультиплет, NH-CH); 5,78
дублет, .J,c« 7 Гц, CO-1NH);
(1Н,
7,0-7,50 (9Н, му льтиплет, ароматичес кие протоны); 7,91 (1Н, уширенный синглет, индол-Ш), м.д.
Фосфат: разлагается, 140 (с 1,0, метанол).
Пример 39. (-)-Гептаметилен имид(1S:12bS)-1тэтил-J,2,3,4,6,7,12,
начиная со С (изопропанол), -35
0
26
Пример 37. (-)-(3)-1-Фенил зтиламид(13:12ЬЗ)-1-этил-1,2,3,4,(5, 7,12,12Ь-октагидроиндоло(2,.3-а)хино- лизин-1-ил-уксусной кислоты.
Осуществляют аналогично примеру 34, однако в качестве ацилируемого ,амина используют 1,33 г (0,011 моль) (3)-1-фенилэтш1амина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола. Выход 1,66 г (40%) соединения, которое может быть Ь 1ищено далее пус 1,10 (ЗН, Гц, Cl-CH-z- CH); 1,34 7 Гц, NH-CH -CH);
):.
Н); 4,91 (1Н, мульти- ,87 (1Н, дублет, -NH); 7,0-7,48 (9Н, матические протоны); нный синглет, индол3,35 (1Н, С12Ь-Н); 4,91 (1Н, мульти- плет, NH-CH); 5,87 (1Н, дублет, JNHCH 7 Ц CO-NH); 7,0-7,48 (9Н, мул ьтиплет, ароматические протоны); 7,65 (1Н, уширенный синглет, индол5
ге
d
5
0
5
0
5
-NH), 2,58 и 2,83 (2Н, дублет, 15 Гц, СО-СН), м.д.
Фосфат: Т.пл. 130°С при разложе- нии (изопропанол),Г(1 .и -125 (с 1, метанол).
Пример 38. (-)-(Ю-1-Фенил- этиламид(18:12ЬЗ)-1-зтил-1,2,3,4,6, 7,12,12Ь-октагидроиндоло(2,.3-а)хино- лизин-1-ил-уксусной кислоты.
Осуществляют аналогично примеру 34, однако в качестве ацилируемого амина используют 1,,33 г (0,011. моль) (Ю-1-фенилэтиламина. Сьфой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола. Выход 1,67 г (40%) соединения, которое может быть очищено далее путем перекристаллизации из этанола. Т.пл. 138-142 С.
1Н.ЯМР (CDClj): (f 1,08 (ЗН, дублет, J 7 Гц, NH-CH-СНз); 1,12 (ЗН, триплет, J 7 Гц, Cl-CHj-CHj); 2,27 и 2,61 (2Н, дублет, Jre« 15 Гц, СО.-СН); 3,32 (1Н, С12Ь-Н); 4,78 (1Н, мультиплет, NH-CH); 5,78
дублет, .J,c« 7 Гц, CO-1NH);
(1Н,
7,0-7,50 (9Н, му льтиплет, ароматические протоны); 7,91 (1Н, уширенный синглет, индол-Ш), м.д.
Фосфат: разлагается, 140 (с 1,0, метанол).
Пример 39. (-)-Гептаметилен- имид(1S:12bS)-1тэтил-J,2,3,4,6,7,12,
начиная со С (изопропанол), -35
271А70193
12Ь-актагидроиндоло(25,3-а)хинолизин- -1-ил-уксусной кислоты.
Осуществляют аналогично примеру 34, однако в качестве ацилируемого амина применяют 1,24 г (0,011 моль) гептаметиленимина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола. Выход 1,84 г (45%) соединения, которое может быть очищено путем перекристаллизации из этанола. Т.пл, 137-139°С.
28
ную смесь перемешивают в течение 30 мин при О С и затем еще следующи 4 ч при комнатной температуре. Смес выпаривают на ротационном испарите- ле и остаток смешивают с 50 мл ди- хлорметана, а также 20 мл воды. Пос ле тщательного встряхивания нераст- воримьй осадок отфильтровывают. Ор- .Q ганическую фазу отделяют., промывают 4 раза по 20 мл водой, сушат над сульфатом натрия и, .наконец, выпаривают. Сырой продукт очищают с пом щью колоночной хроматографии на си1Н ЯМР(CDCU): 1,15 (ЗН, три- is ликагеле при применении содержащего
,,- Ч .. 1-Ч f Г-Л Г 1-.-г П| п-ж гч ълтт1( Rl-TV n (1 cl Т
плет, J 7 Гц, С1-СН2-СНз);- 2,35 и 2,66 (2Н, дублет, J ге,« 15 Гц, СО-СН); 3,32 (1И, С12Ь-Н); 3,0-3,4 (4Н нуль тип лет, два N-C1I.2) ; 6,95 - 7,48 (4Н, мультиплет, ароматические протоны); 7,97 (1Н, ущиренный синглет, индол-NH), м.д.
Гидрохлорид: разложение, начиная со (из смеси диоксана с ди- этиловым эфиром), д -151 С (с 1, метанол).
Рассчитано, %: С 70,33; И 8,63; С1„он 80,00; Ы 9,45.
C HjClN O (молекулярньв вес 444,04).
Найдено, %: С 69,72; Н 8,36; С1,о«8,31; N 9,16.
Пример 40. (+)-Н-Метил-2- -оксиэтиламид-транс-1-зтил-1,2,3,4, 6,7,12,12Ь-октагидроиндоло(2,3-а) хинолизин-1-ил-пропионовой кислоты.
3,26 г (0,01 моль) (±)-транс- -этил-1,2,3,4,6,7.,12,,12Ь-октагидро- индоло(2,3-а)хинолизин-1-ил-пропио- новой кислоты в атмосфере азота и при постоянном перемешивании добавляют к приготовленному с 20 мл безводного тетрагидрофурана раствору 2,04 г (0,02 моль) перегнанного над натрием N-метилформолина. Раствор охлаждают до -5°С и при энергичном перемешивании по каплям, однако не- прерывно, смешивают с 1,10 г (0,01 моль) этилового эфира хлорму- равьиной кислоты, причем внутренняя температура не должна прсвьш1ать . Реакционную смесь перемешивают в течение 30 мин при 0°С и затем при (5) в течение примерно 10 мин по каплям смешивают с раствором 0,83 г (0,011 моль) Ы-метил-2-окси- этиламина в 10 мл безводного тетрагидрофурана при сохранении внутренней температуры ниже О С. Рёакцион10% диэтиламина толуола. Выход 0,43 (11,2%) светло-желтого маслянистого вещества.
1Н-ЯМР (CDClg): 0,65 (ЗН, тр
20 плет, J 7,5 Гц, Cl-CHi-CHj); 3,08 (ЗН, уширенньш синглет, N-CH,); 3,3 (1Н, уширенньй синглет, С12Ь-Н); 3,60 (2Н, уширенный сииглет, N-CH,) 3,78 (2Н, триплет, СИ-гОН); 6,9-7,5
25 (4Н, мультиплет, ароматические протоны); 9,9 + 10,1 (1И, уширенньй синглет, индол-NH), м.д.
Пример 41. (1)-Пирид-2-ил- -металамид-транс-1-этил-1,2,3,4,6,
30 7,12,12Ь-октагидроиндолоС2,3-а)хино лизин- 1 -ил-пропионоБой кислоты.
Осуществляют аналогично примеру 38 с тем различием, чтобы в качеств ацилируемого амина используют 1,19 (0,011 моль) 2-аминометилпиридина. Сырой продукт очищают с помощью кол ночной хроматографии на силикагеле при применении содержащего 10% диэтиламина толуола. Получают 0,26 г (6,,2%) сиропообразного вещества. (CDC1,): rf 0,65 (ЗН; триплет, J 7,5 Гц, СХ-СН -СЬ); 3,40 (1Н, уширенный синглет, С12Ь-Н 4,64 (2П, дублет, JCH.NH Ц. NH-C11,); 7,0 (1Н, CO-NH); 6,9-8,5 (6И, мультиплет, ароматические прот ны + СЗ - Н + С5 -И); 7,65 (1Н, мультиплет, СД -Н); 8,54 (UI, мультиплет, Сб -Н); 10,14 (, уширеннь сннглет, индол-NH), м.д. 50 П р и м е р .. 42. ()-Фурфурялами транс-1-этил-1,2,3,4,6,7,12,12Ь-окт гидроиндоло(2,5-а)хинолизин-1-ил-пр пионовой кислоты.
Осуществляют аналогично примеру 39, однако в качестве ацилируемого амина используют 1,07 г (0,011 мол фурфуриламина. Сырой продукт очищаю с помощью колоночной хроматографии
35
40
45
193
28
ную смесь перемешивают в течение 30 мин при О С и затем еще следующие 4 ч при комнатной температуре. Смесь выпаривают на ротационном испарите- ле и остаток смешивают с 50 мл ди- хлорметана, а также 20 мл воды. После тщательного встряхивания нераст- воримьй осадок отфильтровывают. Ор- ганическую фазу отделяют., промывают 4 раза по 20 мл водой, сушат над сульфатом натрия и, .наконец, выпаривают. Сырой продукт очищают с помощью колоночной хроматографии на сиs ликагеле при применении содержащего
ликагеле при применении содержащего
Л Г 1-.-г П| п-ж гч ълтт1( Rl-TV n (1 cl Т
10% диэтиламина толуола. Выход 0,43 г (11,2%) светло-желтого маслянистого вещества.
1Н-ЯМР (CDClg): 0,65 (ЗН, три0 плет, J 7,5 Гц, Cl-CHi-CHj); 3,08 (ЗН, уширенньш синглет, N-CH,); 3,37 (1Н, уширенньй синглет, С12Ь-Н); 3,60 (2Н, уширенный сииглет, N-CH,); 3,78 (2Н, триплет, СИ-гОН); 6,9-7,5
5 (4Н, мультиплет, ароматические про , тоны); 9,9 + 10,1 (1И, уширенньй синглет, индол-NH), м.д.
Пример 41. (1)-Пирид-2-ил- -металамид-транс-1-этил-1,2,3,4,6,
0 7,12,12Ь-октагидроиндолоС2,3-а)хинолизин- 1 -ил-пропионоБой кислоты.
Осуществляют аналогично примеру 38 с тем различием, чтобы в качестве ацилируемого амина используют 1,19 г (0,011 моль) 2-аминометилпиридина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 10% ди. этиламина толуола. Получают 0,26 г (6,,2%) сиропообразного вещества. (CDC1,): rf 0,65 (ЗН; триплет, J 7,5 Гц, СХ-СН -СЬ); , 3,40 (1Н, уширенный синглет, С12Ь-Н); 4,64 (2П, дублет, JCH.NH Ц. NH-C11,); 7,0 (1Н, CO-NH); 6,9-8,5 (6И, мультиплет, ароматические протоны + СЗ - Н + С5 -И); 7,65 (1Н, мультиплет, СД -Н); 8,54 (UI, мультиплет, Сб -Н); 10,14 (, уширенньй сннглет, индол-NH), м.д. 50 П р и м е р .. 42. ()-Фурфуряламид транс-1-этил-1,2,3,4,6,7,12,12Ь-окта- гидроиндоло(2,5-а)хинолизин-1-ил-про- пионовой кислоты.
Осуществляют аналогично примеру 39, однако в качестве ацилируемого амина используют 1,07 г (0,011 моль) фурфуриламина. Сырой продукт очищают с помощью колоночной хроматографии
5
0
45
29
на силикагеле при применении содер- жащего 10% диэтиламина толуола. Выход 0,47 г (11,6%) сиропообразного вещества.
1Н-ЯМР (CDClj): 0,64 (ЗН, триплет, J 7,5 Гц, ); . . 3,37 (1Н, уширенный синглет, С12Ь-Н)
4,50 (2Н, дублет, JcMa, Ш-СН,); 5,90 (1Н, уширенный три- плет, CO-NH); 6,25 (1Н, двойной дублет, J 3,4 + 0,6 Гц, СЗ -Н); 6,33 (1Н, двойной дублет, J 3,4 и2,ОГц 04 -Н); 6,9-7,5 (5Н, мультиплет, ароматические протоны + С5 -Н); 10,02 (1Н, уширенный синглет, индол-NH), м,д.
Пример 43. (+)-(8)-1-Фенил- этиламид транс-1-ЭТИЛ-1,2,3,4,6,7, 12,12Ь-октагидроиндоло(2,3-а)хиноли- зин-1-ил-пропионовой кислоты.
3,26 г (0,01 моль) (+)-транс-1- -этил-1,2,3,4,6,7,12,12Ь-октагидро- индоло(2,3-а)хинолизин-1-ил-пропио- новой кислоты при перемешивании ив атмосфере азота добавляют к приготовленному с 20 мл безводного тетрагид- рофурана раствору 2,04 г (0,02 моль) перегнанного над натрием N-метилмор- фолина. Раствор охлаждают до -15 С и по каплям, однако непрерывно, смешивают с 1,37 г (0,01 моль) изобути- лового эфира хлормуравьиной кислоты, . причем внутренняя температура не должна превышать -15 С. Смесь пере- мешивают в течение 30 мин при -15 С и затем при этой температуре по каплям смешивают в течение примерно 10 мин с раствором 1,53 г (0,011 моль) (5)-1-фенилэтиламина и 10 мл без- .водного тетрагидрофурана при сохранении внутренней температуры ниже -15°С. Реакционную смесь перемешивают при -15°С в течение 30 мин и затем еще последующие 4 ч, причем позволяют температуре подняться до комнатной. Реакционную смесь выпаривают на ротационном испарителе и остаток смешивают с 50 мл дихлорэтана и 20 мл воды. После тщательного встряхивания отфильтровывают нераст воримый осадок, органическую фазу отделяют, промывают 4 раза по 20 мл водой, сушат над сульфатом магния и затем выпаривают. Сырой продукт перекристаллизуют из изопропанола. Выход 0,64 г (14,8%). Т.пл. 90- 92 С, ;:. -98,4° (с 1, хлороформ) .
Q , 5 20
25 ЗО 50 I
0193ЗО
1Н-ЯМР (CDClj): f
(ЗН, триплет, J 7,6 Гц, Cl-CHi-%) ; 1,49 + 1,52 (ЗН, дублет, J . 7 Гц, NH-CH-CH,); 3,36 (1Н, уширенный синглет, С12Ь-Н); 5,22 (1Н, квадруплет, JCH,N« 7 Гц, Ш-СН); 5,86 (1Н, уширенный дублет, СО-Ш); 6,9- 7,5 (9Н, ароматические протоны); 10,1 (1Н, уширенный синглет, индол-Ш) , м.д.
Пример 44. (±)-(К)-Фенил- этилимид транс-1-этил-1,2,3,4,6,7, 12,12Ь-окт:агидроинзоло (2,3-а) хинолизин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 42 с тем различием, что в качестве ацилируемого амина используют 1,33 г (0,011 моль) (Я)-1-фенилзтиламина. Сырой продукт очищают путем перекристаллизации из изопропанола.
Выход 07 г (16,3%). Т.пл. 90 - 92°С. у +100 (с 1,0, хлоро- . форм).
1Н-ЯМР (CDClj): 0,62 + 0,65 (ЗН, триплет, J 7,5 Гц, сг-СН -СНз); 1,50 1,53 (ЗН, дублет, J 7 Гц, NH-CH-Clb); 3,36 (Ш, уширенньй синглет, C12b-H)j 5-22 (1Н, квадруплет, JCH, мн -7 Гц, Ш-СН); 5,81 (1Н, уширенный дублет, СО-Ш); 6,9-7,5 (9Н, мультиплет, ароматические протоны); 10,07 (1Н, уширенный синглет, индол-NH), м.д.
Пример 45. (±)-(К)-1-Фанил- этиламид транс-1-этил-1,2,3,4,6,7, 12,12Ь-октагидроиндоло(2,3-а)хинолизин- 1-ил-пропионовой кислоты.
Смесь из 1,70 г (0,005 моль) (+) метилового эфира транс-1,2,3,4,6,7, 12,12Ь-октагидроиндоло(2,3-а)хинолизин- 1-ил-пропионовой кислоты, 0,63 г :(0,00§2 моль) (К)-1-фенилэтиламина и 0,324 г (0,006 моль) порошкообразного метилата натрия в 15 мл безвод-. ного толуола при перемешивании и в атмосфере аргона перегоняют так, чтобы отгоняющийся толуол увлекал с собой образующийся метанол. Спустя 6,5 ч продолжительности реакции реакционную смесь разлагают водой. Органическую фазу сушат над сульфатом магния и затем выпаривают. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 10% диэтиламина циклогексана. Выход 0,70 г (32,6%).
Пример 46. (-)-Диэтиламид (15:12Ь5)-1-этил-1,2,3,4,6,7,12,12Ь/-октагидроиндоло(2,3-а)хинолизин-1- -ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве ацилируемого амина используют 1 ,.46 г (0,02 моль) диэтиламина. Сырой продукт очшцают путем перекристаллизации из толуола..
Выход 2,33 г (61%), Т.пл. 222 - , У -124,2° (с 1,5, хлороформ).
1Н-ЯМР (CDClg): 1,09 (ЗН, триплет, J -.7 Гц, Cl-CH -CHg); 0,73 и 0,99 (6Н, триплет, J 7 Гц, N- ); 2,9-3,3 (4Н, муль типлет, N-CHj- CH); 3,34 (1Н, С12Ь-Н); 7,0-7,48 (4Н, мультиплет, ароматические протоны); 8,1 (1Н, уширенный синглет, индол-Ш) , м.д.
Рассчитана, %: С 75,54; Н 9,25; 11,01.
(молекулярный вес 381,54).
Найдено, %: С 75,81; Н 11,10.
Этансульфондт: т.пл.
N
N
9,01,
(изопропанол) , С 3
205-207 С -79, (с 2, вода).
Рассчитано, %: С 63,51; Н 8,41; S 6,52.
(молекулярный вес 491,67).
Найдено, %: С 63,49; Н 8,55; S 6,63.
Пример 47. ()--К-Метилпипе- разид(13:12Ь8)-1-этил-1,2,3,4,6,7, 12,12Ь-октагидроиндоло(2,3-а)хинолизин- 1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве ацилируемого амина используют 2,00 г (0,02 моль) N-метилпиперизина. Сыро продукт очшцают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола.
Выход 2,77 г (68%) пенообразного вещества, all -127,2 (с 2,0, хлороформ).
1Н-ЯМР (CdClj): Г 1,10 (ЗН, триплет, J 7 Гц, С1-СН -СНз); 2,1 (ЗН, синглет, N-CHj); 3,52 (Ш, С12Ь-Н); 7,0-7,48 (4Н, мультиплет, ароматические протоны); 7,98 (1Н, упиренный синглет, нндол-NH), м.д.
бис-Гидробромид: т,пл. 225-240°С
(изопропанол). D 2,0, вода).
-73,1 (с
N
0
5
0
5
0
5
0
5
0
5
Рассчитано, %: С 52,64; Н 6,72; N 9,82; Вг,,„ 28,02.
C2jHjjBr2N40 (молекулярный вес 570,40).
Найдено, %: С 53,09, Н 7,01; 9,56; Вг,,„27,82.
Пример 48. (-)-К-1-Фенил- этиламид(18:12ЬЗ)-1-этил-1,2,3,4,6, 7,12,12Ь-октагидроиндоло(2,3-а)хинолизин- 1-ил-пропионовой кислоты.
1,63 г (0,005 моль) (-)-(1S:12bS)- -1-эти -1 ,2,3,4,6,7, 12, 12Ь-октагид- роиндоло(2,3-а)хинолизин-1-ил-пропи- оновой кислоты при перемешивании и в атмосфере азота слабо кипят.ят в растворе 0,67 г (0,0055 моль) (R)-1- -фенилэтиламина в 30 мл безводного ксилола. Медленно отгоняющийся ксилол время от времени заменяется безводным ксилолом. После кипячения в течение 9 ч реакционную смесь выпаривают в вакууме и остаток экстрагируют дважды по 25 мл дихлорметаном. Раствор выпаривают. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола, затем перекристаллизуют из изопропа- нола. Выход 0,205 г (9,6%), т.пл. 152-155 С.
Пример 49. (-)-Метиловый эфир(13:12ЬЗ)-1-этил-12-метил-1,2,3, 4,6,7,12,12Ь-октагидроиндоло(2,3-а) хинолизин-1-ил-пропионовой кислоты.
в 20-25 мл жидкого аммиака при и при интенсивном перемешивании вносят 0,005 г нонагидрата нитрата железа (III)и затем маленькими порциями 0,25 г натрия. После растворения натрия, исчезновения синей окраски и вьделения серого цвета осадка амида натрия peaKnHOHH To смесь подогревают до (-50) - (-55) С и добавляют в нее по каплям приго- товленньй с 20 мл безводного эфира раствор 3,4 г (0,01 моль) (-)-мети- лового эфира (IS:12Ь5)-1-этйл-1,2,3, 4,6,7,12,12Ь-октагидроиндоло(2,3-а) хинолизин-1-ил-пропионовой кислоты. Смесь перемешивают в течение 10 мин при -50°С и затем смешивают с раствором 1,56 г (0,011 моль) метилирди- да в 5 мл безводного эфира. Оставляют температуру повышаться до комнатной. После испарения аммиака остаток экстрагируют эфиром. Маслянистый сырой продукт очищают с помощью колоночной хроматографии (200 г силикагеля-60, размер частиц 0,0.63 - 0,2 мм; содержащий 10% диэтиламина
толуол) .,
Вькод 2,1 г (59,3%) желтого масла, Rf 0,78 (Polygram SgLG)УФ if.содержащий 10% диэтиламина толуол, УФ-освещение.
Пример 50. (-)-(1S:12bS)- -1-этил-12-метил-1,2,3,4,б,7,12,12Ь7 -октагидроиндоло(2,3-а)хинолизин-1- -ил-пропионовая кислота.
10,0 г (0,028 моль) полученного согласно примеру 48 соединения растворяют в растворе 2,5 г (0,044 моль) гидроксида калия в 200 мл 96%-ного этанола. Раствор кипятят с обратным холодильником в течение 1 ч и затем вьтаривают досуха. Остаток растврря- ют в небольшом количестве воды, раствор подкисляют до рН 6 с помощью уксусной кислоты, выпавший осадок отфильтровывают, промывают водой и затем высушивают.
Выход 6,28 г (66,0%), Rf 0,51 (Polygram s3LG),приуготовленная в соотношении 5:1 смесь изопропанола с. 25%-ным водным аммиаком; УФ-свет.
Гидрохлорид: начиная со 180°С разложение (этанол), о/J -71,5 (с 1,0, вода).
Рассчитано, С 66,91; Н 7,75; N 7,43; С1 9,41.
С .jO- (молекулярный вес 376,9).
Найдено, %: С 67,11; Н 7,81; . N 7,49; С1 9,41.
Пример 51. (-)-Бензиламид (IS:12Ь5)-1-этил-12-метил-1,2,3,4, 6,7,12,12Ь-октагидроиндоло(2,3-а) кинолизин-1-ил-пропионовой кислоты.
3,40 г (0,01 моль) (-)-(1S:l2bS)- -1-этил-12-метил-1,2,3,4,6,7,12,12Ь- -октагидроиндоло(2;3-а)хинолизин-.1- ,-ил-пропионовой кислоты при перемешивании и в атмосфере азота добавляют к приготовленному с 20 мп безводного тетрагидрофурана раствору 2,04 г (0,02 моль) перегнанного над натрием N-метилморфолина. Раствор охлаждают до -5°С и при энергичном перемешивании по каплям, однако непрерывно, смешивают с 1,10 г (0,01 моль) этилового эфира хлорму- равьиной кислоты, причем внутренняя температура не должна превышать О С Реакционную смесь перемешивают в течение 30 мин при 0°С и затем при (-5) - 0°С в течение примерно 10 ми
по каплям смешивают с раствором 1,18 г (0,011 моль) бензиламина в 10 мл безводного тетрагидрофурана при сохранении внутренней температу- ры ниже 0°С. Перемешивают при в течение 30 мин и-затем еще следующие 4ч, в то время как температуре позволяют подняться до комнатной. Затем .реакционную смесь выпаривают на ро- тационном испарителе и остаток смешивают с 50 мл дихлорметана, а также 20 мл воды. После встряхивания органическую фазу отделяют, промыва- 5 ют 20 мл 5%-ного раствора соды и затем трижды по 20 мл водой, сушат над сульфатом магния, выпаривают. Остаток после выпаривания очищают с помощью колоночной хроматографии на 0 силикагеле при применении содержащего 10% диэтиламина толуола. Выход 3,36 г (78%) маслянистого вещества.
.1Н-ЯМР (CDClj): f 0,91 (ЗН, триплет, J 7 Гц, С1-СН - Шз); 3,42 5 (1Н, синглет, С12Ь-Н); 3,53 (ЗН, синглет, индoл-NCHз); 3,85 + 4,35 (2Н, широкая, Ш-СН); 6,9 (1Н, широкая, CO-NH); 6,9-7,4 (9Н, мульти- плет, ароматические протоны), м-Д 0 D-Гидротартрат: т.пл. 167-170 С (из смеси ацетона с этанолом).
Рассчитано, %: С 66,30; Н 7,13; N 7,25.
. (молекулярный вес « 579,67)
Найдено, %: С 66,27; Н 7,29;
N 7,18.
Пример 52. (-)-N-Meтил-2- -оксиэтиламид(18:12Ь8)-1-этил-12- 40 -метил-1,2,3,4,6,7,12,12Ь-октагидро- индоло ( 2,3-а) хинолизин-1 -ил-пропионовой кислоты.
Осуществляют аналогично примеру 48 тем различием, что в качестве аци- 45 лируемого амина используют 0,83 г
(0,011 моль) Ы-метил-2-оксиэтиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 10% диэтиламина толуола.
Выход 2,31 г (58%) сиропообразного вещества.
50
1Н-ЯМР (CDCl,) 0,92 (ЗН, триплет, J 7 Гц, Cl-CH -CHi); 2,74 (ЗН, уширенный синглет, N-CH); 3,32 (2Н, уширенный триплет, N-CH); 3,43 (1Н, синглет, С12b-H); 3,58 (2Н,три- плет, ); 3,58 (ЗН, синглет ,;
35
индол-Ы-СНз); 6,95-7,55 (4Н, мульти- плет, ароматические протоны), м.д.
С-ЯМР (CDClj): d 7,96 (Cl-CH - -СНз); 21,56 21,49 (СЗ); 23,2Г(С7); 26,80 + 26,58 (С14); 27,16 (С13); 30,18 (Cl-CHj-CHj); 34.,21 + 33,85 (индол-NCH-); 35,93 + 34,34 (CO-NCHj) 5 37,85 (С2); 42,65 (Ct); 51,34 (С6); 51,47 + 51,17 (); 56,60 (С4); 61,44 + 59,72 (); 65,90 (С12Ь); 109,88 -t- 110,24 (С11); 113,79 + 113,57 (С7а); 117,74 + +117,67 (С8); 119,52 (С9); 121,49 (CiO); 127,63 (C7b), 137,84 (С12а); 140,55 (С11а); 175,80 + 174,16 (NCO). Пример 53, (±)-(Ю-1-Фенил- этиламид-1-о(-2,3,4,6,7,12,12Ь -окта- гидрбиндоло(2,3-а)хинолизин-1-ил-про- пионовой кислоты.
Осуществляют аналогично примеру 1, однако 3,12 г (0,01 моль) (±)-1«-2,3, 4,6,7,12,12Ь-октагидроиыдоло(2,3-а) хинолизин-1-ил-пропионовой кислоты вводят во взаимодействие с 1,33 г :(0,011 моль) (Ю-1-фенилэтиламина. Выход 1,6 г (36,3%) пенообразного вещества, Rf 0,44 (Polygram 8Л,С), содержащий 5% триэтиламина этилаце- тат, УФ-свет.
Пример 54. (-)--Метиловьш эфир(1S:12bS)-1-этил-8-иитро-1,2,3, 4,6,7,12,12Ь-октагидроиндоло(2,3-а) хинолизин-1-ил-пропионовой кислоты и (-)-метиловый эфир(1S:12bS)-1- -этил-10-нитро-i,2,3,4,6,7,12,12Ь- -октагидроиндоло(2,3-а)хинолизин-1- -ил-пропионовой кислоты.
I
10
4,8 г (0,014 моль) (-)-метилового эфира (15:12Ь8)-1-этил-1,2,3,4, 6,7,12,12Ь-октагидроиндоло(2,3-а) хинолизин- -ил-пропионовой кислоты растворяют в 25 мл безводной уксус147019336
амина толуол) и разделяют на следую-, щие компоненты:
8-нитросоединение: выход 1,15 г (21%), Т.Ш1. 133-136°С (из смеси толуола с диизопропиловым эфиром), Rf 0,43 (Polygram )yOj,j содержащий 10% диэтиламина толуол, УФ-свет. 10-нитросоединение: выход 1,95 г (36%), т.пл. 177-180°С (метанол), Rf 0,60 (измерено в такой же системе) .
Пример 55. (-)-(1S:l2bS)- -1-Этил-10-нитро-1,2,3,4,6,7,12,12Ь- 5 -октагидроиндоло(2,3-а)-хинолизин-1- -ил-пропионовая кислота.
0,385 г (0,001 моль) полученного согласно примеру 53 10-нитросоедине- ния в растворе 0,169 г (0,003 моль) гидроксида калия в 8 молях 96%-ного спирта кипятят с обратным холодильником в течение 20 мин. Раствор выпаривают, остаток растворяют в пе- большом количестве воды, раствор подкисляют уксусной кислотой до рН 6, выпавший в осадок продукт отфильтровывают, промывают водой и затем высушивают.
Выход 0,300 г (81%) соединения, которое без дальнейшей очистки может применяться для получения амида кислоты.
Пример 56. (-)-(R)-l-Фe- нилэтиламид(1S:12bS)-1-этил-10-нит- ро-1,2,3,4,6,7,12,12Ь-октагидроиндо- ло(2,3-а)хинолизин-1-ил-пропионовой кислоты,
0,371 г (0,001 моль) полученного- согласно примеру 54 соединения при AQ перемешивании и в атмосфере азота добавляют к приготовленному с 4 мл безводного тетрагидрофурана раствору 0,111 г (0,011 моль) перегнанного над натрием N-метилморфолина. Раст20
25
.30
IJ I f JLtntV А I- - - f - V
НОЙ кислоты. Раствор по каплям добав- вор охлаждают до и при интенсивг Г г „, ..т.«... л.«. ...,xx«n% i ttTDOtJUU пл ТГЯППСТМ. ППНЯКО
ляют к охлажденному до 0-10 С и интенсивно перемешиваемому раствору 7,5 мл безводной уксусной кислоты в 7,5 мл 100%-ной азотной кислоты (d 1,52). Реакционную смесь дополнительно перемешивают еще 5 мин, затем выливают в 250 мл ледяной воды, нейтрализуют концентрированным аммиаком и экстрагируют хлороформом. Экстракт сушат над сульфатом магния, затем выпаривают. Остаток после выпаривания очищают с помощью колоночной хроматографии (500 г силикагеля-60, 0,063-0,2 мм, содержащий 10% диэтилном перемешивании по каплям, однако непрерывно, смешивают с 0,108 г (0,001 моль) этилового эфира хлор- муравьиной кислоты, причем внутренняя температура не должна превьшать . Смесь перемешивают в течение 30 мин при и затем при той же температуре смешивают с раствором 0,133 г (0,0011 моль) (R)-1-фeнил- этиламина в 1 мл безводного тетра- гидрофурана. Реакционную смесь перемешивают в течение 30 мин при О С, затем еще 4 ч при комнатной температуре, после чего выпаривают на рота вор охлаждают до и при интенсив.. л.«. ...,xx«n% i ttTDOtJUU пл ТГЯППСТМ. ППНЯКО
ном перемешивании по каплям, однако непрерывно, смешивают с 0,108 г (0,001 моль) этилового эфира хлор- муравьиной кислоты, причем внутренняя температура не должна превьшать . Смесь перемешивают в течение 30 мин при и затем при той же температуре смешивают с раствором 0,133 г (0,0011 моль) (R)-1-фeнил- этиламина в 1 мл безводного тетра- гидрофурана. Реакционную смесь перемешивают в течение 30 мин при О С, затем еще 4 ч при комнатной температуре, после чего выпаривают на рота37
ционном испарителе и остаток смешивают с 10 мл дихлорметана, а также 5 мл воды. После тщательного встряхивания фазы отделяют друг от друга Органическую фазу промывают 5 мл 5%-ного раствора соды, затем трижды по 5 мл водой, сушат над сульфатом магния и выпаривают. Сырой продукт
1470193 -38
лоты и добавляют к раствору 0,59 г (0,0033 моль) свежеперекристалпизо- ванного N-бромсукцинимида. Смесь оставляют стоять в течение ночи при комнатной температуре, затем подщела- чивают с помощью 20%-ного водного раствора соды, экстрагируют хлороформом, экстракт сушат над сульфатом
ЛПЛ . - - очищают с помощью колоночной хромато- Q графии на силикагеле при применении содержащего 10% диэтиламина толуола. Выход 0,33 г (69,6%), т.пл. 130магния и затем выпаривают на ротационном испарителе. Сырой продукт очищают с помощью колоночной хроматографии (150 г силикагеля-60, 0,063- 0,2 мм, содержащга 10% диэтиламина
о г п 134/п i;° /in . t MM, СОДерлсицтг iu« ,..
i -
содержащий 10% диэтиламина толуол,
УФ-свет.
Пример 57. (-)-(1S:12bS)-1- -Этил-8-нитро-1,2,3,4,6,7,12,12Ь- -октагидроиндоло(2,3-а)хинолизин-1- -пропионовая кислота.
Осуществляют аналогично примеру 55, однако используют 0,385 г (0,001 моль) полученного согласно, примеру 53 8-нитросоединения.
Выход 0,289 г (78%) соединения, которое без дальнейшей очистки может применяться для получения амида кислоты.
Пример 58. (-)-(Ю-1-Фенилэтиламид(1S:12bS)-1-этил-8-нитpo- -l,2,3,4,6,7,12,1 2Ь-октагидроиндоло (2,3-а)хинолизин-1-ил-пропионовой
кислоты.
Осуществляют аналогично примеру 56 однако в качестве ацилируемого амина используют 0,371 г (0,001 моль) полученной согласно примеру 56 (-)- -(IS:12ЬЗ)-1-этил-8-нитро-1,2,3,4,6, 7,12,12Ь-октагидроиндоло(2,3-а)хинолизин- 1-ил-пропионовой кислоты.
Выход 0,27 г (57%),.пл. 220- ., 1. 7 -232,3 (с 1,0, хлороформ), Rf 0,27.. (Polygram )УФ.,:ц, содержащий 10% диэтиламина толуол, УФ-свет.
Пример 59, (-)-Метиловый эфир(15:12Ь5)-9-бром-1-этил-1,2,3,4, 6 7,12,12Ь-октагидроиндоло(2,3-а)хи- нолизин-1-ил-пропионовой кислоты и (-)-метиловый эфир(15:12Ь5)-8,9-ДИ- бром-1-этил-1,2,3,4,6,7,12,12Ь-окта- гидроиндоло(2,3-а)хинолизин-1-ил- -пропионовой кислоты.
1 02 г (0,003 моль) (-)-метилового эфира(13:12Ь5)-1-этил-1,2,3,4,6, 7 12 12Ь-октагидроиндоло(2,3-а)хинолизин- 1-ил-аропионовой кислоты растворяют в 10 мл трифторуксусной кис20
25
30
35
40
45
50
55
щие компоненты:
9-бромсоединение: выход 0,34 г (27%) пенообразного вещества, Rf 0,26 (Polygram sj)LG)УФ2s . содержащий 10% диэтиламина циклогексан, УФ-свет. 8,9-дибромсоединение: выход 0,12 г (8%) пенообразного вещества, Rf 0,16 (в такой же системе).
П р и м е р 60. (-)-(lS:l2bS)- -9-Бром-1-этил-1,2,3,4,6,7,12,12Ь- -октагидроиндоло(2,3-а)хинолизин-1- -ил-пропионовая кислота.
Осуществляют аналогично примеру 55, однако исходят из 0,419 г (0,001 моль) полученного согласно примеру 58 9-бромсоединения. Выход 0,313 г (77%) соединения, которое без дальнейшей очистки может применяться для получения амидов кислот.
Пример 61. (-)-(К)-1-Фенил- этиламид(18:12Ь5)-9-бром-1-этил-1, 2,3,4,6,7,12,12Ь-октагидроиндоло (2,3-а)хинолизин-1-ил-пропионовой
кислоты.
Осуществляют аналогично примеру 56 однако в качестве ацилируемого амина используют 0,405 г (0,001 моль) полученной согласно примеру 59 кислоты.
Выход 0,2 г (39%) пенообразного вещества, -24,7° (с 1, хлороформ), Rf 0,43 (Polygram з5ЬС)УФ1б,, содержащий 10% диэтиламин толуол, УФ-свет.
П р и м е р 62. (-)-(IS: :12Ь5)-8,9-Дибром-1-зтил-1,2,3,4,6,
7,12,12Ь-октагидроиндоло(2,3-а)хи- нолизин-1-ил-пропионовая кислота.
Осуществляют аналог.ично примеру 55, однако исходят из 0,498 г (0,001 моль) полученного согласно примеру 58 дибромсоединения.
Выход 0,368 г (76%) соединения, которое без всякой дальнейшей очистлоты и добавляют к раствору 0,59 г (0,0033 моль) свежеперекристалпизо- ванного N-бромсукцинимида. Смесь оставляют стоять в течение ночи при комнатной температуре, затем подщела чивают с помощью 20%-ного водного раствора соды, экстрагируют хлороформом, экстракт сушат над сульфатом
магния и затем выпаривают на ротационном испарителе. Сырой продукт очщают с помощью колоночной хроматографии (150 г силикагеля-60, 0,063- 0,2 мм, содержащга 10% диэтиламина
U. t MM, СОДерлсицтг iu« ,..
0
5
30
35
40
45
50
55
щие компоненты:
9-бромсоединение: выход 0,34 г (27%) пенообразного вещества, Rf 0,26 (Polygram sj)LG)УФ2s . содержащий 10% диэтиламина циклогексан, УФ-свет. 8,9-дибромсоединение: выход 0,12 г (8%) пенообразного вещества, Rf 0,16 (в такой же системе).
П р и м е р 60. (-)-(lS:l2bS)- - -9-Бром-1-этил-1,2,3,4,6,7,12,12Ь- -октагидроиндоло(2,3-а)хинолизин-1- -ил-пропионовая кислота.
Осуществляют аналогично примеру 55, однако исходят из 0,419 г (0,001 моль) полученного согласно примеру 58 9-бромсоединения. Выход 0,313 г (77%) соединения, которое без дальнейшей очистки может применяться для получения амидов кислот.
Пример 61. (-)-(К)-1-Фенил- этиламид(18:12Ь5)-9-бром-1-этил-1, 2,3,4,6,7,12,12Ь-октагидроиндоло (2,3-а)хинолизин-1-ил-пропионовой
кислоты.
Осуществляют аналогично примеру 56 однако в качестве ацилируемого амина используют 0,405 г (0,001 моль) полученной согласно примеру 59 кислоты.
Выход 0,2 г (39%) пенообразного вещества, -24,7° (с 1, хлороформ), Rf 0,43 (Polygram з5ЬС)УФ1б,, содержащий 10% диэтиламина толуол, УФ-свет.
П р и м е р 62. (-)-(IS: :12Ь5)-8,9-Дибром-1-зтил-1,2,3,4,6,
7,12,12Ь-октагидроиндоло(2,3-а)хи- нолизин-1-ил-пропионовая кислота.
Осуществляют аналог.ично примеру 55, однако исходят из 0,498 г (0,001 моль) полученного согласно примеру 58 дибромсоединения.
Выход 0,368 г (76%) соединения, которое без всякой дальнейшей очисти может использоваться для приготовления амида кислоты.
Пример 63. (ч-)-(К)-1-Фенил- этиламид(1S:12bS)-8,9-дибром-1-этил- -1,2,3,4,6,7,12,12Ь-октагидроиндоло (2,3-а)хинолиэин-1 -ил--пропионовой кислоты.
Осуществляют аналогично примеру 55 с тем различием, что исходят из 0,848 г (0,001 моль) полученного согласно примеру 61 соединения.
Выход 0,24 г (41%) пенообразного вещества, Со/1э +10,4 (с 0,5, хлороформ), Rf 0,36 (Polygram зЭЬС)УФ содержащий 10% диэтилами- на толуол, УФ-свет.
Пример 64. (1S:12bS)-1- -Этйл-(-)-п-фторбекзи.т1амид-1,2,3,4, 6,7,12,12Ь октагидроищ,оло ( 2,3-а) хинолизин-1-ил-пропионовая кислота.
Осуществляют аналогично примеру 1, однако в качестве ацилируемого амина используют 1,38 г (0,011 моль) п фторбензиламина. Сырой продукт очищают с помощью колоночной хрома- тог рафии на силикагеле при применении содержащего 10% диэтиламина толуола.
Выход 2,93 г (68%) кристаллизующегося при стоянии масла, т.пл. 92
96 С,
-115,8° (с 2,0, хлороформ), Rf 0,37 (Polygram содержащий 5% диэтиламина толуол, УФ-свет,
Пример 65, (-)-2-Тиенилме-. тиламид(18:12ЬЗ)-1-этш1-1,2,3,4,6,7, 12,12Ь-октаги,Цроиндоло( 2,3-а) хинолизин-1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве ацилируемого амина используют 1,25 г (0,011 моль) 1-тиенилметиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола.
Выход 3,10 г (74%) кристаллизующегося при стоянии масла, т.пл. 80- 85°С 0; -101,1 (с 2,0. хлороформ), Rf 0,32 (Polygram з5ЬС)УФ,,5, содержащий 5% диэтиламина толуол..
Пример, 66. (-)-Пиперидид (13:12Ъ5)-1-этил-1,2,3,4,6,7,12,12Ь- -октагидроиндоло)2,3-а)хинолизин-1- -ил-пропионовой кислоты.
Осуществляют аналогично примеру с тем различием, что в качестве ацилируемого амина используют 0,94 г
10
15
20
25
30
35
45
50
55
(0,011 моль) пиперидина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 5% диэтиламина толуола. Выход 2,59 г (65%) пенообразного вещества, « J -125,5 (с 2,0, хлороформ), Rf 0,41 (Polygram )УФ254 содержащий 5% диэтиламина толуол, УФ-свет.
Пример 67. (-)-Морфолид(15: :12Ь5)-1-этил-1,2,3,4,6,7,12,12Ь- -октагидроиндоло(2,3-а)хинолизин-1- -ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием , что в качестве ацилируемого амина используют 0,96 г (0,011 моль) морфолина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 10% диэтиламина толуола. Выход 2,83 г (71%) пенообразного вещества, Ы i/ -119,9° (с 2,1, СНСЦ), Rf 0,38 (Polygram )УФ, содержащий 5% диэтиламина толуол, УФ-свет.
Пример 68. (-)-Циклогексил- амид(13:12ЬЗ)-1-этил-1,2,3,4,6,7,12, 12Ь-октагидроиндоло(2,3-а)хинолизин- -1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве ацилируемого амина используют 1,08 г (0,011 моль) циклогексиламина. Сырой продукт очищают с помощью колоночной хроматографии при применении содержащего 10% диэтиламина толуола.
Выход 3,05 (74%) пенообразного вещества, С., -106, (с 2,0, 40 СНСЦ), Rf 0,46 (Polygram зЭ1с)УФ.,54, содержащий 5% диэтиламина толуол, УФ-свет.
Пример 69. (-)-1-Нафтилме- тиламид(13.12Ь S)-1-этил-1,2,3,4,6,7, 12,12Ь-октагидроиндоло(2,3-а)хинолизин 1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием, что в качестве ацилируемого амина используют 1,73 г (0,011 моль) 1-нафтилметиламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 10% диэтиламина толуола.
Выход 3,41 г (72%) пенообразного вещества, - -95,8 (с 2,1; хлороформ), Rf 0,35 (Polygram )УФ„у4, содержащий 5% диэтиламина толуол, УФ-свет.
Пример 70. (-)-4-Пиридил- амид(15:12Ь5)-1-этил-1,2,3,4,6,7,12, 12Ь-октагидроиндоло(2,3-а)хинолизин- -1-ил-пропионовой кислоты.
Осуществляют аналогично примеру 1, однако в качестве ацилируемого амина используют 1,04 г (0,011 моль) 4-аминопиридина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего .30% диэтиламина толуола.
Выход 1,1 г (28%) пенообразного вещества. Id | -163,5 (с 2,0, СНС1з),К 0,42 (Polygram sSLG),, содержащий 30% диэтиламина толуол, УФ-свет.
Пример 71. (-)-5-Гексенил- амид(15:12Ь8)-1-этил-1,2,3,4,6,7,12, 12Ь-октагидроиндоло(2,3-а)хинолизин- -1-иЛ-пропионовой кислоты.
Осуществляют аналогично примеру 1 с тем различием,, что в качестве ацилируемого амина применяют 1,08 г (0,011 моль) 5-гексениламина. Сырой продукт очищают с помощью колоночной хроматографии на силикагеле при применении содержащего 10% диэтиламина четыреххлористого углерода.
Выход 1,71 г (42%) высокавязкого масла, -101, (с 2,0,
CHCl), Rf 0,40 (Ро1у8гат.-з)ЪС)УФ,54 содержащий 10% диэтиламина четьфех- хлористьй углерод, УФ-свет.
Пример 72. (+)-Бензш1амид- -Ы-этил-9-метокси-1,2,3,4,6,7,12, 12Ь -октагидроиндоло(2,3-а)хинолиг зин-1-р-ил-пропионовой кислоты.
Ацилируют аналогично примеру 1 0,024 г (0,00022 моль) бензиламина с помощью 0,071 г (0,0002 моль) (1)-1-о/-этил-9-метокси-1,2,3,4,6,7 12,12Ь (У -октагидроиндоло (2,3-а) хино- лизин-1-ил-пропионовой кислоты. Сырой продукт очищают с помощью, колоночной хроматографии на силикагеле при применении содержащего 10% диэтиламина толуола. Выход 0,023 г (26%) пенообразного вещества, Rf 0,39 (Polygram зЭЬС)УФ15 « содержащий 10% диэтиламина толуол, УФ-свет.
Гастроцитозащитное действие соединений исследовали в следующем тесте. Результат для (-)-(R)-1-фeншr- этиламида(15:12ЬЗ)-Т-этил-1,2,3,4,6, 7,12,12Ь-октагидроиндоло(2,3-а)хино- лизин-1-ил-пропионовой кислоты представлен в табл. 1.
0
5
0
5
0
5
0
5
Снижение выделения кислоты желудочного сока в случае Shay-крис.
Самок крыс H-Wistar массой по 120-150 г не кормят в течение 24 4, воду они имеют в распоряжении по желанию. Затем под слабым эфирным наркозом перевязывают привратник (желудка). При этом вмешательстве исследуемые соединения вводят отчасти перорально, отчасти интраперитонеаль- но. Спустя 4 ч животных умерщвляют благодаря эфирному наркозу, и после изъятия желудка измеряют объем и рН- значение содержимого желудка. Количество кислоты определяют путем титрования с помощью 0,01 и. раствора Ьидроксида натрия по отношению к фенолфталеину в качестве индикатора.
Результаты этого исследования представлены в табл. 1.
Вызванная аспирином язва желудка.
Исследование вызванной аспирином .язвы желудка хорощо известно в фармакологической практике. Самки крыс H-Wistar массой по 120-150 г в течение 24 ч не получают никакого корма, однако воду по желанию. Язва желудка индуцируется оральной дачей 100 мг/кг аспирина (в виде суспензии в тви- не-80). Исследуемые соединения вводят непосредственно после обработки аспирином. Спустя 4 ч после обработки животных умерщвляют благодаря сверх- дозированному эфирному наркозу. Желуг док вынимают и разрезают вдоль большой кривизны. Содержимое желудка вымывают, подсчитывают кровавые поражения на железистой поверхности.
Результаты приведены в табл. 2.
Вызванное кислым этанолом повреж- ление желудка.
Для исследований используют самок крыс RG-Wiscar массой 120-150 г. Животные в течение 24 ч не получают никакого корма, однако воду - по желанию. В качестве некротизирующего средства используют кислый этанол (получен из 1 мл 36%-ной соляной кислоты и 50 МП абсолютного этанола). Этот раствор дают орально в количестве 0,5 мл/100 г массы тела. Исследу- емые соединения также дают орально, за 30 мин до обработки кислым этанолом. Спустя 1 ч животных умерщвляют сверх- дозированным эфирным наркозом. Желудок удаляют и разрезают вдоль большой кривизны. Массу очищенного желудка определяют. Отек желудка опредеАЗ
«1
1470193
ляют тем, что определяют разницу между измеренной мокрой массой и мокрой массой желудка необработанных кивотных (контроль). Затем желудки BHcyiBHBaWr при комнатной температуре. На следуницрй день визуально оценивают кровавые поражения. В качестве числа измерения служит выраженная в миллиметрах средняя ;щина мест повреждения. Результаты оцениваются
студент
статистически с помощью пробы.
Результаты представлены в табл. 3 Индуцированная индометацином язва тонкого кишечника.
Крыс H-Wistar массой 120-150 г (голодом не морят) обрабатывают орально индометацином. В этих условиях для образования визуально ощутимой язвы тонкого кишечника требуется по меньшей мере 24-48 ч. Для оценки язвы определяют предел прочности при разрьше тонкого кишечника по методу вздутия, так как язвы снижают предел прочности при разрыве стенки ,-кишки. Тонкий |сишечник удаляют от iпривратника вплоть до слепой кишки, конец перевязывают и с помощью полиэтиленовых трубочек свяг1ывают с WtW электронны - манометром В 8005. Тонкий кишечник помещают в 0,9%-ный водный раствор поваренной соли и при повышают давление до тех пор, пока на тонких местах стенки кишки не покажутся воздушные пузырьки. Измеряемое в этот момент времени давление представляет собой числовую меру предела прочности при разрыве стенки кишки.
Результаты представлены в табл. 4 Стимулированное гистамином выделение КИСЛОТЫ- желудочного сока в пер- фузионированном желудке крысы.
Перфузионирование ос уществляют по несколько модифицированному методу Ghosh и Schild. Самцы крыс массой 300-350 г в течение 24 ч не получают никакого корма, однако воду - по желанию. Животных наркотизируют урета- ном (1 мл) 100 г массы тела в виде 10%-ного раствора, интраперитонеаль- но). Брюшную стенку вскрывают путем поперечного разреза и через вырезанное в двенадцатиперстной кишке отверстие в желудок вводят стеклянную канюлю. Через пищевод вводят полиэтиленовую канюлю. Для удаления твердого содержимого желудка промывают
44
5
10
15
желудок 0,9%-ным раствором поваренной соли, причем обращают внимание на то, чтобы желудок не растянулся. Спустя 2 ч после вмешательства желудок снова промывают, чтобы удалить вызванную операционной травмой кислоту. Спустя 1 ч после этой второй промьшки подкожно путем инъекции вводят гистамин в .дозе 30 мг/кг. После этого стимулирования желудок промывают 30 мин. Промьшные растворы титруют 0,01 н. раствором гидроксида натрия по отношению к фенолфталеину. Количество кислоты указывают в м-экв (1/2 ч).
Как видно из результатов, соединения активны на крысах по отношению против вызванных кислым этанолом пов- 20 реждений желудка (отек, желудочные кровотечения), они подавляют стимулированную аспирином язву желудка и оказывают профилактическое действие в случае стимулированньк индометацином язв тонкого кишечника. Активные дозы в Shory-модели меньше, чем необходимые для подавления выделения кислоты. В перфузированных желудках крыс предлагаемые соединения не подавляют вызванное гистамином или карбазолом выделение кислоты, поэтому нужно считать, что механизм подавления вьзделения кислоты новый.
Токсичность предлагаемых соединений низкая. Значение ЛДго соединения
J J -ч. ./i«j 4 lO
25
30
40
(-)-(Е)-1-Фенш1-этиламида(1S:12bS)- -1-этил-1,2,3,4,6,7,12,12Ь-октагидро- индоло(2,3-а)хинолизин-1-ил-пропио-i новой кислоты ( крысах, орально) выше 1500 мг/кг.
Формула изобретения
Способ получения амидов 1,2,3,4, 6,7,12,12b-oктaгидpoиндoлo(2,3-a)xи- нoлизин-1-шl-aлкaнкapбoнoвыx кислот общей формулы
.N-C-G II О
СгНз
R, R,- G С,-С -алкш1;
фенил;
линейная С,-С -алкиленовая
группа.
или их физиологически совместимый солей присоединения кислот, отличающийся тем, что 1,2,3,4, 6,7,12,12Ь-октагидрОиндоло(2,3-а) хинолизин-1-ил-алканкарбоновую кислоту формулы
.
HO-C-G;, «
II CzHg
о
Подавление выделения кислоты желудочного сока на Shay-крысах
по сравнению с контролем i 0,01.
Подавление стимулированной аспирином язвы желудка в зависимости от дозы
по сравнению с контролем по аспирину 0,01 мг/кг перорапьно.
или ее низший алкиловьй эфир подвергают, взаимодействию с амином общей формулы
1Ш
R.
где R, и R имеют указанные значения с выделением целевого п юдукта в свободном виде или в виде физиологически совместимой,соли присоединения кислоты.
Таблица 1
Таблица 2
47
Ав.
рвльво
ЭДуеДЛя подавления поражений кг/кг перораяыю.
- эй--,
по сравнению с контрольной группой iO.OI.
Тавлва«4
Ирофилактическое действие соединения RGH-2961 проти. язвы тонкого кишечника зависимости от дозы
Веобрабставо (вормалъв)
Индометацвновый контроль
RGH-2961 ямдв нетация
ВСВ-2961 + ИНДО метацни
индоме- тацив
Пиреязешш |шдо- метадав (стандарт)
циметидин надо- метацин (стандарт) Ю
50
303jt(Veh.10)
to3x(l2+10)
JO3x() 103x(50+«0)
103x()
3x(50+10)
no сравнеиш с индометацивовш ° ° 1470193
48 т а 6 л.я ц а 3
| Бюлер К | |||
| и Пирсон Д | |||
| Органические синтезы, ч | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| М.: Мир, 1973, с | |||
| Переносный ветряный двигатель | 1922 |
|
SU384A1 |
Авторы
Даты
1989-03-30—Публикация
1985-10-04—Подача