О)
с


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения пирувата в биологических объектах | 1984 |
|
SU1322984A3 |
| Способ определения глутаматоксалацетаттрансаминазы или глутаматпируваттрансаминазы | 1979 |
|
SU1276269A3 |
| Реактив для определения тригицеридов | 1976 |
|
SU641884A3 |
| Способ определения содержания креатинина, креатина и саркозина в биологической жидкости | 1986 |
|
SU1582993A3 |
| Способ определения липазы | 1986 |
|
SU1604167A3 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОЛИВАЛЕНТНОГО АНТИГЕНА В БИОЛОГИЧЕСКОЙ ЖИДКОСТИ | 1989 |
|
RU2032906C1 |
| Способ определения активности антитромбина-ВМ | 1982 |
|
SU1271379A3 |
| Способ определения креатинина в сыворотке крови | 1972 |
|
SU1144629A3 |
| Реактив для определения глицерина фотометрическим методом | 1981 |
|
SU1554765A3 |
| Реактив для определения формиата или соединений, переходящих в формиат | 1978 |
|
SU860718A1 |
Изобретение относится к биохимии. Цель изобретения - повьшение точности способа. Получают пируват или оксалоацетат при трансаминирова- . НИИ с6-кетоглутаровой кислоты. При этом используют D-лактатдегидрогеназу из ряда бактерий или мелатдегидрогена- зу. Затем производят восстановление до лактата или малата в присутствии никотинамиддинуклеотида восстановленного. Измеряют в полученной смеси количество образовавшегося никотинами- даденина окисленного.Способ может быть использован для диагностики заболеваний печении сердца. 6 табл. §
4;
00
о ;D
ы
Изобретение относится к медицине и может быть использовано в клинике при распознавании болезней печени и средца.
Целью изобретения является повьше- ние точности способа.
Цель достигается тем, что согласно способу определения, включающем вза- .имодействие соответствующей аминокис- fnoTbi с об- кетоглутарово кислотой до Получения глутаровой кислоты и об-кето кислоты, соответствующей используемой кислоте, и измерение образовавшейся Ы/-кетокислоты в результате восстанов|пения с NADH в присутствии лактатде- |гидрогеназы и в соответствующем слу- ае малатдегидрогеназы при образова- |нии NAD и сл-оксикислоты, используют lD-лактатдегидрогеназу из ряда бакте - рий.
Изобретение иллюстрируется следующими примерами.
Пример 1. Определение GPT- активности (вариант с фосфатным буфе- ром) .
Материалы пробы: сьшоротка, плазма гепарина или EDTA.
Реагенты (конечные пробы в тесте): фосфатный буфер 80 ммоль/л с рН 7,4 pj-аланин 800 ммоль/л, VDH из DSM |2699 1200 и/л, NADH 0,18 ммоль/л, -кетоглутарат 18,0 ммоль/л. I Определительная насадка: длина вол fcfbi Hg 365, 340 или 334 нм, кювета: толщина слоя 1 см, температура из- Иерения , измерение по отноше- |нию к воздуху (уменьшение экстинкции)
В фотометре при аналогичных показаниях начальная .экстинкция ныше 0,500 компенсируется каскадным регулированием.
В кювету вносят пипеткой 2,5 мл реакционной смеси и 0,5 мл пробы и смешивают. Приблизительно через 1 мин снимают показания экстинкции и одновременно включают .секундомер. Снимают показания через 1,2 и 3 мин.
При разнице экстинкции в минуту (лЕ/мин) от 0,06 до 0,08 (Hg 365) или 0,11-0,18 (Hg 334 и 340 нм) принимают во внимание лишь измерения первых двух минут (1 мин инкубируют и 2 мин измеряют).
Из разницы . кст-инкции в минуту (uE/мин) получают среднее значение и его используют при расчетах.
Активность GPT в пробе рассчитывают следующим образом:
и/л () нм/мин и/л (25°С) 952х4,Е,б5- нм/мин и/л (25°С) 971 &Е,5 нм/мин
Пример 2. Определение GOT- активности (вариант с трис-буфером)(
Материал пробы: сыворотка, плазма гепарина или EDTA.
Реагенты (конечная концентрация в тесте): трис-буфер 100 ммоль/л с рН 7,5, NADH 0,18 ммоль/л, МБНбООи/ LDH из DSM 2694 1200 U/л, об-кетоглу- тарат 12 ммоль/л, L-аспартат 200 ммоль/л.
Определительная насадка: длина волны Hg 365, 340 или 334 нм, кювета: толщина слоя 1 см; температура измерения 25 С, измерение по отношению к воздуху (снижение экстинкции).
Смешивают 2,5 мл раствора реагента с 0,5 мл пробы, раствор заливают в кювету. Через 1 мин снимают показания экстинкции и одновременно включают секундомер. Дальнейшие показания снимают через 1,2 и 3 мин.
Из разницы экстинкции в миНуту (&Е/МИН) получают среднее значение и его используют для расчетов.
Активность GOT в пробе берут из таблицы или рассчитьшают следующим образом:
и/л (25 С) 2059 X нм/мин; и/л (25°с) 1111 ЛЕио НМ/МИН-, и/л (25 С) 1138 X ДЕ,, нм/мин.
Как показали исследования при 25 С в случае использования известного реагента приблизительно через 34 ч весь NADH исчезает, в то время как в случае использования предлагаемого реагента даже через 120 ч получают око ло 71% начальной экстинкции , При 4°С и времени хранения 120 ч для известного реагента - 30% остаточной экстинкции , а для предлагаемого - 90%.
Пример 3. Получение D-ЛДГ.
Получают по способу, описанному в J.of General Microbiology (1970) , 243.
Для этого анаэробно культивируют Lactobacillus ieichmannii 1 М 2699 в ферментаторе вместимостью 10 л при 37 С с пропусканием газов (95% N. 5% С02).В качестве среды применяется среда, описанная в J. of General Microbiology 62, (1970), 223-239,
причем дополнительно добавляют ацетат натрия 0,05 вес.% и цитрат диаммония 0,02 вес.%.
В конце экспоненциальной фазы роста бактерии собирают, промьшают в 0,05 М буферного раствора фосфата калия с рН 7,% и вновь суспендируют в том же буферном растворе. Затем
ультразвуковым прибором Raytheon 1 КС ю калия (рН 7,0) и элюируют градиентом KaCl (0,5-1,0 моль/л)
Получают препарат ЛДГ (выход около 25%) .
Пример 4. Таким же обра- 15 зом, как и описано в примере 3, получают D-ЛДГ из других штаммов семейств. Lactobacillus и Leuconostoc, выход, %:
производится клеточное разложение. Затем центрифугируют при 4 С в течение 30 мин при 15000 g. Доводят рН полученного в виде остатка сырого экстракта микроорганизма с помощью уксусной кислоты до 5,5, разбавляют сульфатом протамина до 0,3% по
Lactobacillus lactis DSM 20072
Lactobacillus plantarum
DSM 20174
Leuconostoc mesenteroides
DSM 20193
1 Пример 5. Получение D-ЛДГ Pediococcus pentosaceus М 20280.
Pediococcus pentosaceus культивируют в MRS-среде с 1% глюкозы в ферментере емкостью 10 л без аэрации. СобранньЪ путем центрифугирования клетки промывают с помощью 0,9 вес. кого раствора NaCl и суспендируют в 0,05 моль/л натрийфосфатного буфера который содержит 0,002 моль/л DTT и 0,002 моль/л DL-лактата натрия. Расворение происходит в гомогенизаторе клеток Брауна при охлаждении. После декантации жидкости ее в течение 30 мин при 4°С центрифугируют при 37000 g. Прозрачную надосадочную жидкость подвергают фракционному осаждению сульфатом аммония, причем фракция осаждается при насьще- нии 40-70%. Эту фракцию, растворен- Hyio в 0,05 моль/л натрийфосфатного буфера и 0,002 моль/л DTT, хроматографируют при соответствующих условиях через колонку с сефарозой 6В. I
В D-ЛДГ-фракциях путем концентри рования и разбавления с помощью 0,05 моль/л трис-буфера, который содержит. 0,002 моль/л ДТТ и 0,05 моль/л NaCl, устанавливают рН и хроматографируют через колонку ;с ДЕАЕ-сефадексом. Элюирование осуществляют с помощью линейных градиентов 0,05-0,5 моль/л NaCl. Выход примерно 10%.
объему и отделяют осадок центрифуги-, рованием.
Доводят рН остатка до 7,7, и получают выделяющуюся фракцию, насыщенную до 50-80% сульфатом аммония. Эту фракцию хроматографируют через слабый анионит (ДЕАЕ - Sephadex®А50) в 0,05 М буферного раствора фосфата
Примерно 20 10 15
Пример 6. Определение ак тив- ности ОРТ.
Материал для испытания: сыворотка, гепарин или плазма EDTA.
В качестве реактива применяют раствор следующих веществ (фирма Берингер Маннхайм), г:
NaHjPO
5
0
5
1,47 13,49
ei-аланина 99,7
D-ЛДГ из Lactobacillu s
leichmannii, DSM 2699 0,037 . NADH . 0,163
(У.-Кетоглютарат 2,042
Вода1 л
2,5 мл этого реактива перемешивают при 25 с с 0,5 мл пробы и определяют активность ОРТ, как описано в пример 1.
Конечные значения концентрации добавленных веществ в опыте соответствуют данным в примере 1.
Пример 7. Одинаковые с при- ме ром 4 результаты получают, если вместо 0,037 г D-ЛДГ из Lactcbacillus leichmannii DSM 2699 применяют 0,048 г D-ЛДГ из Lactobacillus lactis DSM 20072; 0,035 г D-ЛДГ из Lactobacillus plantarum DSM 20174, 0,044 г g D-ЛДГ из Leuconostoc mesenteroides DSM 20193, 0,032 г D-ЛДГ из Pediococcus pentosaceus DSM 20280.
Пример 8. Сравнительный аня- лиз.
0
Используя реактивы, которые хранились при комнатной температуре в течение 2 или 10 ч по примеру 1 определяют в пробе активность GPT. В качестве пробы использовали контрольную сьторотку (Precinorra V589, фирма Берингер Маннхайм), Активность ОРТ 32,5 ед/л.
: Результаты приведены в табл. 1. : Пример 9. Определение актив;НОСТИ GPT.
Действуют аналогично примеру 1, i
причем ЛДГ применяют в различных ко:личествах. В качестве ЛДГ применяют
:ЛДГ Lactobacillus leichnannli DSM
2699, в качестве пробы - контрольную
:сыворотку (Precinorm V589, фирма
; Берингер Маннхайм), активность
:GPT 32,5 ед/л.
ед/л
Активность,
Заданное значение,
1000098
2000099
. Добавка большего количества ЛДГ
неэкономична из-за стоимости энзи: ма.
: Пример 10. Определяют GPT- активность аналогично примеру 6, используя Б-ЛДГ, полученную для раз- личных микроорганизмов.
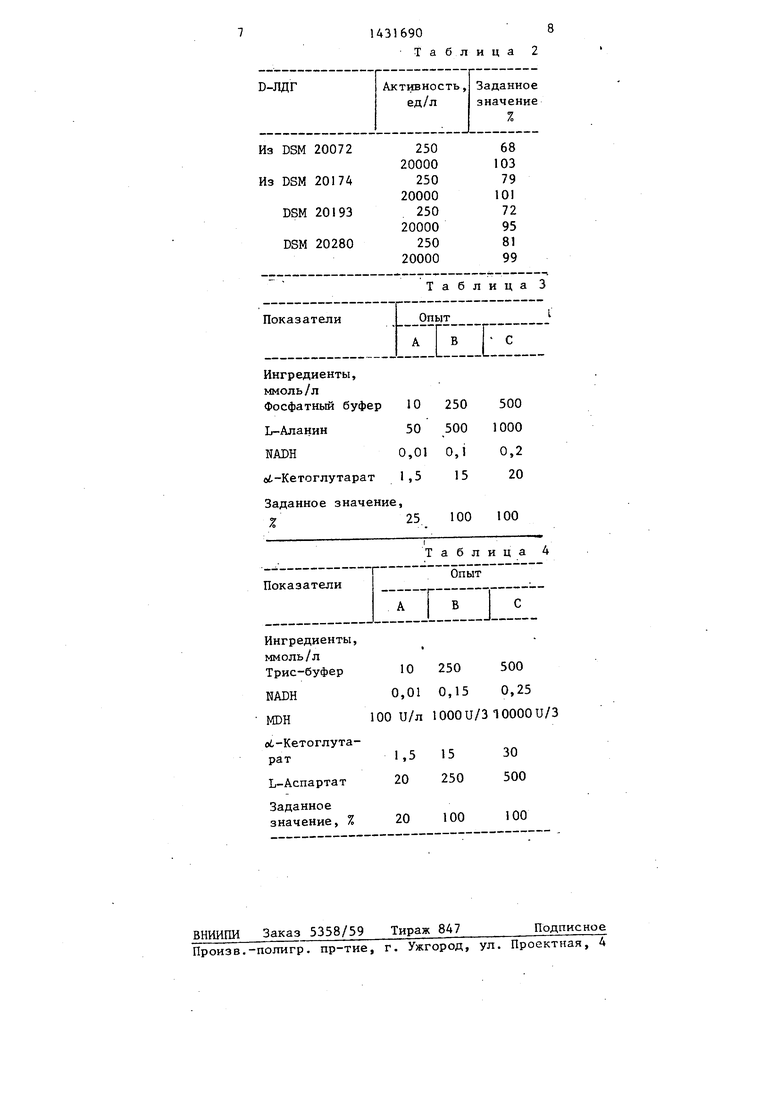
Результаты приведены в табл. 2. Пример 11. Определение GPT- активности в случае различных концен раций ингредиентов реагента.
Проводят олыт аналогично примеру 1 используя буфер. L-аланин, NADH и ot- кетоглутарат в различных концент- рациях. Активность D-ЛДГ составляет, смотря по обстоятельствам, 1200 ед/л
Результаты приведены в табл. 3. П р и м е р 12. Определение GOT- активности при различных концентра- диях ингредиентов реагента.
Определение ведут аналогично примеру 2,причем буфер,NADH,MDН, oi.-кетоглутарат и L-аспартат используют в различных концентрациях. D-ЛДГ-ак- тивность соста:вляет, смотря по обстоятельствам, 1200 ед/л.
Результаты приведены в табл. 4.
5
0
5
Формула изобретения
Способ определения глутамат-пиру- ват- и глутамат-оксалоацетаттрансами- назы, включающий получение пирувата или оксалоацетата путем трансаминиро- вания об-кетоглутаррвой кислоты в присутствии лактатдегидрогеназы и в соответствующем случае малатдегидроге- назы с последующим восстановлением их до лактата. или малата в присутствии никотинамидцинуклеотида восстановленного и измерением в полученной смеси, содержащей буферный раствор, количества образовавшегося никотинамидаде- нина окисленного, о-тличаю- щ и и с я тем, что, с целью повьше- ния точности способа, в качестве лактатдегидрогеназы используют D-лак- татдегидрогеназу из Lactobacillus leichmannii DSM 2699, Lactobacillus lactis DSM 20072,Lactobaqlllus tarum DSM 20174, Leuconostoc mesen- teroides DSM 20193, Pediococcus pen- tosaceus 20290 с активностью 250- 20000 ед/л, при этом используют (в конечной концентрации), ммоль/л:
Буферное вещество L-Аланин
Никотинамидаденин- динуклеотид восстановленный
Малатдегидрогвназа oi -Кетоглутарат L- Аспартат
10-500 50-1000
0,01-0,25
100-20000 ед/л 1 ,5-30 20-500
Таблица 1
| Патент США 4235962, кл | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1988-10-15—Публикация
1984-08-21—Подача