Изобретение относится к химии водорастворимых витаминов и касается определения аскорбиновой кислоты в пищевых продуктах.
Цель изобретения - упрсяцение способа.
Способ заключается в следующем.
При определении аскорбиновой кислоты, предусматривающем добавление к исследуемому экстракту избытка 2,6- дихлорфенолиндофенола (2,6-ДХШФ или реактив Тилманса) и измерение поглощения последнего, величину поглощения 2,6-ДХФИФ определяют в водном экстракте при рН 3,8-4,5 и длине волны 540 нм,
Метод прост, имеет высокую чувст-. вительность (предел обнаружения аскорбиновой кислоты 5 мкг) , позволяет сократить время анализа до 10-15 мин.
Пригоден дпя анализа окрашенных и неокрашенных продуктов.
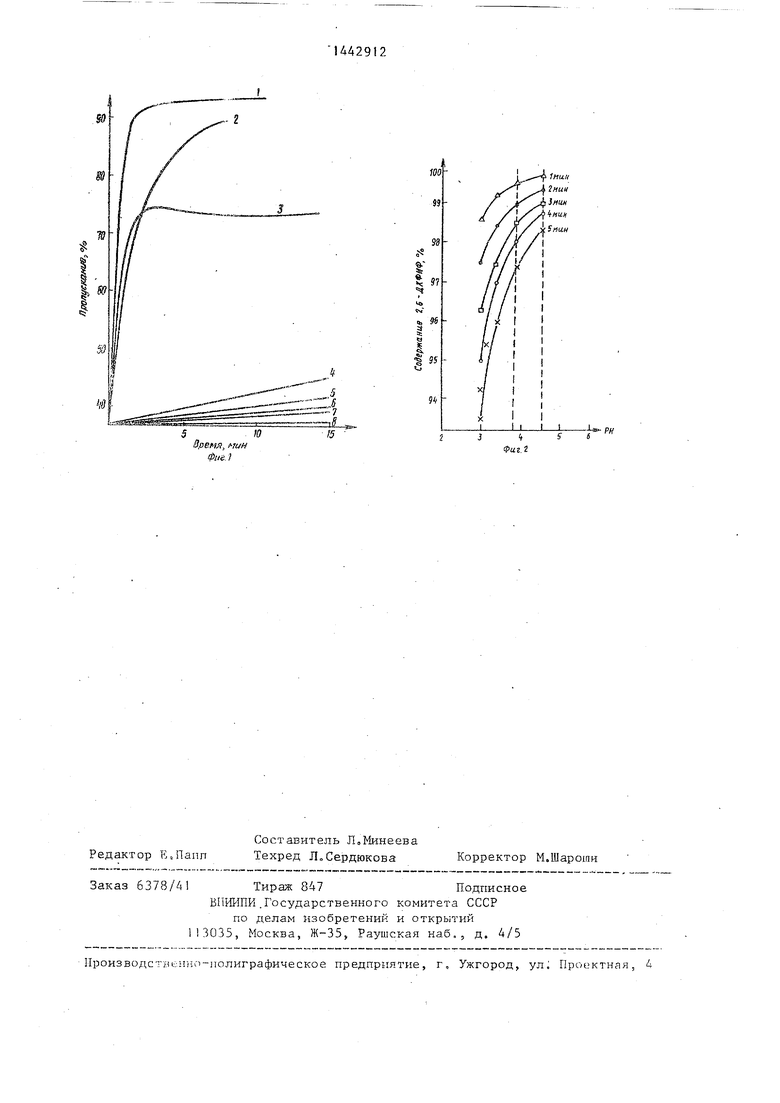
Выбор условий анализа основан на исследовании стабильности 2,6-ДХФИФ при различных рН. Как видно из фиг.1, при рН ниже 3,8 скорость обесцвечивания реактива Тилманса возрастает, что делает метод колориметрического определения мало пригодным.
При рН в интервале 3,8-4,5 2,6- ДХФИФ разлагается достаточно медленно что дает возможность осуществлять его колориметрическое определение При напичии редуцирую0рх примесей взаимодействующих с 2,6-ДХФИФ, интервал рН 3,8-4,5 также пригоден дпя определения аскорбиновой кислоты, поскольку в этих УСЛОВИЯХ аскорбиновую кислоту можно дез активизировать обра- боткой формалином и определить количество фенолята, прореагировавшего с редуктонами.
При рН выше 4,5 разложение фенолята незначительно, а при рН 7,2 не наблюдается совсем, однако в этих условиях измерение проводить нельзя из-за невозможности определения редуцирующих примесей и малой устойчивости аскорбиновой кислоты, При.,5 связывание аскорбиновой кислоты формалином становится неполным, что вносит ошмбку в определение истинного содержания витамина С. Кроме того, при рН более 7 начинает проявляться склонность аскорбиновой кислоты к окислению: при рН 7 витамин С разлагается на 1,7% за 1 ч, при рН 8
Q 5
0
0
О
5 Q г
5
наблюдается 50%-ное разрушение в течение 10 мин.
На фиг.2 представлена зависимость степени разложения 2,6-дихлорфенолин- дофенолята натрия от рН среды при различных интервалах времени. На практике время от момента добавления фенолята до момента колориметрирова- ния, как правило, составляет 2-3 мин. Интервал времени, равный 1 мин, обычно соблюдается редко.
Как видно из приведенных данных, при рН в области 3,8-4,5 реактив Тилманса при выдерживании пробы в течение 2-3 мин разлагается от 0,5 до 1,5%, При рН ниже 3,8 скорость разложения фенолята значительно увеличивается. Следовательно, в выбранном интервале рН ошибка определения не превысит I,5% при условии, если колориметрирование пробы осуществлять непосредственно после добавления реактива Тилманса,
Таким образом, существенным в предлагаемом способе является выбор рН, смещенный в более нейтральную область, при котором замедляется разложение фенолята, а аскорбиновая кислота устойчива и может быть легко дезактивирована формалином дпя определения редуцирующих веществ, а также выбор водной среды, улучшающий условия проведения анализа. Проведение анализа в этой среде исключает необходимость экстракции ксилолом, в результате чего отсутствует ошибка определения, связанная с неполным экстрагированием фенолята ксилолом.
Для осуществления анализа к исследуемому экстракту в 3%-ной метафос- форной кислоте или в 2%-ной соляной кислоте добавляют буфер, в количестве, -необходимом для доведения рН до значения., входящего в выбранный интервал рН, Измеряют оптическую плотность полученного раствора после добавления избытка фенолята при 540 нм. В качестве контрольного (кювета сравнения) .используют раствор, содержащий вместо фенолята равное ему по объему количество дистиллированной воды. Содержание аскорбиновой кислоты в пробе определяют по формуле
- ВЙ-Е-2.1,Ь.10о , ,„
где D - величина поглощения; фенолята в растворителе;
D - величина поглощения фенолята в исследуемом растворе; D - величина поглощения фенолята в растворе стандарта; m - количество аскорбиновой кислоты в пробе стандартного раствора, мг; V( - общий объем экстракта, мл; V - объем экстракта, взятый на
определение, мл; g - навеска или объем пробы,
г (мл);
100 - пересчет на 100 г (мл) продукта.
При анализе во все пробы добавляют одинаковое количество фенолята и ацетатного буфера (рН 4,5), количество растворителя в стандартном и исследуемом растворах таково, что общий объем проб одинаков.
Для учета редуцирующих примесей к пробе, содержащей экстракт, после добавления буфера припивают формалин в количестве, равном 1/4 полученного объема. Через 10 мин добавляют установленное количество фенолята и определяют поглощение при 540 нм против соответствующего раствора, содержащего вместо фенолята равное ему по объему количество воды. Количество акорбиновой кислоты определяют по формуле
X мг%
ul 2i Y 1 Yi2i li Ун 122
(D - D,).Vi-V4-g
5
V, v где D, - величина поглощения фенолят в пробе для определения редуцирующих примесей; объем .пробы для определения редуцирующих примесей после добавления фенолята, мп; объем остальных проб после добавления фенолята, мл, Пример 1: рНЗ,8. 10 мл витаминизированного морковного сока разбавляют 2%-ной соляной кислотой до 100 МП, раствор фильтрую 25 мл полученного экстракта повторно разбавляют 2%-ной соляной кислотой до 100 мл.
Готовят четыре пробы:
1) 5 мл 2%-ной соляной кислоты +
5 мл ацетатного буфера, рН 4,5 (49,75 г трехводного ацетата натрия 70 мл воды + 150 мл ледяной уксусной кислоты) + 1 ,5 мл фенолята (0,2 г фе нолята в 500 кп воды);
429124
2)0,5 стандартного раствора аскорбиновой кислоты (1 мкг/мл) +
+ 4,5 мл 2%-ной соляной кислоты + g 5 МП ацетатного буфера 1,5 мл фенолята;
3)5 мл полученного экстракта + 5 МП ацетатного буфера 1 ,5 мл фенолята;
10 4) 5 нл полученного экстракта + + 5 мл ацетатного буфера + 2 ,5 мл формалина, через 10 мин добавляют 1,5 мл фенолята.
Определяют величину поглощения
15 указанных растворов на колориметре КФК-2 при 540 нм. В качестве растворов сравнения используют соответствующие растворы (1-4) с добавлением вместо фенолята равного объема дис20 тиллированной воды. Содержание аскорбиновой кислоты, определенное по формуле (2)(среднее из двух определений), составляет 54,5 мг%.
Результаты определения аскорбино25 вой кислоты колориметрическим методом, методом индофенол-ксилольной экстракции (известный способ) и прямым титрованием (общепринятый метод анализа) представлены в таблице,
30
35
.
40
Как видно из таблицы, метод удобен для анализа как окрашенных, так и неокраьяенных продуктов. Более высокие значения концентрации аскорбиновой кислоты, полученные колориметрическим методом, по сравнению со значениями для индофенол-ксилольной экстракции связаны с частичным удерживанием фенолята водным раствором в про- .-цессе экстракции.
Пример 2 (известный). Готовят экстракт витаминизированного морковного сока в 3%-ной метафосфорной кис45 лоте аналогично примеру 1,84 колбы с притертыми пробками добавляют по 5 мл ацетатного буфера, рН 4,0 (49,75 г тригидрата ацетата натрия + + 70 мл воды + 225 мл уксусной кисло5Q ты), В первую колбу добавляют 5 мл экстракта, во вторую 5 мл 3%-ной метафосфорной кислоты, в третью 0,5 мп стандартного раствора аскорбиновой кислоты ( мкг/мл) и 4,5 мп 3%gg ной метафосфорной кислоты, в четвертую 5 мл экстракта и 2,5 мл формалина, В колбы 1-3 добавляют 1,5 мл фенолята, в колбу 4 - фенолят добаж- ляют через 10 мин.
514429
Содержимое энергично встряхивают, приливают по 25 мл ксилола и снова встряхивают. Дают отстояться в темноте 20 мин. Измеряют оптическую плотность слоя ксилола при 490 нм. Содержание аскорбиновой кислоты, определенное по формуле
тГВ,- D,.L- 100
Л МГ/0 -
(D - D)
составляет 46,3 мг%,
ПримерЗ. рН4,5,
Экстракт витаминизированного морковного сока и 4 пробы для анализа готовят аналогично примеру 2, используя 1,5 МП ацетатного буфера с рН 5,5 (30 г трехводного ацетата натрия + 70 мл воды + 15 мл ледяной уксусной кислоты). Определяют поглощение водных растворов при 540 нм. Содержание аскорбиновой кислоты 54,4 мг
II р и м е р 4, рН 3,4,
Экстракт витаминизированного морковного сока и 4 пробы для анализа готовят аналогично примеру 1, используя по 3,5 мл ацетатного буфера с рН 4,5 (см,выше). Содержание аскорбиновой кислоты - 54,00 мг%,
П р и м е р 5, рН 5,0,
Экстракт витаминизированного морковного сока и 4 пробы для анализа готовят аналогично примеру 2, используя .по 2,0 мл ацетатного буфера с рН 5j5 (приготовление буфе- ра по примеру 3), Содержание аскорбиновой кислоты - 53,90 мг%, I
Пример бо рН4,2,
Экстракт витаминизированного мор- ковного сока и. 4 пробы для анализа готовят аналогично примеру 2, используя 10 мл буфера с рН 5,2 (100 мл 1 ,0 М соляной кислоты- + 500 мл 1 ,0 М ацетата натрия + дистиллированной
воды до 2,5 л). Содержание аскорбиновой кислоты, определенн,ое аналогично примеру 1, - 54,40 мг%.
Пример, Экстракт и 4 пробы для анализа готовят аналогично примеру 2. Как до, так и после добавления фенолята растворы остаются мутными и прямое колориметрирование невозможно (рН 3,6).
ПримерВ, К смеси, состояще из .0,5 мл витаминизированного газированного напитка Саяны (после дегазации пробы) и 4,5 мл солянокислого буфера (пример 6), добавляют
29
0
°
35
40
Q
126
0,5 мл реактива Тилманса и определяют величину поглощения D , используя в качестве кюветы сравнения раствор, содержащий 0,5 мл напитка, 4,5 мл буфера и 1 мл дистиллированной воды. Аналогично определяют величину поглощения 0,5 мл реактива Тилманса в смеси, состоящей из 4,5 мл буфера и 0,5 мл дистиллированной воды (D), Содержание аскорбиновой кислоты в мг/л напитка определяют по формуле
X 0.225.(рВ, 450(D-DJ,
где 0,225 - коэффициент, найденный
экспериментально и соответствующий величине M/(D-D2) формулы, приведенной в примере 2; 0,5 - величина пробы напитка,
взятой на анализ, мл; 1000 - коэффициент, учитывающий
перевод на 1 л напитка. При сравнении определения аскорбиновой кислоты в витаминизированных газированных напитках методами колориметрического анализа и визуального титрования получено хорошее совпадение результатов, мг/л: колориметрирование 121,50; 130,39; 113,40| 128,70; 119,84; 117,60; титрование 121,98; 129,47; 113,42; 126,26; 121,5; 113,42 соответственно
Анализ газирОБан1- ых напитков не требует осуществления стадии экстрак- 1ЩИ и определения редуцирующих примесей из-за их отсутствия. Это обеспечивает существенное упрощение анализа: повьщ1ает чувствительность метода- в 2 ,раза (2,5 мкг по сравнению с 5 мкг), так как исключает дополнительное разведение пробы,, при этом проведение анализа ускоряется приблизительно в 3 раза по сравнению с методом визуального титрования, делая реальным осуществление автоматизации процесса.
Таким образом, как видно из примеров 1,3 и 6, колориметрический метод анализа аскорбиновой кислоты дает практически одинаковые результаты при рН в области 3,8-4,5, При рН ниже 3,8 наблюдается некоторое занижение результата .(пример 4). При рН 5,0 (пример 5) результаты также отличаются от результатов в интервале 3,8-4,5. Как видно из примера 7, условия метода индофенол-ксилольной
714429
экстракции непригодны для прямого колориметрирования из-за мутности водной фазы. Пример 6 иллюстрирует . также возможность использования в анализе других буферных систем. Me-- тод индофенол-ксилольной экстракции (пример 2) сложнее предлагаемого способа и дает заниженные результаты.10
Формула изобретения
Способ количественного определения аскорбиновой кислоты, предусматривающий приготовление испытуемого образ- 5
128
ца, добавление к нему реагента в виде 2,6-ди5шорфенолиндофенола, определение величины поглощения образца с последующим пересчетом полученных результатов по количеству восстановленного аскорбиновой кислотой реагента, отличающийся тем, что, с целью упрощения способа, перед добавлением реагента устанавливают рН образца буферным раствором до 3,8-4,5, при этом определение величины поглощения ведут в области 540 нм непосредственно после добавления реагента.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ подготовки почвенных проб для анализа соотношения изотопов азота | 1982 |
|
SU1043565A1 |
| КОМПОЗИЦИЯ ДЛЯ КОЛОРИМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ЖЕЛЕЗА В СЫВОРОТКЕ КРОВИ | 1995 |
|
RU2109285C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БАКТЕРИАЛЬНЫХ ЛИПОПОЛИСАХАРИДОВ | 1996 |
|
RU2114436C1 |
| Способ получения белкового антигена фасциол | 1983 |
|
SU1159579A1 |
| Способ определения аскорбиновой или дегидроаскорбиновой кислоты | 1978 |
|
SU971120A3 |
| Способ определения эндо- @ (1-4) глюканазной активности | 1983 |
|
SU1112058A1 |
| Способ определения массовой доли крахмала в пшеничной муке | 1982 |
|
SU1201771A1 |
| Биологически активная добавка к пище капсулированной формы | 2020 |
|
RU2756855C1 |
| Способ определения активности @ -лизин- @ -оксидазы | 1982 |
|
SU1047957A1 |
| Катализатор для окислительно-восстановительных реакций и способ его получения | 1980 |
|
SU952864A1 |
Изобретение относится к химии водорастворимых витаминов и- касается определения аскорбиновой кислоты в пищевых продуктах. Целью изобретения Я1зляется упрощение способа. Способ заключается в тоМ; что к испытуемому образцуf -рН которого с помощью буферного раствора устанавливают в диапазоне 358-4 5, добавляют избыток реагента в виде 2 б-дихлорфенолиндоше- нола и определяют величину поглощения последнего в водной среде при 540 ни непосредственно после добавления реагента. 2 ило табл.
Картофельные хлопья длительного хранения 6,20
Аскорбиновая
Черная смородина486,0
Витаминизиро- ; ванный томатный сок94,60
Вит аминизиро- ванньй яблочно- морковный сок48,00
Витаминизированный мор- I ковный сок 54,50 46,30
460,0 Определению мешают природные пигменты
89,40
94,60
44,04 45,60
52,80
5Ю
, t-iuH
Фче-1
т w
S7
95
9
Фиг. 2
Pff
0
| Руководство к лабораторным занятиям по биологической химии | |||
| - М,: Медицина, 1976, с | |||
| Шкив для канатной передачи | 1920 |
|
SU109A1 |
| - М,; МОИП, 1984, Со 140-141. | |||
Авторы
Даты
1988-12-07—Публикация
1986-10-09—Подача