4;&ь
СП
Изобретение относится к биотехнологии и касается исследования состава экзополисахаридов (ЭПС), образу- емых различными видами микроорганизмов при культивировании их на углеродных субстратах.
Цель изобретения - расширение технологических возможностей способа за счет увеличения диапазона исследуемых молекулярных масс.
Изобретение заключается в том, что для разделения полисахаридов (ЭПС) и растворов декстранов, применяемых в качестве стандартов молекулярных масс, используют комбинированный градиент солей NaCl и CsCl, взятых в соотношении 5;1 - 1:1 при постоянном суммарном объеме, плотности растворов NaCl. f 1,03-1,30 г/см, CsCl f 1.,20-1,60 г/см при n .30000 об/мин в течеьше 19 ч.
Исследование растворов натив 1ых микробных ЭПС исключает необходимость предварительного разделения ЭПС на фракции и их раздельное градиентное центрифугирование. Применение стандартов молекулярных масс (декстранов значительно упрощает определение молекулярных масс, не требует расче- тов гидродинамических параметров. Использование комбинированного градиента NaCl и CsCl позволяет определить молекулярную массу в диапазоне : 13,7 тыс,.- 2 млн.-Кроме того, метод дает возможность одновременного анализа нескольких микробных ЭПС (до 6-8 проб одновременно).
Исследования молекулярно-массовой неоднородности ЭПС, проведены на синтезированных культурой Xanthomo- nas campestris шт, 8162 (0,6)5 смешанной .культурой дрожжей и бактерий на основе этанола (б, г) ксантана фирмы Sigma ; (j) , где: а- ЭПС, полученный на Ладыженском заводе ферментных препаратов; 6- ЭПС, полученный ; в лабораторных условиях; 8, 1- ЭПС синтезированные при различных условиях культивирования.
Стандарты углеводной природы - декстраны (фирмы Pharmacia .Ferac Fluka) различных молекулярных масс используется при определении молекулярно-массовой неоднородности ЭПС, молекулярной массы отдельных компонентов ЭПС методами гель-хроматографии. Дпя упрощения анализа согласно ,способу также предлагается применени
0
5
0
5 п
5
0
декстранов в качестве стандартов мо- лркулярных масс. Применяют декстраны фирмы Fluka. мол.массой 13,7 тыс., 20 тыс., ПО тыс., 500 тыс., 2 млн,
В соответствии с изобретением проведена проверка молекулярных масс декстранов фирмы Fluka методом аналитического ультрацентрифугирования (метод скорости седиментации). Молекулярную массу рассчитывают по уравнению Сведберга. Рассчитанные значения молекулярных масс декстранов не отличаются от значений, указанных фирмой-изготовителем,
В присутствии NaCl и CsCl свойства декстранов не меняются (не наблюдается ни деградация.их, ни структурирование) .
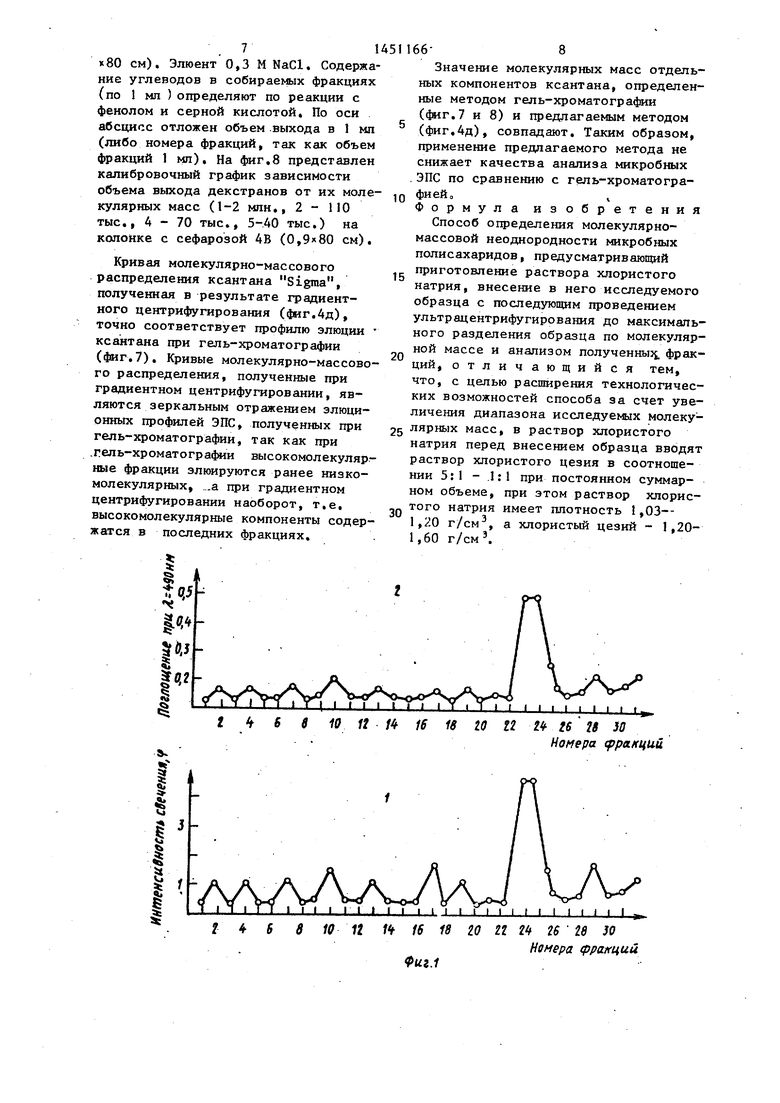
Используют в работе 0,05%-ные растворы ЭПС и 0,02%-ные растворы декстранов. Центрифугирование осуществляют на центрифугах К-32, К-32М, Beckraan в пробирках объемом 9,5 МП и 13,5 мл. Полученные результаты представляют на эмпирических кривых . молекулярно-массового распределения, где по оси ординат отложена интенсивность по.глощения при
Л 490 нм (реакция с фенолом и серной кислотой), а по оси абсцисс - номера фракций об.ъемом 0,25-0,50 мл в зависимости от объема центрифужных пробирок (фиг,1).
Изобретение иллюстрируется сле- дуюпщми пример ами.
Пример 1. Показывают стабильность реологических свойств и гидродинамических параметров исследуемых ЭПС в присутствии различных концеит- :раций NaCl и CsCl,
В табл,1 приведены данные по изменению вязкости 0,1%-ных растворов ЭПС 6, в и ксантана Sigma в зависимости от различных концентраций NaCl и CsCl.
Таблица
5
NaCl 0,005 М 0,010 М
6,87
В,85 6,81
6,44 7,72
6,40 6,40
7,65 7,70
3I
Продолжение табл.1
6,88
6,83
6,85
6,87
6,43 7,75
6,46 7,70 6,39 7,70
6,47 7,70
Таким образом, в присутствии солей NaCl и CsCl вязкость исследуемых ЭПС не изменяется, т.е. не наблюдается ни деградация, ни структурирование ЭПС,
В табл.2 приведены гидродинами- ческие параметры ЭПС f. Гидродинамические свойства изучали в водных растворах на аналитической центрифуге МОМ-3170 6 методом скорости седиментации. Седиментацию проводили в обычной ячейке при 48000 об/мин, диффузию - в ячейке с искусственной границей при 4000-8000 об/мин,
Таблица2
Вода
5,50
0,70
имечание. S°20 W константа седиментации, Д°20 W - константа диффузии.
4511664
Следовательно, в присутствии CsCl и Nad вязкость растворов исследуемых ЭПС, а также их гидродинамические ..параметры остаются неизменными, что
свидетельствует о стабильности структуры ЭПС в условиях градиента. Следует отметить, что способ применяют для анализа микробных ЭПС, проявляющих ,Q свойства, аналогичные исследуемым ЭПС (т„е. стабильность структуры в присутствии NaCl иCsCl).
15
20
П р и М е р 2. Иллюстрируют флуоресцентной метки при определении молекулярно-массовой неоднородности нативного ЭПС в в комбинированном градиенте NaCl и CsCl (вместо качественной реакции с фенолом и серной кислотой).
Перед градиентным центрифугированием проводят обработку ЭПС ь органическим красителем ФИТЦ (Serva). Проводят обработку нативного ЭПС, 25 не разделенного на фракции. Осуществляют центрифугирование меченого и необработанного (контрольного) ЭПС в комбинированном градиенте NaCl и CsCl, взятых в соотношении 1:1 при 2Q п 30000 об/мин в течение 19 ч. Уровень свечения фракций меченого ЭПС измеряют на приборе ЛЮМАМ-И2,. содержание углеводов во фракциях контрольного ЭПС определяют по реакции с фенолом и серной кислотой. На фиг.1 представлено молекулярно-массо- вое распределение ЭПС & в комбинированном градиенте NaCl и CsCl(l -меченый ЭПС, 2 - контрольный ЭПС).
Таким образом, применение реакции с фенолом и серной кислотой для анализа содержания углеводов во фракциях не ведет к снижению качества анализа по сравнению с использованием флуоресцентной метки.
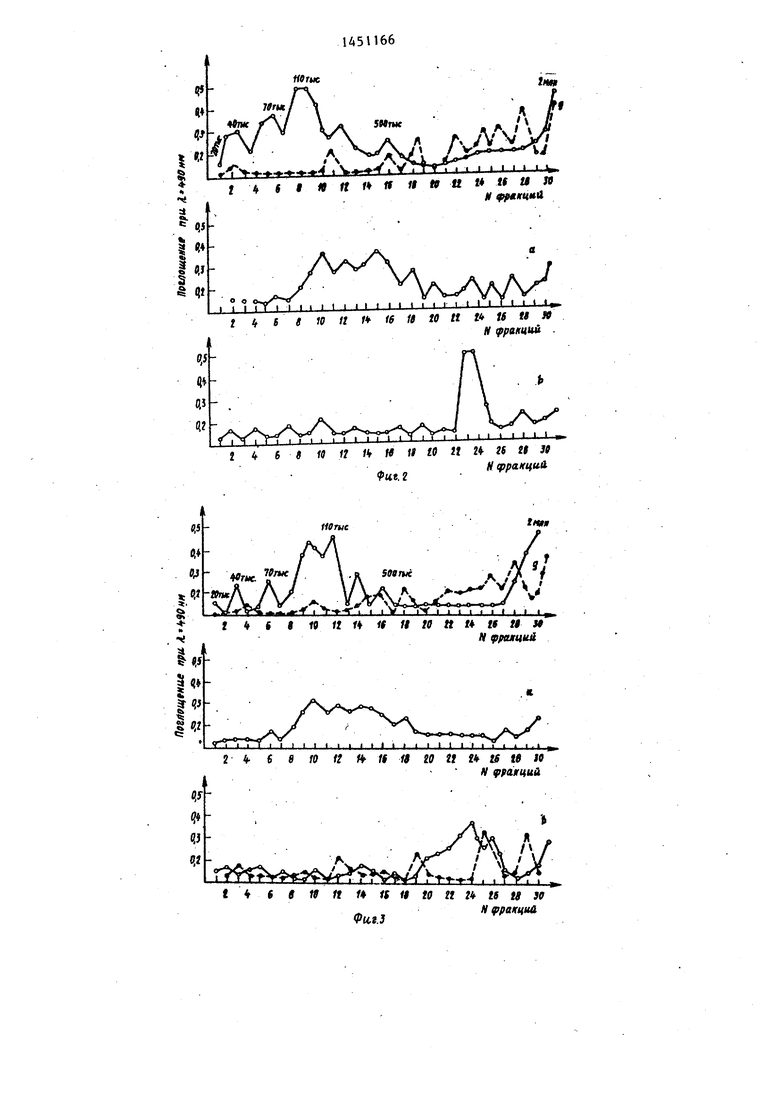
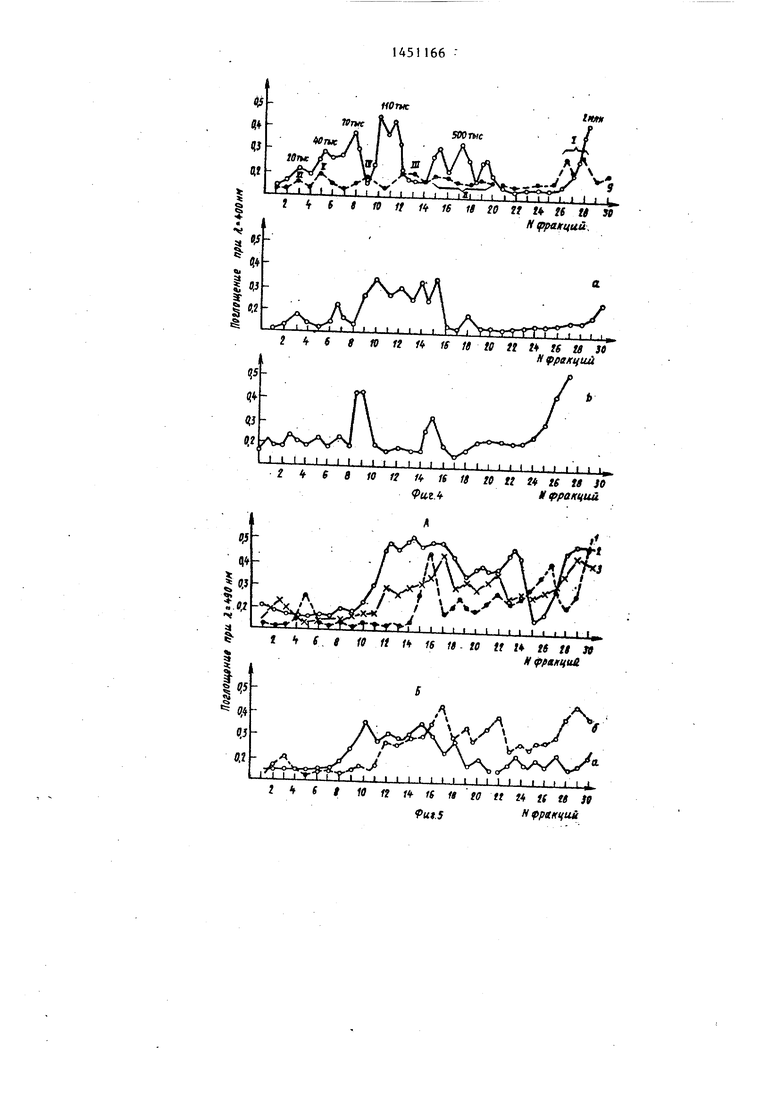
Пример 3. Показывают моле- кулярно-массовое распределение ЭПС и декстранов в комбинированном градиенте NaCl и CsCl, взятых в раз- личных соотношениях при п 30000 об/мин в течение 09 ч (плотность растворов NaCl, р 1,03 - 1,20 г/см , CsCl, 5- 1,20-1,60 г/см На фиг,2-4 показано молекулярно-мас- совое распределение ЭПС о , б, ь, и 5 декстранов в комбинированном градиенте плотности NaCl и CsCl, взятых в соотношении 1:1 (фиг.2), 2:1 (фиг.З), 5:1 (фиг.4).
0
5
5
На фиг,5 показано молекулярно-мас- совое распределение ЭПС, синтезируемого Xanthomonas campestris шт,8162 в комбинированном градиенте плотности солей NaCl и CsCl при их соотношении 2:1 (А, 1) 5П (А,2), 1,4:1 (А,3-,Б).
Как видно из фиг.2-4, изменяя соотношение солей NaCl и CsCl в за- висимос ти от поставленной экспериментатором задачи, можно более де тально исследовать те или иные компо ненты ЭПС различной молекулярной массы. Так, увеличение объема растворов NaCl (соотношение NaCl и CsCl 5:1) даст возможность четкого разделения низкомолекулярных составляющих (до 500 тыс.).(фиг.4) , в то время уак увеличение объемов растворов CsCl (соотношение NaCl и CsCl 2:1, 1:1), обладающих более высокой плотностью, позволяет успешно разделить высокомолекулярные фракции от 500 тыс. до 2 млн, (фиг.2 и 3). Акало- гичные выводы можно сделать исходя из кривых молекулярно-массового распределения, представленных на фиг.5,
При мер 4. Показывают возможности использования предлагаемого метода для анализа ЭПС, синтезируе- мых культурами-продуцентами ЭПС в различных условиях культивирования с целью выбора оптимального режима для получения ЭПС с заданными свойствами (фиг.З, фиг.5, пример 3)-.
П р и м. е р 5. Показывают целесообразность применения комбинированного градиента плотности солей NaCl и CsCl для анализа ЭПС.
На фиг,6 показано молекулярно-мас- сове распределение ЭПС, синтезируемого смешанной, культурой дрожжей и бактерий в градиенте плотности NaCl (А) (п 30000 об/мин, 4 ч (2), 19 ч (1) и в комбинированном градиенте 1ШОТНОСТИ солей NaCl и CsCl (Б) (п 30000 об/мин, 19 ч) при соотноше1ши NaCl и GsCl 2:1 (3) и 1:1 (4).
Применение растворов NaCl более высоких плотностей ( f 1,03-1,20 г/см, р 1,03-1,05 г/см) позволяет получить молекулярно-массовое распределение компонентов с мол. массой 20 тыс. - 500 тыс., т.е. в этом случае удается расширить нижнюю границу определяемых молекулярных масс от 180000 до 20 тыс.
511666
Время центрифугирования, равное 4 ч, является недостаточным для раз- деления компонентов ЭПС по сравнению с центрифугированием в течение 19 ч (фиг.6А). Для.разделения компонентов ЭПС с мол.массой более 500 тыс. использовали растворы CsCl плотностью f 1,20-1,60 г/см(фиг.6В).
10 П р и м е р 6. Показывают возможность одновременного расширения нижнего и верхнего пределов диапазона определяемых молекулярных масс при использовании комбинированного гра15 диента NaCl и CsCl.
Как указывалось,,в примере 5, применение градиентов с плотностью о 1,03-1,20 г/см позволяет расширить нижнюю границу определяемых мо20 ;;1екулярных масс до 20 тыс., введение CsCl плотностью j 1,20-1,60 г/см jB градиент дает возможность анализа .высокомолекулярных компонентов (500 тыс о .- 2 млн).
25 В данном примере в качестве стандарта молекулярных масс, кроме приме- , няемых ранее, используют декстран с молекулярной массой 13,7 тыс,
На рис.ба представлено молекуляр30 но-массовое распределение ЭПС В при центрифугировании в комбинированном градиенте NaCl ( f 1,Q3-1,20 г/См) и CsCl ( р 1,20-1,60 г/см), взятых в соотношении 5:1, в течение 19 ч при п 30000 об/мин.
Применение комбинированного гради-, ента NaCl и CsCl для ЭПС позволяет расширить как нижний предел определяемых молекулярных масс (менее
Q 20 тыс. по сравнению с применением градиента растворов хлористого натрия), так и верхнюю границу диапазона молекулярных масс (500 тыс. - 2 млн).
д При этом результаты, представленные на фиг.6а, согласуются с полученными ранее (см,пример 3, фиг.4в). Наличие пика в первой фракции ЭПС 6 (фиг.4) соответстэуёт фракции с
g мол,массой 13,7 тыс., как показано в данном примере.
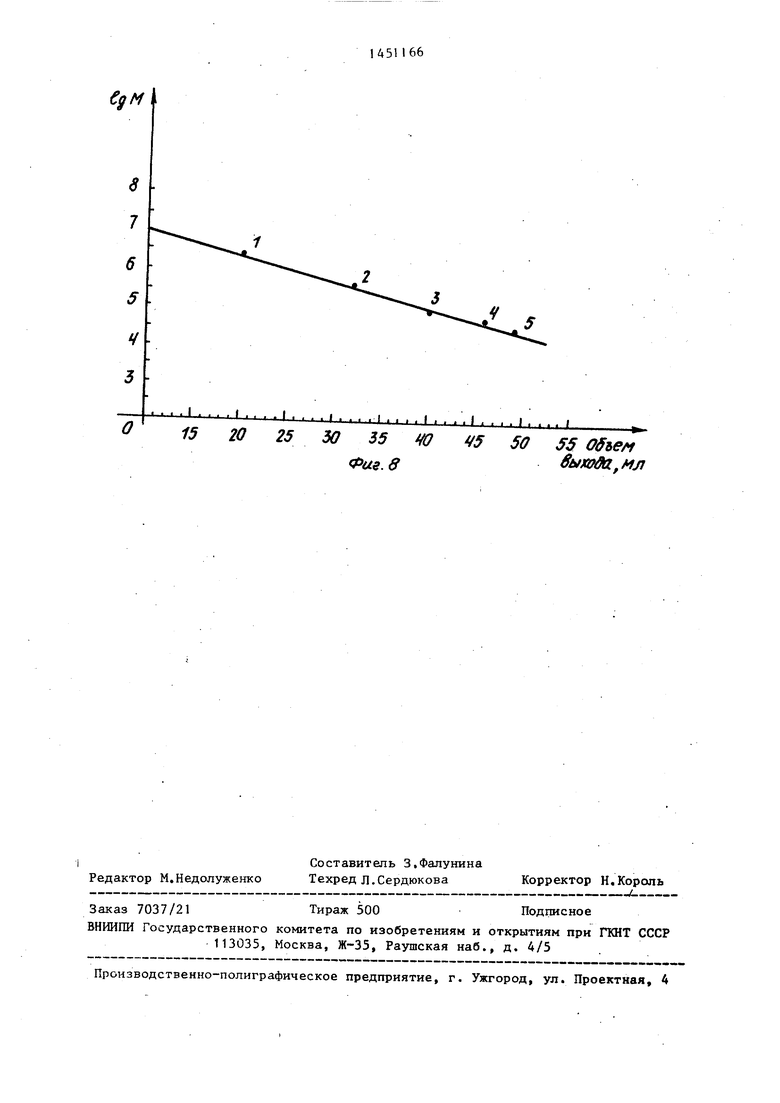
Пример 7. Показывают соответствие результатов, полученных при применении предлагаемого метода для анализа микробных ЭПС и гель-хроматографии. На фиг.7 представлен элюци- онный профиль ксантана Sigma при гель-хроматографии на колонке с се- фарозой 4В (размеры колонки 0,9 х
35
55
8 10 12
12 /« 16 IS
10 гг г гв гв w
Номера {фракций
f /5 18 20 гг г« гв гв зо
Нанера фракций uz.1
t L s t 10 It 1 б II to tt f и M
H fpaiiuuu
I «. 68 19 n W W 2
H ррлкций . 2
tutu


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения молекулярно-массового распределения лектинов и гумусовых соединений почвы | 1988 |
|
SU1756357A1 |
| Способ отделения полирибосомных информосом от свободных | 1986 |
|
SU1412305A1 |
| СПОСОБ ОЧИСТКИ ВИРУСОВ ПУТЕМ УЛЬТРАЦЕНТРИФУГИРОВАНИЯ В ГРАДИЕНТЕ КОНЦЕНТРАЦИИ САХАРА (ВАРИАНТЫ) | 2008 |
|
RU2503719C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФАКТОРА, СТИМУЛИРУЮЩЕГО ОБРАЗОВАНИЕ КОЛОНИЙ ГРАНУЛОЦИТОВ | 1986 |
|
RU2057809C1 |
| Способ получения вакцин против лейкоза крупного рогатого скота | 1977 |
|
SU820015A1 |
| ГЛИКОПРОТЕИН TCF-II И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЭФФЕКТИВНОЕ КОЛИЧЕСТВО ГЛИКОПРОТЕИНА TCF-II | 1991 |
|
RU2097432C1 |
| N,О-СУЛЬФАТИРОВАННЫЕ ГЕПАРОЗАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИТРОМБОТИЧЕСКОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2099353C1 |
| Способ получения сайт-специфической эндонуклеазы @ @ | 1983 |
|
SU1120019A1 |
| СПОСОБ ДИАГНОСТИКИ ЛЕЙКОЗА КРУПНОГО РОГАТОГО СКОТА | 2004 |
|
RU2282854C1 |
| Способ получения синтетической двунитчатой РНК, обладающей интерферониндуцирующей активностью | 1979 |
|
SU933001A3 |


Изобретение относится к биотехнологии и касается исследования состава микроб1шх экзополисахаридов. Целью изобретения является расширение технологических возможностей способа за счет увеличения диапазона исследуемых .молекулярных масс. Способ заключается в том, что фракциони- растворов экзополисахаридов и стандартов молекулярных масс происходит в комбинированном градиенте солей NaCl и CsCl, взятых в соотношении 5:1-1:1, и плотности NaCl р 1,03-1,20 г/см CsCl р 1,2- 1,6 г/см при п 30000 об/мин в течение 19 ч. 8 ил., 2 табл. а 
HOnic
tut
fme
5«r« AV //
ft Д.. /
) о O
; S rVg -rrrrr . . .
t ft t i n It 1 к II to tt tt t 30
H д раяииЛ
2 6 8 n К 1 tf 19 tO tt « tf W W
ft VfMHUU
t ft 6 в n n 1 iS It to tt ti tS tS 30
H фракций Фиг.З
tut
5«r« AV //
ft Д.. /
) о O
; S rVg -rrrrr . . .
« « w « w « 4 w a se
ff ppaxtftiu
г
f В 10 fl II, 16 IS to ti « и te JO Ри.г.H (рракчий
0
f f W It f Г5 «. г ,4 W W лГ
Ж фракций
. Л A
V-. - , ,yVsAy
. , --t J i 1 I I I I r i I I , , , . I ,
г f / w / fv 16 to tt i ts te 39
fut.5И рякциы
/«Mr
US
|Й5
laf
РЛ 0.3 0,2
f tf w /f /4 16 18 го ti 2v tt w
Hipptumuu
fw-g.ff
15 20 25 SO 55 у sO S Одъе
Фае. 8вб/х0да.,мл
| Holzwarth G | |||
| Molecular .weight of xanthan polysaccharide | |||
| Ca rb | |||
| Researoh, 66, 1978, 173-186. |
Авторы
Даты
1989-01-15—Публикация
1986-09-16—Подача