Известен способ получения азотной кислоты из жидких очислов азота, воды и кислорода, осуществляемый путем гетерогенного пронесся.
Предлагаемый способ получения 60-80%-ной азотной кислоты под атмосферным давлением из жидких окислов азота, воды и кислорода, отличается частичным проведением реакции образования азотной кислоты в газовой фазе при температуре не выше 250°, что обеспечивает получение продукта особой чистоты.
Технологический процесс предлагаемого способа сводится к следующему.
Окислы азота, водяные пары и кислород смешивают в реакционном объеме, где -протекает реакция образования азотной кислоты в газовой фазе и окисление вторичной окиси азота, выделяющейся при этом.
Газовая смесь при поступлении в реакционный объем, согласно экспериментальным данным, должна содержать.
При получении 60%-ной НЫОз (отдутой): NO2 22%- Н20 54%О2 24%; 0,41; степень переработки 92-93%.
При получении 66%-ной HNOa: NO2 26%; Н2О 48%; 02 26%; NO2MH2O 0,54; степень переработки 84--86%
При получении 70-71%-ной HNOa: NO2 32%; Н2О 49%; О2 19%; ,65; степень переработки 75%.
При получении 75%-ной НЫОз: NO2 44%; Н2О 34%; О2 22%; ,3; степень переработки 45-50%.
При получении 80%-ной НЫОз: NO2 50%; Н2О 26%- О2 24%; .1,9; степень -переработки 35-38%.
Во всех случаях степень лереработки, может быть увеличена повышением парциального давления окислов азота (при сохранении постоян№ 148795, . ., 2ным соотйошением NOgj/iHzO за счет снижения парциального давления кислорода. Такое снижецде-концентрации кислорода допустимо до концентрации его, необходимой для полной переработки окислов азота в азотнуЮ кислоту заданной концентрации.
Основной процесс образования азотной кислоты протекает в холодильнике-конденсаторе.. Снижение температуры в холодильнике благоприятно отражается на скорости окисления вторичной окиси азота, а также и на реакции взаимодействия четырехокиси с водяным ,паром. Далее, при снижении температуры повышается парциальное давление четырехокиси азота, вследствие смещения равновесия реакции: N204 2NO2B сторону образования N504. Это, в свою очередь, ускоряет процесс кислотообразования, так как скорость образования прямо пропорциональна парциальному давлению четырехокиси азота. Повышению скорости реакции также способствует высокоразвитая поверхность, образующаяся в объеме холодильника-конденсатора при конденсации па.ров воды и азотной кислоты.
Перечисленные обстоятельства дают возможность получать азотную кислоту цод атмосферным давлением с концентрацией до 90%. Отличительной особенностью предлагаемого способа является проведение реакции образования азотной кислоты в газовой фазе.
Необходимой чистоты кислоты достигают за счет использования практически чистых окислов азота, причем испаряют их при температурах ниже 20°, что способствует уменьшению уноса примесей. Испарение дистиллята или ионитной воды также обеспечивает получение паров нужных кондиций, причем последнее проверено в полузаводских условиях.
Ведение процесса при пониженных температурах повышает коррозионную устойчивость аппаратуры и это предполагает возможность получения азотной кислоты (по крайней мере класса В-3) в аппаратуре из некоторых марок нержавеющих сталей.
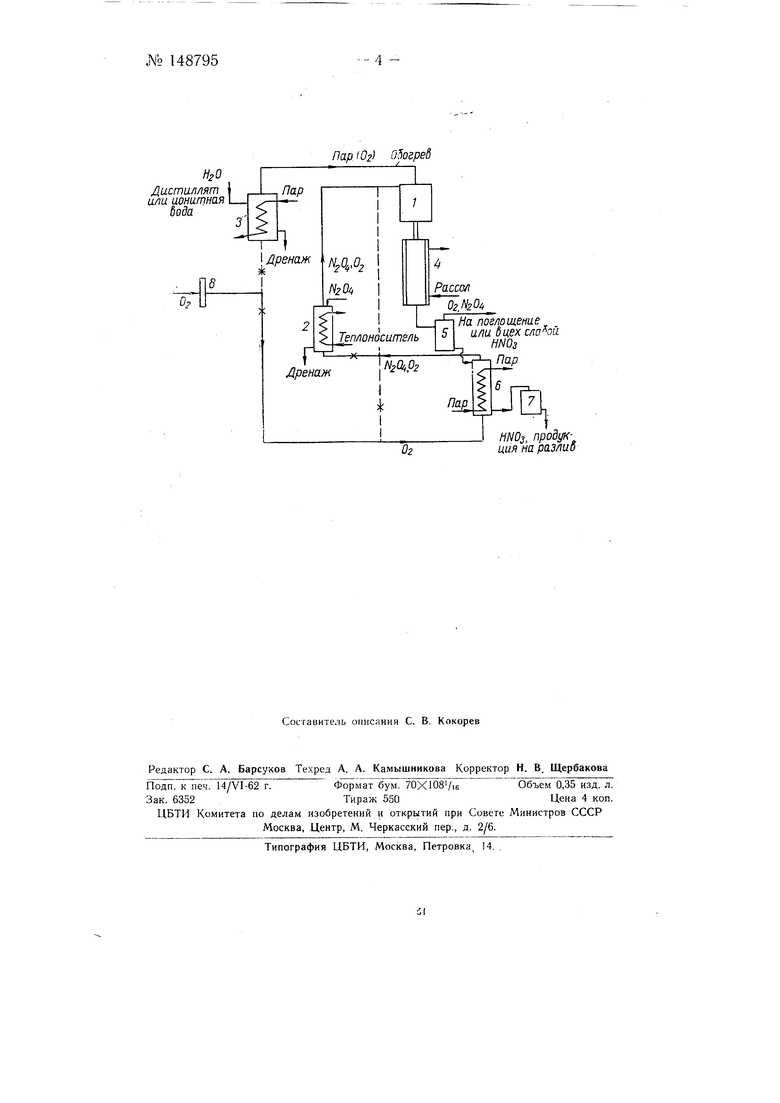
На чертеже показана принципиальная схема получения азотной кислоты.
В реакционный аппарат / (удельный реакционный объем должен составлять 0,3-0,6 миг в сутки) подают окислы азота с кислородом из испарителя 2 и водяные пары (с кислородом или без него) из испарителя 3.
Испарители 2 и 5 изготовляют однотипными из кварцевого стекла, причем в обоих случаях предусматривают дренажные линии для дренажа части воды и окислов азота (последние должны дренажироваться в очень незначительном количестве). Также предусматривают подачу в испаритель 3 пара (через змеевики или другим способом) и в испаритель 2 теплоносителя для поддержания в этих аппаратах необходимой температуры, которая определяется заданной концентрацией продукционной кислоты. Температура в обоих испарителях при необходимости может быть снижена за счет подачи кислорода. Линия подачи .паров должна обогреваться до температуры на 5-10° выще точки росы поступающего по ней водяного пара.
В реакционном объеме аппарата / протекает реакция образования азотной кислоты в газовой фазе и окисление вторичной окиси азота. Из аппарата / смесь газов поступает в холодильник- конденсатор 4, выполненный из кварцевого стекла, типа труба в трубе, где происходит основной процесс кислотообразования.
Охлаждение производят рассолом до температур 5-7°. В целях повышения растворимости окислов азота температура может быть понижена.
При получении 80%-ной HNOs происходит расслаивание жидкой смеси, и в этом случае снижение температуры будет целесообразно.
Необходимый реакционный объем холодильника-конденсатора должен составлять порядка 0,2-0,25 . мнг. в сутки при соотношении объема к поверхности 0,33-0,38 холодильника азотная кислота и окислы азота поступают в кварцевый сепаратор 5 любого типа и затем в отбелочную кОиПонну 6, выполненную из кварцевого стекла. Предусматривают обогрев колонны и подачу .кислорода, необходимого для синтеза HNOs (кислород предварительно должен проходить через фильтры 8. для очистки от примесей). Смесь окислов азота и кислорода подают в испаритель 2 или вводят непосредственно в реакционный объем.
Продукционная кислота поступает в сборник 7, откуда подается на разлив в бутыли или другие емкости.
Переработка окислов азота, выходящих из сепаратора 5, целиком зависит от концентрации получаемой кислоты и от технологических условий данного производства.
Например, при получении 70%-ной HNOs окислы азота (количество окислов азота в выходящих газах будет составлять 4-6% от поступающих в систему при концентрации 14-19% и степени переработки 75%) могут быть направлены в нитроолеумную колонну цеха крепкой азотной кислоты (эта колонна служит в отделении отбелки для улавливания окислов азота из газа после конденсации). Если имеется цех слабой азотной кислоты под атмосферным давлением, то остаточные газы установки могут быть в нем утилизированы. Любой из этих вариантов вполне осуществим в промышленности.
Предметизобретения
Способ получения 60-80%-ной азотной кислоты под атмосферным давлением из жидких окислов азота, воды и кислорода путем гетерогенного процесса, отличающийся тем, что, с целью получения продукта особой чистоты, реакцию образования азотной кислоты частично ведут в газовой фазе при температурах не выше 250°.
148795
Пар. 102) O oepeS
и пи б цех слабой
НИОз, продукция на раз/iuD


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА ДИНИТРОГЕНА ТЕТРАОКСИДА | 2012 |
|
RU2547752C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОТНОЙ КИСЛОТЫ ПОД АТМОСФЕРНЫМ ДАВЛЕНИЕМ | 1965 |
|
SU170922A1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРАТА КАЛИЯ | 1971 |
|
SU310441A1 |
| СПОСОБ ОЧИСТКИ ТЕХНИЧЕСКОЙ АЗОТНОЙ КИСЛОТЫ | 1962 |
|
SU149406A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОТНОЙ КИСЛОТЫ ПОВЫШЕННОЙ КОНЦЕНТРАЦИИ | 1973 |
|
SU370171A1 |
| СПОСОБ ПРОИЗВОДСТВА АЗОТНОЙ КИСЛОТЫ | 2000 |
|
RU2174946C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОТНОЙ КИСЛОТЫ | 1966 |
|
SU183194A1 |
| Способ получения цинкнитратфосфатного концентрата | 1982 |
|
SU1172214A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОТНОЙ КИСЛОТЫ | 1998 |
|
RU2151736C1 |
| СПОСОБ ПРОИЗВОДСТВА АЗОТНОЙ КИСЛОТЫ | 1997 |
|
RU2127224C1 |


Авторы
Даты
1962-01-01—Публикация
1961-09-02—Подача