1
Изобретение относится к способу получения новых о.,-аминоалкил-о -алкилCN
I
фенилацетонит щей формулы
c.-(CHiV- J-()n-o-O «
RS R.
R
фенилацетонитрильных производных общей формулы
i)n-o-O «
04









| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных феноксиэтиламина | 1989 |
|
SU1788953A3 |
| Способ получения производных бензамида | 1988 |
|
SU1627082A3 |
| Способ получения производных пиримидина | 1985 |
|
SU1436872A3 |
| Способ получения производных карбостирила | 1982 |
|
SU1356962A3 |
| Способ получения гетероциклических соединений с конденсированным бензолом | 1985 |
|
SU1375137A3 |
| Способ получения производных карбостирила | 1982 |
|
SU1331426A3 |
| Способ получения 3,4-дигидрокарбостирильных производных или их солей | 1973 |
|
SU580835A3 |
| Способ получения анилинового производного или его фармацевтически приемлемой соли | 1982 |
|
SU1316560A3 |
| Способ получения производных 1,4-дигидропиридина | 1985 |
|
SU1342413A3 |
| Способ получения карбостирильных производных | 1981 |
|
SU1367857A3 |
ИЗОБРЕТЕНИЕ КАСАЕТСЯ НИТРИЛОСОДЕРЖАЩИХ ВЕЩЕСТВ ,В ЧАСТНОСТИ, ПОЛУЧЕНИЯ Α-АМИНОАЛКИЛ-Α-АЛКИЛФЕНИЛАЦЕТОНИТРИЛЬНЫХ ПРОИЗВОДНЫХ ОБЩЕЙ Ф-ЛЫ R1R2R3C6H2-CR4(CN)-(CH2)M-NR5-(CH2)N-O-C6H3R6R7, ГДЕ R1-R3-ОДИНАКОВЫЕ ИЛИ РАЗЛИЧНЫЕ, H ИЛИ НИЗШАЯ АЛКОКСИГРУППА
R4-НОРМАЛЬНЫЙ ИЛИ РАЗВЕТВЛЕННЫЙ НИЗШИЙ АЛКИЛ
R5-H ИЛИ НИЗШИЙ АЛКИЛ
R6 И R7 - ОДИНАКОВЫЕ ИЛИ РАЗЛИЧНЫЕ, H, ГАЛОГЕН, НИЗШИЕ АЛКИЛ- ИЛИ АЛКОКСИГРУППА, NO2,NH2, ГИДРОКСИ НИЗШИЙ АЛКИЛ
M И N = 2 ИЛИ 3, ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ, КОТОРЫЕ МОГУТ БЫТЬ ИСПОЛЬЗОВАНЫ ДЛЯ ЛЕЧЕНИЯ СОСУДИСТЫХ ЗАБОЛЕВАНИЙ, НЕДОСТАТОЧНОСТИ ПЕРИФЕРИЧЕСКОГО И МОЗГОВОГО КРОВООБРАЩЕНИЯ. ЦЕЛЬ ИЗОБРЕТЕНИЯ - СОЗДАНИЕ БОЛЕЕ АКТИВНЫХ И МЕНЕЕ ТОКСИЧНЫХ ВЕЩЕСТВ УКАЗАННОГО КЛАССА. ИХ СИНТЕЗ ВЕДУТ РЕАКЦИЕЙ СОЕДИНЕНИЙ Ф-Л R1R2R3C6H2-CR4(CN)-(CH2)К - CH=O И NHR5-(CH2)N-O-C6H3R6R7, ГДЕ R1-R7, N ИМЕЮТ УКАЗАННЫЕ ЗНАЧЕНИЯ, К=1 ИЛИ 2, В ПРИСУТСТВИИ ОРГАНИЧЕСКОГО РАСТВОРИТЕЛЯ С ПОСЛЕДУЮЩЕЙ ОБРАБОТКОЙ ВОССТАНАВЛИВАЮЩИМ АГЕНТОМ И ВЫДЕЛЕНИЕМ ЦЕЛЕВОГО ПРОДУКТА В СВОБОДНОМ ВИДЕ ИЛИ В ВИДЕ СОЛИ. В СЛУЧАЕ, КОГДА В СОЕДИНЕНИИ R5-H, ТО ЕГО ДОПОЛНИТЕЛЬНО АЛКИЛИРУЮТ, А КОГДА R6-NO2, ТО ПРИ НЕОБХОДИМОСТИ ВОССТАНАВЛИВАЮТ. НОВЫЕ ВЕЩЕСТВА ПРОЯВЛЯЮТ СА-АНТАГОНИСТИЧЕСКУЮ АКТИВНОСТЬ, АНТИАРИТМИЧЕСКОЕ И Α-РЕЦЕПТОРНОЕ БЛОКИРУЮЩЕЕ ДЕЙСТВИЕ ВЫШЕ, ЧЕМ ИЗВЕСТНЫЕ АНАЛОГИ УКАЗАННОГО НАЗНАЧЕНИЯ ПРИ МЕНЬШЕЙ ТОКСИЧНОСТИ (ЛД50 208-510 МГ/КГ). 7 ТАБЛ.
где каждый из радикалов R, Rj,
Rj может иметь одинаковые или раз
1-«
1-«
личные значения и представляют собой водород, или низшую
15
алкоксигруппу;
R низший алкил нормального или разветвленного строения;
Rg - водород или низший алкил; R и 11 каждый может иметь одинаковые
или различные значения и представляет собой водород, галоген, низший алкил, низшую алКОКСИ-, НИТРО-, аминогруппу, |Q
гидроксинизшую алкильную группу;
m и п - целые числа, выбранные из значений рйвных 2 и 3,
или их кислотно-аддитивных фармацевтически приемлемых солей, которые могут найти применение для лечения сосудистых заболеваний, недостаточности периферического кровообращения и нарушения мозгового кровообращения.
Цель изобретения - изыскание способа получения новых фенилацетонит- рильных производных, которые проявляют более высокую активность и меньшую токсичность по сравнению с ми соединениями, близкими по структуре и того же назначения.
Пример 1.0 -Изопропил-Ы- З- (4-метоксифенокси)этил амино пропил -3,4-диметоксифеНИЛацетонитрил.
I
Раствор 3,96 г 4-циано-4-изопропиЛ7 -4-(3,А-диметоксифенил)масляного альдегида и 2,00 г 2-(4-метоксифенокси)- этиламина в 50 мл этанола нагревают с обратным холодильником в течение 1 ч,К полученному раствору добавляют 0,55 г борогидрида натрия при охлаждении сис20
Раствор 6,00 г З-циано-З-изопро- пил-3-3(3,4,5-триметоксифенил)пропи- онового альдегида и 2,26 г 3-фенокси- пропиламина в 50 мл метанола нагревают с обратным холодильником в течение 1ч. К полученному раствору добавляют 0,76 г борогидрида натрия при охлаждении системы льдом и полученный раствор перемешивают в течение 1 ч при комнатной температуре. Раст - воритель удаляют и остаток растворяют в 10%-ном растворе хлористоводородной кислоты и затем промьшают эфм ром. Водный слой подщелачивают карбонатом калия и экстрагируют хлорофо|р- мом. Экстракт промывают водой, сушат и выпаривают с образованием 5,40 г (79%) соединения в виде бледно-желтого масла.
Масс-спектр m/z: 412 (М).
Гидрохлорид такого соединения получают обычным способом.
Пример З. -Изопропил-тоб- З- известны- 25 (2-феноксиэтиламино)пропил -3,4,5триметоксифенилацетонитрил гидрохло- рид.
Раствор 3,05 г 4-циана-4-изопро- пил-4-(3,4,5-триметоксифенил)масля- ного альдегида и 1,37 г 2-фенокси- этиламина в 40 мл этанола нагревают с обратным холодильником в течение 1 ч. К полученному раствору добавляют 0,38 г борогидрида натрия при охлаждении системы льдом и полученный раствор перемешивают в течение 30 мин при комнатной температуре. Растворитель удаляют, к остатку добавляют 10%-иый раствор хлористоводородной
30
35
темы льдом и полученный раствор переме- 40 кислоты и эфир. Осадок отфильтровывашивают в течение 30 мин при комнатной температуре. Растворитель удаляют, остаток растворяют в 10%-ном растворе хлористоводородной кислоты и промьгаа- ют эфиром. Водный слой подщелачивают «с карбонатом калия и экстрагируют этил- ацетатом. Экстракт промывают водой, сушат и вьтаривают. Остаток подвергают хроматографической очистке на си- ликагеле с использованием хлороформа в качестве элюента с образованием 2,93 г (57%) соединения в виде бледно-желтого масла.
Масс-спектр m/z: 426 (М).
50
ют и промьшают эфиром с образованием 2,75 г (59%) соединения в виде бесцветных кристаллов.
Свободное основание такого соединения получают обычным способом.
Масс-спектр m/z: 426 (М.
Соединения, описанные в примерах 4-6, получают тем же способом, что и в примерах 1-3: пример 4 -о6-изопро- пил-ot- (2-метоксифенокси) этил амино пропилЗ-3,4-диметоксифенил- ацетонитрил малеат; пример 5 -об-изо- nponnn-oi. (2-метилфенокси
Гидрохлорид этого соединения полу |этил амино пропилЗ-3,4-диметоксифег-:;
чают обычным способом.нилацетонитрил гидрохлорип; пример 6 Пример 2.oi,-Изопропил-«.- 2-5 -изопропил-х1 - 2- М (2-метоксифе(2-феноксиэтиламино),4,5-три-нокси)пропил -амино ,4,5-триметоксифенилацетонитрил.
15
20
30
35
ют и промьшают эфиром с образованием 2,75 г (59%) соединения в виде бесцветных кристаллов.
Свободное основание такого соединения получают обычным способом.
Масс-спектр m/z: 426 (М.
Соединения, описанные в примерах 4-6, получают тем же способом, что и в примерах 1-3: пример 4 -о6-изопро- пил-ot- (2-метоксифенокси) этил амино пропилЗ-3,4-диметоксифенил- ацетонитрил малеат; пример 5 -об-изо- nponnn-oi. (2-метилфенокси
этил амино пропилЗ-3,4-диметоксифег-:;
метоксифенилацетонитрил гидрохлорид.
51494863
Пример 7 . ui-Изопропнл-ci-(3- (2-метоксифенокси)этил -N-ме- тиламино пропил -3,4-диметоксифенил- ацетонитрил.
Смесь, состоящую из 2,23 г о,-изо- nponiUT-oC-L3- H-L2- (2-метоксифенокси) этил aMHHoJ пропил -3, А-диметоксифе- нилацетонитрила, 8 мл 37%-ного раствора формалина и 16 мл 90%-ной муравьиной кислоты, перемешивают в течение 1 ч при 110°С. После охлаждения к полученной смеси добавляют воду и карбонат калия с целью ее подщелачи- вания. Полученный раствор экстрагируют хлороформом и экстракт промывают водой, сушат и выпаривают. Остаток подвергают хроматографической очистке на силикагеле с использованием хлороформа в качестве эл1оента с образованием 1,30 г (54%) Соединения в виде бледно-желтого масла.
Пример 8. oi-Изoпpoпил-oi. N-L2-(2-мeтилфeнoкcи) этил -Н-метилРаствор 8,09 г 4-циано-4-изопро- пил-4-(3,4,5-триметоксифеНИЛ)масляного альдегида и 4,96 г 3-(2-нитро- g фе 1окси)пропилаьшна в 100 мл метанола нагревают с обратным холодильником в течение 3 ч. После охлаждения к полученному раствору добавляют 0,50 г борогидрида натрия и раствор переме- 10 шивают в течение ночи при комнатной температуре. Растворитель удаляют, . к остатку добавляют воду. Полученный раствор экстрагируют хлороформом и экстракт промывают водой, сушат и вы- 15 паривают. Полученный остаток подвергают хроматографической очистке на силикагеле с использованием в качестве элюента системы 10%-ный метанол - хлороформ с образованием 6,48 г (53%) соединения в виде бледно-желтого масла.
Оксалат такого соединения получают обычным способом.
Пример 1 1. с -Изопропил-(
4,78 Г(х:-изопропил-о(.- 3- Ы-СЗ-(2- нитрофенокси)пропил аминоЗ пропил -З,
амино пропил -3,4-диметоксифенилаце- 25 (2-aминoфeнoкcи)пpoпилaминo тонитрил.пропил -3,4,5-триметоксифенилацетоСмесь, состоящую из 1,84 го -изо- нитрил
пропи.(2-метилфенокси)этил амино пропил -3,4-диметоксифеНИЛацетонитрила гидрохпорида, 5,5 мл 37%-но-зо 4,5-триметрксифенил ацетонитрила гид- го раствора формалина и 11 мл 90%-ной рируют в 100 мл метанола над 50 мг муравьиной кислоты, обрабатывают аналогично примеру 7 с образованием 1,14 г (60%) соединения в виде бесцветного масла.
Пример 9.0 -Изопропил-oi- 2-( (2-метоксифеноксипропил -N-метил- аминб этил -3,4,5-триметоксифенилаце- тонитрил.
Смесь, состоящую из 0,39 roi-изо- пропил-ск:,- З- (2-метоксифенокси) , пропил амино этил -3,4 ,5-триметок- сифенилацетонитрила, 1 мл 37%-но го раствора формалина и 1 мл 90%-ной муравьиной кислоты, нагревают с обратным холодильником в течение 1 ч. После охлаждения к полученной смеси добавляют воду и карбонат калия с целью ее подщелачивания. Полученный раствор экстрагируют хлороформом. Экстрат промьгоают водой, сушат Л выпаривают с образованием 0,23 г (57%) соединения в виде желтого масла.
Пример 10. о6-Изопропил-с -Qjокиси платины при атмосферном давлении и комнатной температуре. Катализатор отфильтровывают и фильтрат вы- 25 паривают с образованием 4,36г (97Z) соединения в виде бледно-желтого масла.
Оксалат такого соединения получают обычным способом.
40 Пример 12. об-Изопропил- оС- З- ( 2-нитрофенокси) пропил - N-метиламино пропил |-3,4,5-триметок- сифенилацетонитрил.
Смесь, состоящую из 2,58 Гск -изо45 лрогтл- - 3-Гн-ГЗ-(2-нитрофенокси)- пропил амино пропил -3,4 ,5-триметок- сифенилацетонитрила, 4,35 мл 37%-ного раствора формалина и 4,35 г 90%-ной муравьиной кислоты, перемешивают в
50 течение 1 ч при . После охлаждения к смеси добавляют воду и карбонат калия с целью ее подщелачивания. Полученный раствор экстрагируют хлороформом и полученный экстракт промы55 вают водой, сушат и выпаривают. Остаток подвергают хроматографической
(2-нитрофенокси)пропил амино|про- очистке на силикагеле с использова- ,4,5-триметоксифенилацетонит- нием в качестве элюента системы рил.1%-ный метанол - хлороформ с образеРаствор 8,09 г 4-циано-4-изопро- пил-4-(3,4,5-триметоксифеНИЛ)масляного альдегида и 4,96 г 3-(2-нитро- g фе 1окси)пропилаьшна в 100 мл метанола нагревают с обратным холодильником в течение 3 ч. После охлаждения к полученному раствору добавляют 0,50 г борогидрида натрия и раствор переме- 0 шивают в течение ночи при комнатной температуре. Растворитель удаляют, . к остатку добавляют воду. Полученный раствор экстрагируют хлороформом и экстракт промывают водой, сушат и вы- 5 паривают. Полученный остаток подвергают хроматографической очистке на силикагеле с использованием в качестве элюента системы 10%-ный метанол - хлороформ с образованием 6,48 г (53%) соединения в виде бледно-желтого масла.
Оксалат такого соединения получают обычным способом.
Пример 1 1. с -Изопропил-(
5 (2-aминoфeнoкcи)пpoпилaминo пропил -3,4,5-триметоксифенилацето4,78 Г(х:-изопропил-о(.- 3- Ы-СЗ-(2- нитрофенокси)пропил аминоЗ пропил -З,
нитрил
4,5-триметрксифенил ацетонитрила гид- рируют в 100 мл метанола над 50 мг
зо 4,5-триметрксифенил ацетонитрила гид- рируют в 100 мл метанола над 50 мг
окиси платины при атмосферном давлении и комнатной температуре. Катализатор отфильтровывают и фильтрат вы- 25 паривают с образованием 4,36г (97Z) соединения в виде бледно-желтого масла.
Оксалат такого соединения получают обычным способом.
0 Пример 12. об-Изопропил- оС- З- ( 2-нитрофенокси) пропил - N-метиламино пропил |-3,4,5-триметок- сифенилацетонитрил.
Смесь, состоящую из 2,58 Гск -изо5 лрогтл- - 3-Гн-ГЗ-(2-нитрофенокси)- пропил амино пропил -3,4 ,5-триметок- сифенилацетонитрила, 4,35 мл 37%-ного раствора формалина и 4,35 г 90%-ной муравьиной кислоты, перемешивают в
0 течение 1 ч при . После охлаждения к смеси добавляют воду и карбонат калия с целью ее подщелачивания. Полученный раствор экстрагируют хлороформом и полученный экстракт промы5 вают водой, сушат и выпаривают. Остаток подвергают хроматографической
очистке на силикагеле с использова- нием в качестве элюента системы 1%-ный метанол - хлороформ с образеванием 1,43 г (57%) соединения в виде желтого масла.
Пример 1 3. oi-Изопропил-сС- (3-гидроксиметилфенокси)про- пил -Н-метиламино пропил -3 ,4 ,5-три- метоксифенилацетонитрил.
Раствор, состоящий из 2,80 изопропил-бб- (3-гидроксиме- тилфенокси)пропилЗамино пропил -3,4, 5-триметоксифенил ацетонитрила и 4,84 г 37Z-Horo раствора формалина в 70 мл метанола, нагревают с обратным холодильником в течение 1 ч. После охлаждения к раствору добавляют 2,25 г борогидрида натрия и раствор перемешивают в течение 1 ч при комнатной температуре. Растворитель удаляют и к остатку добавляют воду. Полученный раствор экстрагируют хлороформом и экстракт промьшают водой, сушат и выпаривают. Остаток подвергают хроматографической очистке на силикагеле с использованием системы 10%-ный метанол - хлороформ в качестве элюента с образованием 0,74 г (26% соединения в виде желтого масла.
Прим ер 14.0Л -Изопропил-о - З- IN- 3-(2-аминофенокси)пропил -N-ме- тиламино пропил -3,4,5-триметоксифе- нилацетонитрил.
0,92 го6-изопропил-е/-р- Н- 3-(2- нитрофенокси)пропил -N-метилaминoJ- пропил-3,4,5-триметоксифенилацетонит- рила гидрируют в 20 мл метанола над 1Q мг окиси платины при атмосферном давлении и комнатной температуре.Катализатор отфильтровьтают и фильтрат вьтаривают с образованием 0,91 г (/v 100%) соединения в виде желтого
масла.
Оксалат такого соединения получают обычным способом.
Соединения, получаемые в примерах 15-185, синтезируют аналогично примерам 1-14.
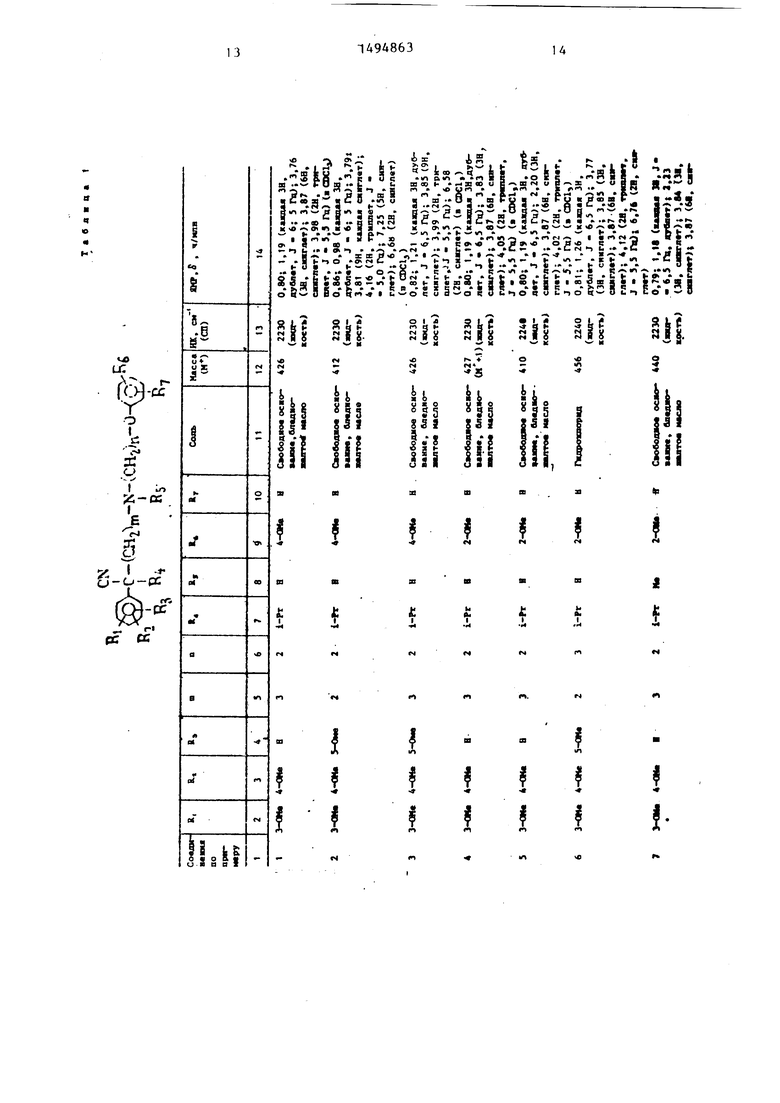
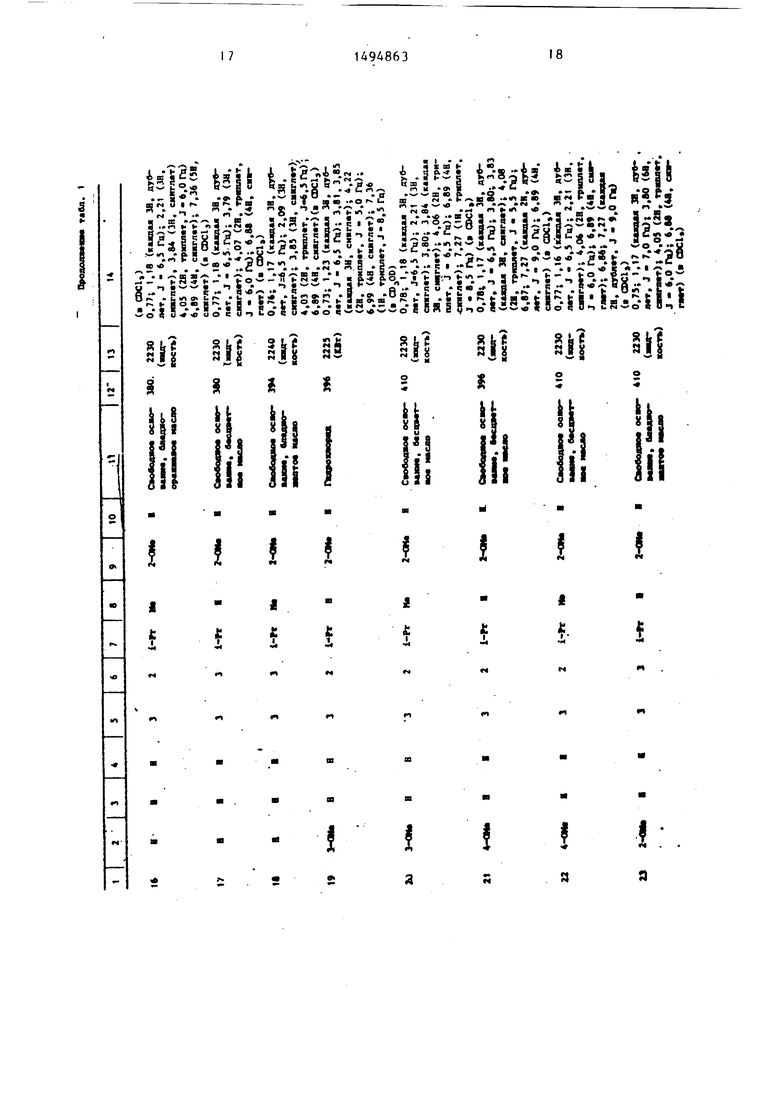
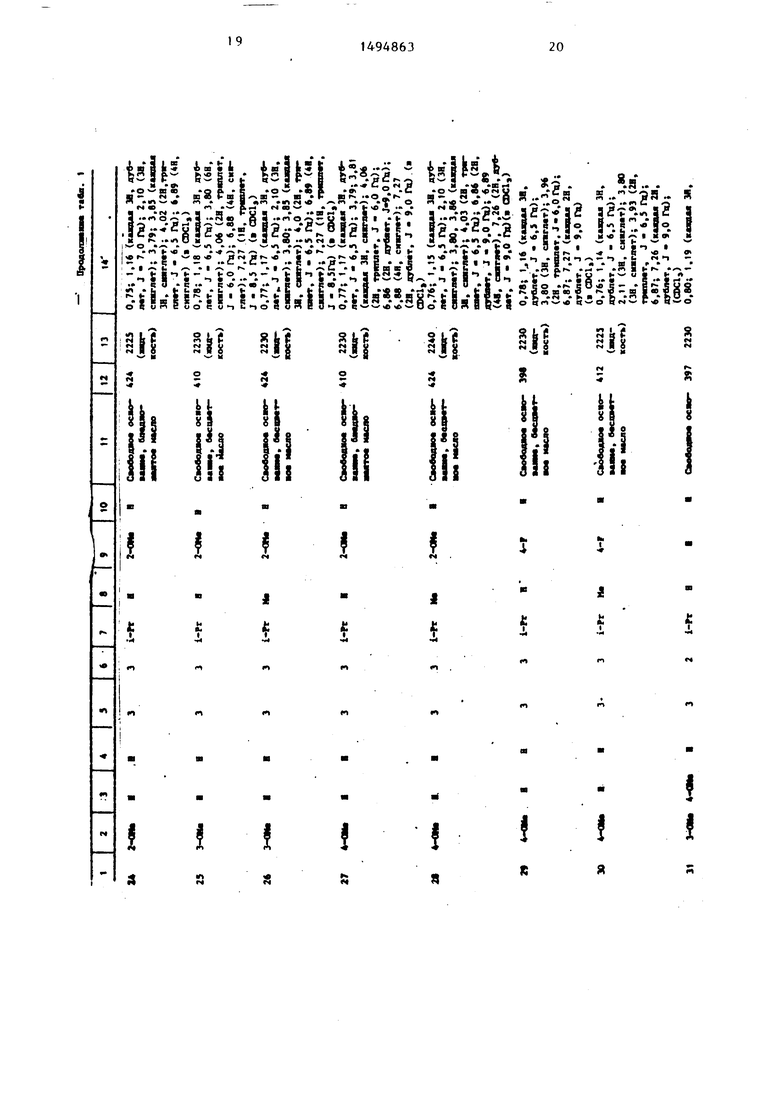
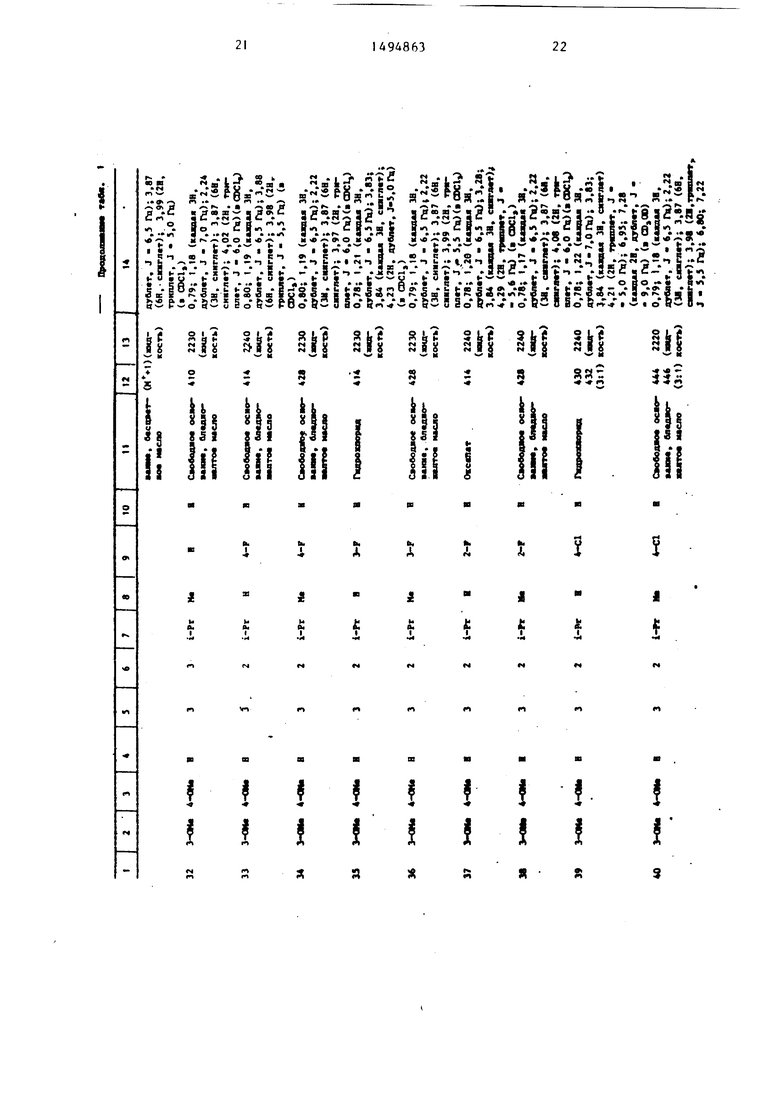
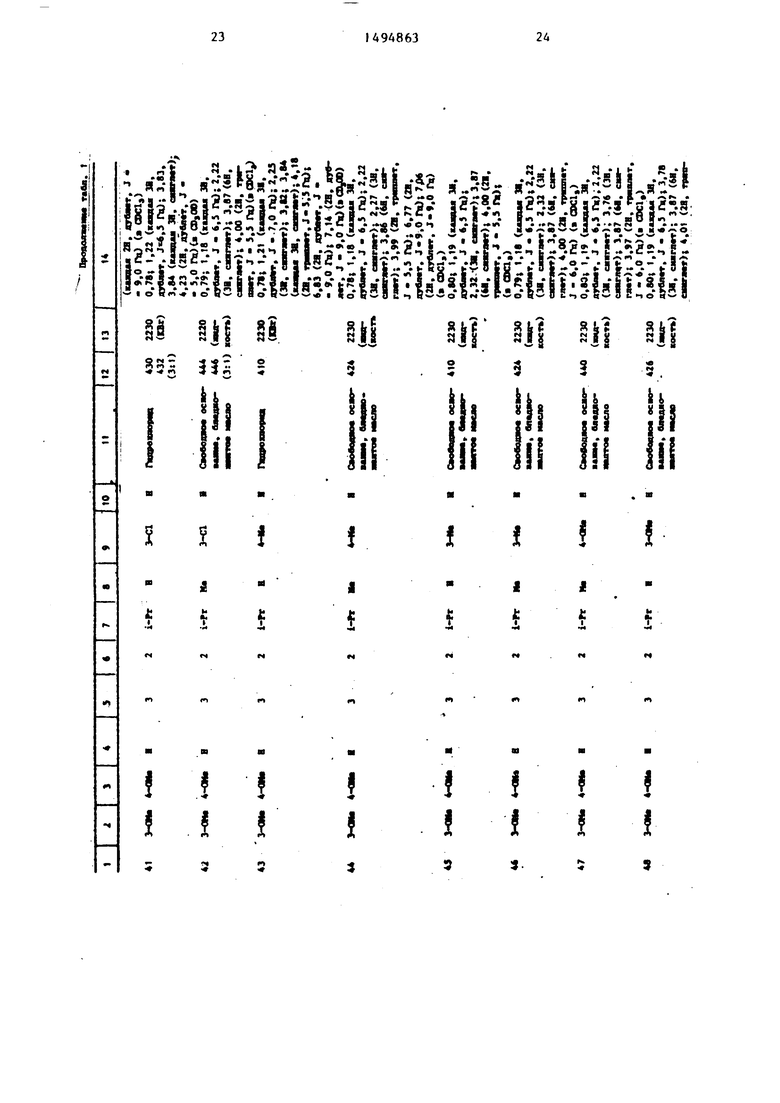
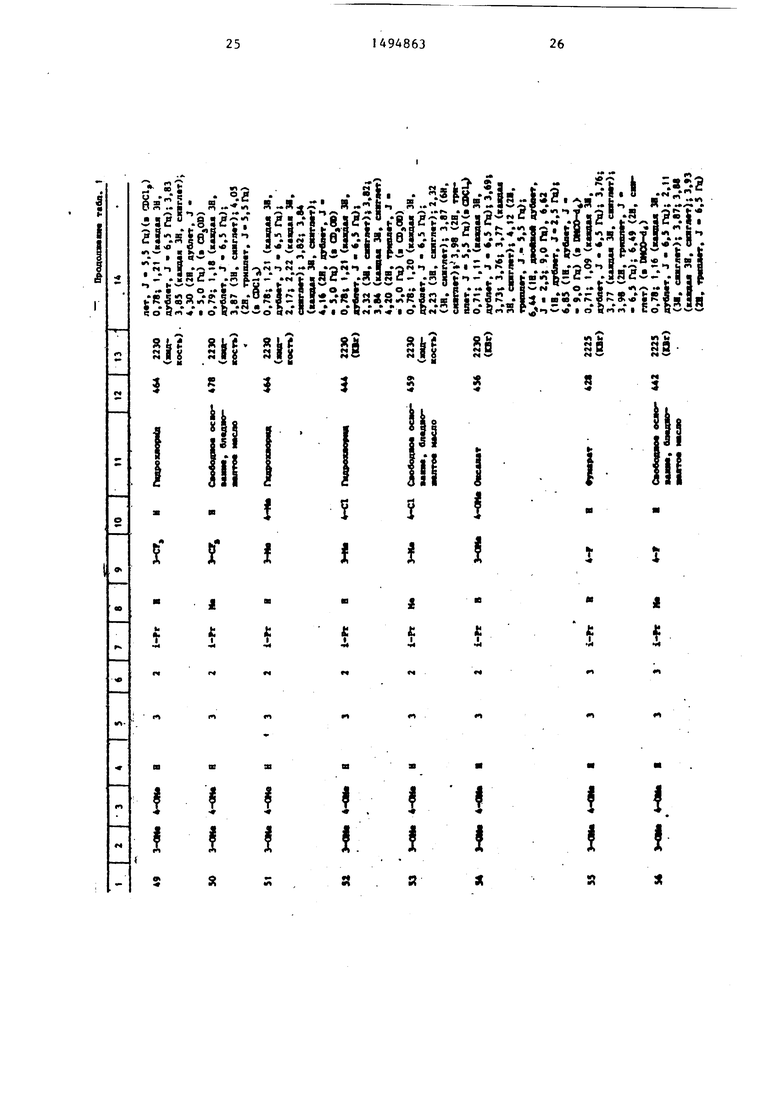
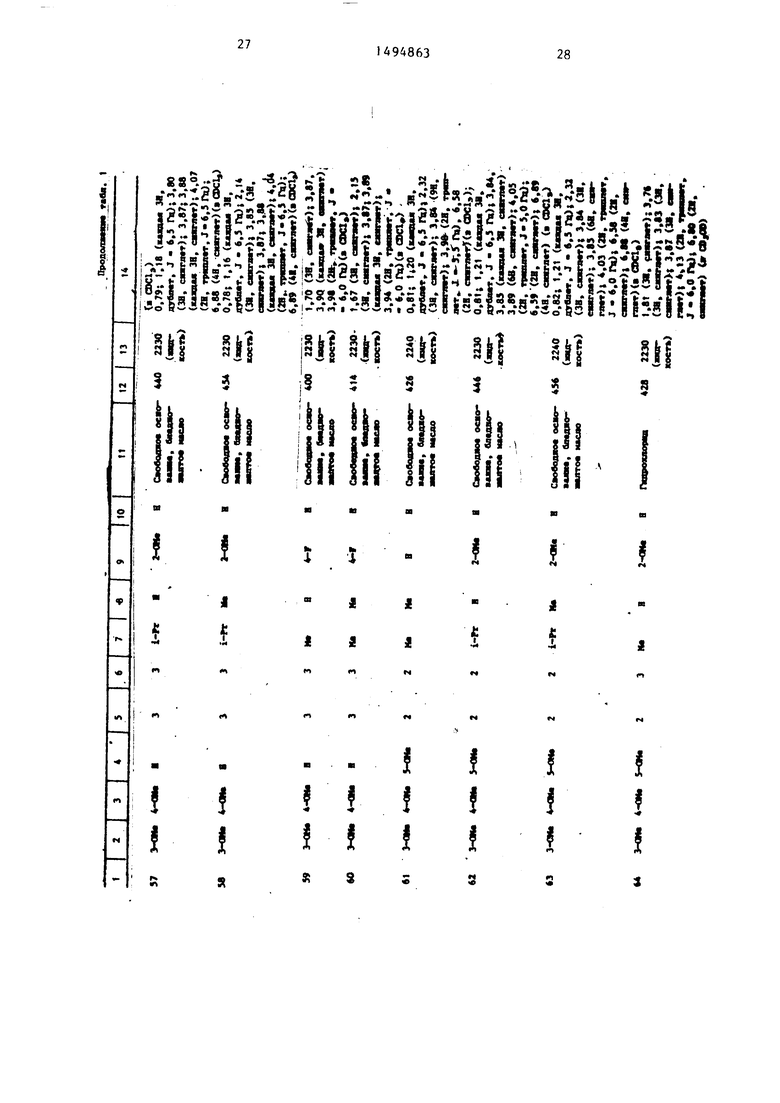
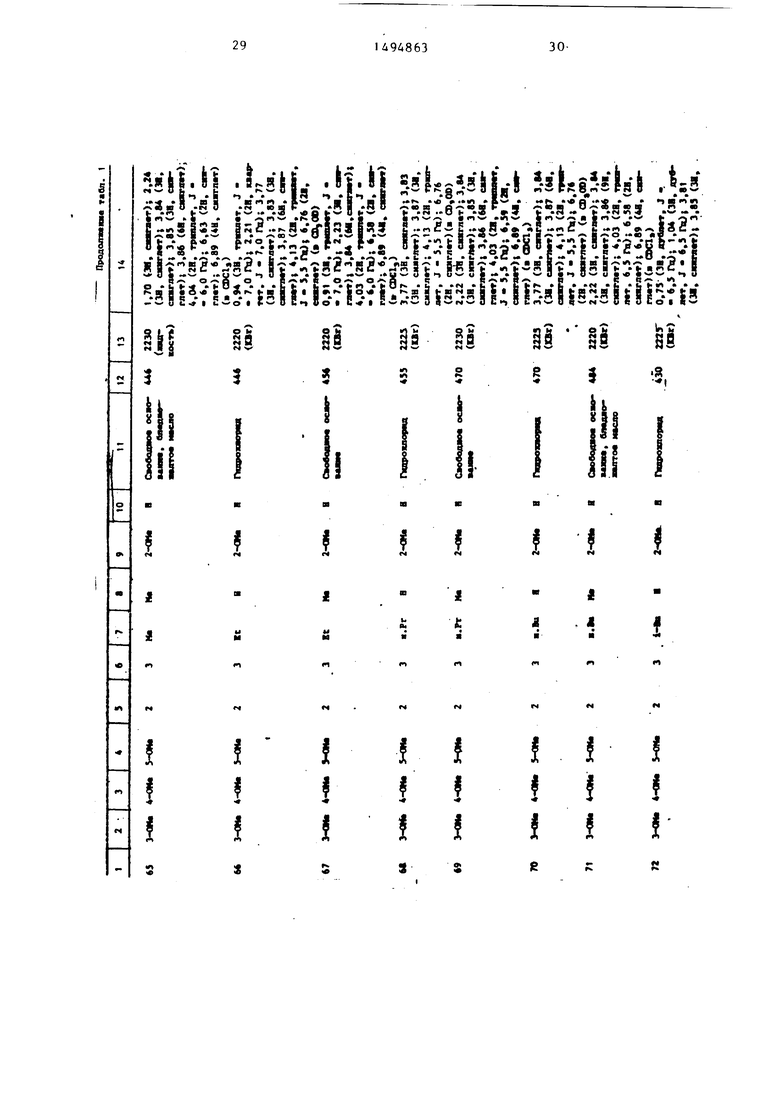
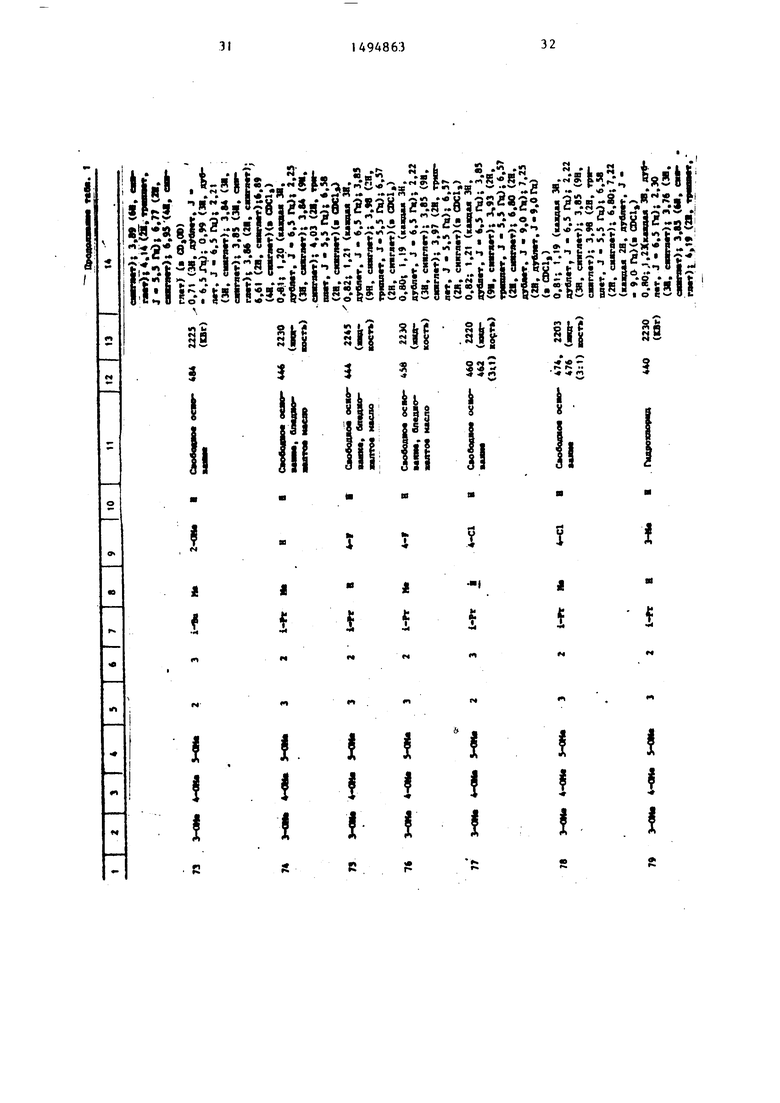
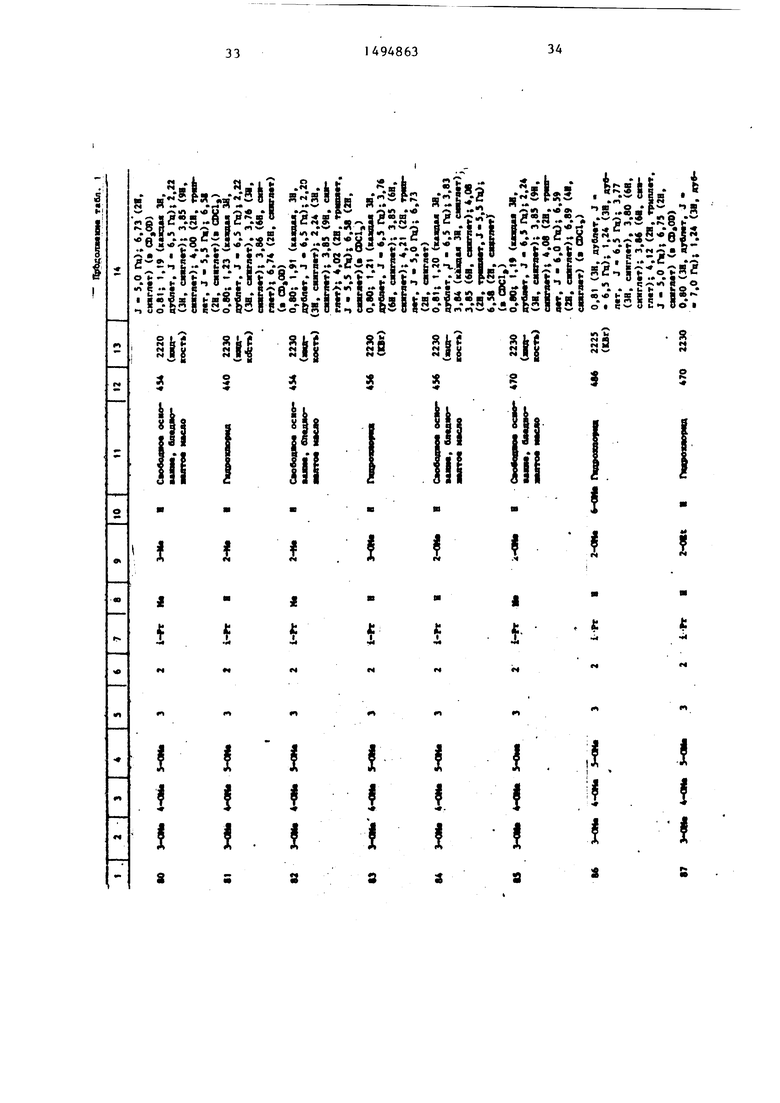
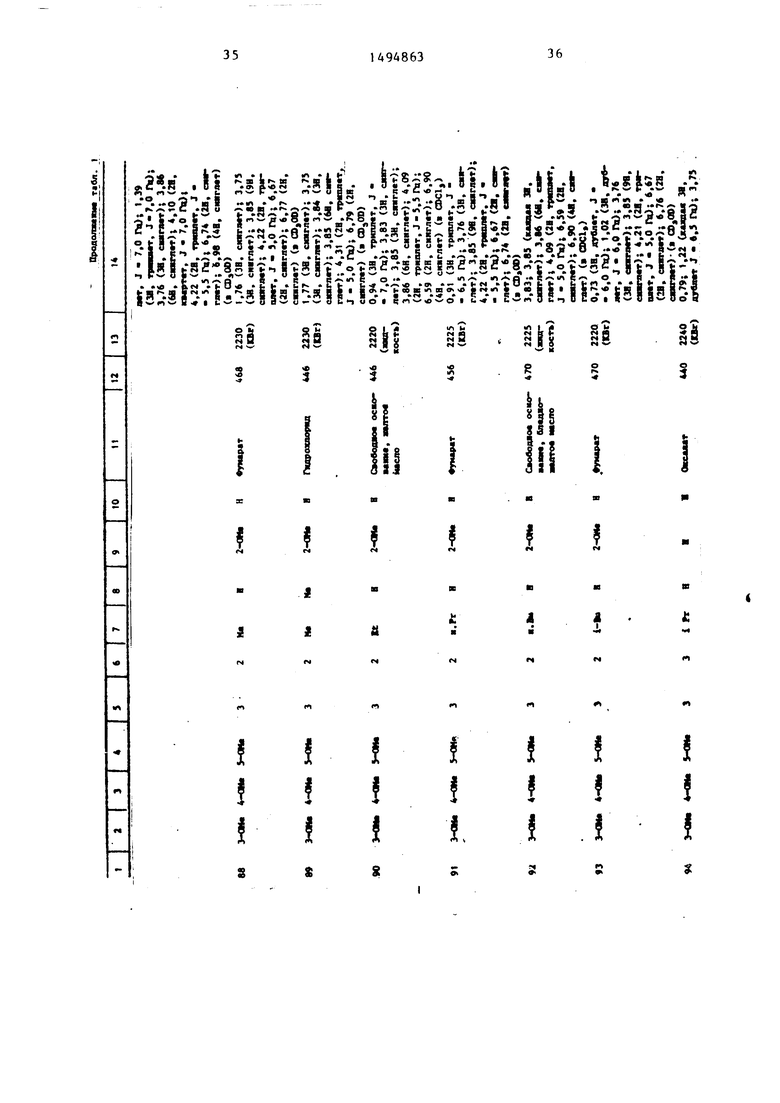
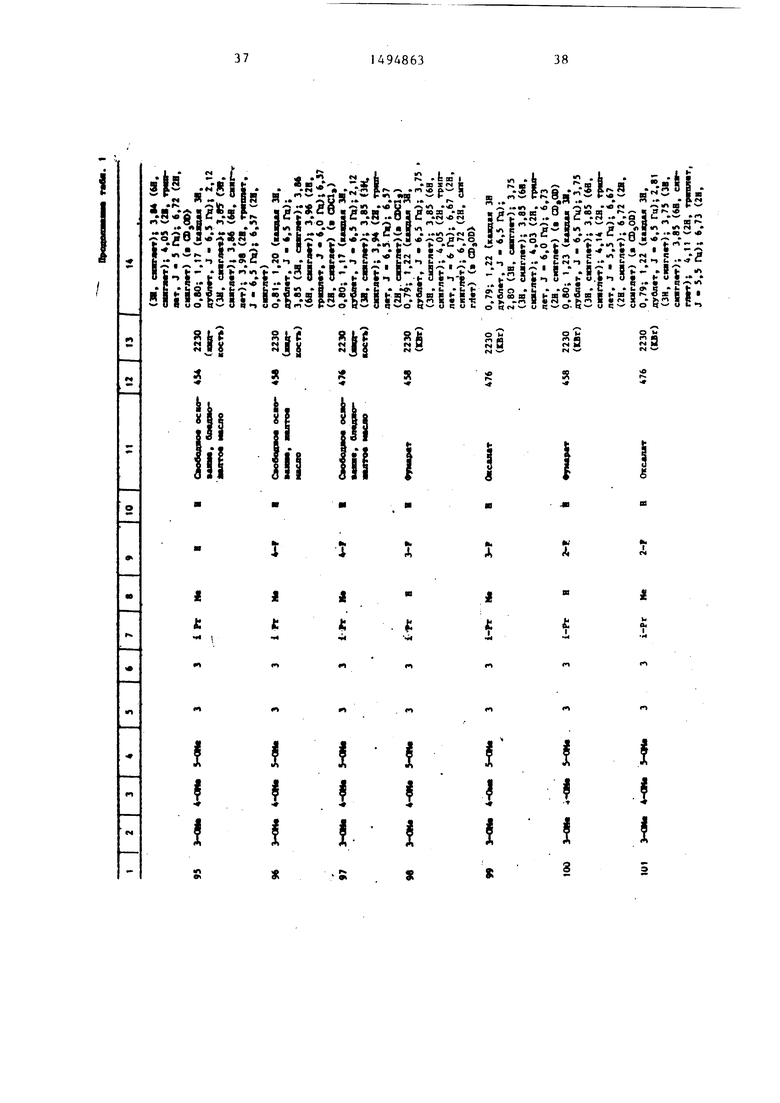
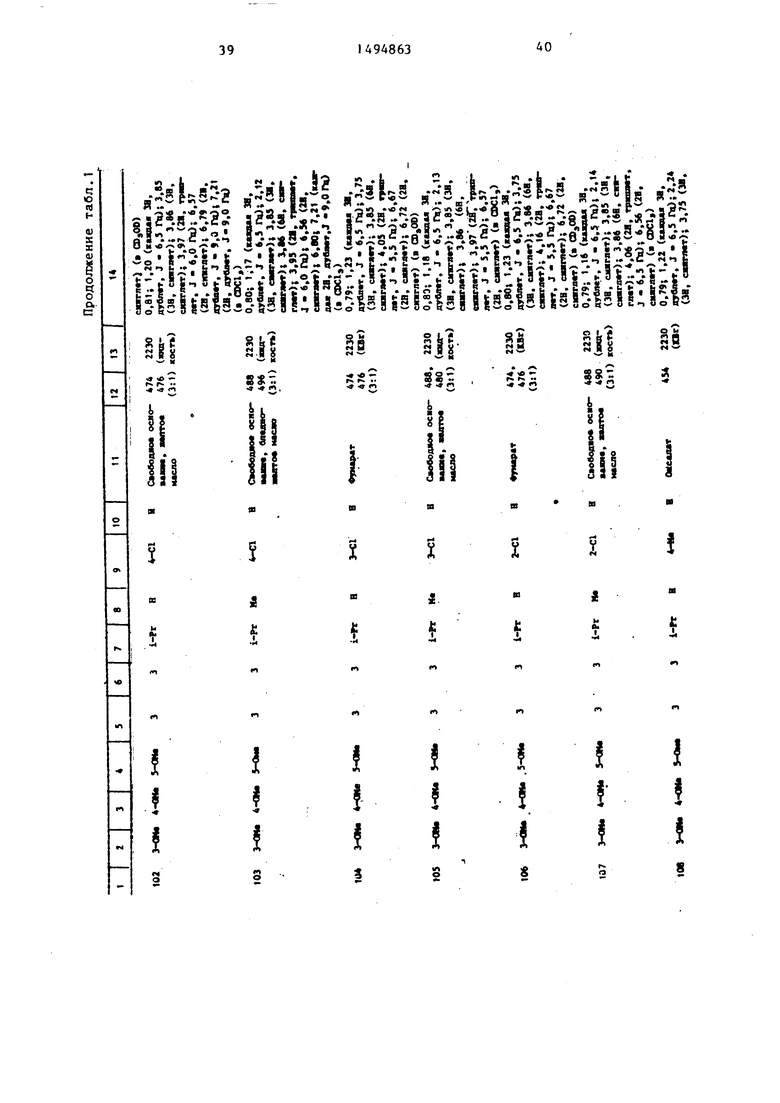
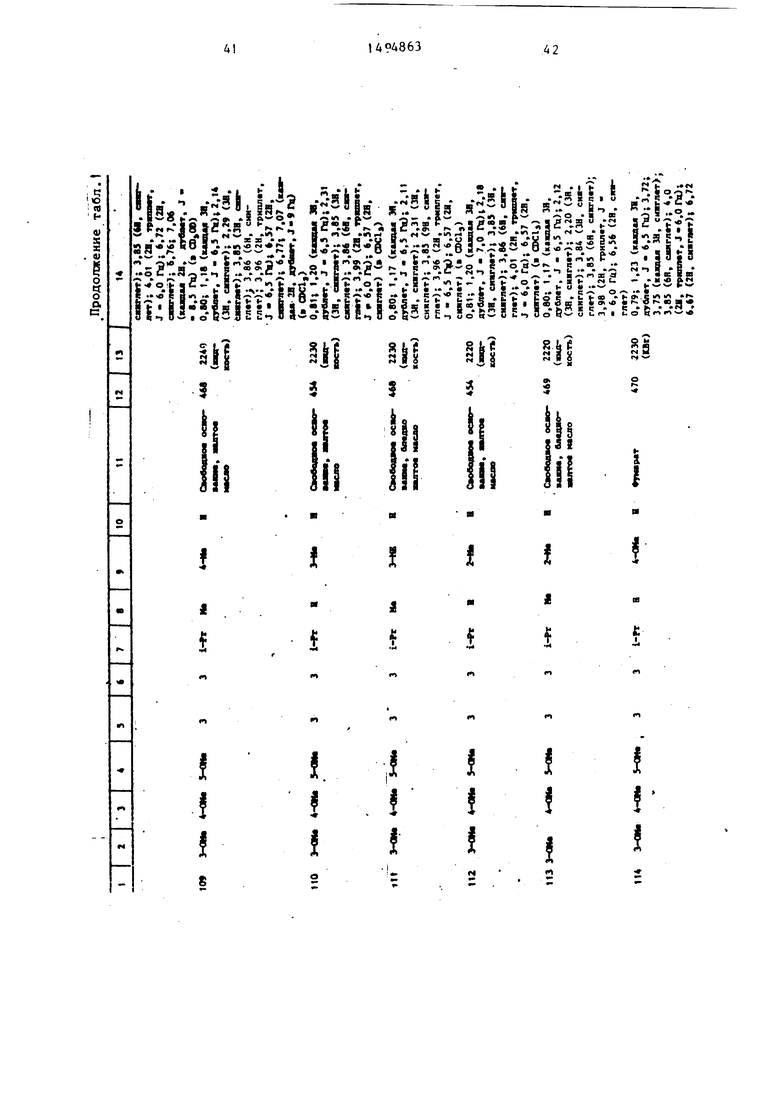
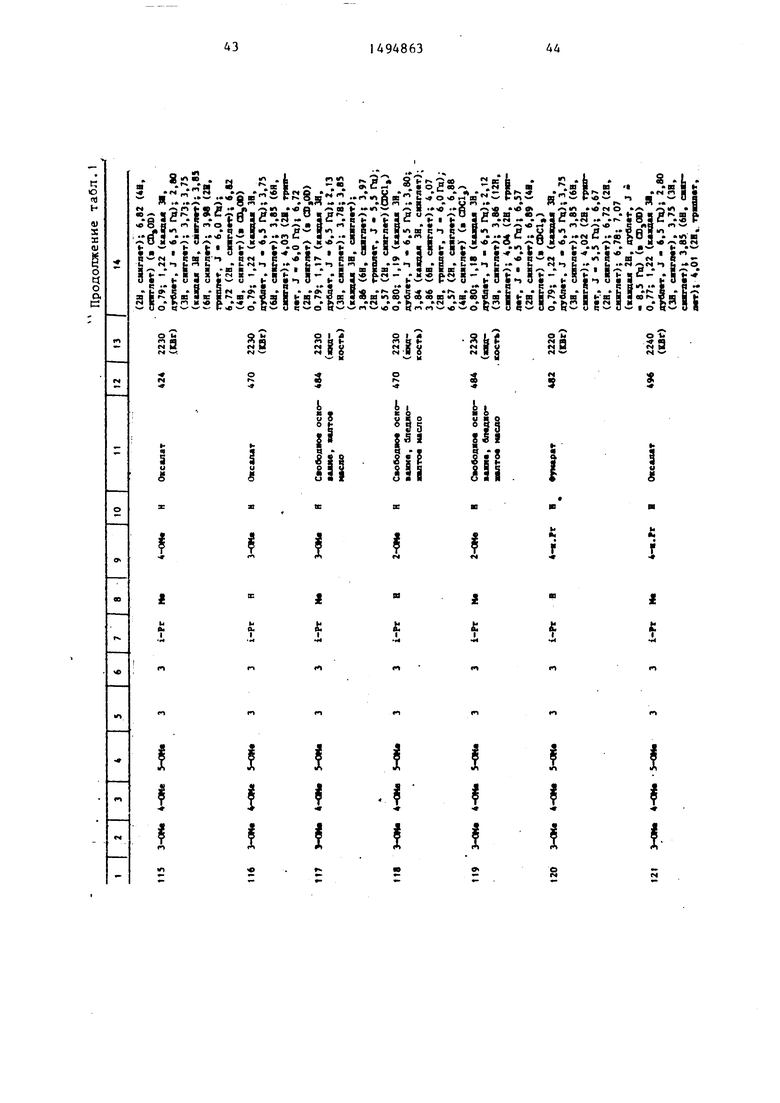
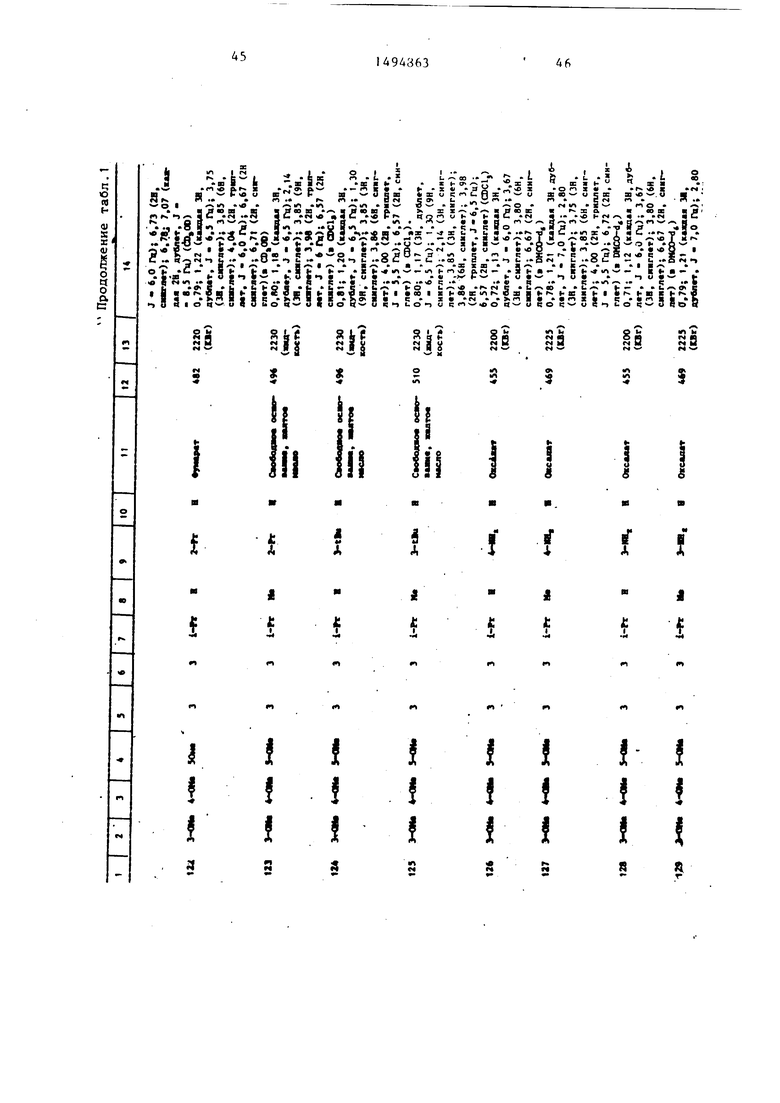
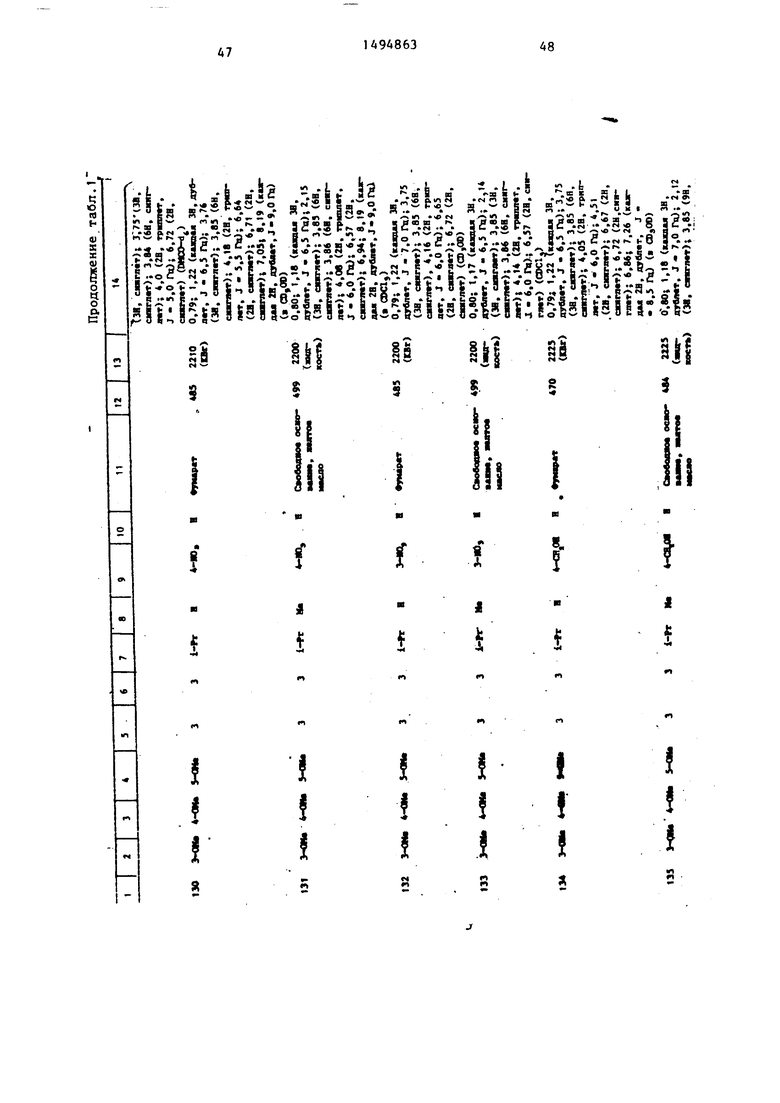
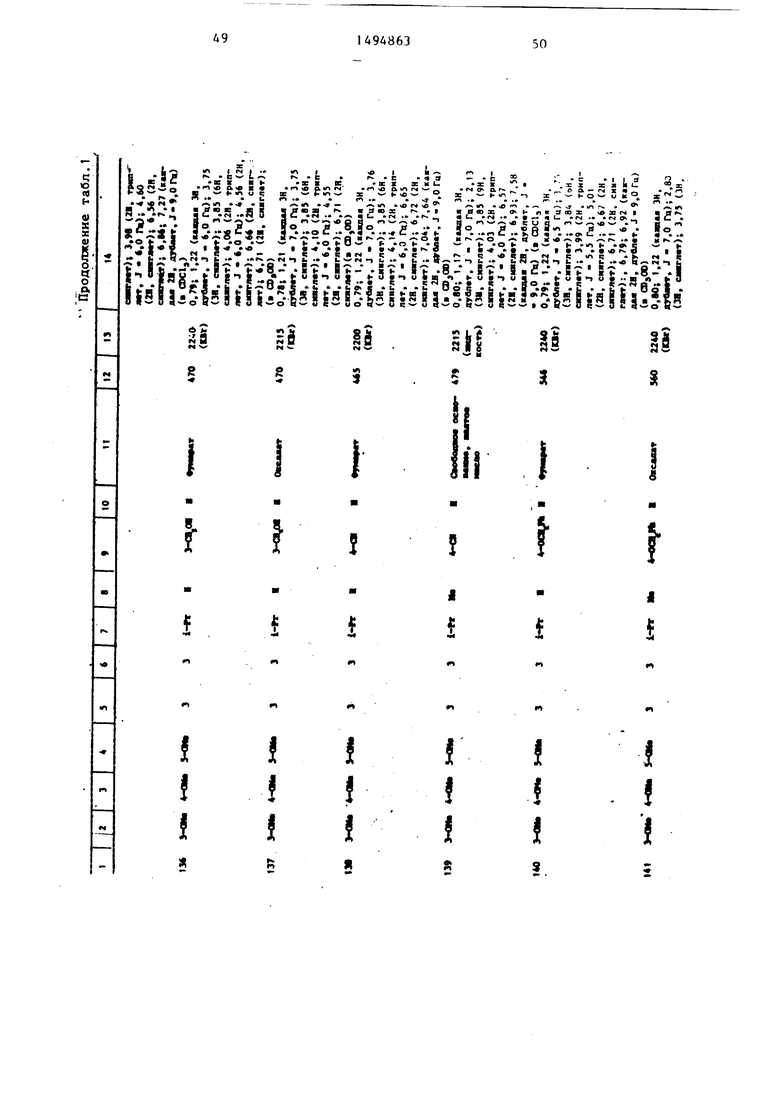
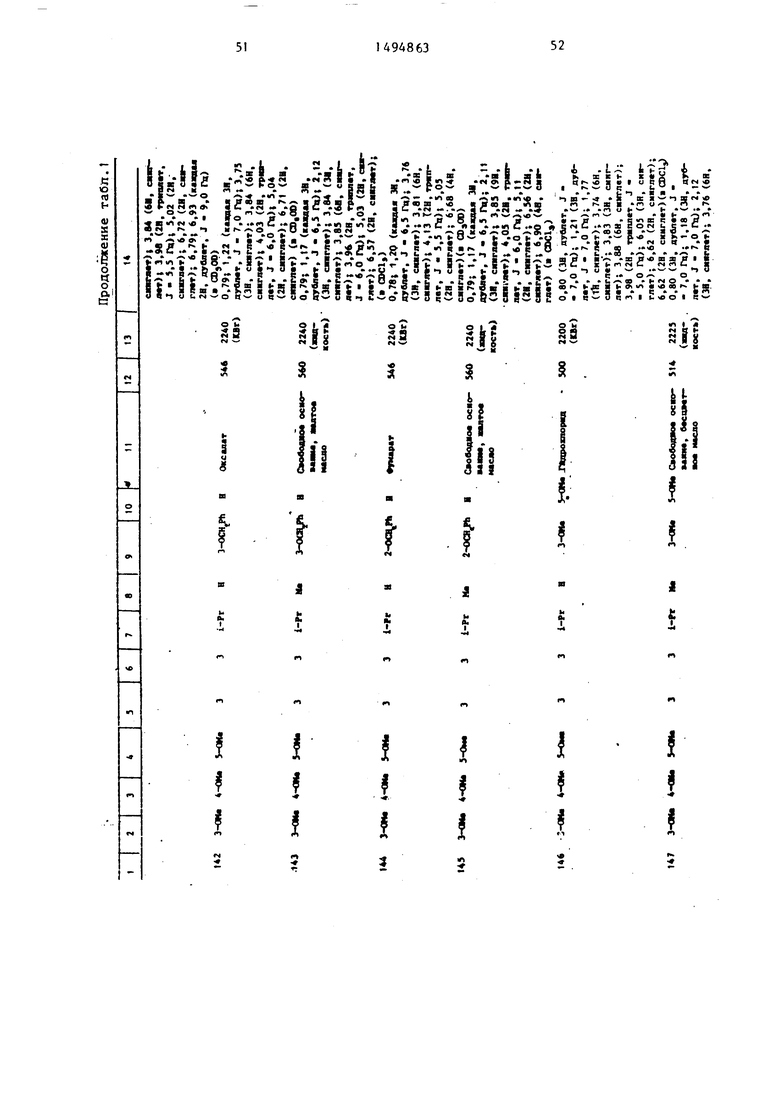
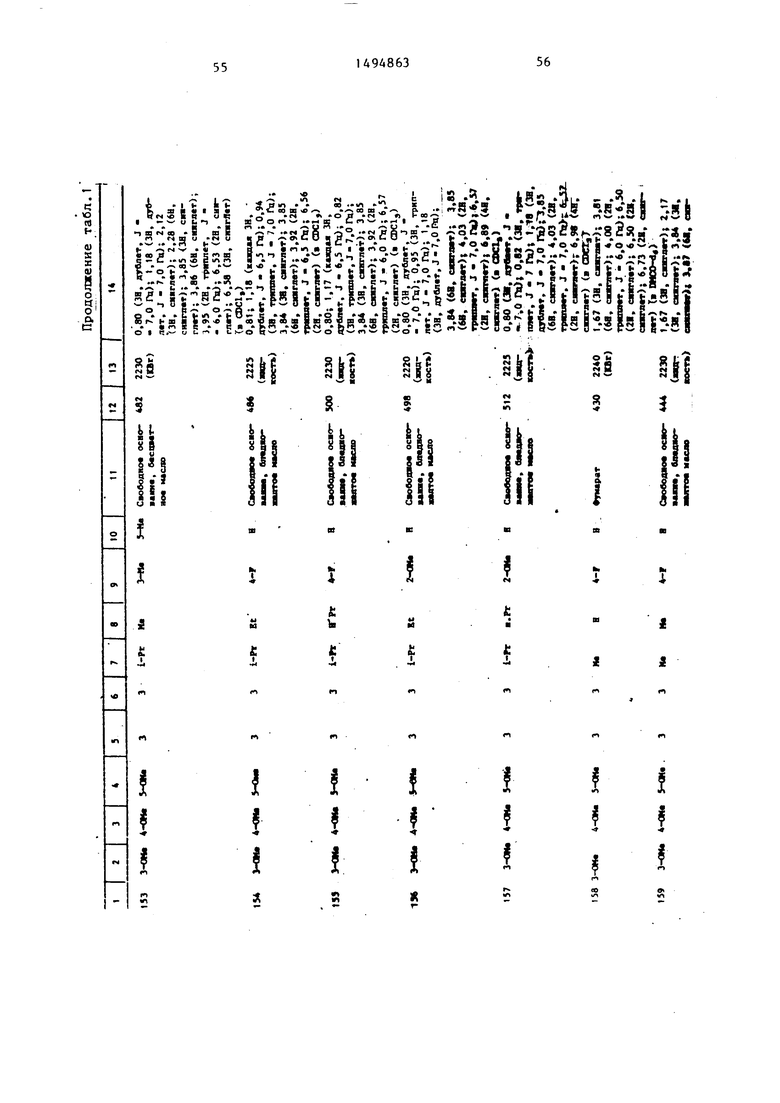
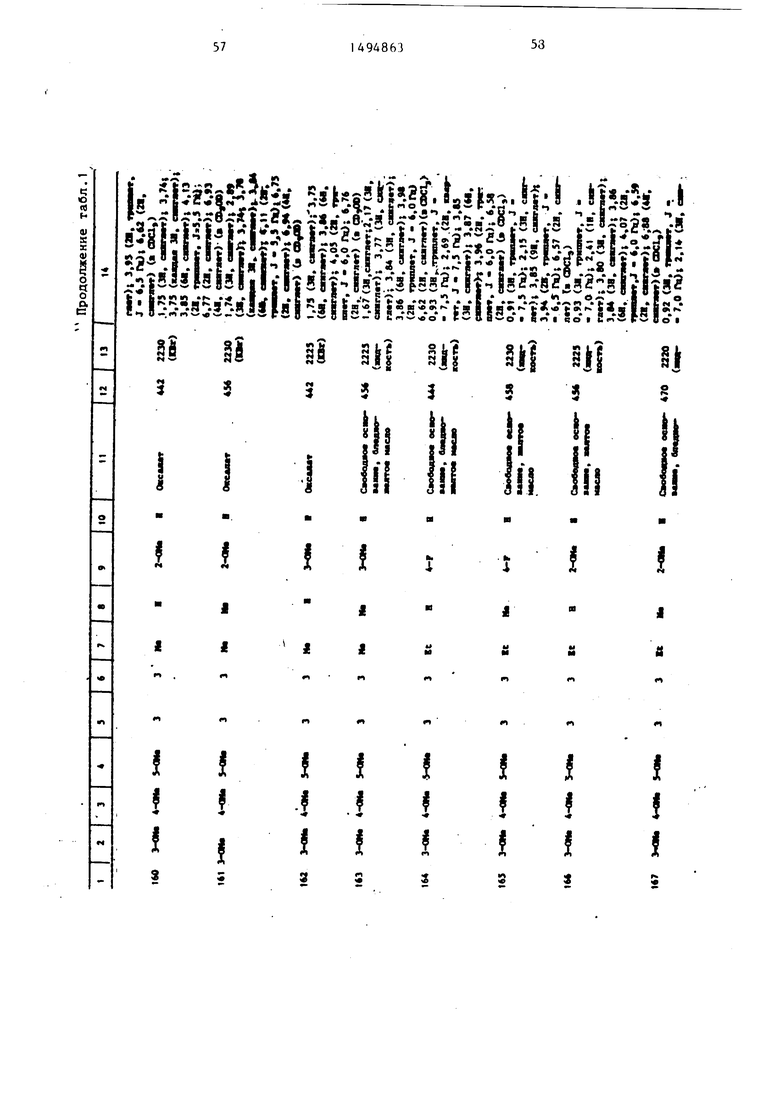
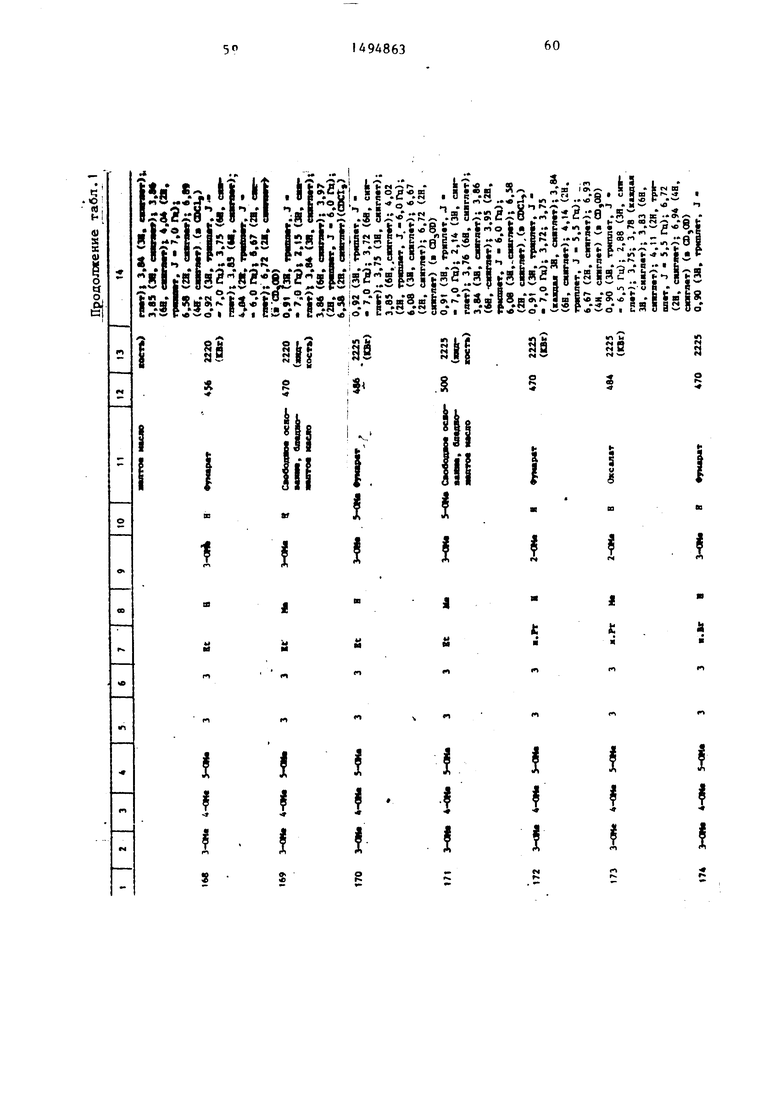
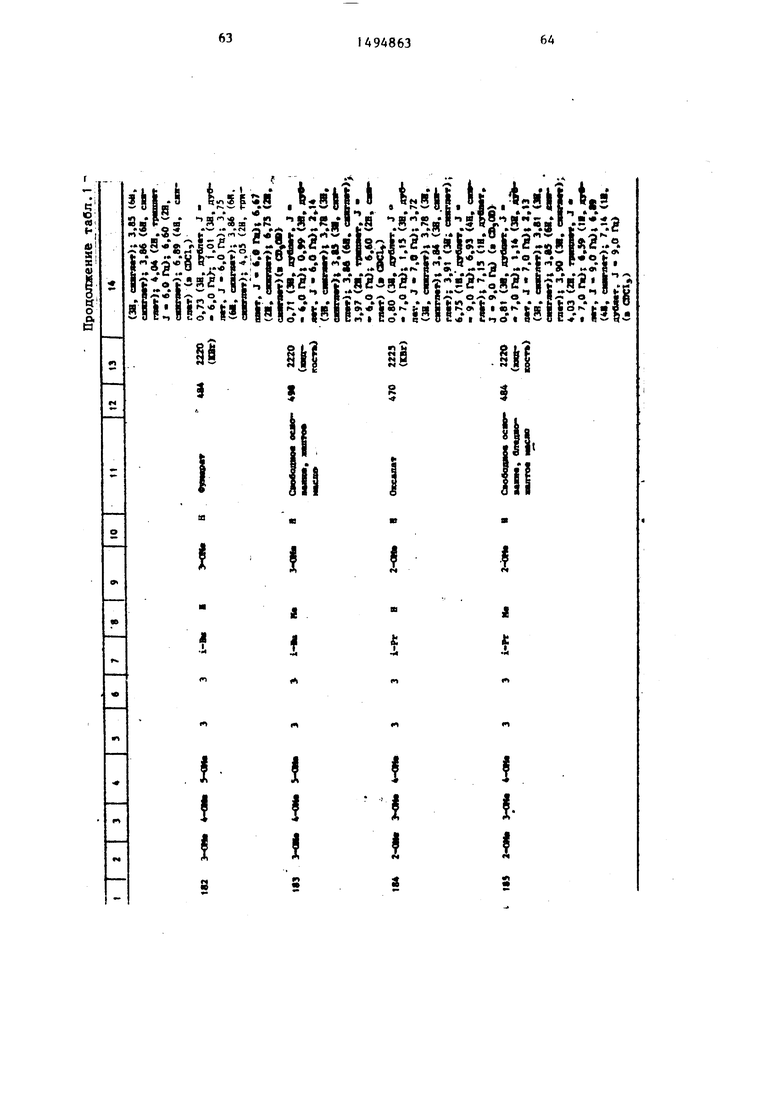
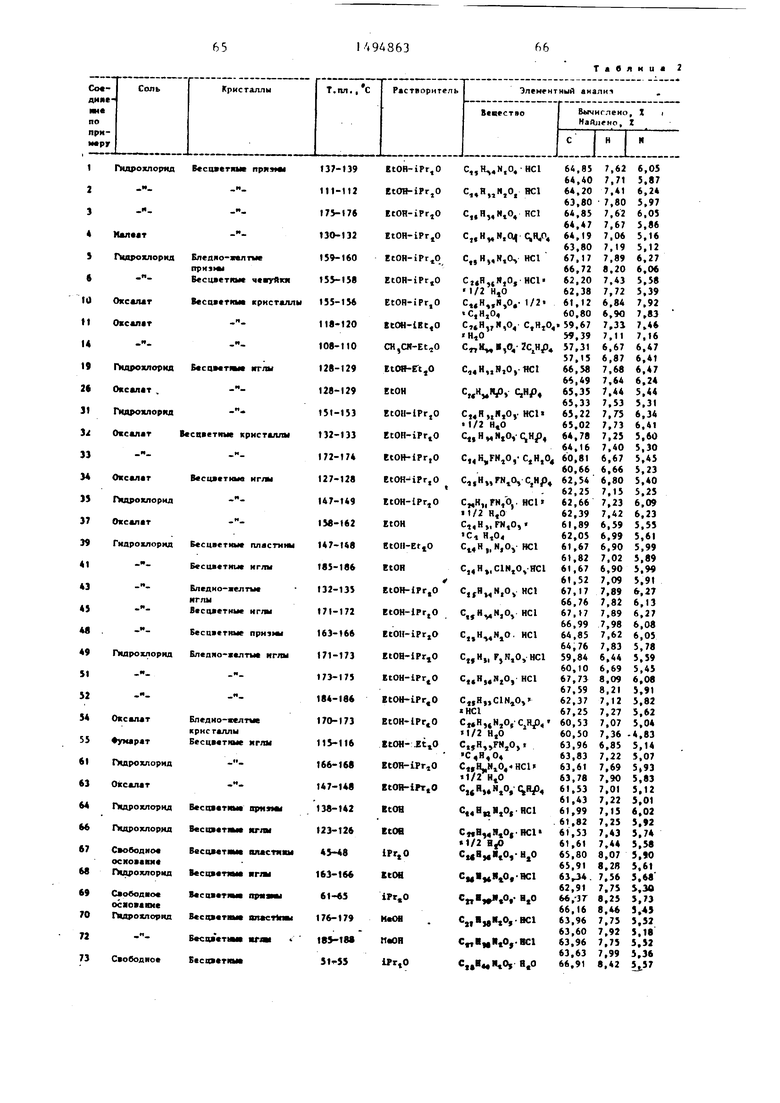
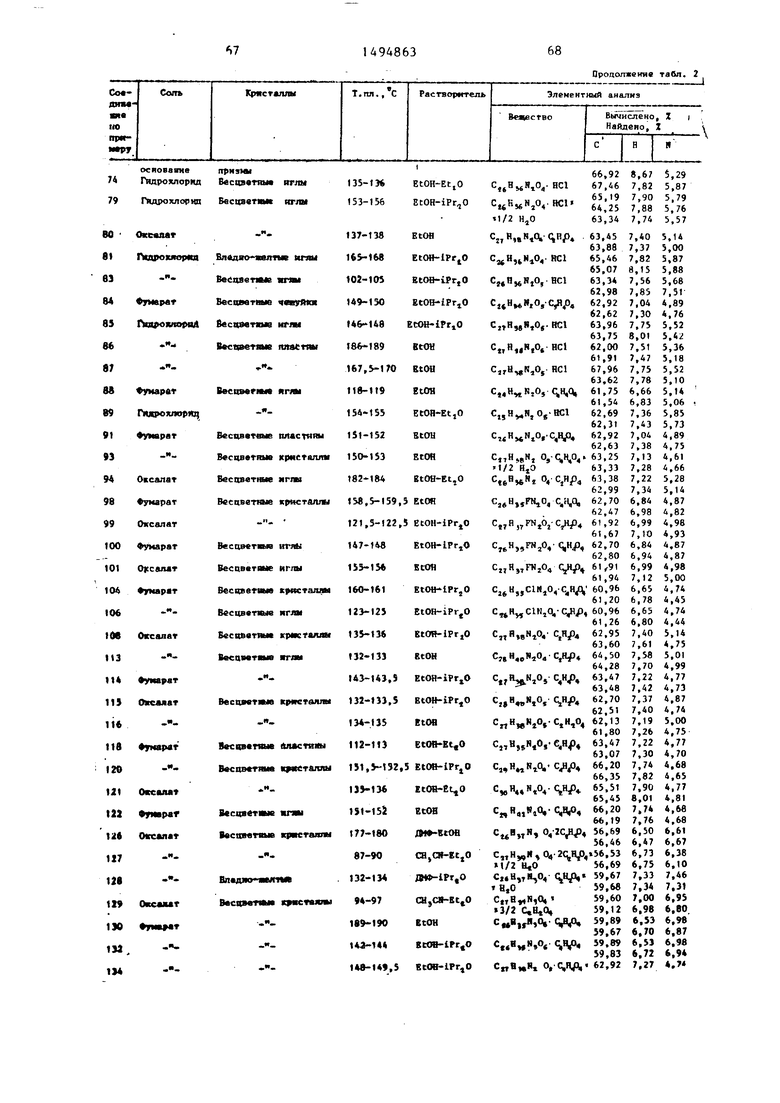
Физические и химические свойства |соединений, полученных в примерах 1- 185, представлены в табл. 1 и 2.
В табл. 1 и 2 приняты следукицие сокращения: Me - метил; Et - этил; Рг - пропил; iPr -изо-пропил; Ви - бутил; i Ви - изо -бутил; tBu -трет- бутил; Ph - фенил; DMF - диметилформ амид.
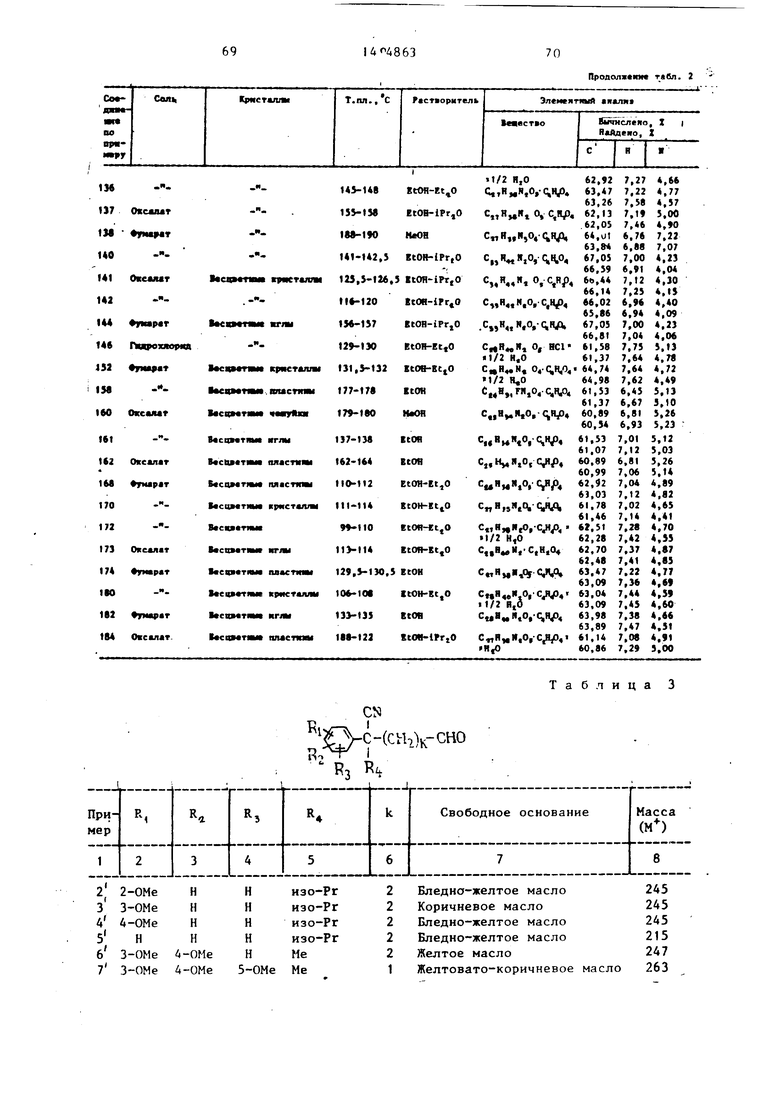
П р и м е р 1 . Иллюстрирует получение исходных соединений формулы II.
3-Циано-З-изопропил-З-(3,4,5-три- метоксифенил)пропионовый альдегид.
5
0
5
0
5
0
5
0
5
К суспензии 4,68 г- амида натрия в 150 мл сухого тетрагидрофурана при перемешивании и охлаждении добавляют 15,00 г о6-изопропил-3,4,5-триметокси- фенилацетонитрила, а затем 11,94 г ди- этилацеталихлорацетальдегида при комнатной температуре, полученную смесь нагревают с обратным холодильником в течение 1,5 ч. После охлаждения к смеси добавляют 40 мл воды и выпаривают растворитель. Остаток растворяют в эфире и полученный раствор промывают водой. Эфирный слой сушат и : выпаривают с образованием 21,99 г о;:- изопропил- /-(/1-диэтоксиэтил)-3,4,5- триметоксифенилацетонитрила в виде бесцветного масла.
Масс-спектр m/z: 365 (М ).
Раствор 21,99 г oC-изolфoпил-c(-(p- диэтoкcиэтил)-3 ,4,5-триметоксифенил- ацетонитрила в 130 мл ацетона и 66 мл 10%-ной водной щавелевой кислоты нагревают в течение 2 ч с обратным холодильником. После охлаждения рН раствора устанавливают равным 6 с помощью насьщ;енного раствора карбоната натрия. Осадок фильтровывают и фильтрат выпаривают. Остаток растворяют в эфире и раствор промывают водой. Эфирный слой сушат и выпаривают с образованием 17,53 г соединения, которое перегоняют с получением бледно- желтого масла, т. кип. 170-172 С/ /6 мм рт.ст.
Масс-спектр m/z: 291 (М ).
Соединения, указанные в примерах 2-16 , получают аналогично примеру 1 и представлены в табл. 3,
Полученные е -аминоалкил -алкил- фенилацетонитрильные производные, а также их фармацевтически приемлемые соли проявляют кальций-антагонистическую активность.
В качестве сравнительных лекарственных средств используют Верапамил и Галлопамил.
Са антагонистическое действие.
У самцов морских свинок Хартли вырезают тяжевую спираль и закрепляют ее в тканевой ванне, содержащей 100 100 rail KCl раствора Лок-Рингера, лишенного ионов Са . К ткани прикладывают силу натяжения, равную 0,5 г. Сжатие, которое вызывается кумулятивным применением СаС, измеряют с помощью изотонического датчика. Раствор, находящийся в тканевой ванне, поддерживают при 37 С и через него барвотируют газовую смесь, содержащую 95% 5% COj. Испытуемые соединения вводят за 30 мин до кумулятивного применения CaCl . Степень тагонистического действия выражают в значениях рА. рА, рассчитывают из зависимости доза - отношения, котору получают как отношение концентраций CaCl, дающих 50% максимальную реак- цию, в присутствии и отсутствии испытуемого соединения.
Получены следуклцие результаты:
Соединение по примеруpAi
138,11
148,15 808,52 95 8,19
978,02
998,29
1058,14
1118,48
1138,31
1198,05
1298,13
1338,17
1638,17
1658,03
1698,85
1758,56
1798,36
1838,30
Верапамил7,59
Галлопамил8,56
Антиаритмическое действие (индуцированная аконитином аритмия у мышей)
Самцов мьшей разновидности массой около 30 г анестезируют пентабарбита лом натрия, который вводят внутрибрю шинно. Аконитин (1,32 |Цг/мин) непре- рьюно вливают в хвостовую вену через 15 мин после применения пентобарби- турата натрия. Стандартную электрокардиограмму на свинцовых дисках регистрировали на катодно-лучевом ос- циллограффе и наблюдают внешний вид экстрасистол желудочков.
Количество аконитина, необходимое для индуцирования аритмии, рассчитывают из времени, требуемого для начала первых экстрасистол желудочков. Испытуемые соединения (100 мг/кг) применяют орально за 60 мин до вливания аконитина. Их относительные мощности по отношению к хинидину сравнивают п процентному количеству увеличения
5
0
5
0
5
5
0
5
аконитина, требуемого для индуцирования аритмии.
Получены следующие результаты: Соединение по Относительная примеру мощность (хинидин 1)
32,01
62,02
111,51
192,28
201,20
252,34
261,60
271,43
571,52
581,64
842,52
853,72 881,34
1182,65
1192,24 1221,21 1261,03 1282,01
Дизопирамид0,97
Верапамил-0,02
Галлопамил 0,30 oL, -Рецепторноё блокирующее действие.
У самцов кроликов удаляют тракаль- ную аорту и разрезают ее по спирали. Спиральные полоски помещают в тканевую ванну, содержащую раствор Кребса- Хенселейта при 37° С. К ткани прикладывают силу растяжения, равную 2,0 г, Изменение натяжений, .которое индуцируют кумулятивным применением норад- реналина, изометрически измеряют с помощью FD-датчика. Через раствор в тканевой ванне барботируют смесь, состоящую из 95% 0 и 5% СОд. Испытуемые соединения применяют за 30 мин перед кумулятивным введением норадре- налина. Степень о 1-блокирующего действия выражают значениями рА.
Значения рА рассчитывают как от- . ношение концентраций норадреналина дающих 50% максимальную реакцию, в присутствии и отсутствии испытуемого соединения.
Получены следукмцие результаты: Соединение по Значение рЛ примеру
48,25
218,02
848,42
888,40
908,79
n
8,46 8,57 8,67 6,41 6,11
Острая токсичность у мьшш. Используют мышей мужского пола в возрасте пяти недель массой 19-25,5 г. Мышей помещают в клетки с основанием из ме- 10 таллической проволоки и закрьшают на всю ночь. Соединения примеров 6 и 113 и Верпамил как сравнительное соединение растворяют в дистиллированной
6
97 113 165
Верапамил Результаты опыта показывают превосходство предлагаемых соединений
(введение через рот) 208,9 262,5 303,9 510,2 163,0
по сравнению с известным с точки зреводе и дают 5-10 группам из 5-10 жи- 15 ния токсичности.
вотных. Соединения примеров 97 и 165 Таким образом, полученные согласно предлагаемого способа соединения имеют более высокую активность и меньшую токсичнЪсть.
суспендируют в 20% макрогола и дают 6-8 группам из 5-10 животных. Каждый образец дают через рот катетером, который имеет объем 0,2-0,4 мл/10 г мае- 20 массы тела, затем животные находятся Формула под наблюдением в течение 7 дней. Одноразовую дозу при оральном назначении вычисляют методом Пробита,
изобретения
основанным на смертности на 7-й день
Способ получения о -аминоалкил-в6- алкилфенилацетонитрильных производных 25 общей формулы I
CN
I
,-N-.:cH,,, RJ к.; R R-где каждый из радикалов R, Rj, Rj может иметь одинаковые или различные значения и представляет собой водород или низшую алкоксигруппу; R - низший алкил нормального или
разветвленного строения; Ry - водород или низший алкил; R и R каящый может иметь одинаковые
или различные значения и представляет собой водород, галоген, низший алкил, низшую алкокси-, нитро-, аминогруппу, гидроксинизшую алкильную группу;
тип- целые числа, выбранные из значений равных 2 и 3,
или их кислотно-аддитивных фармацевтически приемлемых солей, отличающийся тем, что альдегидное производное общей формулы II
CN
с-гсн,)к-сно
R. RU
А863 . 2
Данные по токсичности представлены ниже:
Соединение по примеру
Щ, мг/кг
10
6
97 113 165
Верапамил Результаты опыта показывают превосходство предлагаемых соединений
(введение через рот) 208,9 262,5 303,9 510,2 163,0
шую токсичнЪсть.
Формула
изобретения
0 Формула
Способ получения о -аминоалкил-в6- алкилфенилацетонитрильных производных 25 общей формулы I
где RI, R, R каждый имеет указанные значения:
К - равно 1 или 2,
подвергают взаимодействию с производным амина общей формулы III
40
HN-(CH2)n-045 I
где Ry, Rg, R, n, имеют указанные значения,
в присутствии органического растворителя с последующей обработкой вос5Q станавливающим aгeнтo J и выделением полученного продукта в свободном виде или кислотно-аддитивной фармацевтически приемлемой соли или соединение формулы I при R - водород при необ55 ходимости алкилируют, или при R -. нитрогруппа при необходимости восстанавливают в аминогруппу.
.. . |ь Ь. i-Lt tcLb --Lt S Д -L
.5 |й . g . g S l S2 --.Ir, 9 I .0 fi § .rCS И . .ЯЯ в
Ч -з-в- a я .. i ;s. | ;s..« |R я«trf « tJK шВr-i a
aPug taPu ammf «
J «N flt- te
Hirtf - tfHI V Dcl -4 UFt mN ГчVfttms
ВCf Seinm Rrr т 9 я
«uoiЯ(..гчгч|||Эиг ч я г«Я|е
к в« О1П1|«вя х-- к ininx-чк
v t rf n
ГЧШIWh Ю«r me ШЩл«(nr-lr-s|« Л1Ч Ч| « Ч
Ф 9 - 0 с -ii« п
..х-ч.ММ.. ...C |,
)1 т г- -в§-.
«а(мС 4 - ( m ь ш- -KI ш «.CBl
.- .. U -)« .u
в«. 1 г;.-.1П.« ). tfn-.tn - т в
Оё «иь «о gt- о (. - R t |-в .
ьЯ в g..-. g в.S 5 §я.t а I 46 в g «is а g 1-.я в
oQ oBoqn ib ot ua oriQcinOQoC oS Ub -tCei- O
S fc 5bS
ajg.й|§ Я|§ й|8 Я|8Я|§.
h
I I
Г 4
3s
5
ь е «
95 St
f f
I
II f
i--
n
V «v - - j V - «i « « U о ft
« М Э lA P«х Й 9 4 Cl««nw B«fomP,........2 Я - ..,.--- Е--.2°2«..:г.я-..« . s- ..л-. o-- вт рА- .1 - -p -j- -p- o- -
О tfwe 9 ф «««и «ч ««s.-
л«.. 85 -«и ..5л«5..5 « -5 в й-е-«
ь ei Cht tftfi btff M h «-«Cl btft Cf O bl -(DtfiftlIt W b t
.i9(Bs J tBi i tB8 B tsBi s tiS B. tB i S nei689ioSC8Enlol8 bEoS9g.8o|C8S go iBS s o 88EVot8.s
т
- Ы
S
i
о
a
I
и
h
I
f
I
г
8k i° b
я|§ я1|
s:
11
I
i
i
SA
s
11
2
f
n i
f
л
1 J
f
(kt
h
Ц
«
3b«
-Is
яЗ
I
if 11
I
i
It
2
I
I
I
SRt as:: 2я
-с 5 с 5J
S f
I
f
о
4Г
3
f
I I I
I f
8 ОаР bOti F .хч. - и п fUBiu §. -.х. t
.:|я1вЧ«Ь1 B4;w5s,J :-|Lj .я|«яМ|я|| i|s,-s t;
i7o B«-; :}r oBs3oJiCi l - 4 I I о ц--- О (.-, О С En
Rbe aj§
3
ill ii
f
r
§
II
i
i f
I I
I f
ft 3
SkC «l§
A
s
2 2
I
f
N
:
I I
I I
f
f
f I
ANN
I
t
f I I
. Г I I
in и
39 J
S
S t Sb Sb :$И t i
v и M« ;
I
2
t,
I I
i . I
SfcC
«l§
Sfe
4 R
« u
N 2
14 в
M
S
s ;::
4
П
I I
Ы
i
{:
I
f
I I , ;i
i I i
I ««цh I I I
1Л fet V4 ftf% |f- «o I D«I
У it т r.B||SlO - h it { kк
iCe io« a-niSS Oe 48 -n
n i;«C«i-i u fa|дОВв)и( (Г.ч щ т
I «О о « i С .- у i-i В п Я нЯ -а Я
- . .«о а щ т« гх .« ш -« -а ш Я Я п п« е
«Я и«N« «1 хч2 Р «п 8 «Я 3«Ч Я аш.
A-iSVot. |гг5с -§5„-5 .885-8 7 s.t-.t-. I .и 5 ,: ;:«5о -8 §2 2 e-..-|s5 2..a..fl 5..s«R is E- l issisa gsS o ;8gfi -..n«|
°t4 t I 1 Р....° |.п-55н8 1« |- 5- - 3| -o7t°.C°5«,ie P e o«-«m« u n -o i-o«u« - mP «ПА -««вВ «lAhii
f a p « S g 44 Б « e ч -co Д « S и О .«« I I
I « -ч Ь «Ьо-С «0 D«( Е «|Е-Г4
IBB Ч.О ООШВ Х smjf шЕовв9атшв ла ILnBl-NC о Г1- чЩ|-тВ. о 1пСт«асчЕтС мС опь Я(
1 N о - W9Oe UV - v l s O 1 ««ч 4V9 OV Ь
ь Rе. |Г ча е х1ле« Ои
охв «(LfM (и« (р St о - «i-M иьитьь цьм Cti Сле 8 иЯ 1:вЕвч1 - 9|i Ц|| ЛВе«чВ пВц В q« На
с - -oS - u - u 3m3SnuEot4- Q8 oo8
Q
я5
«
f f
I I I f 1 .
s
s
1Л b N Й
M a
|Л I (Ie b
N H (Г4
N к uCM в
J g
go ГЧ Л«
Ib
i§ I
f
f
f
( 8k SE
-IS «Is «Is йё
I
sli
11 ll
I I
i:
I
I I I Г r I
.
I I- I I I
I
X
s
D
°9
N S
Sb n
N 3 14
Й
«
r
. f
s
ю nj н
0)
s
X
ш
et
8 tl Я1§
lf|,
-&
1
gg
«« -
r« r- .
- n
J
b
I3
i яЭ
4
« - г r
f « n
i: «l§
/-Ч
887
3 -« «
§Q
X
M
i
I J
8
8
се Н
ш
а;
. V
о
т
I
I
{
I
I
CJt «
52:-
З-гЯЕ-
-:и$5
1
8Ь1
Я 38
.С 1Л 1Л «г
к в г- а е к ьч «Ы Е о Б« «
i
IS |9
5
8li
bi
J
Ob
I
I
I
j
I
ю fl н
и
S X OJ
о ц о р.
с
1 г-Ь и вТЬ . г.Ь .§,.
- ...1ваш Кг вш - т п&ае С40« tn ш «ч
П f о f ЙО «А Оп Ш«Ufn М «rvп я
N t t- 9 л J - ««и хчоа|- т - В б 4 «ot m ««по xs
о ai b 9 tfa ш л н о л О « и 5 ш « васот i 1-дк(ш&
оЯС «g Luic. «ы iC. «rii-lf-K I ll iC «oK
«on mCnoi H .H ПЦВ «e & с мЭ n .
jtBin В .цяВт j - в ij5 - i5a Amt i5 a fl уя /
щ «Ч).Я rtC Я цЯ «ть С Я ««чСк охиЯ . т - ы f « Kie-NUB iuvo r«tt
h till--- -о vx I, Hi. 1 s В h В - 4fl fc Ь и e- i« u« « Яо«и« -«« I n
r«t; 4 цг e «61 SB 5 i g re к q mS в (мб Ь n ll.nt,.(,. (.- 4bin«d - I. (, -ON /-ЧГ4 1-1 Ь О
в ааш 1вЕп «вВавя я - 1Я Е |В
16- I s S tcj g-,г8 sA i-,:132 Ь-,-JS ISS и-S бД 3 s-. 8 jjA I s S-
l; Miieц n «t3 «vQцй|Л )
«LOSE «BN «tfsB , 0 ОчЦ IC «r «ОС «h ЦО k hll h
3Ei «Ш MB Бг-вг-оа в авштсовебооштвобвв i l-Bi В KB В В i. к oFiinH b ьЗВ Я р|гпи «IS «h «N « «fcmlBNB - Do F«-- o 3 0 5 oo B о к- i о B о ц
g
Ы
О I л
S
h
о Ё
и
S
8
a. I
.f
I
ь«
ч я
а
И- I.-8
III
о W
яЭ
5
о
$
2
ь
I
е;о ш н
а
X
и
о ч о
«
(k1 iSg Rg
яйх я8§ ЯЯ8 я5 яЗя5 я5
«5 а - В--к
«о1Ло
.
«п«
1
г 1 I .f f 5f J
I Й 4J
I I i i i f I I
I II I I I I- I
f
I I I I f I I J
5
-Л
8 i п t- т { .. ьВое «ЕлСо 1Ё «е go.. -,. (ш|« SemBf-i г авп9ьтВ2вш ц| bf 9 to СЯВЯя ЧЯ R «(кп
е - о9 оН- аЕ лЗЗ 5ои - а5 - во5 0ч
il Со
8
я
| bf 9 R «
il Со
8b
Г4
К
l
ill
I
}
f
I
I
I
I
« о п) ьш
S
и
о
|,
Ь я-Иг , МА М-М .Ш,и
Я
ни
м
Ч
«
я
Я
о ь
а
la
я|2
I
I
И
iil К
i:
a
и
t
I
f
I
I
5
fd
H
a
s
о
.5
II §J
JS
S|§
4
г;1
M
2
f
I I
Sb
st
Ш
я к
a
i I
f
о ft н
0)
s и
I
tfj о о, е
, X , S г. :;; t i8 -Ч-1Й2 - .L
t Ь.Н гз -. I ..:..15«я|
.SiSSS-,«°or,-2... . 29 .,..ав
я .. . .о« -в -.оУ fsinB «о rfo
g
см Ы
14
ill
«
k.
i:
ъ
:
I
II-
I 1
11
s
k.
j|:
I ji
f
5
се f-
V
s
X
o
ё
и
3
§1
5
I II
I
I
II I
f
I I
.1
I i I I I
|
я|2
5
b
8
k1
аг
I
я
it
N I
3
Ь I
«в
II 111 ll
I
II I
f
I I I
.5i я)
О)
0)
tl
о.
s
fe
i
й
;
;l
I
I i
г
§i
4,
v b
S
01
m
о
r
I
1
я
a
Ш
I
I
2с LSI L i
KM to Xe
oiXME5in« e B-Rfuc
in OL о « P .-.Та и|ш8«gu
m f
s
3
K|
§11
-I I I } I
I
t
i
I J I J.
f
Ill If
si
N
Л
9
-Й
aS J
ftВ
П ll
f
t f
г ,
Ч
С
«
l
«
1 ш
., .. L 4 .1 . 4 Ь i.f & i4 L 4
iSL-S .Ui4S .ЬвИ; J.RsU..ig.l Sibb.s
S.Ks. -.шол. in 4««49 in чШМв«Ш |ШЬ8« а 2 И IB P ШЯ Ш ««КД и «Nn r Ш О -eHjR И lOMD
g и
I
I f
f
2
f I
- I
Твблниа 2
Продолжение тавл. 2
Продолжение т«Сл. 2
71
Т.пл. 93-95 С| (изо-пропил 0).
1494863
72 Продолжение табл.3
| Патент ФРГ № 1154810, iai.12g,34, опублик | |||
| Прибор для заливки свинцом стыковых рельсовых зазоров | 1925 |
|
SU1964A1 |
Авторы
Даты
1989-07-15—Публикация
1986-03-14—Подача