I13424132 .
Изобретение относится к получению водных Г,4--дигидропиридина общей новых производных дигидропиридинов, формулы а именно к способу получения произRS
б-О -О сн ъ-А-Ссн Ъ- нснгСн-вн
(I)
RlOOC
РЗ
COOR
R
Сн-вн
ОН
(I)
R-, и R,
R. и R да Р., и Н - одинаковые или различные и означают С, С,(,- алкил или низпшй алкил, который прерывается атомом кислорода, или низиий алкил, замещеН ный алициклической С,С -группой; одинаковые или различные и означают низший алкил;
одинаковые или различные и означают водород, нитрогруппу, галоид, низший алкил, низшую алкоксигруппу, низшую алкилтиогруппу, низший- алкилсульфонил или низ- ший алкилсульфинил; одинаковые или различные и означают водород, галоид, циан, низшзто алкоксигруппу или низ- ,шук1 алканоиламиногруппу или R, и Е„ вместе с
( о
соседним фенилом обра-; зуют нафтил; простая связь, винилен () или этинилен ();
простая связь или группа
тип - одинаковые или различные и каждый равен О
R, и R А В гчили 1-5,
обладающих Са антагонистической и
адренергической, бета-блокируюш;ей ак- 50 мин. Выпавшие кристаллы от-
тивностью,
Пель изобретения - создание на основе известных методов способа по лучения новых соединений, обладающих ценными фармакологическими свойствами.
Ссылочный пример 1,
В изопропаноле растворяют 23 г 2-(2-бромэтокси)-5-нитробензальде
гида, 11,5 г метилового эфира 3-ами- нокротоновой кислоты и 11,6 г метил- ацетоацетата, после чего полученную смесь кипятят 7 ч. Реакционный раствор охлаждают, выпавшие кристаллы собирают фильтрованием. Полученные криста.ллы промывают метанолом и высушивают на воздухе с получением 33 г сырых кристаллов диметилового эфира 4- Г( 2-бромэтокси)-5-нитрофенил -2,6- диметил-1,4-дигидропиридин-З,5-ди- карбоновой кислоты. Полученный продукт без очистки непосредственно используют на следую01ей стадии.
Б 25 мл N,N-диметилформамида суспендируют 17 г диметилового эфира 4-( 2-бромэтокси)-5-нитрофеншГ -2,6- диметил-1,4-дигидропиридин-З,5-ди- карбоновой кислоты и 7,4 г фтальими- да калия, после чего полученную суспензию нагревают 3 ч при 120-130 С.
Полученную реакционную смесь вьши- вают в 750 мл воды со льдом, выпавшие кристаллы собирают фильтрованием. Полученные кристаллы промывают водой и высушивают на воздухе с по-
лучением 19,6 г сырых кристаллов
диметилового эфира -4-(2-фтальимидо- этокси)-5-нитрофеншЛ -2,6-диметил- 1,4-дигидропиридин-3,5-дикарбоновой кислоты.
Раствор 12 г диметилового эфира 4- (.-фтальимидоэтокси)- 5-нитрофе- ,6-диметил-1 ,А-дигидропиридин- 3,5-дикарбоновой кислоты и 6 мл гид- разингидрата в 240 мл этанола кипя-
фильтровывают в горячем состоянии и фильтрат концентрируют при понижен-
ном давлении с удалением растворителя. После добавления к остатку воды
gg продукт экстрагируют этилацетатом. Экстракт промывают водой и высугпи- вают над безводным сульфатом калия, после чего растворитель отгоняют при пониженном давлении. Полученные та313
КИМ образом сырые кристаллы перекрис таллизовывают из метанола с получением 6 г диметилового эфира (2- аминоэтокси)-5-нитрофенил -2,6-диме- ,4 дигидропиридин-3,5-дикарбо- новой кислоты с т.пл. 228 230°С.
Вычислено, %: С 56,29; Н 5,72; и 10,36
C,,H,N,,0,-
Найдено, %: С 56,06; Н 5,82; N 10,10
ЯМР (DMCO-dg)8 (ppm): 2,24 (6Н, синглет); 2,94 (2Н, триплет); 3,48 (6Н, синглет); 4,06 (. Ш, триплет); 5,24 (IH, синглет).
Ссылочный пример 2.
Раствор 18,3 г 5-метилтиосалицил- альдегида, 235 г 1,4-дибромбутана и .1,1 г кислого сульфата тетра-и-бутил аммония в 18 мл воды нагревают при 70-80 С. К полученному раствору при перемешивании добавляют по каплям в течение 4 ч раствор гидроокиси натрия, содержащей 13,1 г гидроокиси натрия в 109 мл воды, после чего полученную смесь нагревают 2 ч. Затем смесь охлаждают и экстрагируют хлороформом. Экстракт (отделенный органический слой) промывают водой, ВЫС у-
шивают над безводным сульфатом магния и концентрируют при пониженном давлении с получением в виде сырого продукта 32,2 г 2-(4-бромбутокси)- 5-метилтиобензальдегида, который без дальнейшей очистки использован на следующей стадии.
В 55 мл дихлорметана растворяют 10,9 г 2-(4-бромбутокси)-5-метилтио- бензальдегида, после чего раствор, охлаждают до О С. Затем к охлажденному раствору добавляют по каплям в течение 3 ч раствор 15,2 г м-хлор- бензойной кислоты в 165 мл дихлорметана. Через 4 ч для нейтрализации раствора к нему добавляют насьш;енный раствор гидрокарбоната натрия и полученную смесь экстрагируют хлороформом. Экстракт (отделенный органический слой) промывают насьщенным раствором гидрокарбоната натрия и водой, высушивают над безводным сульфатом магния и концентрируют при пониженном давлении с получением сырого продукта, которьш перекристал- лизовывают из смеси хлороформ-эфир с получением 7,8 г 2-(4-бромбутокси) 5-метилсульфонилбензальдегида с т.пл 103-105°С.
5
0 5 g
5
0
5 0 5
3
7,6 г 2-(4-бромбутокси)-5-метил- сульфонилбензальдегида, 2,6 г метил- ацетоацетата и 2,9 г метилового эфира 3-аминокротоновой кислоты растворяют в 16 мл изопропанола, после чего полученный раствор нагревают 5ч. Затем раствор охлаждают, выпавгаие кристаллы собирают фильтрованием и перекристаллизовывают из метанола с получением 3,6 г диметилового эфира (4-бромбутокси)-5-метилсульфо- нилфенил | -2,6-диметил- 1 ,4-дигидро- пиридин-3,5-дикарбоновой кислоты с т.пл. 191-20ГС.
В 8 мл 11,1 -диметилформамида суспендируют 6,3 г диметилового эфира (4-бромбутокси)-5-метилсульфо- нилфенил -2,6-диметил-1,4-дигйдропи- ридин-3,5-дикарбоновой кислоты и 2,2 г фтальимида калия, после чего суспензию нагревают 1 ч при 120- 130 С. Затем реакционную смесь выливают в воду со льдом и выпавший твердый продукт отфильтровывают с получением в виде сырого продукта 7 г (4-фтальимидобутокси)-5-метил- . сульфонилфенил -2,6-диметил-1 ,4-ди- гидропиридин-3,5-дикарбоновой кислоты в виде ее диметилового эфира, который без очистки используют на следующей стадии.
Раствор 6,9 г диметилового эфира (4-фтальимидо)-5-метилсульфо- нилфенил -2,6-диметил-1,4-дигидропи- ридин-3,5-дикарбоновой кислоты и 5,9 г гидразингидрата в 170 мл 95%-но- го этанола (5% воды) кипятят 6ч. После охлаждения реакционного раствора его концентрируют при пониженном давлении. Остаток экстрагируют хлороформом, и полученный экстракт промывают водой, высушивают над безводным сульфатом магния и концентрируют при пониженном давлении. Полученные сырые кристаллы перекристал- лизовывают из смеси хлороформ-эфир с получением 2,6 г диметилового эфира (4-аминобутокси)-5-метилсуль- фонилфенил -2,6-диметил-1,4-дигидро- пиридин-3,5-дикарбоновой кислоты, т.пл. 184-186°С.
Ссылочный пример 3.
В 106 мл сухого бензола растворяют 13 г 2-(4-xлopбyтoкcи)-5-нитpo- бeнзaльдeгидa, 7,28 г этилпропионил- ацетата, 0,2 мл пиперидина и 0,62 мл уксусной кислоты, после чего полученную смесь кипятят 9 ч с одновременным 5 далением воды в ловуику Дина-Старка. После охлаждения к раствору добавляют 6,52 г этилового эфира 3-аминокротоновой кислоты и полученную смесь кипятят 11 ч. После охлаждения смеси выпавшие сырые кристаллы собирают фильтрованием и пере- кристаллиэовывают из метанола с получением 13,13 г диэтилового эфира 2-этил-4- 2-(4-хлорбутокси)-5-нитро- фенил -б-метил-,4-дигидропиридин- 355-дикарбоновой кислоты, т.пл. 147-149°С.
В 8 мл К,М-диметилформамида сус- пендируют 10,26 г диэтилового эфира 2-ЭТИЛ-4- 2-(4-хлорбутокси)-5- Нитро- фенил -6-метил-1,4-дигидропиридин- 3,5-дикарбоновой кислоты и 3,84 г фтальимида калия, после чего суспензию нагревают 1 ч при 120-130 С. За- 2п лизовывают из смеси хлороформ -эфир с
получением 6,4 г диэтилового эфира (4-аминобутокси)-5-нитрофенил - 2-этил-6-метил-1,4-дигидропиридин- 3,5-дикарбоновой кислоты, т.пл, 25 173,5-175,5°С.
Пример.
тем реакционную смесь выливают в воду со льдом, выпавший твердый осадок отфильтровывают с получением в виде сырого продукта 12,5 г диэтилового эфира 2-этил-4- 2-(4-фтальимидобу- токси)-5-нитрофенил -6-метил- ,4-ди-
гидропиридин-3,5-дикарбоновой кислоты, который без очистки использован в следующей стадии.
Раствор 12,4 г диэтилового эфира
2-этил-4- 2-(4-фтальимидобутокси)- 5-нитрофенил -6-метил- 1,4-дигидропи- ридин-3,5-дикарбоновой кислоты и
10,4 г моногидрата гидразина в 270 мл 95%-ного этанола (5% воды) кипятят 10 ч. Затем охлажденный реакционный раствор концентрируют при пониженном давлении с получением остатка, который экстрагируют хлороформом. Экстракт промывают водой, высушивают над безводным сульфатом магния и концен- . трируют при пониженном давлении. По- , лученные сырые кристаллы перекристал-
СООСНз
н
НоС
QbO-CH CH-CH,
о
OCH2.CH2.NHCHn СНСН 91
СООСНз
ш
он
4 г диметилового эфира (2- aминoэтoкcи)-5-нитpoфeнш J-2, 6-диме- тил-15 4-дигидропиридин-3,5-дикарбо- новой кислоты (получение см. ссылочный пример ) и 1,5 г глицидилфенило вого эфира растворяют в 200 мл метанола и полученный раствор оставляют на 2 дня при комнатной температуре. Затем реакционную смесь концентрируют, полученный остаток подвергают колоночной хроматографии на силика- геле с применением в качестве элюен- та смеси хлороформ - метанол (98: :2 об,/об.). Сырые кристаллы пере- кристаллизовывают из этанола с получением 1,8 г диметилового эфира 4- , 2- 2-(2 гидpoкcи-3-фeнoкcипpoпил- aминo)-этoкcи3-5-нитрофенил} -2,6- диметил,4-дигидропиридин-З,5-карбо новой кислоты, т,пл, 1В9-190°С,
Вычислено, %: С 60,53; Н 5,99; N 7,56
,
0
5
0
5
Найдено,.%: С 60,43; Н 6,05; N 7,42
ЯМР (DMCO-dg): 2,22 (6Н, синглет); 3,47 (6Н, синглет); 5,21 (Ш, син- . глет).
П РИМ е р ы 2-13. Соединения получены по методике примера I,
П р и м е р 2. Диметиловый. эфир (2-гидрокси-З-феноксипропил- амино)-этокси -3-нитрофенил -2,6- диметил,4-дигидропиридин-3,5-ди- карбоновой кислоты, т.пл. 147-149 С
вычислено, %: С 60,53; Н 5,99; N7,56
Найдено, % N 7,5
ЯМР (CDCl
синглет); 3,68 (6Н, синглет) ; 4,26 (2Н, триплет); 5,01.(Ш, синглет),
Приме,рЗ, Диметиловый эфир .-(2-гидрокси 3-феноксипропилС 60, 47; Н 6,02; (ррт): 2,35 (6Н,
амино)-этокси 3--2-нитрофенил -2,6-ди метил-1,4-дигидропиридин-3,5-дикар- боновбй кислоты, аморфньш порошок.
Вынислено, %: С 60,53; Н 5,99; N7,56
С,Н„И,0,
Найдено, %: С 60,41; Н 6,02; N 7,41
ЯМР ( (ррга): 2,32 (6Н, синглет); 3,58 (6Н, синглет); 5,86 ( 1Н, синглет).
П р и м е р 4. Диизобутиловьш эфир 2-гидрокси-З-фенокси-пропиламино)-этокси -5--нитрофенил - 2,6-диметил--1 ,4--дигидропиридин-3,5- дикарбоновой кислоты, т ,пл. I 65-1 6Й1
Вычислено, %: С 63,83; Н 7,09; N 6,57
C,,H,,N,0,
Найдено, %: С 63,55; Н 7,13;N 6,
J77JТ
ЯМР (CDC10& (ррт): 0,84 (12Н, двойной дублет); 1,86 (2Н, мульти плет); 2,32 (6Н, синглет); 3,78 (4Н дублет); 5,40 (1Н, синглет).
П р и м е р 5. Дигексиловый эфир (2 гидрокси-3-феноксипропил амино)-этокси 5-нитрофенил -2,6 диметил-1,4 дигидропиридин 3,5-дика боновой кислоты, т.пл. 89-90°с.
Вычислено, %: С 65,59; Н .7,68; N 6,04
Найдено, %: С 65,35; Н 7,78; N 5 99
. ЯМР (СБС1з) (ррт): 0,84.(6Н, триплет); 2,30 (6Н, синглет); 5,36 (1Н, синглет).
П р и м е р 6. Бис-(2-метоксиэти ловый)эфир (2-гидрокси-3- феноксипропиламино )-этокси -5-нит- рофенил |-2,6-диметил-1 ,4-дигидропи- ридин-3,5-дикарбоновой кислоты,т.пл 109-110°С.
Вычислено, %: С 59,71; Н 6,42; N 6,53.
C,H4,N,0,,
Найдено, %: С 59,57; Н 6,36; N 6,44
ЯМР (СБС1з) (ррт): 2,28 (6Н, синглет); 2,6-3,2 (4Н, мультиплет); 3,28 (6Н, синглет); 3,48 (4Н, триплет); 5,36 (IH, синглет).
Пример 7,
Oj-NV
СНзОгС.
Н
осНгСН2 1НСНгСН-о- cOzKHji, он
g
0
5
О
Q
„
55
13 .
Метилоктиловый эфир (2- гидpoкcи-3-фeнoкcипpoпилaминo)этoк- cи2 -5-нитрофенилЗ -2,6-диметил-1,4- дигидропиридин-3,5-дикарбоновой кислоты, аморфный порошок.:
Вычислено, %: С 64,3;Н 7,25; N 6,43
С.,5.Н N,,0,
Найдено, %: С 64,23; Н 7,46; и 6,48.
ЯМР (CDCl,) (ррт):.О,88 (ЗН, триплет); 2,32 (6Н, синглет); 3,64 (ЗН,- синглет) ; 5,40 (Ш, синглет),
П р и м е р 8. Диметиловый эфир 4- 2-СЗ-(2-гидрокси-3-феноксипропш1- амино)пропокси1-5-нитрофенил -2,6- диметил-1,4-дигидропиридин-3,5-ди- карбоновой кислоты, аморфный поро- ток.
Вычислено, %: С 61,15; Н 6,19; N 7,38
С,,Н„К,0,
Найдено, %: С 60,91; Н 6,48; N 7,1,
ЯМР (CDC1,)& (ррт): 2-2,2 (2Н, мультиплет); 2,3 (6Н, синглет); 2,8- 3 (4Н, мультиплет); 3,6 (6Н, син- глет); 4-4,2 (4Н, мультиплет); 5,32 (Ш, синглет).
П р и м е р 9. Диметиловый эфир 4- (2-гидрокси-3-феноксипропил- амино)бутокси-5-нитрофенил -2,6-ди- метил-1,4-дигидропиридин-З,5-дикар- боновой кислоты, аморфньш порошок.
Вычислено, %: С 61,74; Н 6,39; N 7,2
C,joH,,
Найдено, %: С 61;66; Н 6,51(N 7,17.
ЯМР ( (ррт): 1,6-2 14Н, мультиплет); 2,28 (бН, синглет); 2,7-2,9 (4Н, мультиплет); 3,56 (6Н, синглет); 3,92-4,16 (4Н, мультиплет); 5,32 (1Н, синглет).
Пример 10. Этилметиловый эфир.4- 2- 4-(2-гидрокси-З-фенокси- пропиламино)-бутокси -5-нитрофенил}- 2,6-диметил-1,4-дигидропиридин-3,5- дикарбоновой кислоты, аморфный порошок.
Вычислено, 7,: С 62,3; Н 6,58; N 7,03
С,, Нз)И,0, i. Найдено, %: С 62,38; Н 6,77;N 6,95.
ЯМР (CDCij) (Г (ррт): 1,16 (ЗН, триплет); 1,6-1,9 (4Н, мультиплет); 2,3 (6Н, синглет); 2,6-2,9 (4Н,мультиплет); 3,94 (ЗН, синглет); 3,8- 4,2 (6Н, мультиплет); 5,28 (1Н, синглет
П р и м е р 11. Днметиловый эфир
913
4-1.- l 0-( 2-гидрокси-З-феноксипропил- амино) децилокси 5- Нитрофеиил -2,6- лиметил-1,4- дигидропиридин 3,5-дИ карбоновой кислоты, аморфный порошок. , Вычислено, %: С 64,75; Н 7,4;;W 6,29 C5feH,NjO,
Найдено, %: С 64,27; Н 7,65;N 6,25 ЯМР CCDCl) 4 (ppm): 1,2-1,6 (16Н,- мультиплет); 2,3.(бН, синглет); 2,5 2,9 (4Н, мультиплет); 3,56 (6Н, синг глет); 3,96-4,1 (4Н, мультиплет); 5,34 (1Н, синглет).
Пример 12. Диметиловый эфир 4- 5(2-гидрокси-З-феноксипропиламино) пентил ок си 5-нитрофенил -2,6-диме тил-1,-дигидропиридин-З,5-дикарбо- новой кислоты, аморфный порошок.
Вычислено, %: С 62,3; Н .6,58; N 7,03.
.,,
Найдено, %: С 62,43; Н 6,87;N 7,18
ЯМР (CDCl) § (ppm): 1,4-1,6 (6Н, мультиплет); 2,3 (6Н, синглет); 2,6-2,9 (4Н, мультиплет); 3,56 (6Н, синглет); 3,9-4,2 (4Н, мультиплет); 5,3 ( Ш, синглет).
Пример 13, Диметиловый эфир ( 2-гидрокси-3-феноксипропил- амино) гексилокси -5-нитрофенил -2,6- диметил-1,4-дигидропиридин-3,5- дикар- боновой кислоты, аморфный порошок.
Вьгчислено, % : С 62, 83; Н 6,76;N 6,8
C7,H4,.N,0,
Найдено, %: С 62,58; Н 6,83;N 6,88
ЯМР (СРС1з) (ppm): 1, 4-1,6 (8Н, мультиплет); 2,3 (6Н, синглет); 2,6- 2,9 (4Н, мульт 1плет); 3,6 (6Н, синглет); 3,9-4,1 (4Н, мультиплет); 5,32 (IH, синглет).-
Пример 14. В 30 мл И,Н-диме- тилформамида растворяют 2 г диметило- вого эфира (2-аминоэтокси)-5- нитpoфeнилJ -2,6-диметил-1,4-дигидро- пиридин-3,5-дикарбоновой кислоты и 0,6 г окиси стирола, после чего по- лученньш раствор оставляют на 2 дня при комнатной температуре. Затем реакционную смесь концентрируют при пониженном давлении, полученный ас- таток подвергают колоночной хроматографии на силикагеле с применением в качестве элюента смеси хлороформ-метанол (95:5 об./об.). Сырые кристаллы перекристаллизовывают из этилаце- тата с получением 500 мг (р- гидроксифенилэтиламино)этокси-5-нит- рофенил-2,б-диметил-1,4-дигидропири- дин-3,5-дикарбоновой кислоты в виде
13 .10,
ее диметилового эфира, т.пл. 135137°С.
Вычислено, %: С 61,71; Н 5,95; N 8
C,,H,,N,08
Найдено %: С 61,88; Н 5,84; N 7,94
ЯМР (DMCO-d) f (ppm): 1,34 (ЗН, синглет); 3,58 (ЗН, синглет); 4,2 (2Н, триплет); 4,82 (Ш, триплет); 5,36 (Ш, синглет).
Пример 15. В 1300 мл метанола растворяют 13 г диметилового эфира (4-аминобутокси)-5-нитрофег ,6-диметил-1,4-дигидропиридин 3,5-дикарбоновой кислоты и 4,5 г глицидилфенилового эфира, после чего полученный раствор кипятят 16 ч. Затем растворитель отгоняют при пониженном давлении. Полученный остаток подвергают колоночной хроматографии на силикагеле с применением; в качестве элюента смеси хлороформ- метанол (96:4 об./об.). Сырые крис таллы перекрист аллизовывают из этанола с получением 9 г диметилового эфира ( 2-гидрокси-З-фенокси пропиламино)-бутокси -5-нитрофенш1 2,6-диметил-1,4-дигидропиридин-3,5- дикарбоновой кислоты, т.пл. 131- 133°С.
Вычислено, %:-С 61,74; Н 6,39;. N 7,2 ,
,
Найдено, %: С 61,61; Н 6,49; N 7,21
ЯМР (CDCl,) 5 (ppm): 1,6-2 (4Н, мультиплет); 2,28,(6Н, синглет); 2,7-2,9 (4Н, мультиплет); 3,56 (6Н, синглет); 3,9-4,2 (.5Н, мультиплет); 5,3 (1Н, синглет); 6,6-7,1 (ЗН, мультиплет); 7,1-7,4 (ЗН, мультиплет); 7,9-8,2 (2Н, мультиплет).
Полученный продукт обрабатывают этанольным раствором хлористого водорода с получением его хлоргидрата который перекристаллизовьшают из этнола с получением хлоргидрата диметилового эфира (2-гидрокси- 3-феноксипропгшамино) бутокси -5- нитрофенил -2,6-диметил-1,4-дигидро- пиридин-3,5-дикарбоновой кислоты, т.пл. 117-120 с.
Вычислено, %: С 56,47; Н 6,32; N 6,59; 01 5,56
, N,0, HCl HzO
Найдено, %: С 56,68; Н 6,38; N 6,32; 01 5,53
Пример 16. По методике примера 15, используя (3)-глицидилфе ниловый эфир, получен (з)-(-)-диме- тиловый эфир (2-гидрокси-3- феноксилпропиламино) -бутокси -З-нит poфeнилJ-2,6-диметил-1,4-дигидропи- ридин 3,5 дикарбоновой кислоты.
т.пл. 144-l46°C./oi/, 2,1
Д
МеОН).
,,08,
Вычислено, N 7,2
C,H,N,Og
%: С 61,74; Н 6,39;
С 61,57; Н 6,55;
Найдено, % N 7,2j
п радукт,полученный на предьщущей стадии,обрабатывают этанольным раство ром хлористого водорода с образованием его хлористоводородной соли, которую перекристаллизовывают из этанола с получением хлоргидрата (з)-(-)-диме тилового эфира ( 2-гидрокси- 2-феноксипропиламино) бутокс и -5-нит-- рофенилЗ , б-диметил 1 ,4-дигидропи- ридин-3,5-дикарбоновой кислоты, т.пл 187-189°С./(//5 -12,5° (,04 МеОН)
Вычислено, %: С 58,11; Н 6,18; N6,78
НС1
30 37
С 58; Н 6,31;
Найдено, N 6,71
Пример 17. По методике примера 16, используя (в)-глицидилфе- ниловый.. эфир, получен (В)-( + )-димети- ловый эфир ( 2-гидрокси-З- феноксипропиламино)бутокси -5-нитро- фенил -2,6-диметил-1,4-дигидропири- дин-3,5-дикарбоновой кислоты, т.пл. 144-146°C./oi/ 2,2 (,07, МеОН).
Вычислено, %: С 61,74; Н 6,39 ; N 7,2
С 61,58; Н 6,56;
0 37
Найдено, %; N 7,17.
Полученный на вьппеописанной стадии продукт обрабатывают этанольным раствором хлористоводородной кислоты с получением соответствующей хлористоводородной соли, которую перекрис- таллизовывают из этанола с получением чистого хлоргидрата (Р)-(+)-диме- тилового эфира (2-гидрокси- 3-феноксипропиламино)бутокси -5-нит- рофенил -2,6-диметил-I,4-дигидропи- ридин-3,5-дикарбоновой кислоты, т.пл 191-193°С.
Вычислено, %: С 58,11; И 6,18; N 6,75
С}рНз, N,0,.HC1
Найдено, %: С 58,04; Н 6,29; N 6,67 .
М +12,1° (,01, МеОН).
Пример 18. В 500 мл метанола растворяют 5,2 г диэтилового эфира 4-С2-(4 аминобутокси)-5-нитрофенилЗ 2,6 Диметил-1,4 дигидропиридин-3,5- дикарбоновой кислоты и 1,7 г глици- дилфенилового эфира. После чего полученный раствор кипятят 16 ч. Затем при пониженном давлении отгоняют растворитель, а остаток подвергают коло-ночной хроматографии на силика- геле с применением в качестве элю- ента смеси хлороформ-метанол (95: :5 об,/об.). Сырые кристаллы пере- кристаллизовывают из этанола с получением 2,2 г диэтилового эфира 4-(2 ГИДрокси-3-феноксипропиламино) бутокси -5-нитрофенил -2,6-диметил- 1,4-дигидропиридин 3,5-дикарбоновой кислоты, т.пл. 141-143 С. . , Вычислено, %: С 62,83; Н 6,76; N 6,87
5
0,2
4,N,0,
0
5
0
5
0
5
Найдено, %: С 62,85; Н 6,86; N 6,86
ЯМР (CDC1,)S (ppm): 1,14 (6Н, триплет); 2-28 (6Н, синглет); 1,5-2 (4Н, мультиплет); 5,24 (Ш, синглет).,
Примеры 19-22. По методике примера. 18 получены нижеследующие соединения.-. .
Пример 19. Нис-циклопропил- метиловый эфир (2-гидрокси- 3-феноксипропиламино)бутокси1-5-нит- ;рофенилЗ-2,6-диметил-1,4-дигидро- пиридин-3,5-дикарбоновой кислоты, т.пл. 148-151°С.
Вычислено, %: С 65,14-; Н 6,83; N 6,33
CH - S-N O,
Найдено, %: С 64,96; Н 6,94; N 6,32
ЯМР (CDC1,)5 (ppm): 0-0,6 (8Н, мультиплет); 0,8-1,3 {2Е, мультиплет); 1,4-2 (4Н, мультиплет); 2,3 (6Н, мультиплет); 5,28 (Ш, синглет).
П р и м е р 20. Дипропиловый эфир (2-гидрокси-З-фенокси- пропиламино)бутокси -5-нитрофекил}- 2,6-диметш1-I,4-дигидропиридин-3,5- дикарбоновой кислоты, т.пл. 148- 151°С.
Вычислено, %: С 63,83; Н 7,09; N 6,75
С,,Н,,КзО,
Найдено, %: С 63,6; Н 7,01; N 6,5
1313424
ЯМР (CDCl, ) .(ppm): 0,84 (6Н, триплет); 1,2-2 (8Н, мультиплет); 2,3 (6Н, .синглет); 5,28 (Ш, син- глет).
П р и м е р 21. Диметиловый эфир (2-гидрокси-З-феноксипропил амино)бутокси -4 нитрофенил -2,6-ди- метил- 1, 4-дигидропиридин-3,5 дикар-- боковой кислоты, т.пл. 22 124 с.
Вычислено, %: С 60,8; Н 6,46; N 7,09
С 5,,-0,
Найдено, %: С 60,71; Н 6,42; N 7,04 ., 5
ЯМР (CDC1,) & (ppm): 1,6-2 (4Н, мультиплет); 2,3 (6Н, синглет); 3,58 (6Н, синглет); 5,32 (Ш, син- глет).
П р и м е р 22. Диизопропиловый 2о эфир (2-гидрокси 3-фенокси- пропил амино )бутокси 5-нитг)офенил 25б-диметил 1 ,4-дигидропиридин- 3,5 карбоновой кислоты хлоргидрат, т.пл 212-213°С.25
Вычислено, %: С 60,39; Н 6,86; К 6,21
,,0,С1
Найдено, %: С 60,19; Н 6,92; N 6,2430
Ж1Р (DMCO-d) (ppm) 0,9 (-бЦ, дублет); 1,16 (6Н, дублет); 2,24 (6Н, синглет); 3,32 (6Н, синглет); 4,74 (2Н, мультиплет); (1Н,
синглет),
35
При мер 23, В44 мл метанола растворяют 2,57 г диметилового эфира (4-аминобутокси}-5-метил- сульфонилфенил -2,б-диметил-1,4-ди д гидропиридин-3,5-дикарбоновой кислоты (получение см. ссьшочный пример 2) и 0,83 г глицидилфенилового эфира, после чего полученный раствор оставляют при комнатной температуре на 43 ч. Затем реакционный раствор концентрируют при пониженном давлении, полученный остаток подвергают колоночной хроматографии на сили- кагеле с применением в качестве элю- gQ ента смеси хлороформ-метанол (95: :5 об./сб.). Сырые кристаллы пере- кристаллизовывают из водного этанола с получением 1,05 г диметилового эфира (2-гидрокси-3-фенокси- прОпиламино) бутокси |-5-метилсульфо- нилфенилЗ 2,6-диметил-1,4-дигидро- пиридин-5 5-дикарбоновой кислоты, т,пл. 145-146°С,
45
5
0
5
д Q
5
13 .14 .
Вычислено, %: С 59,5; Н 6,6; N 4.48; S 5,12
C,,H,,,.0,
Найдено, %: С 59,6; Н 6,63; W 4,29; S 5,28
ЯМР (CDC1,,) (ppm): 2,28 (6Н, синглет); 2,98 (ЗН, синглет); 3,56 (6Н, синглет); 5,28 (Ш, синглет).
Примеры 24-37.
По методике примера 23 были получены нижеследующие соединения.
П р и м е р 24, Диметиловый эфир 4- З-хлор-2- 4-(2-гидрокси-3-фенокси пропиламино)бутокси фенил -2,6-диметил- 1,4- дигидропиридин-3,5-дикар- боновой кислоты, аморфный порошок.
Вычислено, %: С 62,88; Н 6,51; N 4,89
C,,H,,
Найдено, %: С 62,71; Н 6,43; N 4,8
ЯМР (СТС1-)6 (ррп): 1,5-1,9 (4Н, мультиплет); 2,28 (6Н, синглет); 3,6 ,(6Н, синглет); 5,24 (1Н, синглет) .
П р и м е р 25. Диметиловый эфир 4- (2-гидрокси-3-феноксипропил- амино )этокси -5-метоксифенил -2, 6- диметил-1,4-дигидропиридин-З,5-ди- карббновой кислоты, т.пл. 141-143°С.
Вычислено, %: С 64,43; Н 6,71; N 5,18
C,H,,N,0,
Найдено, %: С 64,09; Н 6,68; N 5,8
ЯМР (CDClJS (ppm): 2,23 (6Н, синглет); 3,56 (бН, синглет); 3,68 (ЗН, сир1глет); 5,28 ( Ш, синглет).
П р и м е р 26. Диметиловый эфир 4-( 2-гидрокси-3-феноксипропш1- амино)бутоксиЗ 5-метоксифенил -2,6- диметил-1,4-дигйдропиридин-З,5-дикар- боновой кислоты, аморфный порошок.
Вычислено, %: С 64,46; Н 7,15j N1.4,83
С, H4oNiOg 0,5H,
Найдено, %: С 64,49; Н 7,27; N 4,72
ЯМР (пиридин-d5) 5 (ppm) : 2,51 (6Н, еинглет); 3,65 (9Н, синглетопо- добный); 5,85 (Ш, синглет).
П р и м е р 27. ДиметилоБЬЙ эфир (2-гидрокси-3-феноксипропш1- амино) бутокси -5-метилфенил -2,6- диметил-1,4-дигидропиридин-З,5-дйкар- боновой кислоты, аморфньй порошок.
Вычислено, %: С 66,29j Н 7,36;. N 4,99
С,,Е,0,-0,
15
Найдено, %: С 66,38; Н 7,36; N 4,95
ЯМР (CDC1,) S (ррт): 2,21 (ЗН, синглет); 2,27 (6Н, синглет); 3,57 (6Н, синглет); 5,22 (1Н, синглет); 6,17 (1Н, синглет).
П р и м е р 28. Хлоргидрат диме- тилового эфира (2 Гидpoкcи- 3 фeнoкcипpoпшIaминo )бутокси тилтиофенил -2,6 -диметил 1 ,4--дигидр пиридин-3,5 дикарбоновой кислоты, аморфньвй порошок.
Вычислено, %: С 58,58;,Н 6,76; N 4,41; С1 5,58; S 5,04
С,, .O -HCl-0,8H.jO
Найдено, %: С 58,6; Н 6,91; N 4,25; С1 5,79; S 5,24ЯМР (СБС1з)У (ррт): 2,3 (6Н, сиглет); 2,39 (ЗН, синглет); 3,54 (6Н синглет); 5,14 (Ш, синглет).
П р и м е р 29. Диметиловьй эфир 4- 5-хлор-2-1 2( 2-гидрокси-3-фенокс пропил амино) это к си фенил -2,6 диме- ,4-дигидропиридин-3,5 дикарбо- новой кислоты, т.пл. 184-186°С.
Вычислено, %: С 61,7; Н 6,1; N 5, 14
,
Найдено, %: С 60,91; Н 6,23; N 4,94
ЯМР (СВС1з) (ррт): 2,3 (6Н, синглет); 3,62 (6Н, синглет); (1Н, синглет).
5,26
П р и м е .р 30. Диметиловый эфир (2-гидрокси 3-фенокси пропил амино) бутокси - 5--метилсульфо- нилфенил -2,6-диметил 1,4--дигидро- пиридин--3,5--дикарбоновой кислоты, т.пл. 83-86°С.
Вычислено, %: С 61,07; Н 6,78; N 4,59-; S 5,26
С,, ,
Найдено, %: С 61,02; Н 6,89; N 4,41; S 5,28
ЯМР (CDC1,) S (ррт): 2,28 (6Н, синглет); 2,65 (ЗН, синглет); 3,55 (6Н, синглет); 5,28 (Ш, синглет).
П р и м е р 31. Диметиловый эфир 4- 5 бром-2-f4( 2-гидрокси-3-фенокс пропиламино) бутокси фенил -2,6-диме ТШ1-1,4-дигидропиридин 3,5-дикарбо- новой кислоты, т.пл. 83-85°С.
Вычислено, %: С 58,35; Н 6,04; N 4,54; Бг 12,94,
Найдено, %: С 58,5; Н 6,28; N 4,35;.Вг 12,44
4
13
16
5
0
5
0
5
0
5
0
5
ЯМР (CDClJS (ррт): 2,27 (6Н, синглет); 3,58 (6Н, синглет); 5,21 ( Ш, синглет); 6,46 ( Ш, синглет).
Пример 32. Диметиловый эфир 4- 3,5-дихлор-2- 4-(2-гидрокси-З- феноксипропиламино)бутокси фенил - 2,6-диметил-1,4-дигидропиридин-З,5- дикарбоновой кислоты, т.пл. 72-74 С.
Вычислено, %:С57,6;Н6,12; N 4,48; С1 11,34 .N O Clj-H O
Найдено, %: С 57,9; Н 6,35; N 4,33; С1 11,42
ЯМР (CDC1,)S (ррт-): 2,28 (6Н, синглет); 3,62 (6Н, синглет); 5,22 (Ш, синглет); 6,07 (1Н, синглет).
Пример 33. Диметиловый эфир ,5-дибром-2- 4-( 2-гидрокси-3- феноксипропиламино)6yTOKCHj фенил - 2,6-диметш1-1,4-дигидропиридин-3,5- дикарбоновой кислоты, аморфный порошок.
Вычислено, %: С 51,61; Н 5,23; N 4,01; Вг 22,89
С„Н,бМ,0,Вг.О,1Н20
Найдено, %: С 51,38; Н 5,36; N 3,91; Вг 23,21
ЯМР (CDCl) (ррт): 2,28 (6Н, синглет); 3,64 (6Н, синглет); 5,26 (Ш, синглет); 6,12 ( IH, синглет).
П р и м е р 34. Диметиловый эфир (2-гидрокси-3-феноксипропил- амино) бутокси фенилЗ-2, б иметил- 1,4-дигидропиридин-3,5-дикарбоновой кислоты, т.пл. 129-130°С.
Вычислено, %: С 66,9; Н 7,11; N 5,2
C,oH,
Найдено, %: С 66,7; Н 7,34; N 5,04
ЯМР (CDC1,,)S (ррш): 1,5-U9 (4Н, мультиплет); 2,28 (6Н, синглет); 3,56 (6Н, синглет); 5,2 (Ш, синглет ).
Пример 35. Хлоргидрат динети- лового эфира 4- 3-Г2-(2-гидрокси-3- феноксипропиламино )этокси фенил1-2,6- диметил-1,4-дигидропиридин-З,5-дикар- боновой кислоты, т.пл. 136-139°С.
Вычислено, %: С 61,48; Н 6,45; N 5,12
.HCl
Найдено, %: С 61,27; Н 6,44; N 5,09
ЯМР (CDCl,) (ррт): 2,28 (6Н, синглет); 3,6 (6Н, синглет); 5,24 (1Н, синглет).
П р и м е р 36. Диметиловый эфир 4- 3-С4-(2-гидрокси-3-феноксипрошш
- 17
амино) бутокск фенил -2,6-диметил- 1,4 дигидропиридин-3,5-дикарбоновой кислоты, .т.пл. lOe-IO/jS C.
Вычислено, %:С65,8;Н7,18; N5,12
Найдено, %: С 65,72; Н 7,32; N 4,97
ЯМР (CDClO (ppin): 2,31 (6Н синглет); 3,65 (6Н, синглет); 5 (1Н, синглет); 6,04 (1Н, синглет).
П р и м е р 37. Диметиловый эфир 4- (2-гидрокеи-3 феноксипропил- амино )бутокси (ЪeнилJ 2,6-диметил-1 ,4 дигидропиридин-3,5-дикарбоновой кислоты, т.пл. 83-85°С.
Вычислено, %: С 66,9; Н 7,11; N5,2
Найдено, %: С 66,64; Н 7,2; N 5,08
ЯМР (CDC1,)& (ppm): 2,3 (6Н, синглет); 3,64 (6Н, синглет); 4,95 (1Н, синглет); 5,78 (1Н, синглет).
Пример 38, В 200 мл метанола растворяют 2 г диметилового эфира 4 Z-(4-аминобутокси)-5-нитрофенилЗ - 2 56 диметил-1,4-дигидролиридин-3,5- дикарбоновой кислоты и 0,84 г глици дил-(4-метоксифенилового)эфира, по- лученный раствор кипятят 3 ч. Затем растворитель отгоняют при пониженном давлении, полученный остаток подвергают колоночной хроматографии на силикагеле с применением в качестве элюента смеси хлороформ-метанол (95:5 обо/об,). Сырые кристаллы пере кристаллизовывают из смеси метанола с этиловым эфиром с получением 0,85 г диметилового эфира 4-L2- 4- - 2-гидрокси-3-(п-мeтoкcифeнoкcи)пpo- пшlaминo бутокси -5-нитрофенил -2,6- диметил-1,4-дигидропиридин-З,5-дикарбоновой кислоты, т.пл. 154-155°С
Вычислено, %: С 60,68; Н 6,41; N 6,85
С,, Нз,Г1,0,о
Найдено, %: С 60,57; Н 6,49; N 6,75
ЯМР (00013)5 (ppm): 2,28(6Н, синглет); 3,56 (бН, синглет); 3,76 (ЗН, синглет); 5,3 (1Н, синглет).
П р и м е р ы 39-45. По методике примера 38 получают нижеследующие соединения.
Пример 39. Хлоргидрат диметилового эфира (о-хлорфен- окси)2-гидрокси пропил амнноЗ. си -5-нитрофенил-2,6-диметил-1,41342413
18
0
5
0 5 0
5
0
5
дигидропиридин-3,5-дикарбоновой кислоты, аморфный порошок.
Вычислено, %: С 57,88; Н 5,99; N 6,75
С,оН,бСШ,0-,. НС1
Найдено, %: С 58,13; Н 5,87; N 6,69
ЯМР (DMCO-d)5 (ppm): 1,4-1,8 (4Н, мультиплет); 2,32 (6Н, синглет); 3,64 (6Н, синглет); 5,26 (1Н, синглет) .
П р и м е р 40. Диметиловый эфир (о-цианофенокси)-2-гидр- оксипропиламино бутокси -5-нитрофе- нил -2,6-диметил-1 ,4-дигидропиридин- 3,5-дйкярбоновой кислоты, т.пл. 169-171°С.
Вычислено, %: С 61,18; Н 5,96; N 9,21
Сз, H,6N,0,
Найдено, %: С 61,06; Н 5,91; N 9,08
ЯМР (CDC1,)S (ppm): 2,32 (6Н, синглет); 2,76 (2Н, триплет); (6Н, синглет); 5,24 (1Н, синглет).
П р и м е р 41. Диметиловый эфир 4- 2- 4-С2-гидрокси-3-( 1-нафтилок- си ) -пропил амино бутокси -5-нитрофе- ,6-диметил-1,4-дигидропиридин- 3,5-дикарбоновой ки слоты, т.пл. 180- 18ГС.
Вычислено, %: С 64,44; Н 6,2; N 6,63
C,H3,N,0,
Найдено, %: С 64,17; Н 6,35; N 6,46
ЯМР (CDCl,) (ppm): 2,26 (6Н, синглет); 3,34 (6Н, синглет); 5,3 (1Н, синглет).
Пример42. Диметиловьй эфир (п-ацетамидофенокси)-2- гидроксипропиламино бутокси -5-нит- рофенил-2,6-диметил-1,4-дигидропи- ридин-3,5-дикарбоновой кислоты,т.пл. 75-176°С.
Вычислено, %: С 59,99; Н 6,29; N 8,74
C5iH(,N40,(,
Найдено, %: С 59,98; Н 6,39; N 8,64
ЯМР (CDClj+DMCO-d) S (ppm): 2,08 (ЗН, синглет); 2,28 (6Н, синглет); 3,54 (6Н, синглет); 5,28 (Ш, синглет) .
П р и м е р 43. Диметиловый эфир 4- 2- Г4- (2-гидрокси-3-фрноксипропил- амино J-2-бутинилокси -5-нитpoфeнилJ - 2,6-димetил-1,4-дигиДропиридин-З,51913
дикарбоновой кислоты, аморфный поро- шок.
Вычислено, %: С 58,53; Н 6,06; N 6,83
С,„Н,зК,0,-2Н20
Найдено, %: С 58,73; Н 6,35; N 7,09
ЯМР (CDC1,)8 (ppm): 2,3 (6Н, синглет); 3,6 (6Н, синглет); 4 (2Н, . синглет); 5,3 (1Н, синглет).
Пример 44. Хлоргидрат димети- ловото эфира (Е)4-(2-гидрокси- 3 феноксипропил амино) -2-бутенилок- си -5-нитрофенилЗ 2,6-диметил -1,4- дигидропиридин 3,5-дикарбоновой кислоты, т.пл. 171-173 С.
Вычислено, %: С 58,3; Н 5,87; N 6,8 . C,,H,,N,0,C1
Найдено, %: С 57,97; Н 5,95; N 6,78
ЯМР (DMCO-dJR (ppm): 2,24 (6Н, синглет); 3,46 (6Н, синглет); 5,24 (1Н, синглет).
П р и м е р 45. Хлоргидрат диме- тилового эфира (2)-4-(2-гидрок- си-3-феноксипропиламино -2-бутенилок- си -5-нитрофенил-2,6-диметил-1,6-ди- гидропиридин-3,5-дикарбоновой кислоты, т.пл. 191-193°С.-
Вычислено, %: С 58,3; Н 5,87; N 6,8
СзоН,,С1
Найдено, %: С 58,05; Н 5,87; N 6,88
ЯМР (CDCli)S (ppm): 2,28 (6Н, синглет); 3,58 (6Н, синглет); 4,7 (2Н, дублет); 5,34 (1Н, синглет).
Пример 46. В 46 мл метано- ла растворяют 4,62 диэтилового эфира (4-аминобуток си)-5-нитpoфeнилJ - 2-этил-6-метил-1,4-дигидропиридин- 3,5-дикарбоновой кислоты и 1,46 г глицидилфенилового эфира, после чего полученный раствор кипятят 15 ч. Охлажденный реакционный раствор концентрируют при пониженном давлении, полученный остаток подвергают, коло- ночной хроматографии на силикагеле с применением в качестве элюента смеси хлороформ-метанол (95:5 об./сб.). Сырые кристаллы перекристаллизовыва- ют из этанола с получением 1,22 г ди- этилового эфира 2-этил-4- 2- 4-(2- гидрокси-3-феноксипропиламино)-буток- си -5-нитрофенил -6-метил-1,4-ди- гидропиридин-3,5-дикарбоновой кислоты, т.пл. 159-159,5°С.
1320
Вычислено, %: С 63,35; Н 6,93; N 6,72
35 Н, N,0,
Найдено, %: С 63,18; Н 6,78; N 6,62
ЯМР (CDCl,) (ppm): 2,3 (ЗН, синглет); 5,3 (IH, синглет); 6,57 (1Н, синглет).
Фармакологическое действие предлагаемых соединений иллюстрируется следующими результатами испытаний, а также методами испытаний.
Методы испытаний.
Гемодинамическое действие.
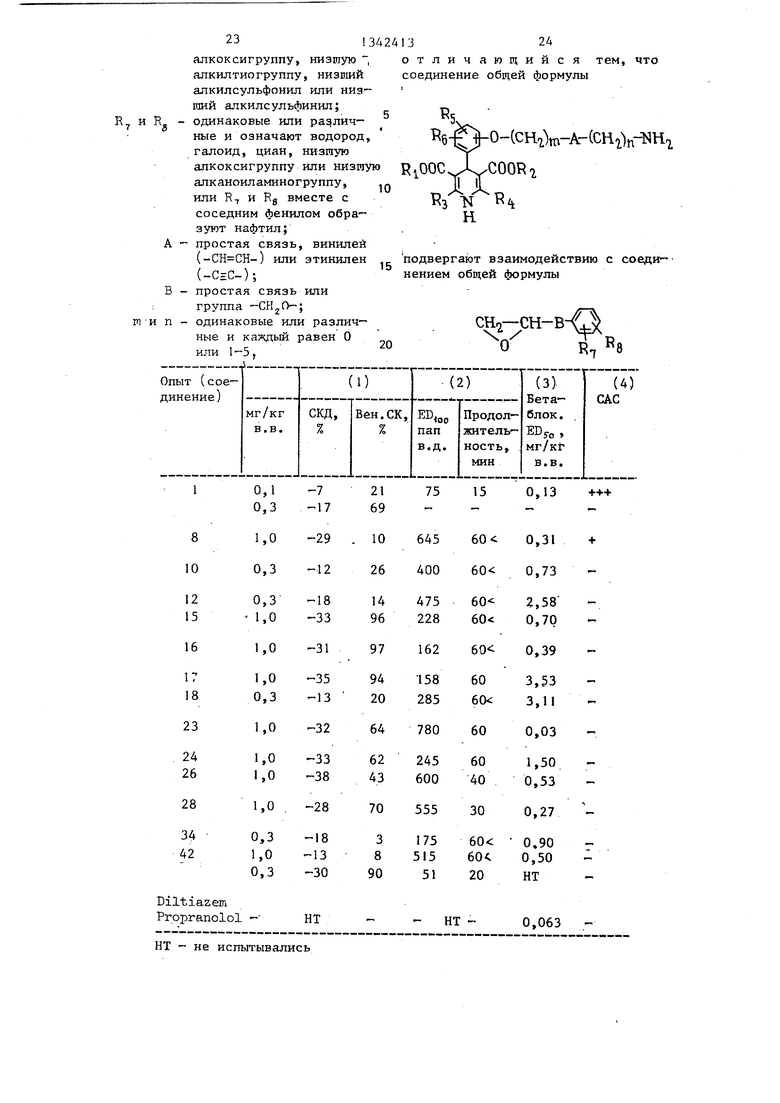
Беспородных собак обоих полов подвергают анестезии с помощью пента- барбитала натрия (ЗО мг/кг в.в.). Животных подвергают искусственному вентилированию окружаюпд1м воздухом. Измеряют среднее артериальное давление крови (СКД), -скорость сердцебиения (СС), давление в левом-желудочке (ДЛЖ), макс, d ДЛЖ/dt среднее легочное артериальное давление крови (СЛАД), минутный объем сердца (но) и скорость венозной крови (Вен. СК). Испытуемые соединения вводят в виде инъекций в бедренную вену. Гемодинамическое действие испытуемых соединений сравнивают с действием хорошо известных Са - антагонистов.
В таблице (столбец 1) показано процентное изменение СКД и Вен. СК- от контрольных значений, вызванное внутривенной инъекцией испь1туемого соединения.
Венечное сосудорасширяющее действие.
Беспородных собак подвергают анестезии и вентилированию так, как указано выше. Проводят трахотомию .в четвертом межреберном пространстве. Вслед за внутривенной инъекцией гепраина (1000 ед/кг) кровь из отдаленного конца канулированной сонной артерии перекачивают с помощью сер- ворегулируемого перисталтического насоса в круговую ветвь левой венечной артерии при постоянном давлении пропускаемой крови 120 мм HQ, контролируемом регулятором насоса.В цепь введен электромагнитный датчик потока для регистрации скорости кровяного потока в канулированной венечной артерии. Испытуемые соединения вводят непосредственно в вую трубочку, присоединенную рядом с канюлей венечной артерии. Венечное
211
сосудорасршряющее действие испытуемых соединений подсчитывают на основе дозы, необходимой для увеличения на 100% Вен. СК ( пап), когда максимальный ответ на введение папа- верина при дозировке 300 мкг выражается как 100%-ньй ответ. В таблице (столбец 2) приведены ( пап и продолжительность венечного сосудора ширяющего действия испытуемых соединений .
Бета-адреноцепторное блокирующее действие,
Бета-адреноцепторное блокирующее действие испытуемых соединений определяют по методике Tachikava и Takenaka (Фармакологические испытания I-(7-инденилокси)-З-изоцропил- аминопрЬпан-2-ола гидрохлорида (УВ-2-), Apch. I pharmacodyn, 202, 79-92, (1973) на мужских особях крыс Вистара. Предварительно крысам дают резерпин (8 мг/кг в.м.) за 18 ч до испытаний. Крыс подвергают анестезии с помощью пентабарби- тала натрия (55 мг/кг в.м.), после чего подвергают двусторонней вагото- мз-ш в области шеи. Скорость сердцебиения измеряют кардиотахометром, запускаемого одновременно с желудочковым компонентом ЭКГ (ввод П), регистрируют сердцебиение на полиграфе. После получения контрольного отклика на внутривенное введение изопротеренола в дозе 0,1 мг/кг вводят внутривенными инъекциями испытуемое соединение в возрастающей дозировке с интервалом в 20 мин. Средняя доза, приводящая к 50%-ной блока де йоложительного хронотропного отклика на изопротеренол (), уста
3
22
5
0
5
0
5
0
навливается на основании кривых дозировка-отклик, полученных отложением зависимости процента ингибирования от log кумулятивной дозы испытуемого соединения (таблица, столбец З).
В ряде опытов была также выявлена собственная активность по отношению к симпатической нервной системе (САС), Полученные результаты приведены в таблице (столбец 4), где знаком - обозначно почти полное отсутствие увеличения скорости сердцебиения, знак + означает увеличение СС на 10-19 ударов/мин, знак ++ означает, что наблюдалось увеличение СС на 20-29 ударов/мин, знак +++ означает, что наблюдалось увеличение СС на более чем 30 ударов/мин.
Необходимая дозировка устанавливается в каждом случае особо, принимая во внимание такие факторы, как симптом, возраст, пол пациента. Взрослому пациенту ежедневно внутри венными инъекциями вводят в общей сложности 1-200 мг одной или несколькими, дозами, при этом хорошо известно, что много известных соединений, , очень близких предлагаемым соединениям не проявляют какой-либо значительной токсичности.
Таким образом, как видно из данных таблицы, способ позволяет получить новые производные 1,4-дигидро- пиридина, обладающие комплексом ценных фармакологических свойств..
Форму л-а изобретения
Способ получения производных 1,4-дигидропиридина общей формулы:
0(CHr,m-A-(CH l -NHCH2CH-B
COOR2.
R
R( и RJ одинаковые ихш различные и означают С,-С,о- алкил или низший алкил, который прерывается . атомом кислорода, ил. НИ5ИИЙ алкил, замещенный алициклической С,-Cg-группой;
R, и R
одинаковые или различные и означают низший алкил;
R j. и Rg - одинаковые или различные и означают водород, нитрогруппу, галоид, низщий алкил, низшую
23134241324
алкоксигруппу, низшую , отличающийся тем, что
соединение общей формулы
алкилтиогруппу, низвшй алкилсульфонил или низший алкилсульфинил; R и R - одинаковые или различные и означают водород, галоид, циан, низшую алкоксигруппу или низшую I.OOC алканоиламиногруппу, Q или R-, и Rg вместе с Яо R it соседним фенилом образуют нафтил;
А - простая связь, винилей () или этинилен ( Г-Г V
/ 9
В - простая связь или
группа
тип- одинаковые или различ-СНо-СН-В
ные и какдьй равен
или 1-5,
15
R
6- 0-(сНг)т-А-(СНг) COOR
-RV н.
подвергают взаимодействию с соеди- нением общей формулы
RT 8
I.OOC Яо R it
R
6- 0-(сНг)т-А-(СНг) COOR
-RV н.
подвергают взаимодействию с соеди- нением общей формулы
RT 8










| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных катехина | 1984 |
|
SU1424729A3 |
| Способ получения гетероциклических соединений или их фармацевтически приемлемых солей щелочного металла | 1986 |
|
SU1454249A3 |
| Способ получения производных дигидропиридина (его варианты) | 1983 |
|
SU1258324A3 |
| Способ получения производных пирроло [2,1- @ ] тиазола | 1990 |
|
SU1836374A3 |
| Способ получения гетероциклических соединений | 1985 |
|
SU1470186A3 |
| Способ получения производных индолилпиперидина или их солей | 1989 |
|
SU1814645A3 |
| Способ получения производных тиазола или их аддитивных солей с кислотами | 1988 |
|
SU1753948A3 |
| Способ получения производных имидазола | 1985 |
|
SU1530093A3 |
| Способ получения феноксиалкиловых эфиров или их солей | 1985 |
|
SU1422998A3 |
| Способ получения гетероциклических соединений | 1986 |
|
SU1452481A3 |
Изобретение касаетсд получения производных 1,4 дигидропиридина общей формулы I C(o)ORr , С(0)ОВ2 где ( CHjJm-A-( CHj )„ -NH-CH - -СН(ОН)-1 R, и Rj одинаковые или разные С,-С,-алкил, или низ1чий алкил, пре- рьшаемьй атомом кислорода, или низший алкил, замещенный алицикпической С,-С -группой; R, и R - одинаковые или разные низший алкил; Н;- и К - одинаковые или разные Н, NOj, , галоид, низший алкил или низиая алкокси-, низшая алкилтиогруппа, алкилсульфо- . НИЛ или алкилсульфинил; R., и Rg - одинаковые или разные-Н, галоид, CN, низшая алкокси- или низшая алканоил- аминогруппа или с атомом азота наф- тил; А - простая связь, -СН-СН-; В - простая связь; m,n - одинаковые или разные - целые числа О или 1-5, обладающих Са(2+) антагонистической и адренегической р-блокирзтощей активностью. Цель - создание новых активных веществ указанного класса. Их синтез ведут из соединений формул II и III C(0)OR, И. (II) СО R, (III) где Х,-0(СН2)-А-(СН2)п-Ж,г; R,-Re, п, т. А, В - указаны выше. Новые вещества оказывают гемодинамическое, венечное сосудорасширяющее и /5-адре- ноакцепторное блокирующее действие. 1 табл. со 4 Ю 4 СО см
Diltiazem Propranolol -
НТ
нт - не испытывались
нт
0,063 
| Бюлер К., Пирсон Д | |||
| Органичес кие синтезы | |||
| Ч | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| М.: Мир, 1973, с | |||
| Букса для железнодорожного подвижного состава | 1922 |
|
SU329A1 |
Авторы
Даты
1987-09-30—Публикация
1985-06-27—Подача