Изобретение относится к гибридом- ной технологии и может быть использовано для создания диагностических препаратов.
Цель изобретения - получение мышиной лимфоцитарной гибридомы, продуцирующей моноклональные антитела (монАТ) к гемагглютинину вируса кори, которые обладают высокой авидностью и проявляют иммунологическую активность в нескольких реакциях.
Штамм получают следующим образом.
Самок мышей линии BALB/c массой 8-10 г иммунизируют внутрибрюшинно двукратно с интервалом в две недели
цельным частично очищенным препаратом вируса кори, пропассированным в первичной культуре клеток эмбрионов японских перепелов, выращенных на микроносителях ДЕАЕ - сефадекс
А-50.
Первую иммунизацию проводят вирусным антигеном в полном адъюванте Фрейнда в дозе 5,0 Ij на мышь, вторая иммунизация - в той же дозе в неполном адъюванте Фрейнда. За три дня до слияния интраорбитально вводят 0,1 МП вирусосодержащего материала в солевом растворе в дозе 4,0 Ij на мышь.
СЛ
00
со а со
В качестве злокачественного партнера используют мьппиную лимфоцитар- ную линию NSO в фазе логарифмического роста, Миеломные клетки выраЕ1ивают в среде RPMI-I640 с 0,13% NaHCOj, глюкозой до 4 г/л, 5% сыворотки эмбрионов коров и 57о сыворотки суягных овец (очищены полиэтиленгликолем), пируватом натрия 0,05 мг/л, оксало- ацетатом 0,15 мг/л, инсулином 0,2 ед/мл, 2-меркаптоэтанолом 5 0 М, HEPES 5-10 мМ, гентамицином 50 мкг/мл, Имунные спленоциты получают на третий день после бустерног инъекции антигена из стерильно извлеченных селезенок, Спленоциты извлекают путем мисггократного введения в пульпу селезенки 0,1-0,2 мл холодной ростовой среды RPMI-1640 с помощью тонкой иглы со шприцем. Извлечение спленоциты собирают в пластиковые охлажденные пробирки, осаждают центрифугированием при 1000 об/мин в течение 10 мин, осадок клеток с эритроцитами обрабатывают в течение 5 мин на холоду 0,8 3%-ным раствором Ш 4С1 в пятикратном объеме, Поспе лизиса эритроцитов клетки повторно
саждают и дважды промывают в бессы- вороточной среде RPMI- 640c Для слияния используют 50%-ный раствор поли- этиленгликоля с м,в, 1000, Иммунные спленоциты сливают с клетками NSO в соотношении 4:1 и распределяют на двадцать 96-луночных пластик со сло- ем-кормилкой из непммунных спленоци- тов. Селекцию гибридных клеток проводят в среде HATj составленной ил ростовой сроды с И гипоксантина (Н)
I ,6 -lO М тимидина (Т) и 4 амино- птерпна (А),
Начиная с трех суток с момента культивирования и в последующие дни, в лунки культуральных пластин каждые дня вносят по 2 капли свежей сепективной среды или из пластин удаляют 0,1 мл культуральной среды и заменяют на свежую. Начиная с 20 сут с момента культивирования, клетки из лунок, в которых наблюдается рост гибр1здньгх клеток, пересевают в 24-лу ночные пластины со слоем-кормилкой из неиммунных спленоцитов. Неиммунные спленоциты ресуспендируют в гиб- ридомной среде ИХ (селективная среда без аминоптерина) и по 0,1 чл распределяют в 24-луночные пластины (спленоциты, полученные от одной
М1.1ШИ, распределяют на две 24-луночные пластины), Кпоны гибридных клеток, раступще в 24-луночных пластинах со слоем-кормилкой, выращивают до фор№1рования сплошного слоя, а затем клетки пересевают в 24-луночные nnacTHiibi без слоя-кормилки, После формирования сплошнот о слоя клеток проводяг первичный скрининг культуральных жидкостей на наличие вирусо- специфических антител в твердофазном иммyнoфep eнтнoм анализе (PiOA), В качестве твердой фазы используют клетки Vero, инфицированные вирусом кори, штамм Л-16, Антителопродуцирую щие клоны гибридных миелом выр. ;щипаю в пластикоиых флаконах площадью 25 см со слоем-кормилкой из сплеио- цитоп и после накоппения клеток в достаточном количестве (сплогинор покрытие ростовой поперхно; ти флакона) проводят оценку монАТ и культуральных жидкостях на активность и слеЦ;-:- фичность. По данным проведенного ис- сле17,овапия осуществляют пыбор кленов для их накопления в массовой в:ульту- ре и криоконсервацир.
В результате счияшш получена коллекция гибридов, продуцирушщтх -.jbAT к вирусу кори ( штамм Л-16),. Из них практический интерес представляю гпбридома ВК-93,2, г{онАТ класса IgG 2а, Hanyjai fHHbie к гемагглютинину р-нруса корИ: Харак- TtTpHCTHKa активности иммуFIOглобул - HOR, продуцируеЬмх г-нбр домоч ВК- 93,2; представлена в табл,1,
Приведенные данные позволяют заключить, что монАт, продуцируемие гибридомой ВК-93„2, обладают одинаки вой высокой реактивностью с двумя исследованными штз 1мами вируса кори (штамм Л-16 и Ш гамм LEC-вирус KOIJH) в различных тестах и не выявляют вирус чумы плотоядных (штамм ЭГМ)«
Штамм гибридомь депонирован под номером BCKJ (И) № 148Д и имеет следующие признаки,
Культуральные признаки.
Стандартные условия выращивания о Среда дня культивирования - RPMI-164 с 0,13 MaHCOj, глюкозой до 4 г/л, 5% сыворотки эмбрионов коров и 5% сыворотки суягных овец (очищенна с помощью полиэтиленгликоля),, пируватом натрия 0,05 иг/мл, оксалоацетатом 0,15 иг/мл, инсулином 0,2 ед/мл, 2-мегкаптоэтанолом 5-10 М. HFPES
5-10 мМ. Температура культивирования 36,5 С. Клетки растут в суспензии, обладают слабой адгезивной способностью к поверхности пластика или стекла. Посевная доза 200-300-10 клеток/мл, кратность рассева 1:4-1:6 два раза в неделю.
Культивирование гибридомы в организме животного.
Самок мышей линии BALB/c в возрасте 2-2,5 мес сенсибилизируют 0.5 мл пристана внутрибрюшинно за 7-10 дней до введения 2-4-10 гибридных клеток, через 10-14 дней формируется асцитная опухоль. Перевиваемост гибридомы в 100% случаев.
Характеристика полезного продукта
Гибридтя линия ВК-93.2 продуцирует моноклональные антитела, выявляемые в иммуноферментном анализе (ГТФА), п рс-акции непрямой иммунофлуо ресценции (НИФ), в реакции торможени гемаглютинации (РТГА), в реакции нейтрализации на культуре клеток (Н).
Активность антител в иммунных ас- цитных жидкостях: в ИФА - 1:720000; н НИФ - 1:32000; в РТГА - 1:5120; ;з РН -1:64 МонАТ относятся к классу и гмуноглобулинов G2a. Стабильность продуцирования антител сохраняется на протяжении 50 пассажей в культуре клеток (время наблюдения) и 6 пассажей на мьшах линии BALB/c (время наблюдения) .
Способ криоконсервации.
Среда для замораживания включает сыворотку эмбрионов коров 90%, ди- метилсульфоксид 10%. 1 мл клеточной суспензии с плотностью не ниже 2-10 жизнеспособных клеток, ресуспендиро- ван1{ых в холодном криоконсерванте, переносят в пластиковые 1,8-мнллит- ровые ампулы, укладывают в пеноплас- тиковую коробку с толщиной стенок не меньше 1,5 см и немедленно помещают на холод - (-70 )-(-80 )° С, .На следующие сутки ампулы переносят в жидкий азот Замороженные ампулы оттаивают в воде с температурой 37-39°С. Клетки разводят в 10 раз сывороткой эмбрионов корон или суягных овец и осаждают центрифугированием при 500 об/мин в течение 10 мин. Восстановленные клетки ресуспендируют в ростовой среде в концентрации 2.5
40--3,0-10 жизнеспособных клеток в 1 мл, переносят в пластиковые куль- туральные флаконы. Жизнеспособность
после размораживания составляет 60- 70% и устанавливается по дифференциальной окраске клеток с помощью 0,25%-ного раствора трипанового синего, приготовленного на физиологическом фосфатно-буферном растворе, рН 7,2-7,3.
Пример 1. На сонове монАТ, продуцируемых гибридомой ВК-93,2, создан диагностический препарат пероксидазный конъюгат для иммуно- ферментного анализа. Основной для его получения является иммунная асцитная жидкость (ИАЖ) с титром в ИФА 0,72-10. Иммуноглобулины из ИАЖ высолены с помощью 50%-ного сульфата аммония а Фракция IgG очищена методом аффинной хроматографии на белке А - сефарозе 4В,
В табл. 2 представлены результаты
экспериментов по идентификации вируса кори в прямом иммуноферментном анализе с помощью конъюгата на основе монАТ, продуцируемых гибридомой ВК-93.2„
Как видно из табл.2, конъюгат, приготовленный на основе ИАЖ, содержащей монАТ к гемагглютинину, вируса кори (штамм Л-16), специфически выявяет вирус кори (штамм Л-16, и вирус
кори (штамм LEC) и не выявляет вирус чумы плотоядных.
Использование гибридомы позволяет получать монАТ, специфичные к гемаг- глютинину вируса кори.
Формула изобретения
Штамм гибрдикых клеток животных us rausculis BCKK(II) N 148Л, используемый для получения моноклональных антител к гемагглютинину вируса кори.
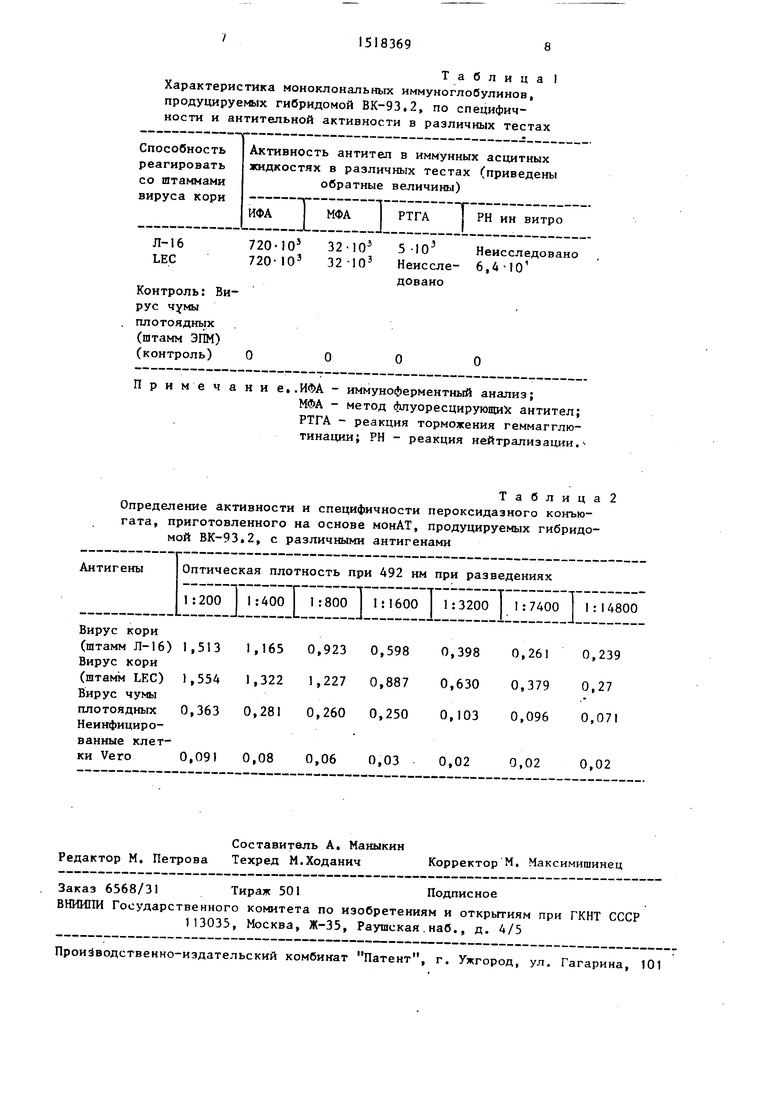
Таблица 1
Характеристика моноклональных иммуноглобулинов, продуцируемых гибридомой ВК-93,2, по специфичности и антительной активности в различных тестах
Способность Активность антител в иммунных асцитных реагировать жидкостях в различных тестах (приведены со штаммамиобратные величины)
вируса кори гг
ИФА МФА РТГА РН ин витро
Л-16 720-10 32-10 5-10 Неисследовано LEG 720-10 32-10 Неиссле- 6,4-10
довано
Контроль: Вирус чумы плотоядных (штамм ЭПМ) (контроль) 0000
Примечани е..ИФА - иммуноферментный анализ;
МФА - метод флуоресцирующих антител; РТГА - реакция торможения геммагглю- тинации; РН - реакция нейтрализации,
Таблица2
Определение активности и специфичности пероксидазного конъю- гата, приготовленного на основе монАТ, продуцируемых гибридомой ВК-93.2, с различными антигенами
Антигены Оптическая плотность при 492 нм при разведениях
1:200 I 1:400 1:800 1:1600 1:3200 1:7400 1:14800
Вирус кори
(штамм Л-16) 1,513 1,165 0,923 0,598 0,398 0,261 0,239 Вирус кори
(штамм LEC) 1,554 1,322 1,227 0,887 0,630 0,379 0,27 Вирус чумы
плотоядных 0,363 0,281 0,260 0,250 0,103 0,096 0,071 Неинфицированные клетки Vero 0,091 0,08 0,06 0,03 0,02 0,02 0,02
Составитель А. Маныкин Редактор М. Петрова Техред М.Ходанич Корректор М. Максимишинец
г --гт1-- - - -
Заказ 6568/31 Тираж 501Подписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКИТ СССР 113035, Москва, Ж-35, Раушская.наб., д. 4/5
Производственно-издательский комбинат Патент, г. Ужгород, ул. Гагарина, 101


Изобретение относится к области гибридомной технологии и может быть использовано для создания диагностических препаратов. Цель изобретения - получение мышиной лимфоцитарной гибридомы, продуцирующей моноклональные антитела (монАТ) к гемагглютинину вируса кори, которые обладают высокой авидностью и проявляют иммунологическую активность в нескольких реакциях. МонАТ могут быть использованы в качестве иммунодиагностикумов. Штамм депопирован под номером ВСКК(П) N148Д. ПРОДУЦИРУЕТ МОНАТ КЛАССА JGG2A, СПЕЦИФИЧНЫЕ К ГЕМАГГЛЮТИНИНУ ВИРУСА КОРИ. МОНАТ ВЫЯВЛЯЮТ В ИММУНОФЕРМЕНТНОМ АНАЛИЗЕ, АКТИВНОСТЬ В ИФА 1:72000. Продукция антител сохраняется в течение 50 пассажей. На основе монАТ к гемагглютинину вируса кори создан пероксидазный конъюгат, который может быть использован для выявления JGM и JGG антител человека к вирусу кори. 2 табл.

| Birrer M.I | |||
| Virology, v | |||
| Приспособление для останова мюля Dobson аnd Barlow при отработке съема | 1919 |
|
SU108A1 |
| Подвесная канатная дорога | 1920 |
|
SU381A1 |
Авторы
Даты
1989-10-30—Публикация
1987-10-19—Подача