.L
Г|1(,о-(о)-н11-Гп -о-1-о „
СН. №-CHi-0-(o)-X4
о
-гДгК11-(§ -0-СН,-СП-СНг
нУнY
) , Я п
F
m-(c))u-f)
HoXoVwi
( НуН
ш и;оупи
51529687б
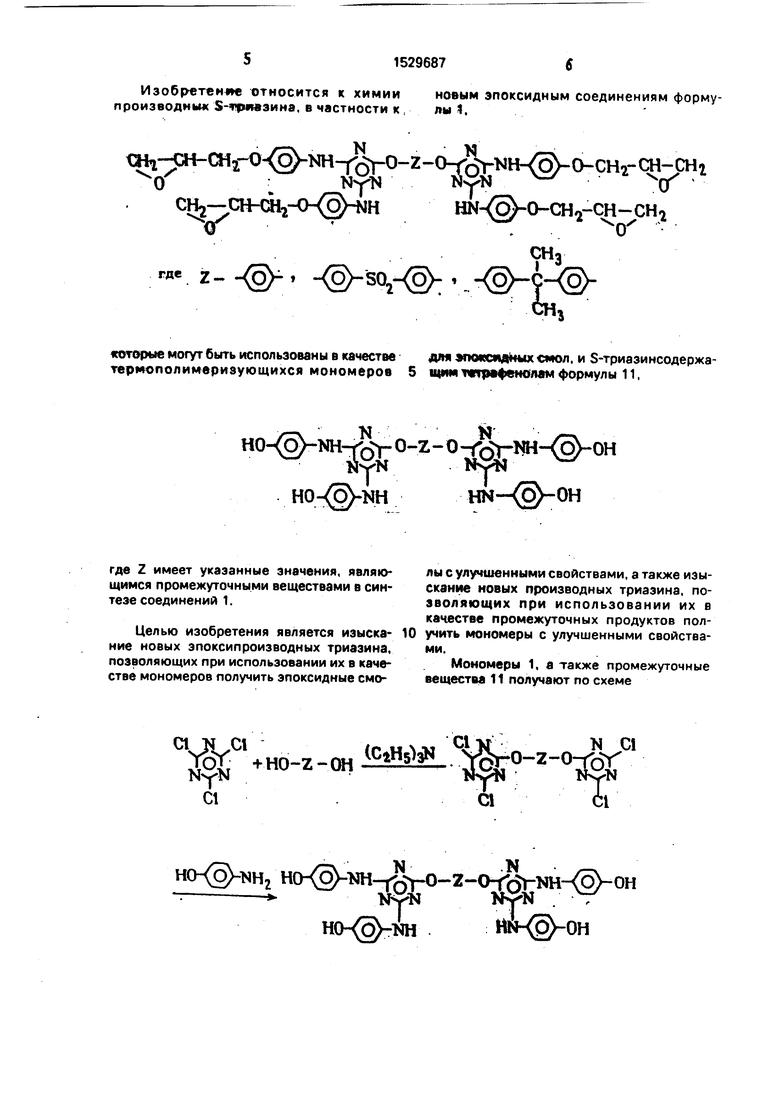
Изобретемте относится к химии новым эпоксидным соединениям форму- производниж 5-ч р 1вэина, в частности к , лы 1.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения смеси 2-оксо-2,3-дигидро-4,6,-бис-(3 @ -диэтиламинометилен-4 @ -оксифенил)-1,3,5-триазина и 2,4,6-трис-(3 @ -диэтиламинометилен-4 @ -оксифенил)-1,3,5-триазина | 1985 |
|
SU1313854A1 |
| Эпоксидная композиция | 1975 |
|
SU688135A3 |
| Способ получения замещенных 4,5-этилендитио-1,3-дитиол-2-тионов | 1986 |
|
SU1428753A1 |
| Способ получения производных 1,3-пропилендифосфоновых кислот | 1985 |
|
SU1375141A3 |
| ТРИАЗИНСОДЕРЖАЩИЕ АНИОННЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1997 |
|
RU2170731C2 |
| Способ получения производных тиазолидина | 1984 |
|
SU1240355A3 |
| Хлорсодержащие ди- или триэпоксиды в качестве мономеров для получения эпоксидных полимеров | 1981 |
|
SU1126571A1 |
| Бис-/2-(п-оксифениламино)-нафтил/-метан,проявляющий свойство стабилизатора полистирольных пластиков | 1979 |
|
SU857113A1 |
| Способ получения модификаторов оптических эпоксидных композиций | 1986 |
|
SU1395634A1 |
| Способ получения замещенных винилцефалоспоринов | 1984 |
|
SU1407400A3 |
Изобретение относится к гетероциклическим соединениям, в частноаи к 5-триазиисодержащим эпоксидным соединениям ф-лы I, где Z которые используются в качестве термололимерм- зующихся мономеров для лолимеров и S-триазии- содержащим тетрафенолам ф-лы II , где используются в качестве промежуточных соединений для синтеза S-триазинсодержащих элоксидных соединений. Цель - выявление новых соединений при использовании которых получают элоксидные смолы с улучшенными свойствами. Получение соединений формулы II ведут конденсацией цианурхлорида с соот- ветств тощим бис-фенолом в среде диоксана в лрисутствии триэтиламина На образующееся вещество действуют 4-аминофеноТ10м в присутствии ацетата натрия Полученные целевые соединения фор-лы II конденсируют с эпихлоргидрином и об

Ш1--сн-Шг о-@-ын-упгО-2-о-( 0NVNNvN
Nyt J-CH-CH2-0-@-NI
1
ш-ю -о-сн сн- сн
0
где z .УОГ
1юторые могут быть использованы в качестве дм эгммесмдйых смол, и S-триазинсодержа- термополимеризующихся мономеров 5 щим 1«ф фен0лам формулы 11,
КN/ ч
Ho--(o)-iw-Yor - - -TOT-W- -OH
где Z имеет указанные значения, являющимся промежуточными веществами в синтезе соединений 1.
Целью изобретения является изыскание новых зпоксипроизводных триазина. позволяющих при использовании их в качестве мономеров получить зпоксидные смо Чно-г-он 2
N Y N С1
luTJ
HC)-(g), H()-(im-YKr-o-z-o-rKrNH- o)-OH
. V
НОЧОЬШHN- 0)-OH
( NvN
1
ш-ю -о-сн
лы с улучшенными свойствами, а также изыскание новых производных триазина, позволяющих при использовании их в качестве промежуточных продуктов пол- 10 учить мономеры с улучшенными свойствами.
Мономеры 1, а также промежуточные вещества 11 получают по схеме
IN С1 0-z-OYoV
NY
Cl
CH.,-CH-CH7.-0- Oy-NHn QVO-Z-0-fQ №--(
I Cl
OH
)H Cl
CHn-CH-CH,-0 I I
Cl OH
MaOH
CH -CH-CH -O
CHo-CH-CH, i
-o
Пример 1. (4 -оксифенила- мино) 1, 3. 5-триазинилокси -бензол.
к 92.0 г (0,5 моля) цианурхлорида в 400 см диоксана при 5°С приливают раствор 25,3 г (0,25 моля) гидрохинона в 100 см диоксана. При интенсивном перемешивании в течение 20 мин к смеси прибавляют 70 см (0,5 моля) триэтиламина, затем смесь нагревают до 80°С и выдерживают в течение 1 ч. Охлажденную до комнатной темпе- ратуры массу фильтруют и к раствору в течение 0,5 ч добавляют смесь 109 г (1,0 моль) 4-аминофенола и 82 г (1.0 моль) плавленного ацетата натрия в 300 см диоксана. Реакционную массу при перемешивании нагревают до 80°С, приливают 100 см воды и выдерживают в течение 1 ч. затем массу выливают в 2000 см холодной воды. Осадок отфильтровывают, промывают водой и высушивают. Выход 165 г (94.8%). т. пл, 257- 259°С.
Найдено, %: С 62.39: Н 4.07; N 20.24.
СзбН28М1оОб.
Вычислено, %: С 62.07; Н 4.02; N 20,11.
ИК-спектр (КВг. );3290-3400; 1590-1615.
Пример 2. Бис-{2.4-ди(4 -глицидилок- сифениламино)-1. 3. 5-триазинилокси бен- зол.
К 34.8 г (0.05 моля) .4-ди(4 -окси- фениламино)-1, 3, 5-триазинилокси бензола в 400 см эпихлоргидрина добавляют 0.48 г (0.005 моля) триметиламина солянокислого и кипятят в течение 2 ч. После охлаждения до комнатной температуры к реакционной массе при интенсивном перемешивании в течение 1 ч порциями прибавляют 9.0 г (0.225 мояя) тонкоизмельченного гидрокси)H Cl
O-CHj-CH-CH
OH
I
Cl
СНгч,
0-z-o
Ъ1Н
да натрия. Смесь выдерживают при перемешивании 1.5 ч и фильтруют. Раствор промы- вают 4 порциями воды по 100 см и растворитель отгоняют при 60-79°С в вакууме. Осадок промывают спиртом, водой. Выход конечного продукта 48.5 г (91,5%). т. пл.124-125°С.
Найдено. %: эпоксидные группы 18.6; С 62.28; Н4.52; N 15,01.
C48H44NloOlO.
Вычислено. %; эпоксидные группы 18,7; С 62.60; Н4.78; N 15.22.
ИК-спектр (КВг. v , см): 3310-3390; 1580-1620; 1040-1090.
Пример 3. .4-ди(4 -оксифенила- мино)-1. 3, 5-триазинилокси дифенилсуль- фон. Получение и выделение продукта аналогично примеру 1, только в качестве бис-фенола берут 62,5 г (0.25 моля) 4.4-диок- сидифенилсульфона. Выход 202 г (96.7%), т. пл.249-252°С.
Найдено. %; С 59,83; Н 4.06; N 16.84,
C42H32Nlo08.
Вычислено, %; С 60.29; Н 3.83; N 16,75. И К-спектр 1580-1620.
(КВг. ):3300-3400,Пример 4. .4-ди(4 -глицидолок- сифениламино)-1. 3. 5-триазинилокси дифе- нилсульфон. Получение и выделение продукта аналогично примеру 2. только в качестве тетрафенола берут 41.8 г (0.05 моля) .4-ди(4 -оксифениламино)-1, 3, 5- триазинилокси дифенилсульфона. Выход 45.0 г (97.8%); т. пл. 90-95°С.
Найдено, %; эпоксидные группы 15,9; С 60.59; Н 4.31; N 12,91.
C54H48NloOl2.
Вычислено, %; эпоксидные группы 16,2; С 61,13: Н4/53; N 13.22.
ИК-спектр (КВг. ): 3348; 3060; 1580-1610; 1340-1360; 1080-1120.
Пример 5. .4-ди(4 -оксифенила- мино)-1. 3. 5-триазинилокси}-2.2-дифенилп- ропан.
Получение и выделение продукта аналогично примеру 1, только в качестве бис-фенола берут 55 г (0.25 моля) 4.4-ди- оксифенилпропана. Выход 197 г (97,3%); т. пл. 290-294 С.
Найдено, %: С 65.58; Н 5.00; N 17.19.
C45H38Nlo06,
Вычислено, %; С 66,34; Н 4,67; N 17.20.
ИК-спектр (КВг. Vсм):3290-3400; 1590-1620.
Пример 6. Бис-{2.4-ди(4 -глицидилок- сифениламино)-. 3. 5-триазинилокси}-2,2- дифенилпропан. Получение и выделение продукта аналогично примеру 2, только в качестве тетрафенола берут 40.7 г (0.05 моля) бис-{2.4-ди(4 -оксифениламино)-1. 3. 5Свойства соединений I и их известных аналогов III а также полимеров на их основе
триазинилокси -2.2-дифенилпропана. Выход 49.2 г (94,8%). т. пл. 95-100°С.
Найдено. %: эпоксидные группы 16.2; С 65,52; Н 5.02; N 13.11
C57H54N40040.
Вычислено. %: эпоксидные группы 16,6; С 65,90; Н 5,20; N 13.49. ИК-спектр (КВг. VCM ); 3340. 3050.1580,- 1620.1080-1120.
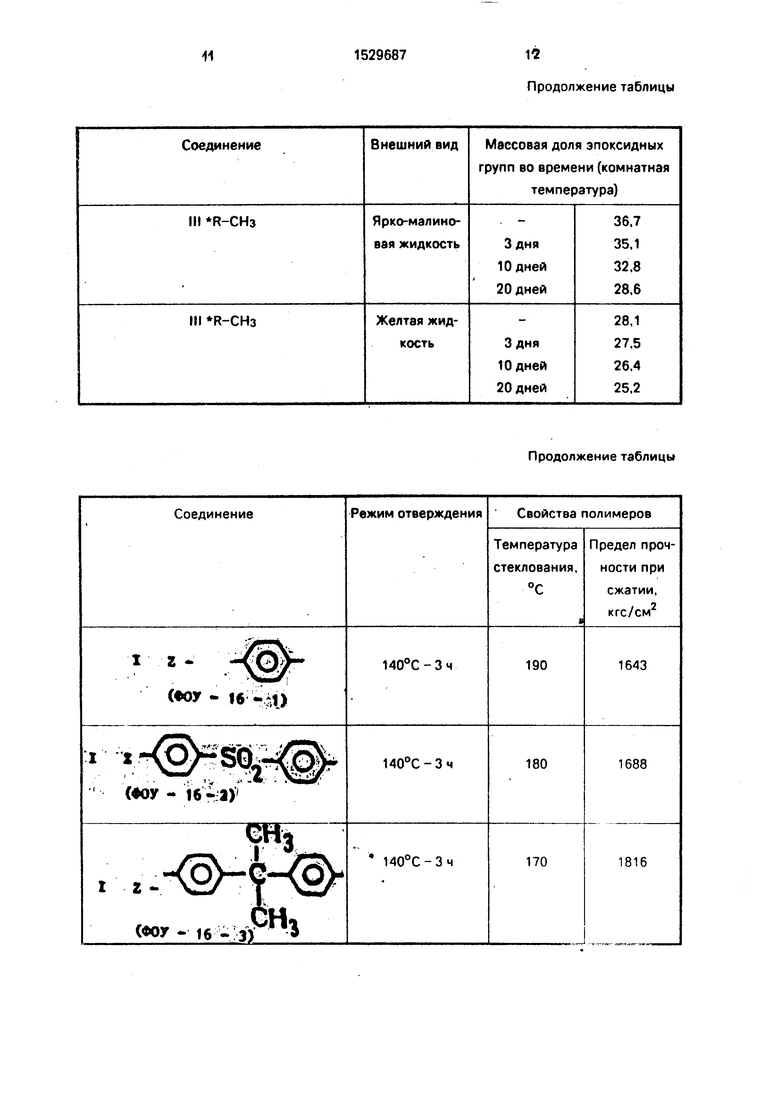
Данные по свойствам соединений формулы I и полученных полимеров на их основа приведены в таблице.
Как видно из таблицы предложенные II позволяют получить соединения 1 с улучшенными свойствами (самоотверждение происходит за более короткое время), а также соединения I позволяют получить полимеры с высокими прочностными показателями при снижении времени и температуры переработки.
(56) Авторское свидетельство СССР N 765267. кл. С 07 D 405/14, 1978.
Продолжение таблицы
Продолжение таблицы
1,4-Диглицидил-1,2,4-триазолтионы-5 формулы
.V/CH-CH,-y
cHi-qj i
где R -.-СНз, СбНб
Формула изобретения 1. S-триазинсод соединения формулы
$$$
меров для полимеров.
,общей формулы
но
ob «- -0-zo-j|- «.OH
V-° T °- - &-KO -O-CH..,,
сп,-си-ачч он-нH}.XoXo-o,,-cfi-GH, - 1
сн,
где
где
)- -(o -sOj- o -. -(
CHJ )
См,
в качестве промежуточных соединений для
в качестве термополимеризующихся моно- Jliri ® поксидных - -.соединений.
Составитель Н. Куликова . ,
Редактор М. Самерханова Техред М.МоргенталКорректор С.Патрушева
Продолжение таблицы
но
ob «- -0-zHO-@-NH
где
z- - (so -.
CHJ )
Авторы
Даты
1993-10-15—Публикация
1988-03-16—Подача