to
f560
-тиазолидин, т. пл,
Найдено, %: С 52,72 Н 4,18- 16,49.
СуН,„:СШз8(251, 74)
Вычислено, %: С 52,48; Н 4,00; 16,69.
ИК-спектр (КВг): 2185 , , 1092 см-, -Ar-Cl.
ЯМР-спектр (CDCI; + ДМСО - d): ,3. м.д. мультиплет (2) -S-GHj ; ,8 м.д. мультиилет (2) N-CHj- (ге- ероцикл.) 4,50 м.д, синглет (2) N-CHj -(СбН4-С1); 7,12 м.д. синг- е.т (4) .
2. 2-Цианимино-3-(3,4-дихлорбен- ил)-тиазолидин, т. пл. 130-132 с.
Найдено, %: С 46,12, Н 3,18 11,22. - С, EjClzNjS (286,18)
(5
Изобретение относится к полу 1ения новых биологически активных химических соединений, а именно к способу получения новых производных тиазолидина, обладающих противоязвенной активностью.
Цель изобретения - получение но- вьпс производных тиазрлидина, обладаю щих высокой противоязвенной актив- . ностью - новым видом активности в ряду производных тиазоЛидина.
При м е р 1. 3-Бензш1-2-:-цИан- иминотиазолидин (соединение А). .
2,21 г (13,2 ймоль N-бензид-цис- теамина ( т.кип.90°С при 0,2 мм рт.ст.) и ,1,98 г (13,5 ммоль) диметилово- го эфира дианиминодитиоугольной кислоты кипятят в 10 мл этанола;
Интенсивное газовьщеление прекращается за. 15 мин. Реакционнзпо смесь вьщерживают в течение ночи при и затем отфильтровывают. Получают 2,57 г 3-бензш1-2-цианиминотиазоли- дина (89,6% от теории), т. пл. 102- 104°С.
Найдено, %: С 60,98 Н 5,02 N 19,57} S 14,96.
Вычислено, %: С 60,80 ; Н 5,10;. N 19,34i S 14,76.
ИК-спектр (КВг): 2190 см- , 30 1570 см , . ;;;;C N (широкая).
ЯМР-спектр OCDClj): 3,38 м.д. мультиплет (2), 3,85 м.д. мультиплет (2), N (гетероциклич.)j 4,65 м.д. синглет (1), N (фенил) 7,38 м.д. синглет (5) - Аг-Н.
Согласно примеру 1 получают сле- дзтощие соединения:
1. 2-Цианимино З-(4-кцорбензил)- 131-133°С.
1240355 способам Вычислено,
S 11,21.
ИК-спектр ( 1570 см
ЯМР-спектр типлет (2), -S плет (2), N 4,56 м.д. синг гдихлорфенил) плет (3), -Аг3. 2-Циаяим -тиазолцдин, т
Найдено, % N 21,46.
C,,H,,N,0,
Вычислено, N 21,36.
ИК-спектр ( 1575 см , :::c 20-NO.
ЯМР-спектр 3,4 м,д. мульт 3,8 м.д. мульт 4,65 м.Дс синг 25 n-NOj/i 7,37 -Аг-Н (2,6), 8 (2), -Аг-Н (3,
4. 2-Цианим бензил)-тазоли
Найдено, %: N 20,01.,
С,,Н, Вычислено, N 20,13.
ИК-спектр ( кая), ОН; 2190
35
, 1522, 13
40
45
50
55
ЯМР-спектр 3,4 м.д. мульт 3,8 м.д. мульт тероцикл) ; 4,5 :;N-CH2-(2-OH, триплет (1), мультиплет (2) дублет (1), -О
Найдено,- %: S 13,75, N 17,8
С, Н4, N3OS
Вычислено, % S 13,75rN 18,0
ИК-спектр (К -ОН; 2190см .
ЯМР-спектр 3,3 м.д о мульти 3,7 МоД, мульти тероцикл.), 4,4 N-CH2- (оксиф
to
(5
0
40355 Вычислено,
%: С 46jl6 Н 3,17
S 11,21.
ИК-спектр (КВг): 2190 , 1570 см 1060 , Ar-Gl.
ЯМР-спектр (CDClj): 3,4 м.д. мультиплет (2), -S-CHj- , 3,7 м.д. мультиплет (2), N - CHj- (гетероцикл.); 4,56 м.д. синглет (2), iN-CH2-(3,4- гдихлорфенил) 6,9-7,Ь м.д. мультиплет (3), -АгН.
3. 2-Циаяимино-3-(4-нитробензил)- -тиазолцдин, т. пл. 171°С.
Найдено, %: С 50,36; Н 3,94; N 21,46.
C,,H,,N,0, (262,29)
Вычислено, %: С 50,37; Н 3,84; N 21,36.
ИК-спектр (.КВг): 190 , 1575 см , 1505 - 1343 , 20-NO.
ЯМР-спектр (CDClj + ДМСО - dg): 3,4 м,д. мультиплет (2), -S-CH - 3,8 м.д. мультиплет (2),O N-CHj-, 4,65 м.Дс синглет (2), 5 n-NOj/i 7,37 м.д. дублет Г9Н,,Л (2), -Аг-Н (2,6), 8,05 м.д. дублет (9Н.). (2), -Аг-Н (3,5).
4. 2-Цианимино-3-(2-окси-5-нит;ро- бензил)-тазолидин, т. пл. 253-255 С.
Найдено, %: С 47,78, Н 3:,71;- N 20,01.,
С,,Н, (278,29) Вычислено, %: С 47,47; Н 3,62 N 20,13.
ИК-спектр (ЮВг): 3100 см (широкая), ОН; 2190 , 1575 ,
5
, 1522, 1338 см
-NO,
0
5
0
5
ЯМР-спектр (СВС1з ДМСО - dg): 3,4 м.д. мультиплет (2), -S-CHj-i 3,8 м.д. мультиплет (2),N-CHj- (ге- тероцикл) ; 4,54 м.д. синглет (Z), :;N-CH2-(2-OH,5/N02-C6H3); 6,88 м.д. триплет (1), Аг-Н (3); 8,00 м.д. мультиплет (2), -Аг-Н (4,6); 5-9 м.д. дублет (1), -ОН. .
Найдено,- %: С 56,70; Н 5,07; S 13,75, N 17,83 .
С, Н4, N3OS (231,29)
Вычислено, %: С 56,63; Н 4,75; S 13,75rN 18,02.
ИК-спектр (КВг): 3260, 1230 , -ОН; 2190см , , 1570 см- , .
ЯМР-спектр (CDClj + ДМСО г- d,) : 3,3 м.д о мультиплет (2), -S-CHj-,- 3,7 МоД, мультиплет (2),N-CH2- (ге- тероцикл.), 4,48 м.д. синглет (2) N-CH2- (оксифенил) 6,5-7,4 м.д.
20
ультиплет (4), -Arr-H,« 8,6 м.д. дубет (1), -ОН.
5.2-Цианимино-3-(1-нафтилметил)- тиазолидин,.т. пл, 167 С.
.Найдено, %: С 65,32, Н 4, N 15,78; S 11,96..
С,уК„Ыз8 (267,34)
Вьиислено, %: С 67,39; Н 4,90; N 15,72 S 12,00.
ИК-спектр(КВг): 2180 см, О 1570 .
ЯМР-спектр (ДМСО - dg): 3,4 МоД. мультиплет (4), -S-CHj-; 3,7 м.д. мультиплет (4), -N-CHj- (гетероцикл.); 4, 5р м.д. синглет (4), -N-rCHj- (фени-15 лен); 7,18 м.д. синглет (4), тАг-Н.
6.2-Цианимино-Зг(6-метил-2-пири- дилметил)-тиазолвдин или по другой
номенклатуре 2-(2-цианимино-3-тиазо- лидинил)-метш1}-5-метилпиридин, т. пл. 114°С.
.Найдено., %: С 56,77; Н 5,12, N 24,18.;.. .. ./
C,, H,jjN4S (282,30)
Вычислено, %: С 56,67, Н. 5,20, N 24,12.
ИК-спектр (РГ): 2190 см, 1570 см , .. .
ЯМР-спектр (CDClj): 2,48 м.д. синглет (3), -пиридил-СНд 3,3 м.д. 0 мультиплет (2), -S-CH -, 3,9 м„д. мультиплет (2), . 4,60 м. д. синглет (2), 6,9 м.д. дублет (2),-PY-2,5 Hi7,4 м.д.(1),-РУ4-Н.
7.2-Цианимино-3-(6-дихлорметил- 35- -2-пирндилметил)-тиазолидин или по другой номенклатуре; 2- 2- цианимино-З- -тиазолидинил)-метил -6-дихдорметил- пйридин, т. пл. 122°С, .
Найдено, %: С 43,91, Н 3,46;.40
S 10,80..
C«H,eCl,N4S (301,19)
5
Вычислено, %: С 43,86, Н 3,34| S 10,64.
; ИК-спектр (КВг): 2180 см , 1560 (широкая), 718 см , -СН-С1.
ЯМР-спектр (CDClj): 3,34 м.д, триплет (2),-S-CHj-j 3,97 м.д. триплет (2), : N-CHj -, 4,62 м.д. синглет (2), N-CHj- (фенил)i 6,50 м.д. синглет (1), -PY-CHjj-i 7,0-7,8 м.д. мультиплет (3), PY-H.
В. 3-Вензш1-2-(карбамош1Иминотиа- золидин), т. пЛ. lAS C.
Найдено, %: С 56,10; Н 5,46; N 18,10.
N,OS (235,31)
Вычислено,. %: С 56,15 И 5,57 N 17,86.
-I
ИК-спектр (КВг): 3320, 3260 , NH, 1645 , 1540см ,
2
ЯМР-спектр (CDCl + ДМСО - dg): 3,05 м.д. триплет (2), -S-GHj-i 3,05 м. д. триплет (2), iN-CHj-;. (ге- тероцикл)i 4,75 м.д. синглет Л2), N-CHj- (фенил); 5,6м,д. -NHjj 7,32 м.д. синглет (5), -Аг-Н.
9. 2-Цианимино-3-(2-фурилметил)- тиазолидин, т. пл, 124-125 С,,
Прим е р 2. 3-Вензш1-2-нитро- метилентиазолидин.
3,34 г (20 ммоль) N-бензилцисте- амина и 3,3 г 1,1-бис-метилтио-2- -нитроэтилена в 50 мл этанола кипятят с обратным холодильником 1. ч. Газовьщеление прекращается после 20 мин кипячения„ После кипячения в течение 1 ч реакционную смесь охлаждают, осадившийся продукт отфильтровывают, получают 4,52 г неочищенного плавящегося при 136-138 6 З-бензил-2- -нитромётилентиазолидина. После пе- рекристаллизации из 140 мл этанола получают 4,08 г чистого продута, т. пл. .
Найдено, %: С 55,81 Н 4,99i N 11,89.,
С„ H jNjOjS (236,30)
Вычислено, %: С 55,91, Н 5,12, N 11,86.
ИК-спектр (КВг): 1633 , 1354 см - , -NO,.
1535, 1354 см - , -NO . ЯМР-спектр (CDClj): 3,1 м.д. триплет, -S-CHj-j 3,8 м.д. триплет, N-CHj- (гетероциклич.); 4,43 м.д, синглет, ::;N-CHj-()V 6,97 м.д. синглет, 7,0-7,3 м.д. мультиплет, Аг-Н,.
Примерз. 2-Цианимино-3-(4- -метоксибензил)-тиазолидин.
3,65 г (23,5 ммоль) диметилового эфира цианиминодитиоугольной кислоты (чистота 94%) и 5,91 г (30 ммоль) Ы-(4-метоксибензил)-цистеамина в. 30 мл этанола кипятят до прекращения вьщеления метилмерк птана. Затем ре акционную смесь, вьшаривают и кристаллический остаток передристаллиэуют из 15 мл изопропанола. Получают 5,35 г 2-цианимино 3-(4-метоксибен- зил)-тиазолнцина (92% от теории), т. пл. 99-102 С.
Найдено, %: С 58,33; Н 5,17. . (247,31)
Вычислено, %: С 53,28; Н 5,30.
ИК-спектр (КВг): 2840 , -О-СН, 2185 ; 1570 см , 1608, 814 , -Аг.
ЯМР-спектр (CDClj): 3,3 м.д. муль- типлет, -S-CHj-; 3,7 м.д. мультиплет b;N-CHj-i 3,75 м.д. синглет, -0-СНз , 4,43 м.д.. синглет, ji N-CH -/Cg Н, /} 6,9 м.д. квадруплет, Ar-Hо
Используемьй в качестве исходного соединения N-(4-метоксибензил)-цис- теаьшн получа1от следуняцим образом.
4-Метоксибензальде1 ид вводят во взаимодействие с дистеамином, полученный 2-(4-метоксифенил)-тиазолидин (TO пЛо 93-94 с) восстанавливают в изопропаяоле боргядридом натрия, N- -(4-метоксибензш1)-цистеамин представляет собой маслообразный продукт т. кип. при 0,4 мм рт. ст. 120-125 С
Найдено, %: N 20,38; S 15,44.
C,HqN,,OS (207,25) . .
. Вьтчислено, %: N 20,28 S 15,47.
ИК-спектр (КВг): 2185 , 1570 см , 123.8 , С-О-С 795 см.- .
ЯМР-спектр (СОС1з): 3,3 м.д. мультиплет, S-CHj-; 3,7 м.д. мультиплет, N-CHj- (гетероциклич.)j 4,.57 м.д. синглет, N-CHj-Аг 6,3 м.д. дубл ет, Аг-(3,4)Н} 7,3 м.д. мультиплет, -Аг(.
2-Цианимино-3-(4-метилбензил)-тиа золидин, т. пл. 102-104 с.
Найдено, %: С 62,16; Н 5,52- S 13,96.
(231,31) :
Вычислено, %: С 62,26 Н 5,66) S 13,85.
ИК-спектр (КВг): 2190 CM- ,, 1590 см- , -C-N-)1260 см- , -S-CHj-, 792 , -Аг.
ЯМР-спектр (CDClj): 2,31 м.д. . синглет, -CHj ; 3,3 м.д.. мультиплет, -S-CHj-i 3,7 М.Д. мультиплет, XN-CH (гетероциклич,); 4,54 м.д. синглет, SN-CHj-CjH - (фенилен), 7,10 м„д.
синглет, Аг-Н.
3-(2-Фурилметил)-2-иитрометилен- тиазолидин, т. Ш1. 190-192°С.
ИК-спектр (КВг): 1543, 1340 , -liOj ; 1640 см , 3130 757 смфуран, ггС-Н , 1243 , ,- С-О-СS .
ЯМР-спектр (трифторуксусная. кислота): 3,7 м.д. триплет, -S-CH ;
4,6 м.д. триплет, N-CHjV 5,07 м.д. синглет, JiN-CHj- , 6,3 м.д. дублет, -CH-NOjV 6,5 м.д. мультиплет, уран, 3,4 Н, 7,5 м.д. мультидлет, фуран, 5Н.
2-Цианимино-3-(4-оксибег1зил)-тиа- золидин, т. пл. 175-177°С.
ИК-спектр (КВг) : 2190 , 1570 , , 3210 , -OHJ 1610, 840 , -Аг. , .ЯМР-спектр (CDCij): 3,4 м.д. мультиплет, -S-CHj-J 3,7 м.д. мультиплет, N-CH2- 4,5 м.д. синглет, Ar-CH - j 6,9 м.д. квадруплет, Ar-CH,j-i. 9,47 м.д. синглет, -ОН.
Лекарственный препарат.
Для приготовления таблеТированно- iro лекарственного препарата (1000 таб- гаеток) используют следующие вещества, г: .
З-бензил-2-цианимино-тиазолйдин (биологически акти:вное вещество) 50; крахмал 75; молочный сахар 55, тальк 10; поливинилпирролидон 6; стеарат магния 3; коллоидальная кислота 1,.
Тонко размолотое биологически активное вещество смешивают с молочным сахаром и тальком, порошковую смесь смешивают с раствором поливинил пирролид о на до получения пасты и гранулируют через сито. Высушенные зерна смешивают со стеаратом магния и коллоидной кислотой и эту смесь прессуют в 1000 таблеток весом 0,2 г.
Новые соединения на основании своего широкого спектра действия пригодны для лечения происходящих из различных патомеханизмов желудочных и кишечных язв, они подавляют также вызванное нестероидными противовоспалительными средствами язвенные образования. Некоторые особенно активные представители зтой группы как, например, З-бензил-2-цианиминотиазо- лидин (далее обозначается как соединение А), в противоположность из- вестным антагонистам к рецептору гис- тамина. Hj не содержат групп, которые могУт вызывать в организме образование нежелательных из-за своего канцерогецногр действия N-нитрозо- соединений.
Дпя фармакологического исслёдова- ния новых соединений использовали нижеописанные методы.
Язва Shay.j
Самок крыс H-Wistar весом 120- 150 г выдерживают без пищи в течение 24 ч, в решетчатых клетках и дают им только питьевую воду. Затем прив- ратник желудка животных подвергают мягкому эфирному наркозу и одновременно обрабатывают интраперитонеалъ- но предлагаемым (подавляющим язву) соединением. Спустя 4 ч животных умерщвляют эфирным наркозом. Желудок животных вынимают, измеряют объем и рН содержимого желудка. Иногда образование соляной кислоты определя- ют путем титрования о
Язва, вызванная аспирином,
Нестероидцные противовоспалитель- -ные средства в различной мере могут вызывать образование желудочных и ки шечных язв .На основании этого для пода лянлцих язвы средств используется так назьшаемая аспириновая модель,
Самок крыс H-Wistar весом 120 - 150 г 24 ч вьщерживают без пищи, снабжая только водой, затем путем орального введения с помощью приготовленной с твином-80 суспензии со 100 мг/кг ацетилсалициловой кислоты вызывают образование язв в желе.зис- той части желудкЭ животных. Одновременно с ацетилсалициловой кислотой жи- вотным вводят предлагаемое соединение оральным путемо Спустя 4 ч животных Умерщвляют и подсчитывают находящиеся на железистой части желудка коричнево-красные эрозиио При оценке результатов указьюается среднее число находящихся в желудке язв и, соответственно, . количество животных без язв.
Язва, вызванная индометацинон.
Нестероидное противовоспалительное средство индометацин - 1-(n-xлop бeнзoил)-5-мeтoкcи-2-мeтилиндoл-3- -уксусная кислота вызывает образова- .ние язвы желудк а, а также приводит к чрезвычайно сильному образованию язв в тонком кишечнике. Образование язв в тонком кишечнике в зависимости от дозы может быть фатальным, так как наступаняцее за счет перфорации кишечника воспаление брюшины смертельна.
Вызываемая индометацином фаталь- ная модель кишечной язвы.
Для этих опытов используют самок крыс H-Wistar весом 120-150 г, которых кормят нормально. Путем оральных доз 15 мг/кг индометацина (в приготовленной с твином-80 суспензии) вызывают фатальное обра13ование язв кишечника. Исследуемые соединения вводят также орально животным .после обработки индометацином. Для развития кишечных язв, в противоположность желудочным язвам, требуется более продолжительное время (примерно 48-72 ч),
Для оценки язвообразования примег няется метод вздутия. Благодаря -этому методу возможно количественное прослеживание процесса язвообразования. Прочность стенок кишечника в момент разрыва постепенно падает с возрастанием интенсивности язвообра- зоваяия.
Индуцированная индометацином не- фатальная модель кишечной язвы.
Нормально питакнцихся крыс H-Wistar весом 120 - 150 г обрабатьшают перорально. с помощью 7,5 мг/кг индометацина для индуцирования нефатальных кишечных язв. Спустя 4 ч также орально животным вводят дозы исследуемого соединения и эту обработку (лечение) повторяют через 24 и 48 ч. Спустя 24 ч .после последней обработки, т.е. 72 ч после вызывающей образование язв индукции с помощью индометацина, животных умерщвляют, для оценки ячвообразования используют также метод вздутия. .Индуцированная с помощью абсолют- ного спирта модель некроза желудка,
Самок крыс H-Wistar весом 120 - 150 г вьщерживают 24 ч без пищи,. Давая им только питьевую воду.. Затем животных орально обрабатывают исследуемым соединением и через 30 ник дают по 0,5 мл на 100 г веса абсолютного спирта через зонд. Через 2ч животных умерщвляют, извлекают желудок, разрезают вдоль больной выпук- лости, слегка промьщают и растягивают. Видимые на железистой части продольные невротические полосы измеряют в миллиметрах. Указывают среднкйо длину поражений на желудок: меру желудочной цитозащиты (цитопротек- ции) выражают в процентах в расчете на контрольных животных.
Посредством исследований, проведенных фармакологическими методами, установлено, что новые производные
тиазолидина явддются эффективными противоязвеннь1 в1 веществами.
Особенно сильнодействзтощимипокаг зали себя соединение А(3-бензил-2- j -циaни шнoтиaзoлидин) и средннение В (3-бензш1-2- Нитррметилентиазрли- ин). Данные фармакологических иссле- inofiaHHft соединений А и В на противоязвенную активность представлены в ю табл. 1,
В сравнении с применяемыми в противоязвенной тер.апии циметидином ы-нано-Ы -метил-К - 2-(5-метил-1Н- имидазол- А-ил)метил -тиоэтилгуани- 15 ин,- а также пиренцепином 5,11-ди- педро-11- (4-метил-1-пиперазинил)- . -ацетш1 -6Н-пиридо-(2,3-б)-(1,4)- бeнзoтиaзeпин-6-oн| новые производ- ные тиазолвдина обладают преимзпцест- 20 вами Сравнение биологинеской активности соединения В с циметидином и пиренцепином (тест по Роберту на язве, вызванной кисль1м этиловым спиртом) дано в . табл. 2, . - 25
Циметидин не может подавлят| ин- уцированное индометацином язвообра- зование в кишечнике. Вызываемое индометацином язвообразование кишечника также не может подавляться с помо- ЗО ЩЬЮ известных антихилинэргических средств как (2-оксиэтил)диизопррпил- метиламмонийбромид-(пропантелинбро- мид) и метилбромида - сложного тропино- эфира ксантен-9-карбоновой кислоты ,j (трантелиниумбромил, гастриксон.
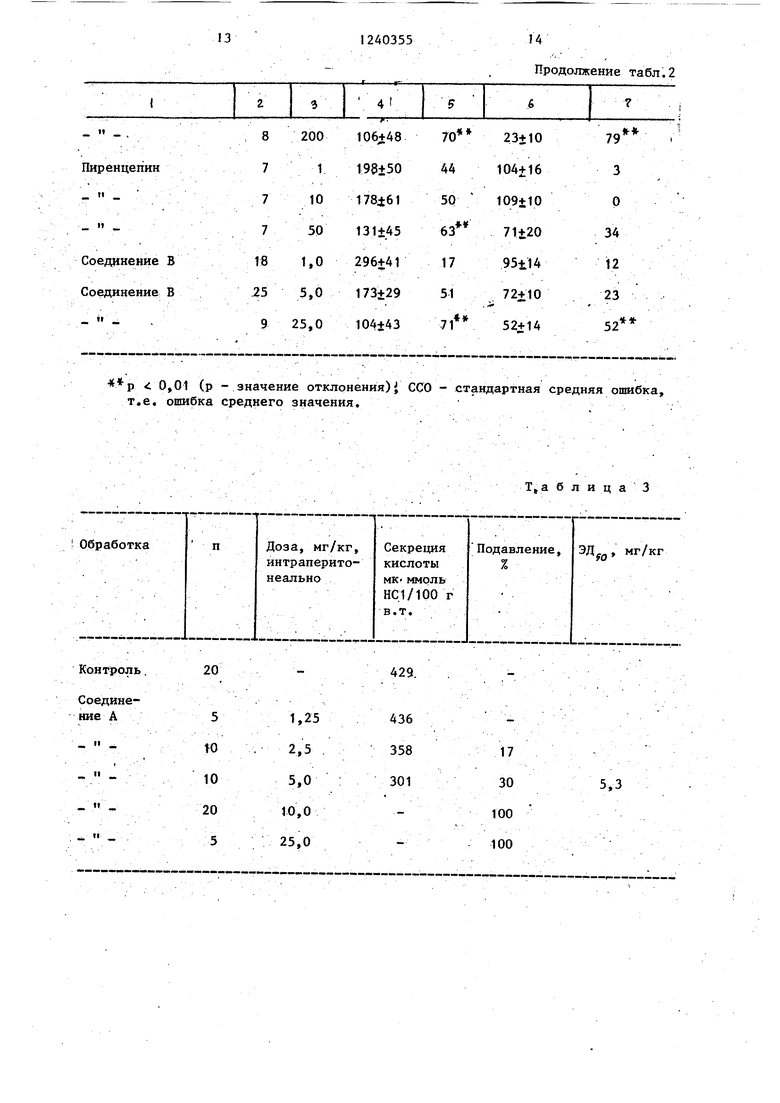
Результаты описанных фармакологических опытов представлены в табл,3-9 (в относящихся к названию колонках таблиц используются следующие сокра- щения: п - число животных, в,т, - вес тела),
45
Из представленных данных в табл.3 видно, что соединение в зависимости от дозы Уменьшает выделение кислоты желудочного сока Очень важно, что соединение А активно подавляет у крыс Shay также при оральном применении выделение кислоты желудочного сока, как это следует из данных табл. 4,
, Индуцированное ацетилсалициловой кислотой язвообразование в желудке подавляется, в зависимости от дозы, одновременной обработкой (лечением) с помощью соединения А, также как и
индуцированные дозами по 20 мг/кг индометацина перорально язвы желудка. Подавляющее действие соединения А
j
5 0 5
О j
5
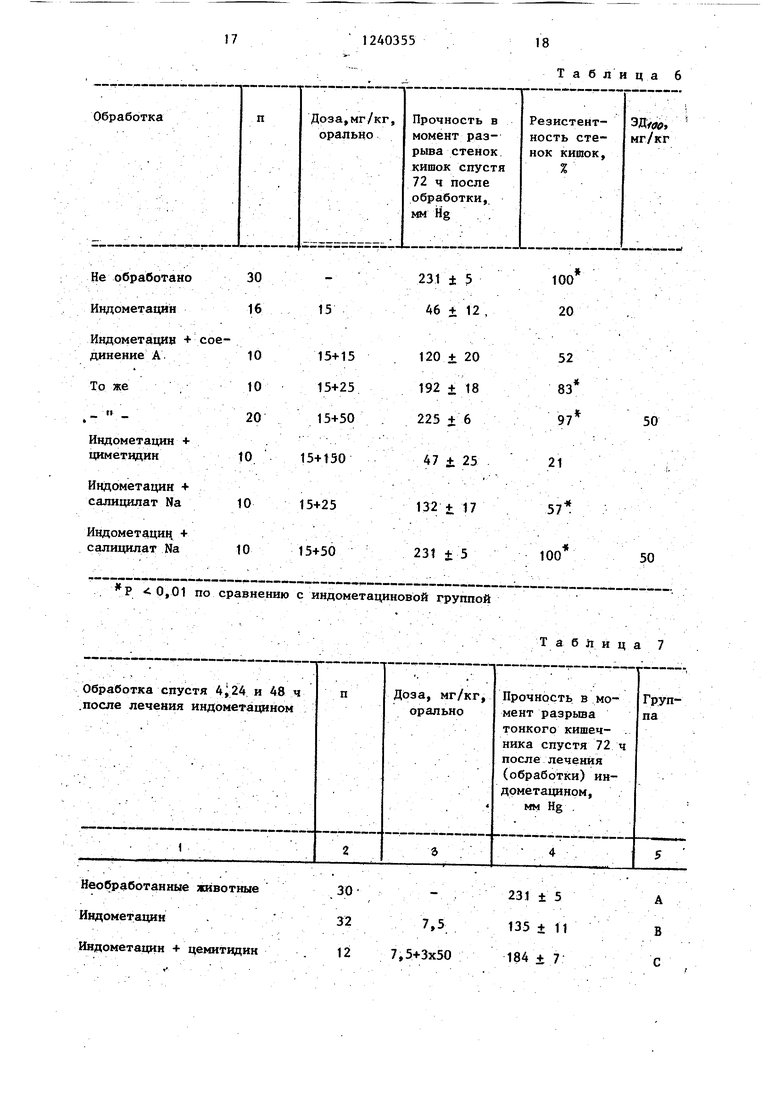
по отношению к индуцированному ацетилсалициловой кислотой язвообразо- ванию представлено в табл. 5, Данные табл. 6 показывают подав-i : ляющее действие против индуцированных С помощью 15 мг/кг перорально доз индометацина язв тонкого кишечника. Здесь- подавляющее действие тйкже завис:ит от дозы соединения А.
Важны результаты, получанные в опытах с нефатальной моделью кишечной язвы. Обработка с помощью Соединения А начинается лишь тогда, когда яз- вообразованйе у животных индуцировано уже на 4 ч раньше за счет 7,5 мг/кг перорально введенного индометацина. В этом случае речь идет о дополнительной обработке, а. именно, спустя 4,24 и 48 ч после введения индометацина. Из данных табл. 7 видно, что циметидин в таких условиях неактивен, в то время как соединение А может нормализовать в зависимости от дозы прочность в момент разрыва кишки кишечника),
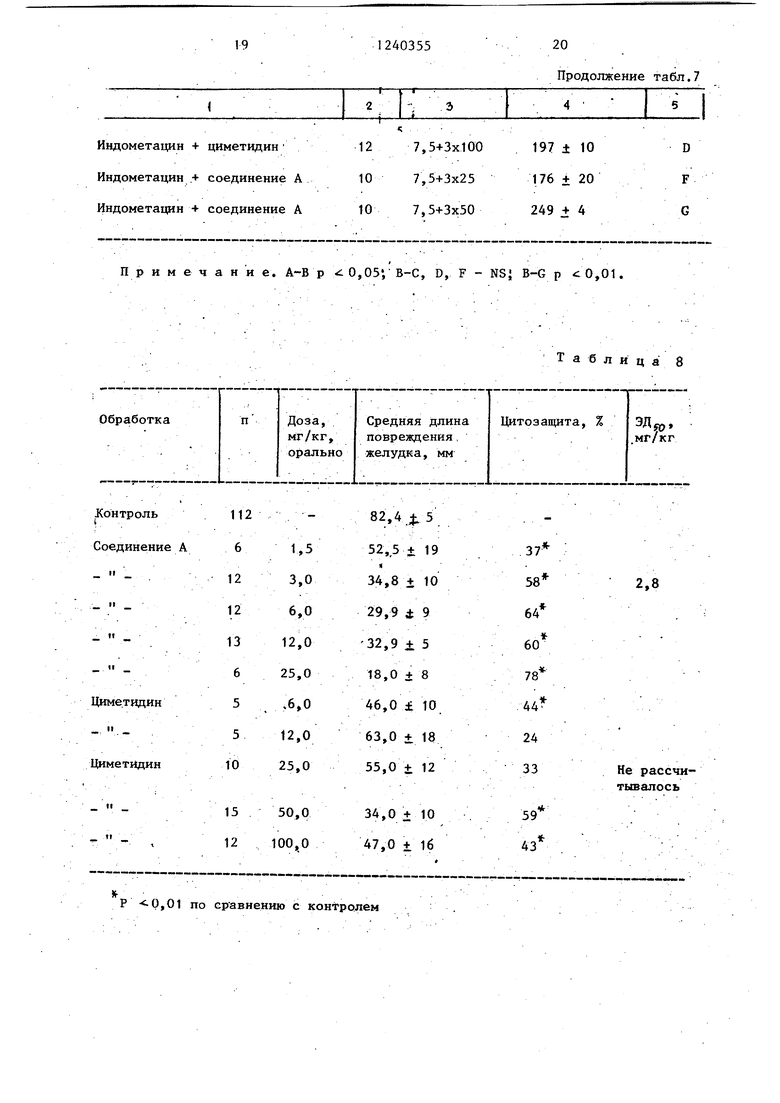
Соединение А также активно против индуцированного абсолютным спиртом некроза желудка. Как показьшают данные табЛо 8 эта цитозащита зависит от дозы.
На основании результатов фармако- логических испытаний Соединение А можно рассматривать как чрезвычайно активное, подавляющее язвы, средст-; во, спектр действия которого по ширине превосходит получаемые в настоящий момент лучшие продукты в этой области показаний. Комплексный меха- нид1М действия соединения А указывает на то, что это соединение активно в трех моделях язв с различными пато- механизмами: в модели с индуцированной ацетилсалициловой кислотой язвы желудкаJ в модели с индуцированной индометацином язвы тонкого кишечника и в модели с индуцированным абсо- лютным спиртом некроза желудка.
Сравнение полученных при оральном, интраперитонеальном и подкожном введении результатов действия показывает, что соединение А при оральном применений хорошо абсорбируется.
На основании результатов прежних токсикологических наблюдений -соединение А обладает высоким терапевти- ческим индексом.
Так как соединение А нерастворимо в воде, при токсикологических исследованиях использовали приготовленную с твином 80 суспензию для орального интраперитонеального применения биологически активного вещества. Для внутривенного введения биологически активное вещество растворяли в диме- тилформамиде. Были сделаны следукнцие наблюдения:
1) 100 мг/кг внутривенно: животные чувствуют себя плохо, однако ни одно животное не погибает в течение трех
Подавление секреции желудочной кислоты.у крыс
Подавление язвы, вызванной аспирином
Тест на циуосекрецию (по Ро- ЕД д 25 мг/кг берту)78% защиты
Подавление язвы, вызванной ИНДометацином
Вода (контроль) Циметидин
58 - 353+20.О107+1.0
8 25 44li82О82+21
15 too 274+443348+9
2)250 мг/кг интраперитонеально: в течение двух недель ни одного погибшего
3)1500 мг/кг интраперитонеально: животные погибают в течение 30 мин.
Сравнение терапевтических индексов соединений А и В и циметндина с пиренцепином дано в табл. 9, Из результатов табл. 9 следует, что предлагаемые соединения дают положительное цитозащитное действие и их терапевтический индекс не хуже, чем у известных противоязвенных препаратов.. .
Таблица 1
ЕД- 5,3 мг/кг
О
... 21 мг/кг
ВД Wii.0 мг/кг
ЕД уо,,.о 25 мг/кг 52% защиты
ЕДуо 50 мг/кг 97% Защиты
ЕД 50 50 мг/кг 962;защиты
Таблица 2
О 24 56
В В
8 7 7 7
18
25
9
200 1
10
50
1.0
5.0
25,0
р i 0,01 (р - значение отклонения)J ССО - стандартная средняя ошибка, т.е. ошибка среднего значения.
Контроль,
20
Продолжение табл.2
70
44
,
50
63 17 51
.
71
,«
23+10
104+16
109±10
71+20
95±14
72+10
52+14
79
3
Р
34
12
23
52
б лица 3
429.
5,3
.
5 5
10
10
10
20
е- 10
А 17
сое17
ое14
сое17
100
100 + 1,5 100 + 3,0 100 + 6,0 100 + 12,0 100 +25,0
«
р о,05;
р :0,1; ЭД„, 2,1 мг/кг
Таблица 4
42
35
47
3,7 1,5
4,1 1,0
Таблица 5
Не имеющие язв животные, %
15,7+3,0
40 57 71 86 85
23
29
66
.41
Р 0,01 по сравнению с индометациновой группой
Необработанные животные Индометацин Индометацин + цемитцдин
Таблица 6
Т а б л и ц а 7
Примечание. А-В р 0,05, В-С, D, F - NSJ B-G р 0,01.
А
112
6 12 12 13
6
5
5 10
1,5
3,0
6,0
12,0
25,0
.6,0
12,0
25,0
15 50,0
12
100,0
Р 0,01 по сравиению с контролем
Продолжение табл.7
Таблица 8
5
19
10
9 5
10 18 12
0 6
37 58 64 60 78 .44 24 33
59 43
2,8
Не рассчи- тьталось
Редактор А.Шишкина
Составитель Н.Капитанова
Техред В.Кадар Корректор M,CaM6opcKaHj
3416/60
Тираж 379Подписное
ВНИИ1Ш Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб.., д. 4/5
Производственно-полиграфическое предприятие,, г, Ужгород, ул. Проектная, 4
Таблица 9







| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных тиазолидина | 1984 |
|
SU1240356A3 |
| Способ получения производных 2-пиридин-тиола или их кислотно-аддитивных солей (его варианты) | 1985 |
|
SU1346042A3 |
| Способ получения амидов 1,2,3,4,6,7,12,12 @ -октагидроиндоло(2,3- @ )-хинолизин-1-ил-алканкарбоновых кислот или их физиологически совместимых солей присоединения кислот | 1985 |
|
SU1470193A3 |
| Способ получения 2-галоген-никэрголинов | 1986 |
|
SU1445557A3 |
| Способ получения производных 2-тиазолидинона | 1988 |
|
SU1657062A3 |
| Способ получения производных 3-азабицикло 3,3,1 нонана,или их изомеров,или их фармацевтически приемлемых солей присоединения кислот (его варианты) | 1984 |
|
SU1395141A3 |
| Способ получения оптически активных 9-или 11-замещенных производных аповинкаминовой кислоты или их солей | 1985 |
|
SU1398775A3 |
| Способ получения N-сульфамил-3-(2-гуанидинотиазол-4-илметилтио)-пропионамидина | 1986 |
|
SU1450743A3 |
| Способ получения производных 9-или 11-нитроаповинкаминовой кислоты или их солей | 1985 |
|
SU1440347A3 |
| Способ получения 2-галогенированных 1,8-замещенных производных эрголена | 1987 |
|
SU1500161A3 |


| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| Р.Эльдерфилда - М..: Изд-во иностранной лит-ры, 1961, т | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Стрелочный замыкатель | 1922 |
|
SU544A1 |
| - Патент США № 4143148, кл | |||
| Способ приготовления хлебного вина | 1925 |
|
SU424A1 |
| Дверной замок, автоматически запирающийся на ригель, удерживаемый в крайних своих положениях помощью серии парных, симметрично расположенных цугальт | 1914 |
|
SU1979A1 |
Авторы
Даты
1986-06-23—Публикация
1984-03-16—Подача