где Ia-R, Тб-R, IB-R,
Rt OCH,j H; Рг OCH,; ОСИ,; R OCCHj j б
tr-R, Н; R2 ОСПН,,
обладающим антиаллергическим и целеб ропротекторным действием.
Цель изобретения - поиск новых з.-i- мёщенных амидов коричной кислоты,обладающих улучшенными антиаллергически ми и церебропротекторными свойствами.
г
Пример) Получение гидрохлорида днэтиламияоэтнлового эфирА 4- (3,4-диметоксНцИинамамид)бензойной кислоты (вещество Та),
К раствору 2,2( г (О.ОГмоль) япорангидрида 3,4-диметоксикоричной кислоты в 50 мл толуола припивают раствор 2,73 г (0,01 моль) новокаина гидрохлорида в 30 мл пиридина.Реек- ционную смесь оставляют на 12 ч« Вы- павшнй осадок фильтруют и промывают толуолом, Кристаллизуют из пропано- ла-2.
Выход 3,5 г (76%). Т.пл. 197 - 198°С.
Найдено,: С 62,48; И 6,81; С1 7,80; N 6,20;
; c44H,,caiito,
Вычислено,: С 62,27; Н 6,70;
С1 7,68; N 6,05.
Данные УФ-спектров: 252, 340 им. Данные ИК-спектров: 3400, 1720, 1675, 1630, 1600, 1520, 1270, 1230, 1150, 1100, 1000, 850 см 1.
Пример 2, Получение гидрохлорида диэтиламиноэтипового эфира 4-(4-метоксициннаммид)бензойной кислоты (16).
К раствору 1,97 г (0,01 моль) 4-иетоксикоричной кислоты в 50 мл толуола приливают раствор -2,73. г (0,01 моль) -новокаина гидрохлорида в 20 мл пиридина. Реакционную смесь оставляют на 12 ч. Выпавший осадок фильтруют, промывают толуолом и кристаллизуют из пропанола-2.
Выход 4,03 г (93%). Т.пл. 192 - .
Найдено,: С 63,65; Н 6,63; С1 8,21; N 6,60. Ct,Ht,ClHtO
Вычислено,: С 63,81; Н 6,71; С1 8,09; N 6,47.
Данные УФ-спектров: 226, 332 нм. Данные НК-спектров: 3400, 1710, 1680, 1630, 1590, 1520, 1270,1240, 1160, 1100, 970, 820 .
Приме р 3. Получение гидрохло- ряда диэтиламиноэтнлового эфира 4- (4-ацетокси-З-метоксициннамамид)бен- эойной кислоты (Тв).
К раствору 2,55 г (0,01 моль) 4-ацетокси-З-метоксикоричяой кисло- ты в 50 мл толуола приливают раствор 2,73 г (0,01 моль) новокаина гидрохлорида в 20 мл пиридина. Реакционную.смесь оставляют на 12 ч. Выпав
,
5
0
ший осадок фильтруют, промывают толуолом и кристаллизуют ия пропанола-2.
Выход 4,17 (Я5). Т.пл. 162-164°С.
Найдено,: С 61,28; Н 6,48; С1 7,32; Н 5,88.
C H ClNtOt
Вычислено,: С 61,16; Н 6,32; С1 7,24; N 5,71.
Данные УФ-спектров: 240, 320 нм.
Данные ИК-спектров: 3400, 1720, 1680, 1595, 1520, 1260, 1235, 1150,
1100, 970, 890 .
П р и м е р 4. Получение гидрохлорида диэтиламиноэтнлового эфира 4- (4-ацетоксициннамамид)бензойной кис- Лоты (I г).
К раствору 2,25 г (0,01 моль) хлорангидрнда 4-ацетоксикоричной кислоты в 50 мл толуола приливают раствор 2,73 г (0,01 моль) новокаина гидрохлорида в пиридине. Реакционную смесь оставляют на 12ч, Выпавший осадок фильтруют, промывают толуолом и кристаллизуют из пропанола-2.
Выход 3,73 г (81Z). Т.пл, 169 - 170вС.
Найдено,: С 62,66; Н 6,45} С1 N 6,22. Cz4Hz,ClNj05
Вычислено,%: С 62,54} Н 6,30; С1 7,71; N 6,08.
Данные УФ-спектров: 222, 312 нм.
Данные ИК-спектрон: 3400, 1770, 1675, 1590, 1530, 1250, 1230, 1160, 1090, 960, 850 .
Исследование антиаллергического действия соединений общей формулы (I) проводили на модели реакции пассивной кожной анафилаксии (РПКА).
Сыворотку,содержащую специфические гомоцитотропные антитела,получали на третьей неделе после сенсибилизации мывей линии СВА овальбумином (0,5 мкг) с гидроокисью алюминия (2,5 мг/мымь). Полученную мышиную сыворотку в разведении 1:30 (после определения титра грмоцитотропных антител в РПКА) вводили внутрикож- но в 6 выстриженных участков спины белых крыс - самцов линии Вис- тер (180-2Ю г) в количестве 30 мкл. Через 24 ч крысам внутривенно вводилась разреяающая доза овальбумина (I мг/кг)( в 1 мл 0,5 -ного раствора красителя синего Эванса на физиоло- . гическом растворе, Спустя 30 мин
крыс под эфирным наркозом декапитн- ровапн, кожу выворачивали, прокрашенные участки вырезали и экстрагировали краситель Лормамидом при 37вС в течение 4 сут. Количество красителя в экстравязате определяли спектрофотометрически при 600 им по калибровочному граЛику.
Исследуемые вещества вводили внут рибрюпинно в дозе 10 мг/кг за 60 мин до разрешающей дозы антигена,
В качестве объекта сравнения использовали антиаллергическир препарл ты кромогликат натрия, таяегил и cvn- растин. Кромогликат натрия вводипи в дозе 50 мг/кг (в 5 раз бопьтей, чем соединения (И, т.к. в дозе 10 мг/кг выряженного антилппергичес- кого действия в РПКА он не проявлял) внутрибрюгаинно за 60 мин до введения антигена. Тавегил и супрястин вводили в дозе 10 мг/кг. Контрольным крысам внутрибрюшинно вводили фичиоло- гический раствор.
Процент ингибирования РПКА вычисляли по Лормуле:
(
мкг синьки в участках кожи крыс,получавших исследуемое
соединение
мкг симьки п участках кожи контрольных крыг
Результаты опытов статистически обработаны и приведены в табл.1.
Далее исследовалось влияние горди нений Аормулы (I) на проявление местной сосудистой реакции, вызванной внутрикожными ппедениями гигтаминл (1 серия) и серотонина (2 серия).
Белым крысам (210-240 г) внутривенно вводили по 1 мл 0,5%-но- го раствора синьки Эванса и сразу после этого в 6 предварительно выстриженных участков кожи спины - по 30 мкл гистами- на (80 мкг/мл) (1 серия) и серотонина (2 мкг/мл) (2 серия) на физиологическом растворе, Через 5 мин у де капитированных под эАирным наркозом крыс интенсивность местной сосудистой реакции оценивали по количеству красителя в экстравазате,определяемому по вышеописанной методике.
За 60 мин до внутрикожных инъекций гистамина и серотонина крысам внутрибрюшинно вводили растворы ис6bf 4 +Л
следуемых веществ в дозе 10 мг/кг. Ч качестве объекта сравнения нгспедорп- пн кромогликят натрия, который вводился в дозе 50 мг/кг тем же путем. Контрольным крысам внутрнбрюшинно вводили (Ъичиологическнй раствор.
Процент ннгнбирования кожной реакции, вызванной введением гист.JQ мина (| серия) и серотонина (2 серия), вычисляли но вышеуказанной Формуле. Результаты опытов статистически обработаны и приведены в табл. 2 и 3.
15
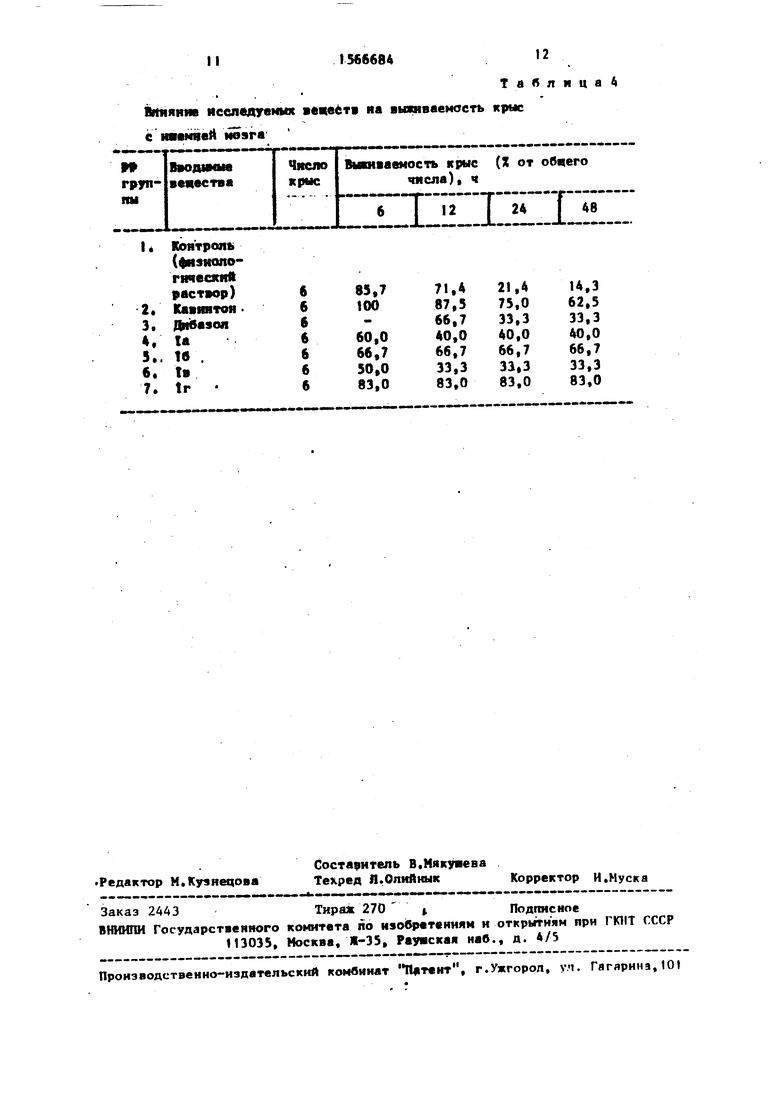
Изучалось влияние веществ на выживаемость крыг с ишемией мозг,а методом цнркупяторнон гипоксии.
Келые крыгы (180-750 г) наркоти- 20 зировались внутрнбркмттинным введением этлминлл-натрия (30 мг/кг). Выделялись сонные артерии, на которые накладывались толковые лигатуры, Через 24 ч, после прекращения дейст- 25 вия наркоза, вводились вещества внут- рибрюпжнно в дозр 10 мг/кг.
Через 60 мин сонные артерии перевязывались и проводилось наблюдение за животными не менее 48 ч. Критерием 30 активности вещества служит процент выживаемости животных через 48 ч. В качестве объектов срлчнения исследовали клвинтон и дибазол, вводимые в дозе 2 мг/кг за 60 мин до перевязки сонных артерий.
Результаты опытов приведены в табл.4.
35
Определение острой токсичности И расчеты осуществляли по методу Керберл.
Белым мышам массой 18-20 г внутрибрюшинно вводили по 0,5 мл раствора исследуемых веществ. На каждую дозу в опыте брали по 6 мышей. Получили следующее значение LD, мл/кг: 1а - 325; 16 - 345; Гв - 375; I г - 275.
Антиаллергическая активность сое- дннений общей формулы (Т) превосходят таковую кромогликата натрия в 10-12 раз, К тому же, в отличие от последнего, соединения (I) проявляют антагонистические свойства по отно- тению к медиаторам аллергии - гиста- мину и серотонину, снижая кожные реакции, вызываемые ими.
Кроме того, для соединения 1в выявлены свойства предотвращать гибель
морских свинок от анафилактического шока и анафилактического бронхоспаз- ма, подавлять анафилактическую контрактуру изолированной подвздошной кишки морской свинки и снижать чувствительность Ъе к гнстамину, ацетнл- холнну, серотонину, тормозить высвобождение гнетанина из тучных клеток мышей, индуцированное антигеном и либераторон гнстамина - веществом А8/80.
Кроме того,соединения (I) повышают вьисиваемость животных с ишемяей мозга. Наиболее активным церебропро- текторным действием обладают соеди- нения 1г и 16 (соответственно 83 и 66,7%), активность которых превосходит таковую кавинтона (62,5%) и дибазола (33,3%).
Формула изобретения
Гндрохлориды анидов коричной кислоты общей формулы:




Изобретение касается производных арилалифатических ненасыщенных кислот, в частности гидрохлоридов амидов коричной кислоты общей ф-лы: 2R,, 4Rt-CbH,(0)-NH-06H4- -4-C(0)-0-(CH,)2-N-(C2Hy )2 HC1, где a) R, Rt ОСН5; б) в) P,-OCH,;R2 0-С(0)СН,; г) R, Н; R e 0-C(0)-CHj, обладающих янтиаллергическим и церебропротекторным действием, что может быть использовано в медицине. Цель - создание новых, более активных веществ укаэанно- го класса. Синтез ведут реакцией хлорангидрида замещенной коричной кислоты с гидрохлоридом новокаина Р среде пиридина (или толуола). Выход, %: т.пл., С; брутто ф-ла; степень ингибирования аллергена - гис- тамина, серотонина, %; степень пижи- ваемости крыс с игпемией мозга через 6 и 48 ч, %; ГЛ5о мг/кг: а) 76; 197-198; Сг,Н31С1КгО ; 27,1} 31,0; 60 и 40; 325; б) 93; 192-194; C2,H2,C1N204; 20,4; 30,9; 66,7 и 66,7; 345; п) R5; I62-164;C2JHVC1N/V; 29,6; 41,1; 50,0 и 33,3; 375; г) 81; 169-170; C7,H49C1N 05; 34,7; 37,6; 83 и 83, 275, против 3,8 и 5,6% для кромогликата натрия и 100 и 62,5 для кавинтона, 4 табл. г to
;2- -CH CH-C-NH- -C -0-(CH2)2-N-lC2H5)2-Hci ()
де 1а 16 Гв
- R
- R«
- R
Н; R,
ОСИ
ОСН}{
осн
Я RI
ОССН,; О
Влияние соединений общей формулы (т) на проявление РПКА у крыс
201г - R, Н; В4 ОССИ9,
О
обладающие янтиаллергическим и цереб- ропротекторным действием.
т а б л и ц а 1
Таблица 2,
Влияние исследуемых веществ на интенсивность местной реакции, вызванной в/к введением гнстамина
Влияние исследуемых веществ на интенсивность местной реакции, вызванной в/к введением серотонина
ТаблнцаЗ
Х),25 0,001 0,002 0,001 сО,001
11156668412
Таблица
Влияние иеел«дуемыя «цеств на выживаемость крыс с ишвмней мозга
| Маяковский М.Л | |||
| Лекарстпенные средства | |||
| - М, 1985, т.1, с.319. |
Авторы
Даты
1991-05-15—Публикация
1988-05-24—Подача