Изобретение относится к усовершенствованному способу получения замещенных 7-диалкиламинокумаринов, а именно 3-йод-7-диалкиламинокумаринов, которые могут найти применение в производстве лазерных красителей и оптических отбеливателей.
Цель изобретения - увеличение выхода и расширение ассортимента целевых продуктов за счет взаимодействия соответствующего 7-аминокумарина с Йодом в среде диокеана или тетрагид- рофурана в присутствии в качестве катализатора пиридина при соответствующем молярном соотношении реагентов и катализатора.
Способ иллюстрируется следующими пример ами.
Пример 1. 3-Йод-4-метил 7- диэ тил ами но ку м ар и н,
К раствору 1 г (4,33 ммоль) 4-ме- тил-7-диэтиламинокумарина в 50 мл диоксана при перемешивании приливают раствор 5,5 г (2Г,65 ммоль) йода в 20 мп диоксана и 4 мл пиридина.Перемешивают 3 ч при 20°С. Реакционную массу обрабатывают насыщенным раствором тиосульфата натрия, экстрагиру
ют бензолом. Органический слой упаривают, остаток перекристаллизовы- вают из смеси гексан-ацетон. Выход 1,52 г (98,3%).5
П р и м е р 2. 3-Йод-4-хлор-7-ди- этиламинокумарин.
К раствору 0,5 г (2 ммоль) 4-хлор- 7-диэтиламинбкумарйна в 30 мл диок- сана при перемешивании приливаютJQ
раствор 3,0 г (12 ммоль) йода в 30 мл диоксана и 2 мл пиридина. Перемешивают 5 ч при 25°С, Реакционную массу обрабатывают так же, как в примере 1. Выход 0,68 г (90,7%).15
П р и м е р 3. З-Йод-4-морфолино- 7-диэтиламинокумарин,
К раствору 0,5 г (1,66 ммоль) 4- морфолино-7-диэтиламинокумарина в 30 мл диоксана при перемешивании20
приливают раствор 1,7 г (7,6 ммоль) йода и 2 мл пиридина. Перемешивают 6 ч при 20 С. Реакционную массу обрабатывают так же, как в примере 1. Выход 0,6 г (84,5%).25
П р и м е р 4, 2,3,6,7-Тетрагид- ро-9-метил-10-йод-1Н, 5Н-хинолизино- 9,9а, 1-gh 3 кумарин.
К раствору 0,25 г (1 ммоль) кумарина- 102 в 30 мл ТГФ приливаютзо раствор 1 г (4 ммоль) йода в 20 мл ТГФ и 1 мл пиридина. Перемешивают 5 ч при , Реакционную массу обрабатывают как описано в примере 1. Выход 0,32 г (85,3%).35
П р и м е р 5. 2,3,6,7-Тетрагид- ро-9-хлор-10-йод, 1Н, 5Н-ХИНОЛИЗИНО- С9,.9а, 1-gh 3 кумарин.
К раатвору 0,28 г (1 ммоль) исходного кумарина в 50 мл диоксана 40 приливают раствор 1,6 г (6 ммоль) йода в 20 мл диоксана и 2 мл пиридина. Перемешивают 6 ч при 20 С.Реакционную массу обрабатывают так же как в примере . Выход 0,35 г45
(87,6%).
Физико-химические характеристики 3-йодкумаринов представлены в табл.1.
Зависимость выхода целевых про- JQ дуктов и конверсии от условий проведения реакции представлены в табл.2 и 3 на примере получения З-йод-4- метил-7-диэтиламинокумарина.
Таким образом, из табл.2,3 еле- 5 дует, что применение пиридина в количестве менее 5:1 приводит к уменьшению конверсии и увеличению продолжительности процесса, увеличение
количества пиридина не приводит к увеличению эффективности процесса.
Использование 4-6-кратного молярного количества йода по отношению к исходному кумарину оптимально, так как применение меньшего количества йода существенно снижает конверсию и увеличивает время реакции, а применение больших избытков йода приводит к уменьшению выхода целевого продукта из-за протекания побочных реакций полийодирования и окисления. Для достижения указанной цели оптимальным является также применение апротонных малополярных кислородсодержащих растворителей, диоксана и тетрагидрофу- рана (ТГФ), в которых хорошо растворяются исходные кумарины и удовлетворительно растворим йод, В других растворителях реакция идет медленнее или связана с образованием побочных продуктов.
Снижение температура ниже 20°€ несколько уменьшает выход целевого продукта, а увеличение ее выпе 40°С также снижает выход целевого продукта.
Данный способ позволяет увеличить выход целевых продуктов на 10-13% и расширить их ассортимент (все полученные соединения, кроме З-иод-7-ме- тил-7-диэтиламинокумарина;являются ,новыми).
i
Формула и.з обретения
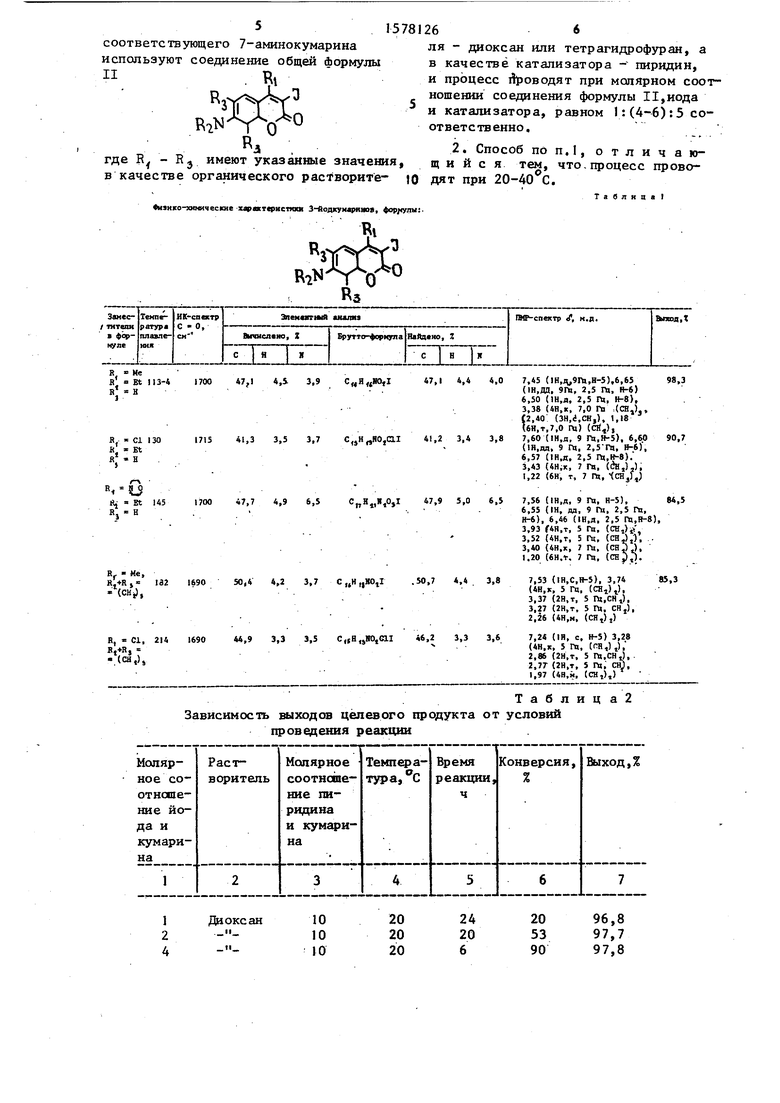
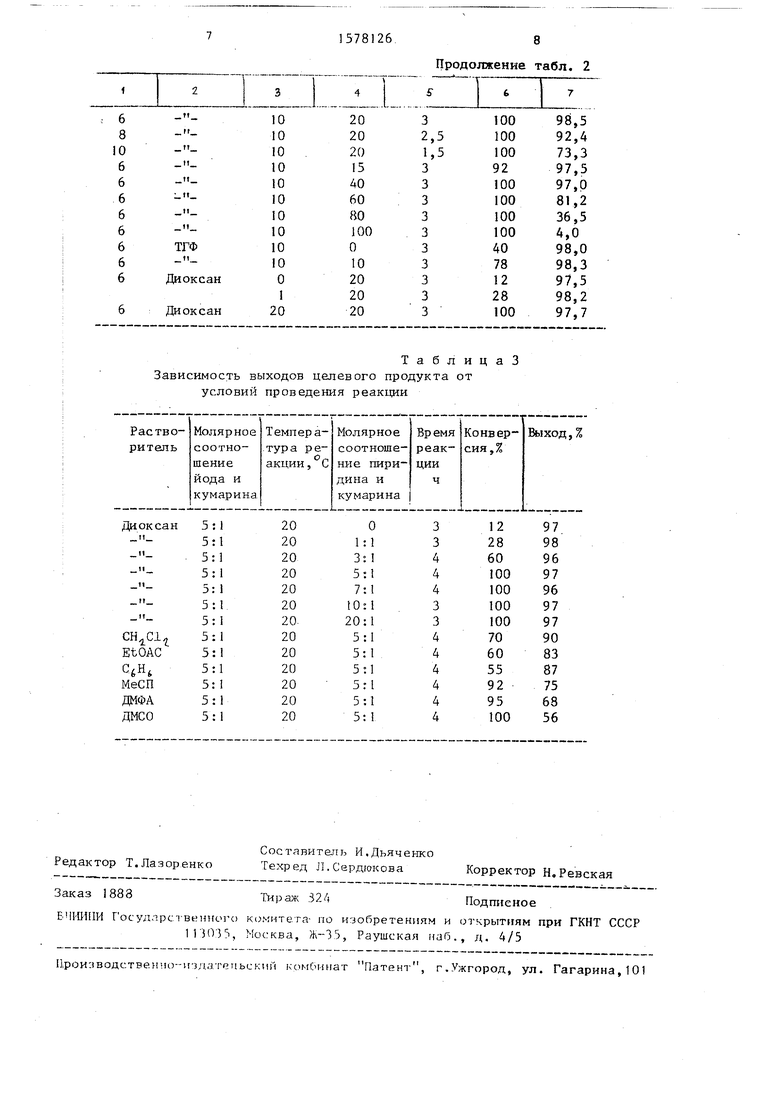
1. Способ получения замещенных 3-йод-7-диалкиламияокумаринов общей формулы I
ft
R3YYV3
RaN VV Из
где R - метил, атом хлора, группа QQ
при RJ - водород и этил, или E вместе образуют группу (СНд), взаимодействием соответствующего 7-аминокумарина с иодом в среде органического растворителя в присутствии катализатора, отличаю- .. щ и и с я тем, что, с целью повышения выхода и расширения ассортимента целевых продуктов, в качестве

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 3-нитропроизводных кумаринов | 1985 |
|
SU1328347A1 |
| Способ получения 3-алкенил- или 3-алкинилзамещенных 4-метил-7-диэтиламинокумаринов | 1987 |
|
SU1505941A1 |
| Способ получения замещенных 2-алкилиден-7-диэтиламино-2Н-1-бензопиранов | 1987 |
|
SU1505942A1 |
| Способ получения 4-хлор-7-диалкиламинокумаринов | 1988 |
|
SU1594177A1 |
| Способ получения производных гетразепина | 1989 |
|
SU1738089A3 |
| Способ получения 3,5-диметил-4-(N-замещенных аминоэтил)пиразолов | 1987 |
|
SU1466208A1 |
| Способ получения оптически активных пенемов или их солей с щелочными металлами | 1982 |
|
SU1389680A3 |
| АНАЛОГ ПИРИДИНО[1,2-А]ПИРИМИДОНА, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ ИНГИБИТОРА mTOR/PI3K | 2015 |
|
RU2658912C1 |
| Способ получения производных 1-гидрокси-2-оксо-1,2-дигидропиразина | 1984 |
|
SU1268580A1 |
| Способ получения производных 1,3-пропилендифосфоновых кислот | 1985 |
|
SU1375141A3 |
Изобретение касается замещенных кумаринов, в частности соединений общей ф-лы, где R 1=CH 3, CL, морфолиногруппа
R 3-H и R 2 - C 2H 5 или (R 2+R 3) - (CH 2) 3 -, которые могут быть использованы в производстве лазерных красителей и оптических отбеливателей. Цель - увеличение выхода и расширение ассортимента целевых продуктов. Синтез последних ведут иодированием соединения общей ф-лы @ , где R 1, R 2 и R 3 имеют указанные значения, с помощью иода в присутствии катализатор - пиридина при их молярном соотношении 1:(4-6):5 в среде диоксана или тетрагидрофурана при температуре, преимущественно, 20-40°С. В этих условиях возможно расширить ассортимент целевых веществ и повысить их выход на 10-13% (до 98,4%). 1 з.п. ф-лы, 3 табл.
1I3-4
1700
«,
4,i 3,9
С «Н «110,1
ci 130
Et
н
1715
41,3 3,5 3,7С,4Н„НО,С1141,2 3,4 3,8
1A5
1700
,7,7 4,9 6,5CpH HjO,47,9 5,0 6,5
132
1690
50,4 4,2 3,7
214
1690
44,9 3,3 3,5 С ,su tt,2 3,3 3,6
Таблиц
Зависимость выходов целевого продукта от условий проведения реакции
Диоксан
и
10 10 10
ПМР-спектр Ј, к.д.
&птд,Т
,1 4,4 4,0
,2 3,4 3,8
,9 5,0 6,5
(1Н,ДД, 9Га, 2,5 Та, Н-6)
6,50 (Ш,д, 2,5 Га, Н-8),
3,38 (4Н,к, 7,0 Гп (СН),,
{2,40 (3H,d,CH,), 1,18
(6Н,т,7,0 ГЧ) (СЙ),
7,60 (1Н,д, 9 Га,Н-5), 6,60 90,7
(1Н,дд, 9 Га, 2,5 Гц, В-6),
6,57 (1Н,д, 2,5 т.Н-8).
3,43 (4H.it, 7 Гц, (СН,),),
1,22 (6Н, т, 7 Га, XCH/J
7,56 (1Н,д, 9 Га, Н-5),84,5
6,55 (IH, да, 9 Гц, 2,5 Гп, Н-6), 6,46 (Ш,д, 2,5 Гц,Н-8), 3,93 f4H,r, 5 Гц, (CHj) 3,52 (4Н,т, 5 Гц, (СН,),1, 3,40 (4Н,х, 7 ГЦ, (CHJ-), 1.20 («Н.-Г. 7 Гц, (СН,),).
4,4 3,8
3,3 3,6
7,53 (1H,C,H-S), 3,74 (4Н,к, 5 ГН, (CHt)t), 3,37 (2H.T, 5 nt.CHj, 3,27 (2H.T, 5 ГЦ, СН,), 2,26 (4Н,м, (CHt),)
7,24 (IH, с, Н-5) 3,28 (4H.K, 5 ГИ, (fH,)t), 2,86 (2H.T, 5 rn.CHj, 2.7T (2H.T, 5 Гц, СИ, 1,97 (4Н,м, (CHt),)
85,3
а 2
24 20 6
20 53 90
96,8 97,7 97,8
15781268
Продолжение табл. 2
ТаблицаЗ
Зависимость выходов целевого продукта от условий проведения реакции
| Способ получения 3-алкенил- или 3-алкинилзамещенных 4-метил-7-диэтиламинокумаринов | 1987 |
|
SU1505941A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1990-07-15—Публикация
1988-07-04—Подача