HjCOOC
СООСНз
которое может быть использованр в качестве желтой цветообразующей компоненты в цветоделенных слоях цветных фотографических материалов.
Целью изобретения является разря- ботка способа получения нового соединения .
П р и м е р 1. К раствору 24,5 г 2-хлор-5-{N 3,5-ди(метоксикарбонил) фенилЗаминосульфонилIанилид-(2-окта- децилоксибензоил)уксусной кислоты (0,03 г/м.) в 300 мл хлороформа прибавляют при комнатной температуре при перемешивании раствор 4,45 г сульфурилхлорида в 50 мл хлороформа и перемешивают 12 ч. Хлороформ отгоняют в вакууме, остаток - смолистое бесцветное вещество кристаллизуют из 220 мл смеси этиловый спирт-гексан 10: 1 и получают с -хлорпроизводное-2- хлор-5-{н- 3,5-ди(метоксикарбонил) фенил аминосульфонил анилид-2-(2-ок- тадецилоксибеНзоил)-2-хлоруксусной кислоты (А), Выход 21,7 г (85%), т.пл. 114-120 С.
Пример2.К5,4млЗн. ме- танольного раствора метилата натрия по каплям прибавляют 2,5 г диметило- вого эфира 5-оксиизофталевой кислоты (0,0135 г-моль) в 9 мл диметилсульф- оксида. Смесь перемешивают при комнатной температуре в течение 0,5 ч. В эту смесь по каплям прибавляют 8,48 г вещества А, полученного по примеру 1 (0,01 г-моль) в 15 мл диме- тилсульфоксида. Реакционную смесь перемешивают в течение 2 ч при 100 С в масляной бане, .что соответствует в реакционной смеси, переносят в стакан с 200 г льда и 20 мл конценрированной соляной кислоты. Выпавший хлопьевидный осадок отфильтровывают, промывают водой до рН 7,0 промывных
вод. Остаток высушивают на воздухе. Технический продукт кристаллизуют из
25 мл смеси этанол:гексан 1,5:1.
Выход 5,6 г (55%), т.пл. 127-132
R.0,6 (силуфол, этилацетат:гексан
13:1).
. Найдено, %: С 62,37 Н 6,31;
N 2,72; С1 3,83; S 2,78. Q П ClNjO S . Вычислено, %: С 62,31; II 6,41,
N 2,74, С1 3,47, S 3,13.
П р и .м е р 3. К 5,4 мл 3 и. метанольного раствора метилата натрия по
к аплям прибавляют 2,8 г диметилового
эфира 5-оксиизофталевой кислоты
0
5
0
5
0
5
0
5
0
5
(0,0135 г-моль) в 9 мл диметилформа- мида. Смесь перемешивают при комнатной температуре в течение 0,5 ч. Затем по каплям прибавляют 8,48 г полученного по примеру 1 вещества А (0,01 г-моль) в 15 мл диметилформами- да. Реакционную смесь перемешивают в течение 2 ч при температуре в масляной бане , что соответствует температуре в реакционной массе 90 С, переносят в стакан с 200 г льда и 20 мл концентрированной соляной кислоты. Выпавший осадок отфильтровывают, промывают водой до ,0 промывных вод. Осадок высушивают на воздухе . Технический продукт кристаллизуют из 25 мл смеси метанол:гексан 3:1. Выход 5,1 г (50%), т.пл. 130-133°С. R|.0,6 (силуфол, этилацетат: гексан
1,3:1).. :
Найдено, %: С 62,36; Н 6,8; N 2,70i С1 3,78,- S 2,81.
,W .fl.,S,
Вычислено, %: С 62,31 Н 6,41; N 2,74i С1 3,47, S 3,13.
Пример 4. К 5,4 мл 3 Н. мета- нольного раствора метилата натрия по каплям прибавляют 2,8 г диметилового эфира 5-оксиизофталевой кислоты (0,0135 г-моль) в 50 мл ацетонитрила. Смесь перемешивают при комнатной температуре в течение 0,5 ч. В эту смесь по каплям прибавляют 8,48 г вещества А,полученного по примеру (0,01 г-моль) в 50 мл ацетонитрила. Реакционную.смесь перемешивают в течение 2 ч при 85 с, температура в масляной бане 100°С, переносят в стакан с 200 г льда и 20 мл концентрированной соляной кислоты. Выпавший осадок отфильтровывают, промывают водой до ,0 промывных вод. Осадок высушивают на воздухе. Технический продукт кристаплизугот из 30 мл смеси этанол:гексан 2:1. Выход 5,3 г (52%), т.пл. 126-129°С. ,6 (силуфол , этилацетат:гексан 1,3:1).
Найдено, %: С 61,92; Н 6,56; N 2,65j С1 3,05; S 3,35.
.
Вычислено, %: С 62,31; Н 6,41; N 2,74; С1 3,47; S 3,13.
,Пример5. 8,48 г веа1ества А, полученного по примеру 1,(0,01 г-моль) и 2,8 г диметилового эфира 5-оксиизофталевой кислоты (0,0135 г-моль) растворяют в 24 мл диметилсульфоксида.
Прибавляют 7 мл триэтиламина (0,05 г-моль). Реакционную смесь перемешивают в течение Ч,5 ч при температуре в масляной бане 125 С, что со соответствует температуре реакционно смеси 115 С, переносят в стакан с 200 г льда и 20 мл концентрированной соляной кислоты. Выпавший С1,садок отфильтровывают, промывают водой до ,О промывных вод. Остаток высушивают на воздухе. Технический продукт кристаллизуют из 20 мл смеси этанол: ггексан 2: 1. Выход 5,1 г (50%), т.пл 128-130 С. ,6 (силуфол, этилаце- тат:гексан 1,3:1).
Найдено, 7,: С 61,83; Н 6,62 N 2,54i С1 3,12-, S 3,45/
jHfjClNjO S .
Вычислено, %: С 62,31, Н 6,41; N 2,74; С1 3,47, S. 3,13.
Строение полученного вещества подверждают данными ПМР. I
Спектр снимают на спектрометре частота 360,13 МГц, Образец растворяют в дейтерохлороформе.
Группа сигналов в сильном поле спектра с 60,9, 1,35, 1,85.м.д. относится к протонам метильной и мети- леновых групп (кроме метиленовой группы, связанной с атомом кислорода) . Сигнал с 6 3,9 м.д. относится к метильным протонам двух метоксикар- бонильных групп. Синглетный сигнал с Ь 6,054 м.д. относится к протону метиновой группы, связанной с хлором. Сигнал с 64,24, м.д. относящийся к группе -CO-CH,j-CO-, отсутств-ует. Это свидетельствует о том, что про-- дукт реакции не содержит указанной группировки. Химические сдвиги протонов в слабом поле относятся к протонам замещенных бензольных колец и протонам, связанным с атомами азота
Методом ПМР подтверждают также строение целевого соединения.
Синглетный сигнал с & 6,772 м.д. относится к протону метиновой группы, связанной с остатком 5-оксиизофтале- вой кислоты. Отсутствие сигнала с 6 6,054 м.д. свидетельствует о полной замене атома хлора в (/-хлорпро- изводном промежуточного соединения на остаток 5-оксиизофталевой кислоты, что. подтверждает предложенное строение целевого соединения.
П р и м е р 6 (сравнительный). К раствору 24,5 г 2-хлор-5- ы- 3,5- ди(метоксикарбонил)фенилJ-аминосуль-
0
0
фонил анилида-(2-октадецилоксибензо- ил)-уксусной кислоты (0,03 г-моль)-; в 300 мл хлороформа прибавляют при комнатной температуре и перемешивании раствор 4,45 сульфурилхлорида в 50 мл хлороформа, после этого размешивание продолжают еще 12 ч при указанной температуре. Затем хлороформ отгоняют в вакууме. Остаток - смолистое бесцветное вещество кристаллизуют из 220 мл смеси этиловый спирт:гексан 10:1. Получают о -хлорпроизводное-2- хлор-5- Ы С-3,5-ди(метоксикарбонил) 5 аминосульфонил анилид-2- (2октадещшоксибензоил)-2-хлор-уксусной кислоты. Выход 21,7 (85%), т.пл. 114-120 с.
Затем к 5,4 мл 3 Н. метанольного раствора метилата натрия по каплям прибавляют 2,8 г диметилового эфира 5-оксиизофталевой кислоты (0,0135 г- моль) в 50 мл ацетонитрила. Смесь перемешивают при комнатной температуре в течение 0,5 ч. Затем по каплям прибавляют 8,48 г вещества А, полученного по примеру 1, (0,01 г-моль) в 50 мл ацетонитрила. Реакш онную смесь перемешивают в течение 2 ч при в масляной бане (80 с s реакци- онной массе), переносят в стакан с 200 г льда и 20 мл концентрированной соляной кислоты. Выпавший осадок отфильтровывают, промывают водой до ,0 промывных вод. Осадок высушивают на воздухе. -Технический продукт очистить кристаллизацией не удалось, выделяют на колонке с силикагелем, используя в качестве элюента смесь гексан:этш1ацетат 2:1. Выход 0,516 (5%), т.пл. 127-131 С. ,6 (силу- фол, этилацетат:гексан 1,3:1).
П р и м е р 7 (сравнительный). К 5,4 мл 3 Н. метанольного раствора метилата натрия по каплям прибавляют 2,5 г диметилового эфира 5-оксииэо- фталевой кислоты (0,0135 г-моль) в 9 мл диметилсульфоксида.
5
0
5
0
5
Смесь перемешивают при комнатной 50 температуре в течение 0,5 ч. В эту смесь по каплям прибавляют 8,48 г вещества, полученного по примеру 1, (0,01 г-моль) в 15 мл диметилсульфок
сида. Реакционную смесь перемешивают в течение 2 ч при в масляной бане (125°С в реакционной массе),переносят в стакан с 200 г льда и 20 мл концентрированной соляной кислоты. Выпавший смолистый осадок отфильтровывают, промывают водой до рН 7,0, промывных вод. Осадок высушивают на воздухе. Технический продукт очистить кристаллизацией не удается, выделяют на колонке с силикагелем, используя в качестве элюента смесь гексангэтнл- ацетат 2:1. Выход 3,1 г (30%), т.пл.
127-132 С, ,6 (силуфол, этилаце- тат:гексан 1,3:1).
Таким образом, соблюдение приведенных условий способа позволяет получать новое соединение, которое мо- зрсет быть использовано в качестве жел- 15
той цветообразующей компоненть1 в . цветоделеннцх слоях цветных фотографических материалов и обуславливает высокую их чувствительность по сравнению с желтой компонентой, выпускаемой фирмой Конксироку.
Форхула изобретения
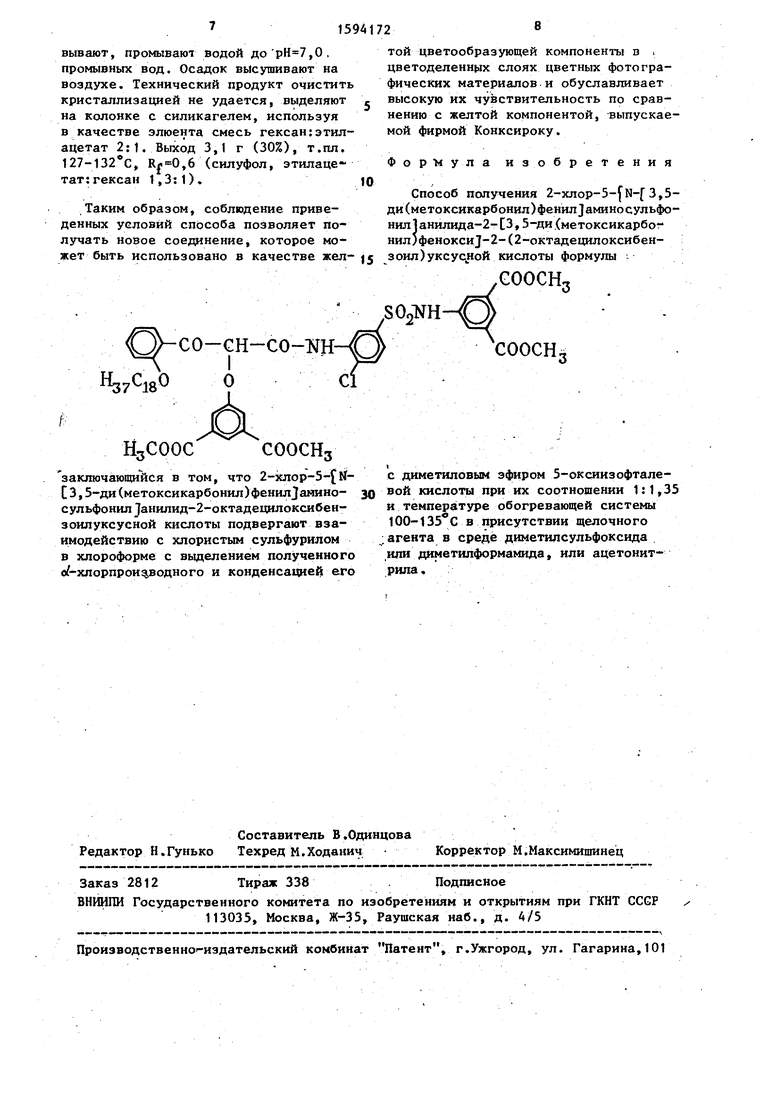
Способ получения 2-хлор-5- ы- 3,5- ди(мeтoкcикapбoнил)фeнилJaминocyльфo- ншI 1 анилида-2- 3,5-ди .(метоксикарбог нил5феноксиД-2-(2-октадецилоксибен- зоил)уксусной кислоты формулы :


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2-хлор-5- @ -(2,4-ди-трет-амилфенокси)-бутироиламино @ -анилида @ -(1-бензилгидантоинил-3)-пивалоилуксусной кислоты | 1985 |
|
SU1293178A1 |
| Способ получения 2-хлор-5-[ @ -(2 @ ,4 @ -ди-трет-амилфенокси)-бутироиламино]-анилида @ -хлорпивалоилуксусной кислоты | 1988 |
|
SU1574591A1 |
| Способ получения производных 2.4-диамино-5-бензилпиримидина | 1983 |
|
SU1222194A3 |
| Способ получения 2-хлор-5- @ -(2,4-ди-трет-амилфенокси)бутироиламино @ анилида @ - @ 4-нитро-2-(1-фенилтетразолил-5-тио)метилфенокси @ пивалоилуксусной кислоты | 1986 |
|
SU1384585A1 |
| ПРОИЗВОДНЫЕ БУТАДИЕНА И СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОИЗВОДНЫЕ АМИДОБУТАДИЕНА И СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОИЗВОДНЫЕ ПИРРОЛИДИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1997 |
|
RU2167863C2 |
| ПРОИЗВОДНЫЕ 2-АМИНО-1,3,4-ТИАДИАЗОЛА, ПРОЯВЛЯЮЩИЕ АНТИМЕТАСТАТИЧЕСКУЮ АКТИВНОСТЬ | 1995 |
|
RU2114109C1 |
| ИНДОЛИНОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2104268C1 |
| Способ получения оптически активных @ -арилалкановых кислот | 1985 |
|
SU1598863A3 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТОКСИИЗОМАСЛЯНОЙ КИСЛОТЫ | 1990 |
|
RU2026855C1 |
| 11,21-ДИАЦЕТАТ (22RS)-16α,17α -БУТИЛИДЕНДИОКСИ- 11β,21 -ДИГИДРОКСИПРЕГНА-1,4-ДИЕН-3,20-ДИОН В КАЧЕСТВЕ ПРОМЕЖУТОЧНОГО ПРОДУКТА В СИНТЕЗЕ БУДЕСОНИДА | 1989 |
|
SU1660379A1 |
Изобретение касается получения 2-хлор-5-{N-(3,5-ди(метоксикарбонил)фенил]аминосульфонил}анилида 2-[3,5-ди(метоксикарбонил)фенокси)-2-(2-октадецилоксибензоил)уксусной кислоты для использования в качестве желтой цветокомпоненты в фотоматериалах. Цель - создание нового способа получения нового цветокомпонента. Синтез ведут реакцией 2-хлор-5-[N-(3,5-диметокси-карбонилфенил)аминосульфонил]анилида-2-октадецилбензоилуксусной кислоты с хлористым сульфурилом в среде CHCL 3. После выделения полученного продукта его конденсируют с диметиловым эфиром 5-оксиизофталевой кислоты (соотношение 1:1,35) при температуре обогревающей системы 100-135°С в присутствии щелочного агента в среде диметилсульфоксида, или диметилформамида, или ацетонитрила. Выход 50%
т.пл. 128-130°С, брутто-ф-ла C 53H 65CLN 2O 14S.
со-GH-CO-lsfHEj qgO ос
НзСООС
GOOCHg
заключающийся в том, что 2-хлор-5-{ Nf- 3,5-ди(метоксикарбонил)фенилЗанино- ЗО сульфонил}анилид-2-октадецилоксибен- зоилуксусной кислоты подвергают взаимодействию с хлористым сульфурилом в хлороформе с вьщелением полученного о/-хлорпрои%водного и конденсацией его
,
,еооснз
о
соосн.
с диметиловым эфиром 5-оксиизофтале- вой кислоты при их соотношении 1:1,35 и температуре обогревающей системы 100-135 с в присутствии щелочного агента в среде диметилсульфоксида . или диметилформамида, или ацетонит- рила.
| Цветной многослойный кинофотоматериал с цветным проявлением | 1972 |
|
SU443356A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Бншер К., Пирсон Д | |||
| Органические синтезы | |||
| Мир | |||
| Приспособление для склейки фанер в стыках | 1924 |
|
SU1973A1 |
| Нефтяная топка для комнатных печей | 1922 |
|
SU326A1 |
| Синтезы органических препаратов | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
1990-09-23—Публикация
1987-08-24—Подача