Изобретение относится к химии замещенных сульфамидов нафталина, в частности к новым монозамещенным сульфамидам нитронафталина формулы I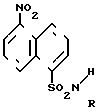 где R СН3, С2Н5, С3Н7, циклогексил, в качестве полупродуктов для получения несимметрично-замещенных 5-аминонафталин-1-сульфамидов, которые могут найти применение при анализе пептидаз.
где R СН3, С2Н5, С3Н7, циклогексил, в качестве полупродуктов для получения несимметрично-замещенных 5-аминонафталин-1-сульфамидов, которые могут найти применение при анализе пептидаз.
Целью изобретения является изыскание в ряду монозамещенных сульфамидов нитронафталина новых соединений, позволяющих при использовании их в качестве полупродуктов получать несимметрично-замещенные 5-аминонафталин-1-сульфамиды, которые в свою очередь могут быть использованы в качестве детектируемых групп для флуоресцентного анализа ферментов, повышающих информативность метода.
П р и м е р 1. 5-Нитронафталин-1-(N-циклогексил)сульфамид.
Смешивают 2 мл (0,02 моль) циклогексиламина, 50 мл толуола, 100 мл воды и 26,5 г двузамещенного карбоната натрия. При перемешивании и охлаждении ледяной водой добавляют 2,7 г (0,01 моль) 5-нитронафталин-1-сульфохлорида. Смесь выдерживают 3 ч при комнатной температуре, нейтрализуют концентрированной HCl до рН 5, отделяют толуольный слой, водный слой экстрагируют хлороформом. Оба органических раствора соединяют, упаривают и остаток перекристаллизовывают из бензола. Получают 2,7 г (выход 82%) целевого продукта; т. пл. 125-127оС.
П р и м е р 2. 5-Нитронафталин-1-(N-метил)-сульфамид.
15 г (0,055 моль) 1-нитронафталин-5-сульфохлорида растворяют в 300 мл абсолютного хлорофора. При охлаждении ледяной водой через раствор в течение 2 ч пропускают метиламин. Реакционную смесь фильтруют, промывают водой, сушат, упаривают и перекристаллизовывают из бензола. Получают 12,4 г продукта (выход 84%); т.пл. 145-147оС.
П р и м е р 3. 5-Нитронафталин-1-(N-этил)-сульфамид получают аналогично примеру 1 из 2,5 г хлоргидрата этиламина с выходом 75%
П р и м е р 4. 5-Нитронафталин-1-(N-пропил)-сульфамид.
Получают аналогично примеру 1 из 1,2 г (0,02 моль) пропиламина с выходом 85% (2,5 г); т.пл. 131-133оС.
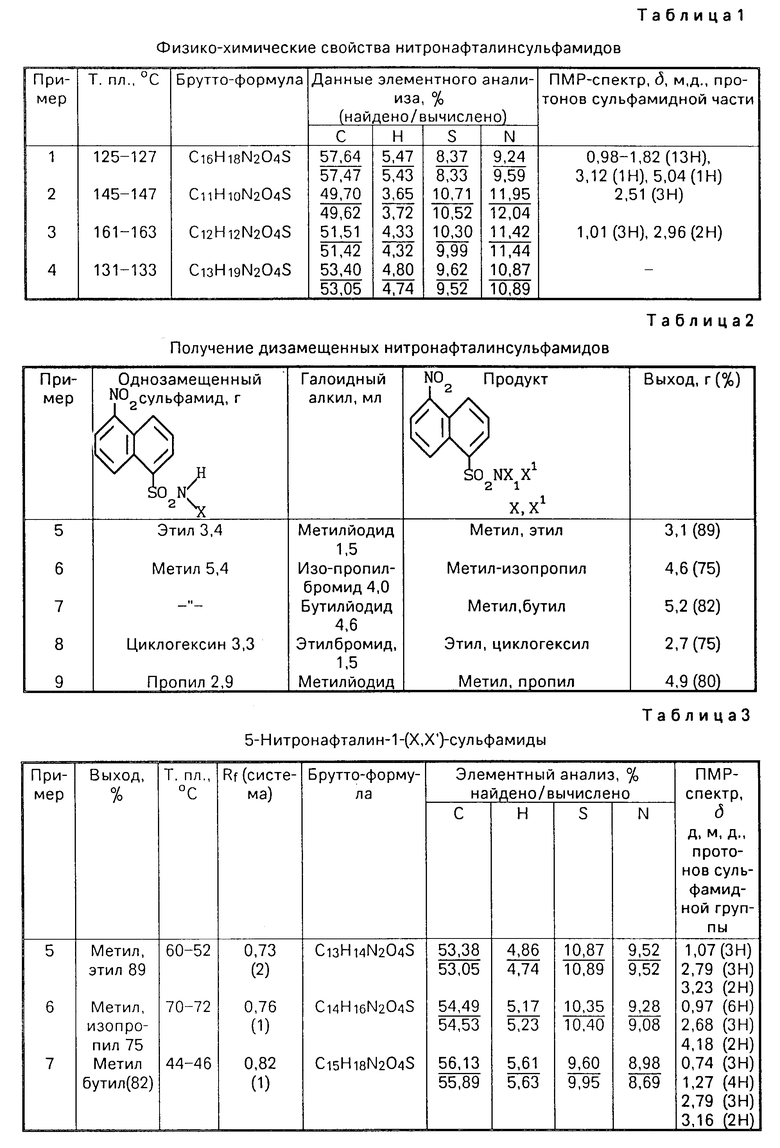
Физико-химические свойства нитронафталинсульфамидов формулы I приведены в табл. 1.
Использование соединений общей формулы I в качестве полупродуктов для получения несимметрично-замещенных 5-аминонафталин-1-сульфамидов приведены в примерах 5-14.
П р и м е р 5. 5-Нитронафталин-1-(N-метил, N-этил)-сульфамид.
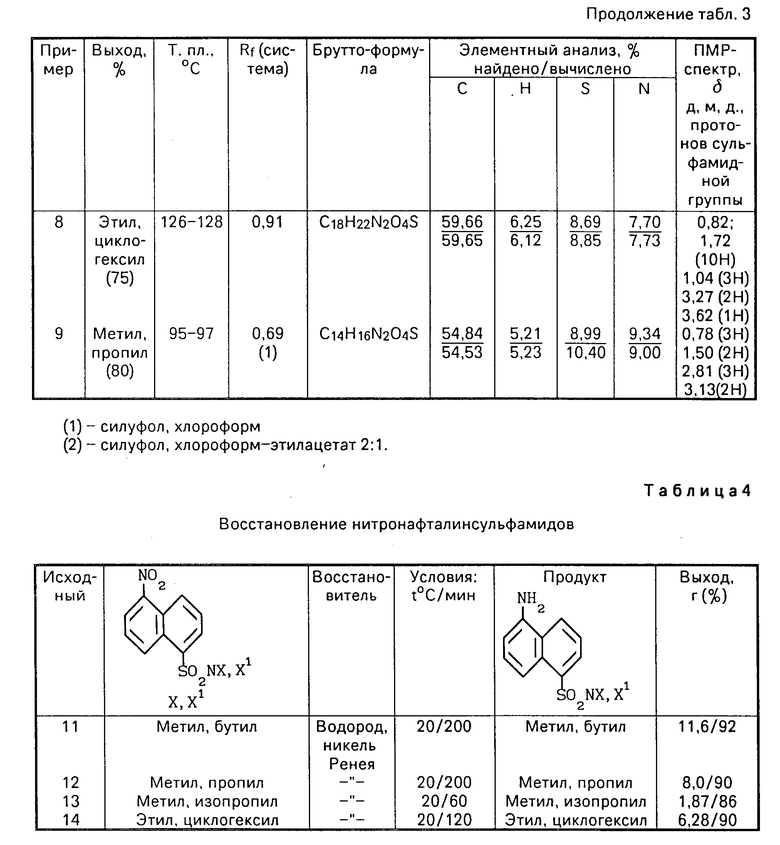
К смеси 3,4 г (0,012 моль) 5-нитронафталин-1-(N-этил)-сульфамида, 200 мл бензола 9,9 мл 50%-ного раствора NaOH и 5,12 г тетрабутиламмония бромида при перемешивании приливают 1,5 мл (0,02 моль) метилйодида. Смесь нагревают до 60оС 0,5 ч, охлаждают, бензольный слой промывают разбавленной HCl до нейтральной реакции. Продукт сушат, упаривают и перекристаллизовывают из четыреххлористого углерода. Получают 3,1 г целевого продукта; выход 89% т.пл. 60-62оС. Другие примеры 6-9 использования заявляемых веществ даны в табл. 2. Физико-химические свойства дизамещенных нитронафталин сульфамидов представлены в табл. 3.
П р и м е р 10. А-Аминонафталин-1-(N-метил, N-этил)-сульфамид.
12,9 г (0,04 моль) 5-нитронафталин-1-(N-метил, N-этил)-сульфамида растворяют в 400 мл метанола, добавляют никель Ренея, и гидрируют водородом при атмосферном давлении и 20оС. После поглощения рассчитанного количества водорода катализатор отфильтровывают, раствор упаривают досуха и получают 10,5 г; выход 81% целевого продукта; т.пл. 83-85оС (метанол).
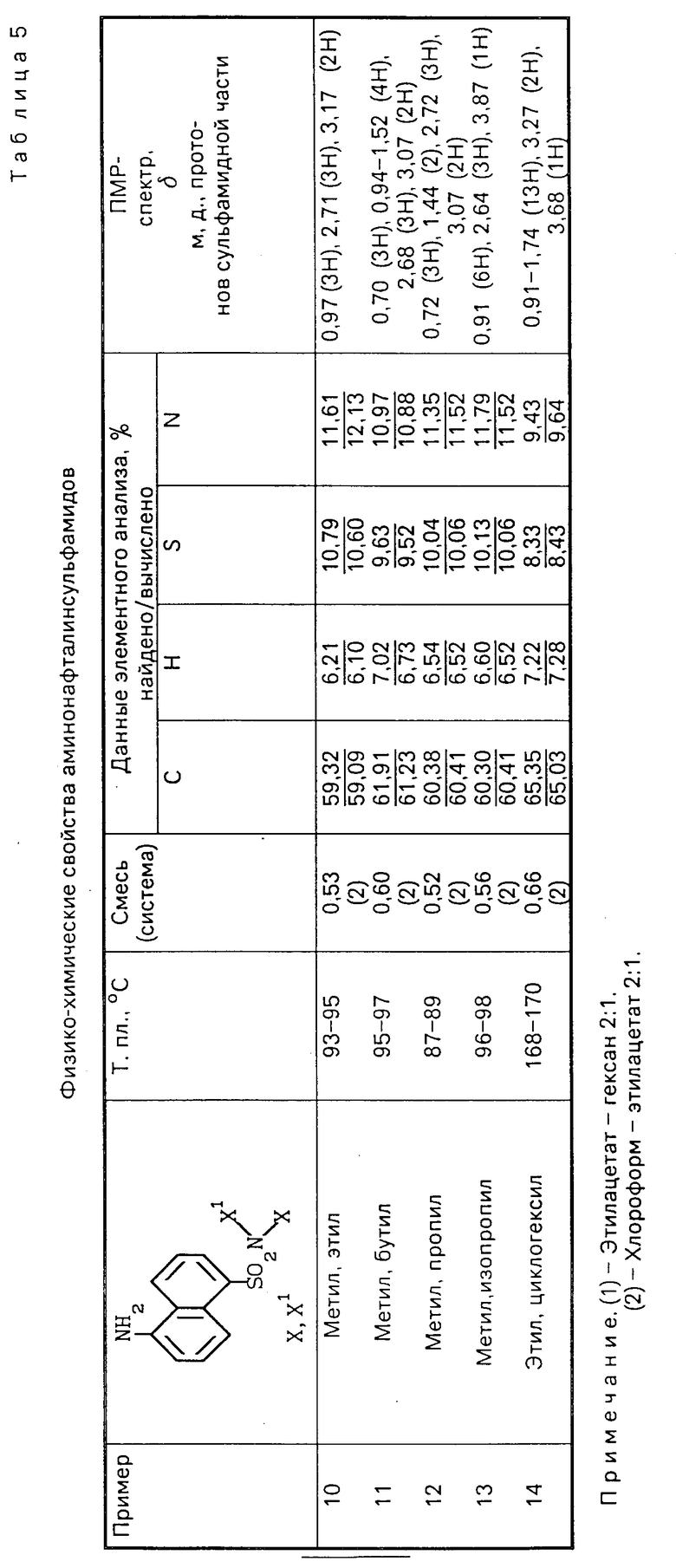
Другие примеры 11-14 получения аминонафталинсульфамидов даны в табл. 4. Физико-химические свойства дизамещенных аминонафталинсульфамидов представлены в табл. 5.
Таким образом использование монозамещенных сульфамидов нитронафталина общей формулы I в качестве полупродуктов для получения несимметричнозамещенных 5-аминонафталин-1-сульфамидов позволяет повысить информативность метода.
Изобретение касается монозамещенных сульфамидов нитронафталина, в частности соединений общей ф-лы 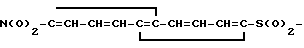 -NHR, где R=C1-C3- алкил или циклогексил, которые как полупродукты могут быть использованы для синтеза несимметричных 5-аминонафталин-1-сульфамидов, применяемых в качестве детектируемых групп для флуоресцентного анализа ферментов. Цель создание новых полупродуктов для указанного назначения с достижением лучшей информативности анализа ферментов. Синтез ведут реакцией соответствующего алкил- или циклогексиламина с 5-нитронафталин-1-сульфохлоридом в присутствии Na2CO3 в среде водного толуола с последующей нейтрализацией до pH 5 и выделением целевого продукта. Выход, т.пл.°С; брутто-ф-ла: а)82; 125-127; C16H16N2O4S; б) 84; 145-147; C11H10N2O4S; в) 75; 161-163; C12H14N2O4S; г) 85,131-133; C13H14N2O4S. 5 табл.
-NHR, где R=C1-C3- алкил или циклогексил, которые как полупродукты могут быть использованы для синтеза несимметричных 5-аминонафталин-1-сульфамидов, применяемых в качестве детектируемых групп для флуоресцентного анализа ферментов. Цель создание новых полупродуктов для указанного назначения с достижением лучшей информативности анализа ферментов. Синтез ведут реакцией соответствующего алкил- или циклогексиламина с 5-нитронафталин-1-сульфохлоридом в присутствии Na2CO3 в среде водного толуола с последующей нейтрализацией до pH 5 и выделением целевого продукта. Выход, т.пл.°С; брутто-ф-ла: а)82; 125-127; C16H16N2O4S; б) 84; 145-147; C11H10N2O4S; в) 75; 161-163; C12H14N2O4S; г) 85,131-133; C13H14N2O4S. 5 табл.
Монозамещенные сульфамиды нитронафталина общей формулы I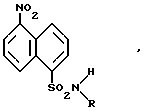
где R CH3, C2H5, C3H7, циклогексил, в качестве полупродуктов для получения несимметричнозамещенных 5-аминонафталин-1-сульфамидов.
| 5-(N-КАРБОБЕНЗОКСИ)АМИНОНАФТАЛИН-1-СУЛЬФОНАТ НАТРИЯ В КАЧЕСТВЕ ПОЛУПРОДУКТА ДЛЯ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 5-АМИНОНАФТАЛИН-1-СУЛЬФАМИДОВ, ИСПОЛЬЗУЕМЫХ В КАЧЕСТВЕ ДЕТЕКТИРУЕМЫХ ГРУПП ФЕРМЕНТНЫХ СУБСТРАТОВ | 1985 |
|
SU1419107A3 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-10-20—Публикация
1989-02-08—Подача