Изобретение относится к химии нафталинсульфамидов, а именно к новым N, N-дизамещенным 1-нитронафталин-5-сульфамидам общей формулы I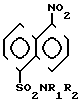 где группа NR1R2 -N(CH3)C2H5; -N(CH3)C3H7; -N(CH3), изо--N
где группа NR1R2 -N(CH3)C2H5; -N(CH3)C3H7; -N(CH3), изо--N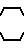 O; -N
O; -N , C3H7, -N(CH3)C4H9; -N(C2H5)-циклоС6Н11; в качестве полупродуктов для получения 1-аминонафталин-5-сульфамидов, которые используют в качестве детектируемых групп для качественного АНСА-анализа ферментов, обладающих аргиниламинопептидазной активностью.
, C3H7, -N(CH3)C4H9; -N(C2H5)-циклоС6Н11; в качестве полупродуктов для получения 1-аминонафталин-5-сульфамидов, которые используют в качестве детектируемых групп для качественного АНСА-анализа ферментов, обладающих аргиниламинопептидазной активностью.
Целью изобретения является изыскание в ряду 1-замещенных нафталин-5-сульфамидов новых нафталинсульфамидов, использование которых в качестве полупродуктов для 1-аминонафталин-5-сульфамидов позволяет упростить процесс получения известных 1-аминонафталин-5-сульфамидов, исходя из товарных продуктов, и расширить ассортимент получаемых 1-аминонафталин-5-сульфамидов.
П р и м е р 1. 1-Нитронафталин-(N-циклогексил)сульфамид.
Смешивают 2 мл (0,02 моль) циклогексиламина, 50 мл толуола, 100 мл воды и 26,5 г двузамещенного карбоната натрия. При перемешивании и охлаждении ледяной водой добавляют 2,7 г (0,01 моль) 1-нитронафталин-5-сульфохлорида. Смесь выдерживают 3 ч при комнатной температуре, нейтрализуют концентрированной HCl до рН 5, отделяют толуольный слой, водный слой и экстрагируют хлороформом. Оба органических раствора соединяют, упаривают и остаток перекристаллизовывают из бензола. Получают 2,7 г (82%) целевого продукта с т. пл.125-127оС.
П р и м е р 2. 1-Нитронафталин-5-(N-метил)сульфамид.
15 г (0,055 моль) 1-нитронафталин-5-сульфохлорида растворяют в 300 мл абсолютного хлороформа. При охлаждении ледяной водой через раствор в течение 2 ч пропускают метиламин. Реакционную смесь фильтруют, промывают водой, сушат, упаривают и перекристаллизовывают из бензола. Получают 12,4 г продукта (84%) с т.пл.145-147оС.
П р и м е р 3. 1-Нитронафталин-5-(N-метил,N-этил)сульфамид.
К смеси 2,7 г (0,01 моль) 1-нитронафталин-5-(N-метил)сульфамида, 200 мл бензола, 8,5 мл 50%-ного раствора NaOH и 0,8 г тетрабутиламмония бромида при перемешивании приливают 1,5 мл (0,02 моль) этилбромида. Смесь нагревают до 60оС 2 ч. Реакционную массу охлаждают, бензольный слой отделяют и промывают разбавленной HCl до нейтральной реакции, сушат и упаривают, остаток перекристаллизовывают из четыреххлористого углерода. Получают 2,5 г целевого продукта (88%) с т.пл.60-62оС.
П р и м е р 4. 1-Нитронафталин-5-(N-метил,N-пропил)сульфамид.
Аналогично примеру 3 из 5,4 г (0,02 моль) 1-нитронафталин-5-(N-метил)сульфамида получают 4,9 г (80%) целевого продукта с т.пл. 95-97оС.
П р и м е р 5. 1-Нитронафталин-5-(N-этил,N-циклогексил)сульфамид.
Аналогично примеру 3 из 3,3 г 1-нитронафталин-5-(N-циклогексилсульфамида) и 1,5 мл этилбромида получают 2,7 г (75%) продукта с т.пл.126-128оС.
П р и м е р 6. 1-Нитронафталин-5-[N-(3-окси)пентаметилен]сульфамид.
Смешивают 1,8 мл (0,02 моль) морфолина, 50 мл толуола, 100 мл воды и 26,5 г дизамещенного карбоната натрия. При перемешивании и охлаждении ледяной водой добавляют 2,7 г (0,01 моль) 1-нитронафталин-5-сульфохлорида. Смесь выдерживают 3 ч при комнатной температуре, нейтрализуют концентрированным раствором HCl до рН 5, толуольный слой отделяют. Водный слой экстрагируют хлороформом. Оба органических раствора соединяют, упаривают, перекристаллизовывают из бензола и получают 2,6 г (выход 82%) продукта с т.пл. 123-125оС.
П р и м е р 7. Аналогично примеру 6 из гексаметиленимина получен 1-нитронафталин-5-(N-гексаметиленимина)сульфамид. Выход 1-нитронафталин-5-(N-гексаметилен)сульфамида 90% т.пл.78-80оС.
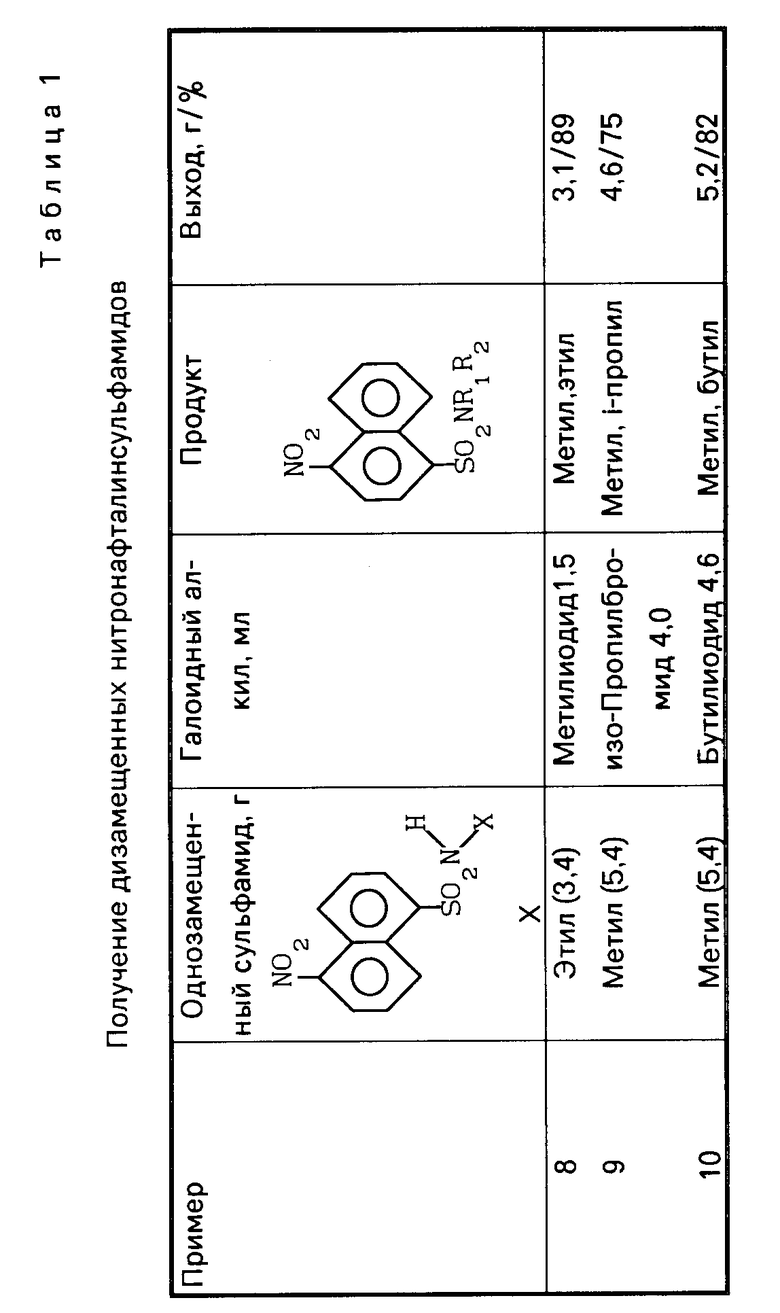
Данные для получения других соединений в условиях примера 3 приведены в табл.1.
П р и м е р 11. 1-Аминонафталин-5-(метил,этил)сульфамид.
12,9 г (0,04 моль) 1-нитронафталин-5-(N-метил,N-этил)сульфамида растворяют в 400 мл метанола, добавляют никель Ренея и гидрируют водородом при 20оС. После поглощения рассчитанного количества водорода катализатор отфильтровывают, раствор упаривают досуха и получают 10,5 г (выход 81%) целевого продукта с т.пл.83-85оС (метанол).
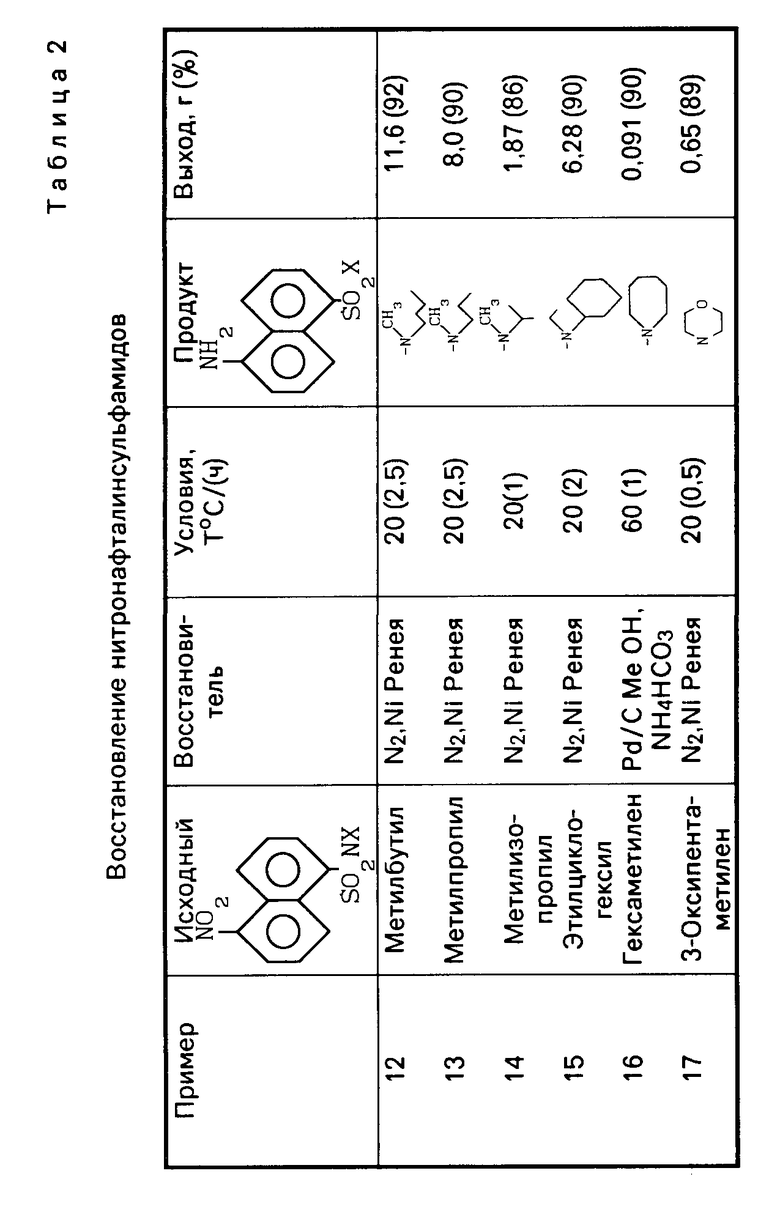
Другие примеры получения 1-аминонафталин-5-сульфамидов в условиях примера 11 сведены в табл.2.
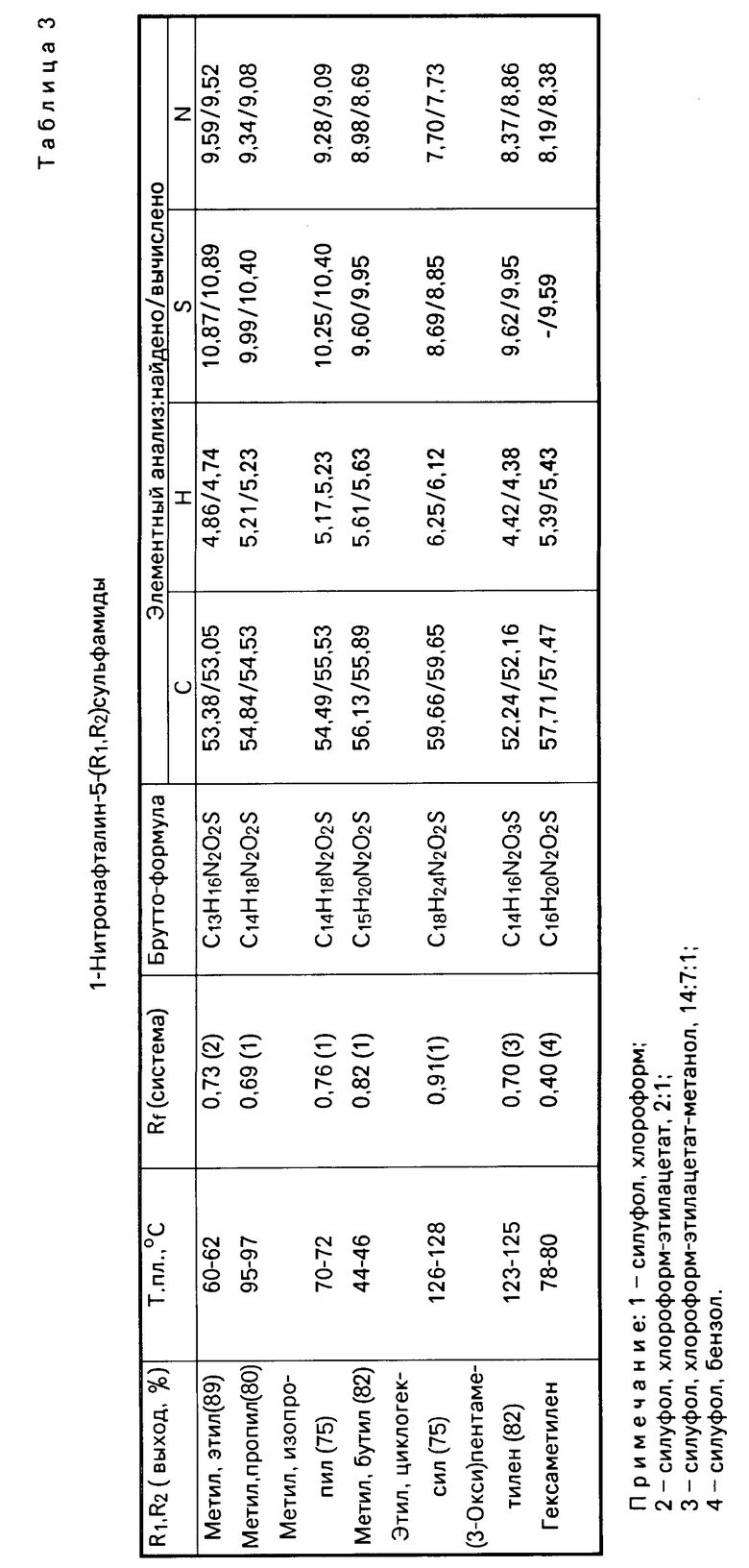
Физико-химические свойства 1-нитронафталин-5-сульфамидов приведены в табл. 3. В табл.4 приведены физико-химические свойства новых 1-аминонафталин-5-сульфамидов, полученных из 1-нитронафталин-5-сульфамидов.
Использование известных и новых 1-аминонафталин-5-сульфамидов для качественного АНСА-анализа ферментов, обладающих аргиналаминопептидазной активностью, иллюстрируется следующим примером.
П р и м е р 18. К раствору 3,5 г карбобензоксиаргинина в 20 мл диметилформамида приливают при 10оС полученный при 30оС и выдержанный при 20оС в течение 40 мин раствор 1 мл SOCl2 в 10 мл диметилформамида, перемешивают 30 мин при 4оС, охлаждают до 20оС, добавляют раствор смеси аминонафталин-1-сульфамидов в 10 мл диметилформамида (по 1 ммоль каждого из пяти или эквимолярные количества каждого из серии, в сумме 5 ммоль), вливают 1,5 мл триэтиламина, перемешивают 4 ч при 4оС и 12 ч при 20оС, добавляя триэтиламин до слабощелочной реакции. Приливают 150 мл этилацетата и 200 мл гексана, осадок промывают смесью этилацетата и гексана, растворяют в смеси бутанола и воды, верхний слой отделяют, водный экстрагируют бутанолом. Бутанольные вытяжки промывают 5%-ной NaHCO3, 10%-ной KHSO4, упаривают досуха, заливают 40 мл 2,5 М HBr и CH3COOH. Через 1,5 ч добавляют 600 мл диэтилового эфира. Осадок растворяют в воде, экстрагируют этилацетатом. Водный слой подщелачивают NaOH до рН 7,5, экстрагируют бутанолом, упаривают, растворяют в воде до концентрации 300 О.Е./мл. Экстрагируют смесью этилацетата (4) и гексана (1), экстракт отбрасывают, водный слой упаривают в вакууме до удаления этилацетата и используют для приготовления субстратных смесей, растворяя аликвоту в буферном растворе (например, 0,005 М трис-HCl + 0,005 М дитиотреита, рН 7,4) и разбавляя водой до концентрации 7 О.Е./мл.
Добавляют один из неиспользованных для приготовления субстратной смеси АНСА в качестве внутреннего стандарта до концентрации 0,1 О.Е./мл, аликвоту 0,5 мл помещают в кювету спектрофотометра и термостатируют. Добавляют 10 мкл исследуемого фермента, регистрируют изменение поглощения λ 360 нм во времени, по возрастании поглощения вдвое от первоначального останавливают реакцию добавлением, например, ингибитора протеаз данного класса. Смесь экстрагируют 0,5 мл этилацетата, экстракт упаривают, остаток растворяют в 30 мкл 38% -ного ацетонитрила с добавкой 0,1 М ацетата аммония, анализируют ВЭЖХ с элюированием тем же раствором, интегрированием пиков определяют количества образовавшихся АНСА. (Колонка Zarbax С-18, 250х4,6 мм, при 40оС, скорость потока 1 мл/мин, УФ-детектор λ255 нм). При определении относительных величин используют высоты пиков при графической регистрации хроматограммы.
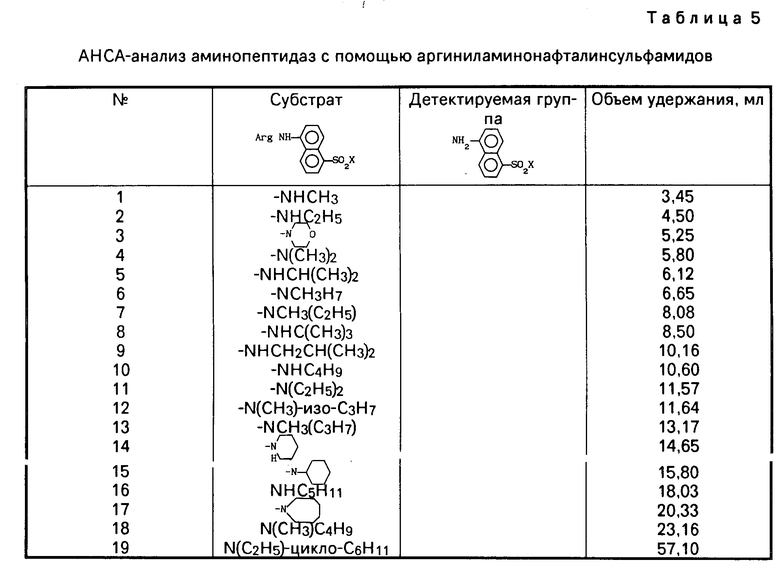
В табл.5 приведены объемы удерживания для различных 1-аминонафталин-5-сульфамидов.
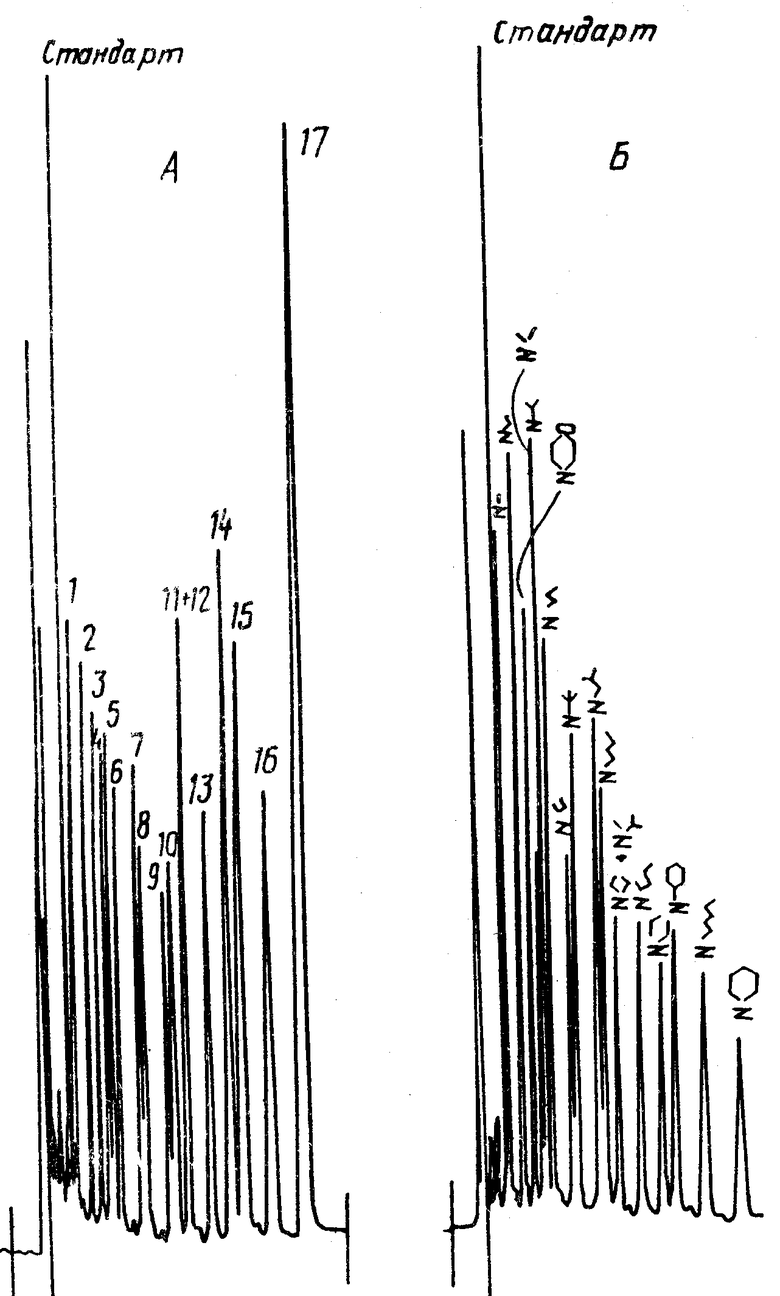
В качестве примера получения АНСА-спектров ферментов приведен чертеж (позиции на чертеже соответствуют номерам в табл.5).
Спектры аргиниламинопептидазной активности коммерческих препаратов панкреатической пептидазы (A) и протеиназы К (B) сняты на хроматографе фирмы ВЭЖХ фирмы Дю-Пон (США) с использованием колонки Zorbax C-18 (4,6х250 мм) при 40оС и скорости потока 1 мл/мин с детекцией по поглощению λ255 нм и элюированием 38%-ного ацетонитрила с добавкой 0,1 М ацетата аммония.
Таким образом, использование соединений формулы I в качестве полупродуктов позволяет упростить процесс получения известных 1-аминонафталин-5-сульфамидов (три стадии против четырех) с использованием известных полупродуктов, исходя из товарных продуктов (1-нитронафталин-5-сульфокислоты соответственно).
При этом выход конечных аминонафталинсульфамидов составляет 65-72% против 69-75% при использовании известных полупродуктов, а также значительно уменьшается их себестоимость благодаря исключению из числа реагентов дорогого трифторуксусного ангидрида.
Использование полупродуктов формулы I также позволяет получить изомерно чистые целевые продукты с меньшими затратами на очистку и расширить ассортимент получаемых целевых продуктов.

Изобретение касается замещенных сульфамидов, в частности N, n- диалкилзамещенных 1-нитронафталин-5-сульфамидов, в которых NR1R2 остаток метилэтиламина метилпропиламина, метилизопропиламина, метилбутиламина, этилциклогексиламина, морфолина или азепина, которые могут быть использованы в качестве полупродуктов для синтеза 1-аминонафталин-5-сульфамидов. Цель создание новых полупродуктов для указанного назначения. Синтез ведут реакцией 1-нитронафталинсульфохлорида с соответствующим амином в присутствии карбоната натрия в среде растворителя (толуола). Новые полупродукты получают с высоким выходом и они обеспечивают получение целевых аминонафталинсульфамидов с меньшей себестоимостью за счет исключения использования дорогого трифторуксусного ангидрида и меньшими затратами на очистку. 1 ил. 5 табл.
N, N-Диалкилзамещенные 1-нитронафталин-5-сульфамиды общей формулы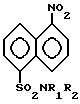
где группа R1R2 -N(CH3)C2H5; -N(CH3)C3H7; -N(CH3)-изо-C3H7; -N(CH3)C4H9;
-N(C2H5)-цикло-C6H11;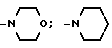
в качестве полупродуктов для получения 1-аминонафталин-5-сульфамидов.
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 1-АМИНОНАФТАЛИН-5-СУЛЬФАМИДОВ | 1987 |
|
SU1648054A3 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-12-20—Публикация
1989-02-08—Подача