Изобретение относится к медицинской микробиологии и биотехнологии, касается штамма бактерий, служащего эталоном для получения цитолизина, и может найти применение при изучении механизма действия цитолизина на мембраны клеток и клеточные культуры, в роли цитолизина в патогенезе заболевания, при этом цитолизин может использоваться при создании диагностических препаратов, получении гибридом, продуцирующих антитела к этому токсину, а также при решении вопросов таксономии холерных вибрионов.
Известен штамм бактерий Vibrio metscnnikovii, способный продуцировать
биологически активный цитолизин, но он относится к другому виду.
Известен штамм бактерий V. cholerae non-01 2194 с, продуцирующий цитолизин. Последний является белком с мол.м. 52711 и изоэлектрической точкой (р1)8,65. Данный цитолизин лизирует эритроциты кролика, клеточные культуры У-1 и СНО, вызывает накопление жидкости в лигированной петле кролика в дозе 600 мкг.
Однако известный штамм относится к другой серологической группе (по соматическому 0-антигену). Продуцируемый им цито- лизин отличается от полученного цитолизина по молекулярной массе и изоVI
Ю Ю О
электрической точке, а также слабо выраженной биологической активностью.
Целью изобретения является получение штамма бактерий Vibrio choierae 01 eltor KM 169, используемого в качестве эталона для получения очищенного препарата биологически активного цитолизина.
Штамм получен из мизид, отловленных в районе спасательной станции северного побережья Капчагайского водохранилища, путем секции по 01-антигену при помощи 01-холерной сыворотки.
Оптимальные условия хранения - в ли- офилизированном состоянии при 4°С.
Штамм имеет следующую характеристику.
Культурально-морфологические признаки.
На жидких и плотных питательных средах дает типичный рост, характерный для вибрионов; в поле фазово -контрастного микроскопа типичная для вибрионов морфология микробных клеток с характерной для этого микроба подвижностью.
физиолого-биохимические признаки.
Реакция на индофенолоксидазу положительна, расщепляет глюкозу в аэробных и анаэробных условиях, обладает лизин- и орнитиндекарбоксилазой, не обладает ар- гининдегидролазой, образует индол и сероводород, разжижает желатину, обладает лецитиназной активностью, расщепляет без газа маннозу, сахарозу, маннит и инозит, не разлагает лактозу и арабинозу, дает положительную реакцию Фогес-Проскауэ- ра, лизирует эритроциты овцы в пробе по Грейгу (30 мин при 37°С), агглютинирует эритроциты курицы.
Отношение к холерным диагностическим сывороткам - агглютинируется 0-хо- лерной сывороткой до титра, сывороткой Инаба до титра, не агглютинируется сывороткой Огава.
Отношение к холерным диагностическим фагам (ХДФ): чувствителен к фагу Эль Тор и не лизируется фагом С, лизируется фагом ХДФз и не чувствителен к ХДФ 4,5, относится к 10-му фаготипу по Дрожевки- ной-Арутюнову. Питательные потребности - прототроф.
Генетические особенности: чувствителен к тетрациклину (МЗК-0,015 мкг/мл). растет на 50 ед./мл полимиксина.
На фиг.1 и 2 приведены кривые распределения при исследовании нового штамма. При м е р 1. Получение и очистка цитолизина.
Штамм выращивают при 37°С в течение 18 ч на агаре Мартена. Из выросших колоний готовят суспензию в 0,15 М растворе
NaCI с концентрацией микробных к/.еток 1 млрд/мл колониеобраэующих единиц (КОЕ). Суспензию используют в качестве по- . севного материала, который вносят из расчета 1 млрд КОЕ на 100 мл среды в
модифицированную среду Davis следующего состава, г/л: К2НР04 7,0; КНаРО 2,0; (NH4)2S04 1,0; цитрат натрия 0,5; MgS04- 7Н20 0,1; дистиллированная вода - до 1 л. После автоклавирования при 120°С в тече0 ние 15 мин добавляют 3% (o64/o6J стерильного глицерина.
Культивирование проводят в плоских флаконах емкостью 1 л (в каждый флакон вносят200 мл среды) при 37°С в течение 48
5ч без встряхивания. После добавления мер- тиолата натрия до концентрации 0,02% и экспозиции в течение 20 ч культуральную жидкость освобождают от клеток центрифугированием при 10000 g в течение 30 мин.
0 Извлечение гемолитически активного белка из стерильного культурального супер- натанта производят путем добавления сухого сульфата аммония до 50% насыщения при 4°С. Смесь перемешивают до полного
5 растворения соли и центрифугируют при 10 тыс. g в течение 30 мин. Осадок суспендируют в 20 мМ трис-HCI буфере с 1 мМ ЕДТА, рН 7,6(ТЕ-буфер). Освобождение препарата от сульфата аммония осуществляют путем
0 диализа против -20 объемов ТЕ-буфера в течение 18 ч. Полученный на предыдущем этапе препарат наносят на колонку размером 50 х 15 мм с ДЕ-52, уравновешенную ТЕ-бу- фером. Элюцию проводят буфером ТЕ с 2005 мМ NaCI. Для концентрирования активного белка используют преципитацию сульфатом аммония (50% насыщения). Полученный после центрифугирования при 10 тыс. g в течение 30 мин осадок растворяют в ТЕ-буфере
0 и освобождаются от (NH4)aSO4 на колонке (1,6 х 40 см) с SephadexG-25, уравновешенной буфером 20 мМ трис-HCI, 1 мМ ЕРТА, 0,14 М NaCI, рН 7.6 (TEN-буфер).
Полученную на предыдущем этапе
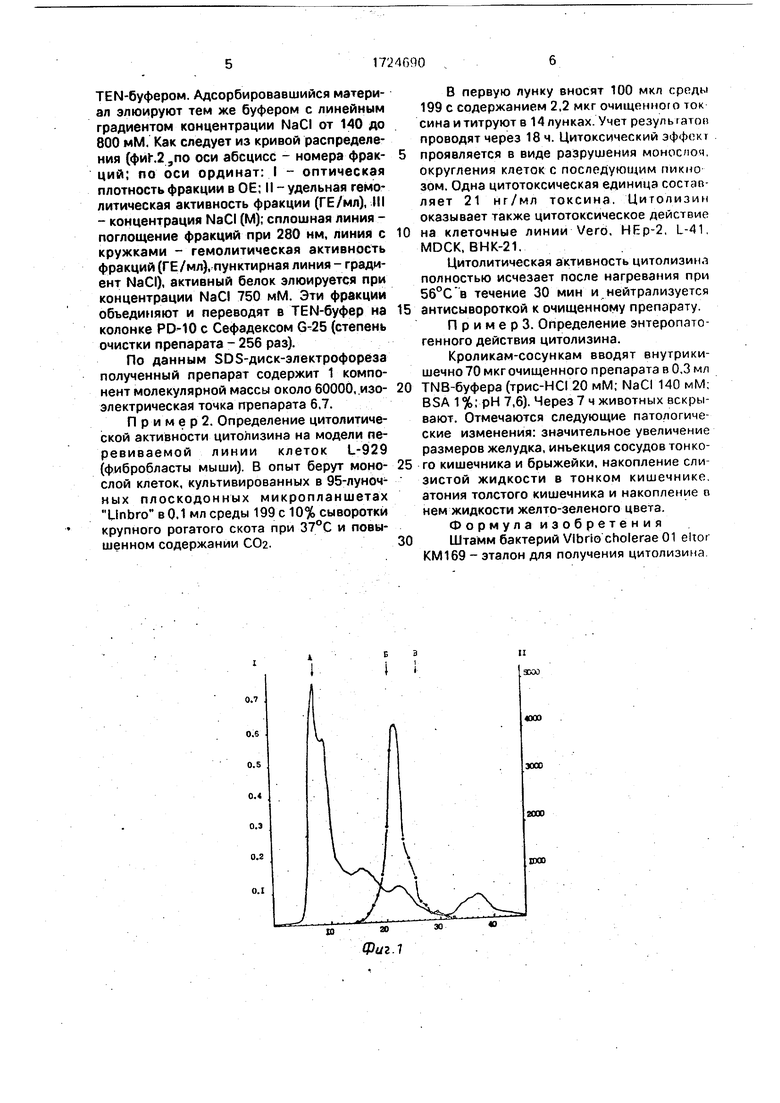
5 фракцию наносят на колонку с ультрагелем АсА-44, уравновешенную буфером ТЕ (2,5 х XI00 см). Типичный профиль элюции представлен на фиг. 1 (по оси абсцисс - номера фракций; по оси ординат: I - оптическая
0 плотность фракций в относительных единицах (ОЕ), а II - удельная гемолитическая активность (ГЕ/мл); сплошная линия - поглощение фракций при 280 нм, линия с кружками - гемолитическая активность
5 фракций).
Активный белок элюируется в объеме, соответствующем элюции белков с мол. массой 60 + 3 кДа. Далее препарат наносят на колонку 0,5 х 5 см MonoQ, уравновешенную
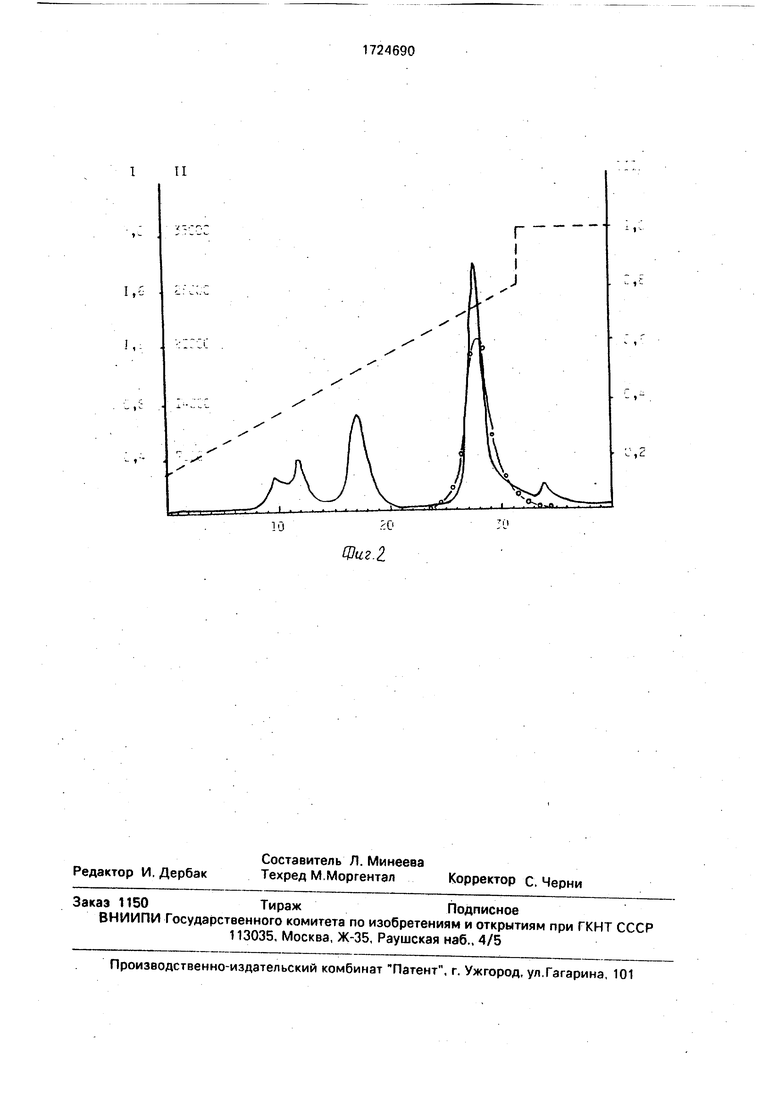
TEN-буфером. Адсорбировавшийся материал элюируют тем же буфером с линейным градиентом концентрации NaCI от 140 до 800 мМ, Как следует из кривой распределения (фиг.2,по оси абсцисс - номера фрак- ций; по оси ординат: I - оптическая плотность фракции в ОЕ; II - удельная гемолитическая активность фракции (ГЕ/мл), III - концентрация NaCI (М); сплошная линия - поглощение фракций при 280 нм, линия с кружками - гемолитическая активность фракций (ГЕ/мл), пунктирная линия - градиент NaCI), активный белок элюируется при концентрации NaCI 750 мМ. Эти фракции объединяют и переводят в TEN-буфер на колонке PD-10 с Сефадексом (степень очистки препарата - 256 раз).
По данным SDS-диск-электрофорёза полученный препарат содержит 1 компонент молекулярной массы около 60000, изо- электрическая точка препарата 6,7.
П р и м е р 2. Определение цитолитиче- ской активности цитолизина на модели перевиваемой линии клеток L-929 (фибробласты мыши). В опыт берут моно- слой клеток, культивированных в 95-луноч- ных плоскодонных микропланшетах Llnbro в 0.1 мл среды 199 с 10% сыворотки крупного рогатого скота при 37°С и повышенном содержании СОа.
В первую лунку вносят 100 мкл среды 199 с содержанием 2,2 мкг очищенного ток синаи титруют в 14 лунках. Учет результатов проводят через 18 ч. Цитоксический эффект проявляется в виде разрушения монослоч, округления клеток с последующим пикно зом. Одна цитотоксическая единица составляет 21 нг/мл токсина. Цитолизин оказывает также цитотоксическое действие на клеточные линии Verb. HEp-2, L-41, MDCK, ВНК-21.
Цитолитическая активность цитолизина полностью исчезает после нагревания при 56°С в течение 30 мин и нейтрализуется антисывороткой к очищенному препарату.
Примерз. Определение энтеропато- генного действия цитолизина.
Кроликам-сосункам вводят внутрики- шечно 70 мкг очищенного препарата в 0,3 мл TNB-буфера (трис-НС 20 мМ; NaCI 140 мМ; BSA 1 %; рН 7,6). Через 7 ч животных вскрывают. Отмечаются следующие патологические изменения: значительное увеличение размеров желудка, инъекция сосудов тонкого кишечника и брыжейки, накопление слизистой жидкости в тонком кишечнике, атония толстого кишечника и накопление о нем жидкости желто-зеленого цвета.
Ф о р м у л а и з о б р е т е н и я
Штамм бактерий Vibrio cholerae 01 eltor КМ169 - эталон для получения цитолизина

| название | год | авторы | номер документа |
|---|---|---|---|
| АВИРУЛЕНТНЫЙ ТЕСТ-ШТАММ БАКТЕРИЙ Vibrio cholerae БИОВАРА eltor СЕРОВАРА Ogawa (ctxA-, tcpA-, toxR-, zot-), ИСПОЛЬЗУЕМЫЙ В ИММУНОЛОГИЧЕСКИХ, ГЕНЕТИЧЕСКИХ ИССЛЕДОВАНИЯХ И УЧЕБНОМ ПРОЦЕССЕ | 2004 |
|
RU2254371C1 |
| Штамм бактерий VIвRIо сноLеRае еLтоR INава - продуцент @ -амилазы | 1990 |
|
SU1726514A1 |
| Штамм бактерий VIвRIо сноLеRае еLтоR OGaWa - продуцент внеклеточной нейтральной протеазы | 1990 |
|
SU1726515A1 |
| СПОСОБ ВНУТРИВИДОВОЙ ДИФФЕРЕНЦИАЦИИ Vibrio cholerae О139 | 2004 |
|
RU2268942C1 |
| Штамм бактерий VIвRIо сноLеRае еLтоR, используемый для получения диагностических сывороток | 1989 |
|
SU1684333A1 |
| Рекомбинантная плазмида, экспрессирующая клонированный ген гемолизина Vibrio cholerae, и штамм Escherichia coli - суперпродуцент прогемолизина Vibrio cholerae | 2017 |
|
RU2671099C1 |
| Штамм бактерий VIвRIо сноLеRае еLтоR - источник умеренного фага х1 серотипа 1х гетероиммунной категории | 1988 |
|
SU1551735A1 |
| Штамм бактерий VIвRIо сноLеRае еLтоR, используемый для получения диагностических сывороток | 1989 |
|
SU1684332A1 |
| Штамм вибриона VIвRIо сноLеRае сноLеRае - продуцент гемолизина | 1986 |
|
SU1391091A1 |
| Штамм бактерий VIвRIо сноLеRае еLтоR серовара 2, используемый для приготовления диагностической сыворотки | 1989 |
|
SU1701741A1 |

Изобретение относится к медицинской микробиологии и биотехнологии, касается штамма бактерий, служащего эталоном для получения цитолизина, и может найти применение при изучении механизма действия цитолизина на мембраны клеток и клеточные культуры, роли цитолизина в патогенезе заболевания. Цитолизин может использоваться при создании диагностических препаратов, получении гибридов, продуцирующих антитела к этому токсину, а также при решении вопросов таксономии холерных вибрионов. Целью изобретения является получение штамма бактерий Vibrio cholerae 01 eltor KM 169, используемого в качестве эталона для получения очищенного препарата биологически активного цитолизина. Из штамма выделен цитолизин, имеющий молекулярную массу 60 кДа, изоэлектрическую точку 6,7 и обладающий выраженной цитолитической, энте- ропатогенной, летальной, отекогенной активностью. 2 ил. ел С

| Miyake M | |||
| e.a | |||
| Purification and characterization of Vibrio metschnikovl cytolysin.- Infection and Immunity, 1988, v | |||
| Приспособление для разматывания лент с семенами при укладке их в почву | 1922 |
|
SU56A1 |
| p | |||
| Приспособление для выверки планиметра | 1923 |
|
SU954A1 |
| Me Cardell B.A | |||
| e a | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| J | |||
| Microblol., 1985, v | |||
| Способ очистки нефти и нефтяных продуктов и уничтожения их флюоресценции | 1921 |
|
SU31A1 |
| p | |||
| ШТАНГЕН-ЦИРКУЛЬ С ВЫДВИЖНОЮ НОЖКОЮ | 1922 |
|
SU711A1 |
Авторы
Даты
1992-04-07—Публикация
1990-04-28—Подача