Указано на образование амидразона А, который не был выделен в виду легкости его рециклизации в производное пиррола и поэтому охарактеризован как гипотетический амидразон.
Целью изобретения является разработка способа получения (1-адамантил)-М -{2,4- динитрофенил)-3-бром-4-(п-Н-фенил}-2,4-ди- оксобутанамидразонов, обладающих высокой антимикробной активностью.
Указанная цель достигается тем, что смесь эквимолекулярных количеств (1- адамантил)имино -4-бром-5-(п-Н-фенил)-2,3- дигидро-3-фуранов и 2,4-динитрофенилгидразина в диоксане выдерживают при комнат- ной температуре в течение 1,5-2 ч с последующим выделением продукта по схеме
1|Нг NH
Вг О
nWAffy ud п
№г
;г
Вг
-R-c6Hrc-CKcfMH NO
6 и о о
Исходный (1-адамантил)имино -4- бром-5-(п-толил)-2,3-дигидро-3-фуранон об- разуется с высоким выходом при взаимодействии эквимолекулярных количеств 4-бром-5-(п-толил)-2,3-дигидро-2,3- фурандиона и 1-адамантилизоцианида в ксилоле при температуре кипения в течение 1-2 ч. (1-Адамантил)имино -4-бром-5- (п-хлорфенил)-2,3-дигидро-3-фуранон получен по аналогичной методике.
Полученные соединения представляют собой светло-оранжевые кристаллические вещества, хорошо растворимые в хлороформе, бензоле, ДМФА и ДМСО.
П р и м е р 1. (1-Адама нтил)-М2(2,4-ди- нитрофенил)-3-бром-4-п-толил-2,4-диоксо - бутанамидразон.
В раствор 0,8 г (0,002 М) (1-адаман- тил) имино -4- бром-5-(п-толил)-2,3- -дигид- ро-3-фуранона в 15 мл абс. диоксана вливают раствор 0,40 г (0,002 М) 2,4-динит- рофенилгидразина (2,4-ДНФГ) в 15 мл абс. диоксана. Через 1,5 ч растворитель упаривают, остаток кристаллизуют из смеси диэ тилового эфира и гексана (2:1), получают 0,90 г (76%) целевого продукта с Т.пл. 152- 153° С.
5
0
5
0
5
0
5 0
5
0
5
Найдено, %: С 54,53; Н 4,35; Вг 13,83; N 11,98.
С27Н28ВгМбОб
Вычислено, %: С 54,18; Н 4,68, Вг 13,38; N11,71.
П р и м е р 2. Ы -(1-Адамантил)-Мг-(2,4- динитрофенил)-3-бром-4-(п-хлорфенил)-2,4- -диоксобутанамидразон.
В раствор 0,84 г (0,002 М) (1-ада- мантил)имино -4-бром-5-(п-хлорфенил)-2,3 -дигидро-3-фуранона в 15 мл абс. диоксана вливают раствор 0,40 г (0,002 М) 2,4-ДНФГ в 15 мл. абс. диоксана. Через 2 ч растворитель упаривают, остаток кристаллизуют из ацетонитрила, получают 0,87 г (71 %) целевого продукта с Т.пл, 132-133° С.
Найдено, %: 050,84; Н 4,39; N 11,02.
C26H25BrCIN506
Вычислено, %: С 50,44; Н 4,04; N 11,32.
Уменьшение времени проведения реакции ведет к понижению выхода целевых продуктов.
ПримерЗ. В раствор 0,8 г (0,002 М) (1-адамантил)имино -4-бром-5-(п-толил) -2,3-дигидро-З-фуранона в 15 мл абс, диоксана вливают раствор 0,40 г ( М) 2,4- ДНФГ в 15 мл абс. диоксана. Через 1 ч растворитель упаривают, остаток кристаллизуют из смеси диэтилового эфира и гексана (2:1), получают 0,83 г (70%) целевого продукта с Т.пл. 152-153° С.
Увеличение времени проведения реакции не ведет к увеличению выхода целевых продуктов.
П р и м е р 4. В раствор 0,84 г (0,002 М) (1-адамантил)имино -4-бром-5-(п-хлор- фенил)-2,3-дигидро-3-фуранона в 15 мл абс. диоксана вливают раствор 0,40 г (0,002 М) 2,4-ДНФГ в 15 абс. диоксана. Через 3 ч растворитель упаривают, остаток кристаллизуют из ацетонитрила, получают 0,87 г (71%) целевого продукта с Т.пл. 132-133° С.
Замена диоксана на неполярный растворитель - бензол - является нецелесообразной, так как 2,4 -ДНФ Г труднорастворим в последнем.
Замена диосксана на метанол или этанол не представляется возможным, так как имеющиеся экспериментальные данные указывают на протекание химического взаимодействия между (1-адамантил)ими- но -4-галоген-5-(п-Р-фенил)-2,3-дигидро-3- фуранонами и алифатическими спиртами.
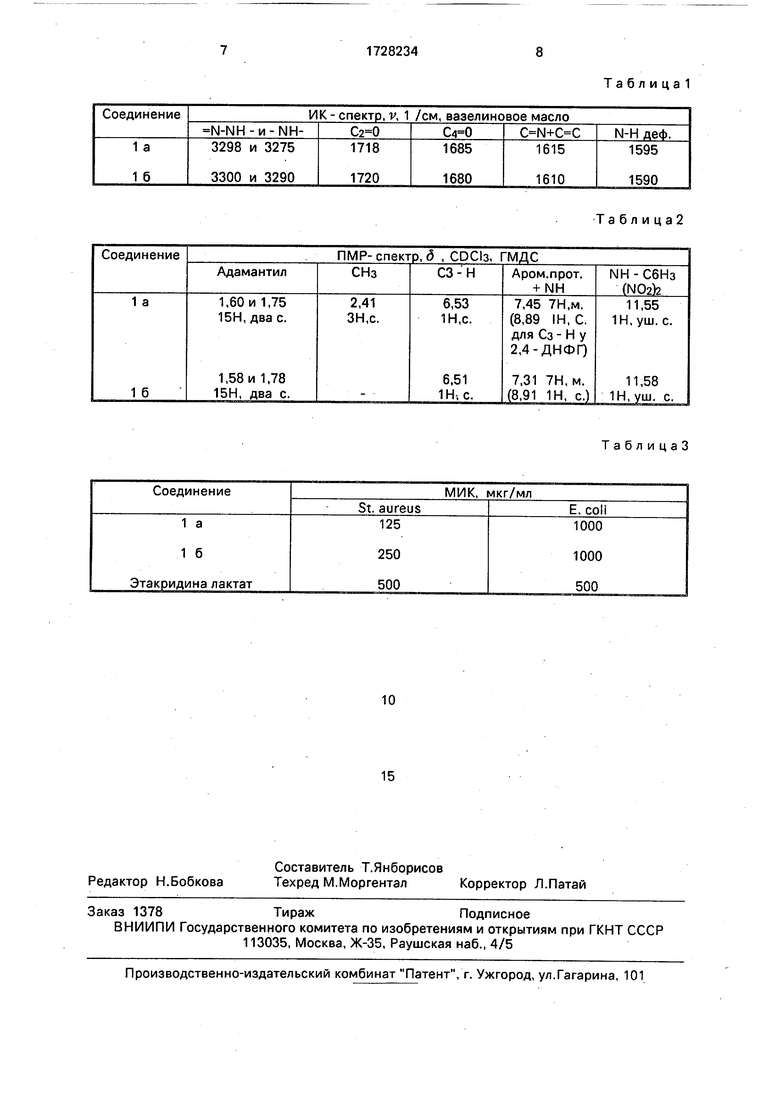
В ИК-спектрах полученных соединений, снятых на приборе UR-20 в вазелиновом масле, присутствуют две полосы поглощения при 3300-3298 и 3290-3275 относящиеся к валентным колебаниям групп -N-NH и -NH-; полосы валентных колебаний карбонильных групп: Са-О при 1720-1718
Т а б л и ц а 1


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1,6-ДИАРИЛ-3,4-ДИГИДРОКСИ-2,4-ГЕКСАЛИЕН-1,6-ДИОНОВ | 1990 |
|
SU1767835A1 |
| Способ получения производных пиперидинилалкилхиназолина или их солей с фармацевтически приемлемыми кислотами | 1980 |
|
SU1041034A3 |
| N, N', N'-ТРИЗАМЕЩЕННЫЕ ИЗОСЕЛЕНОМОЧЕВИНЫ | 2010 |
|
RU2434852C1 |
| Способ получения N-(1-адамантил)амидов 4-п-R-фенил-2,4-диоксобутантиовых кислот | 1990 |
|
SU1715805A1 |
| НОВЫЕ СОЕДИНЕНИЯ, ОБЛАДАЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ, И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2001 |
|
RU2288225C2 |
| N-(5-БРОМ-2-ПИРИДИЛ)-АМИД П-МЕТИЛБЕНЗОИЛПИРОВИНОГРАДНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНУЮ И АНАЛЬГЕТИЧЕСКУЮ АКТИВНОСТЬ | 1991 |
|
RU2021262C1 |
| Способ получения N-ацил-2-окси-1,3-диаминопропанов | 1978 |
|
SU910114A3 |
| СПОСОБ ПОЛУЧЕНИЯ 5-АРИЛ-1-П-ТОЛИЛ-4-ДИФЕНИЛМЕТИЛ-4-ЭТОКСИКАРБОНИЛТЕТРАГИДРОПИРРОЛ-2,3-ДИОНОВ | 1987 |
|
SU1482148A1 |
| Способ получения /1,2/-аннелированных 7-фенил-1,4-бензодиазепинов или их солей | 1979 |
|
SU904526A3 |
| Способ получения N,L-стирил-N-фениламидов ароилпировиноградных кислот | 1980 |
|
SU956462A1 |
Изобретение касается амидразонов, в частности получения М -(1-адамантил)- М г(2,4-динитрофенил)-3-бром-4-(п-Р-фенил) -n-R-C6H4C(-0) CH(Br)C(-0)C(-N-NH-2,4-flnнитро-СеНз-1МН-адамантил), где R СНз. CI, которые обладают противомикробной активностью и могут быть использованы в качестве лекарственных средств. Цель - разработка способа получения вышеуказанных амидразонов, обладающих высокой противомикробной активностью. Процесс ведут выдержкой смеси эквимолекулярных количеств (1-адамантил)имино -4- бром-5-(п-Р-фенил)-2,3-дигидро-3-фуранона и 2,4-динитрофенилгидразина в диоксане при комнатной температуре в течение 1,5-2 ч с последующим выделением целевого продукта. Выход 76%, Т.пл. 152-153° С для C27H28BrNs06, выход 71%, Т.пл. 132-133 для C26H25BrCINs06. Новые соединения обладают противомикробной активностью, в 2-4 раза превышающей активность этакри- дино лактата. 3 табл. (Л С
Таблица2
ТаблицаЗ
| Capuano L, Jammer T, Chem | |||
| Ber., 114, №2, 1981, с | |||
| Подвижной рельс для пересечений железнодорожных путей | 1922 |
|
SU456A1 |
Авторы
Даты
1992-04-23—Публикация
1990-03-23—Подача