Изобретение относится к органической химии, в частности к способу получения ди- ариловых эфиров, которые могут быть использованы в качестве полупродуктов для синтеза пиретроидных инсектицидов, в производстве лекарственных препаратов и высококипящих органических теплоносителей.
Известен способ получения замещенных диариловых эфиров реакцией хлортолу- ола и крезола в присутствии водного раствора щелочи при 230-400°С и давлении 100-300 атм.
К недостаткам этого способа следует отнести высокие температуру и давление, создаваемое водными растворами щелочи, что затрудняет осуществление его в промышленности. Проходящие в приведенных жестких условиях процессы не селективны и конечный продукт м-фенокситолуол выделяется из смеси диариловых эфиров с незначительным выходом - порядка 15-20%.
Известен способ получения м-фенокси- толуола из м-крезола и бром- или хлорбензола, гидроксида калия в жидкой фазе при 200°С в растворителе диметилсульфоксиде. Выход м-фенокситолуола составляет 47,5%.
К недостаткам приведенного способа относится применение малодоступного и высокотоксичного растворителя диметил- сульфоксида. Кроме того, в условиях данного процесса диметилсульфоксид не является инертным продуктом, а на 30 мас.% диспропорционируется в диметилсульфид и диметилсульфон. Диме- тилсульфид имеет температуру кипения 36°С, и это значительно осложняет ведение основного процесса при 200°С, к тому же он обладает очень неприятным запахом.
Диметилсульфон в условиях процесса (в щелочной среде) превращается в калиевую соль метилсульфиновой кислоты, которая переходит в водный слой при последующей обработке реакционной мае- сы и значительно усложняет дальнейшую переработку сточных вод данного процесса, что является немаловажным с точки зрения экологии.
В приведенных способах получения м- фенокситолуола из м-крезола и галоидаро- матических соединений, чаще всего бромбенэола, иногда используются и медные катализаторы, которые несколько повышают выход целевого продукта. В целом же эти, так называемые крезолятные способы, в промышленном масштабе трудно осуществимы, поскольку м-крезол, бромбензол и бромтолуол являются труднодоступными продуктами.
Наиболее близким по технической сущности и достигаемому результату к изобретения является способ получения м-замещенных диариловых эфиров взаимодействием галоидзамещенных ароматиче- ских соединений с фенолом в присутствии едкой щелочи при 110-400°С,
Получение м-фенокситолуола указанным способом осуществляется путем взаимодействия о-галоидароматического соединения х-хлортолуола с фенолятом калия1 в присутствии гидроксида калия (85%- ней концентрации) в автоклаве при 110-400°С и соотношении фенолят калиятидроксид калия:о-хлортолуол, равном 1:0,3-3:3. Содержание изомеров фенокситолуола составляет 13-80% при соотношении м/о изомеров 0,64-2,14:1, конверсия в ор- томета-фенокситолуол составляет 12-80%. Выход м-фенокситолуола 5,2-52,02%.
Недостатком способа является низкий выход м-фенокситолуола.
Цель изобретения - повышение выхода м-фенокситолуола.
Поставленная цель достигается взаимодействием орто-хлортолуола с фенолятом калия при 240-250°С в присутствии гидроксида калия 92-98% концентрации и каталитических количеств соли или оксида меди (I или II) по схеме
СН3
C1© KOH
Си
+ш
при соотношении фенолят калия:КОН:о- хлортолуол, равном 1:2:3-4, и 240-250°С.
Конверсия фенолята калия в смесь изомеров фенокситолуола при использовании гидроксида калия 92-98%-ной концентрации составляет 86-96% при соотношении изомеров м:о 2,6:1, т.е. выход м-фенокситолуола соответственно от 62,1 до 69,3%,
При использовании гидроксида натрия или гидроксида лития выход м-фенокситолуола снижается до 10-25%.
Заявляемое техническое решение отличается от известного тем, что для получения м-фенокситолуола взаимодействием фенолята калия с о-хлортолуолом в присутствии гидроксида калия при 240-250°С при соотношении фенолята калия и гидроксида калия 1:2, с целью повышения выхода, процесс ведут в присутствии соли или оксида меди (I или И), используя 92-98 %-ный гидроксид калия при соотношении фенолят калия:о-хлортолуол, равном 1:3-4.
Предлагаемый способ характеризуется повышенным выходом продукта-сырца. В процессе используются доступные виды сырья: фенол, являющийся крупнотоннажным продуктом, о-хлортолуол - побочный продукт в производстве п-хлортолуола. Квалифицированного применения в настоящее время о-хлортолуол не находит и частично используется в качестве дешевого растворителя.
Большим преимуществом предложенного метода получения м-фенокситолуола является простота переработки реакционной массы: после добавления к ней воды и разделения водного и органического слоев из органического слоя методом ректификации выделяется товарный м-фенокситояуол.
а из водного (после нейтрализации соляной кислотой и очистки от органических примесей) - чистый кристаллический хлористый калий.
Пример 1. В автоклав из нержавеющей стали емкостью 70 мл загружают 6,61 г (0,05 М) фенолята калия, 5,91 г (0,1 М)95,0%- ного гидроксида калия. 18,98 г (0,15 М) о- хлортолуола и 0,37 г (0,0038 М) хлорида меди ().Реакционную смесь нагревают при встряхивании и 235°С в течение 4 ч. Охлаждают, содержимое автоклава обрабатывают 50 мл воды.Органическую часть из реакционной смеси экстрагируют 3 раза по 25 мл о-хлор- толуола, сушат сульфатом магния, отгоняют экстрагент до 165°С в парах, остаток взвешивают, анализируют методом ГЖХ.
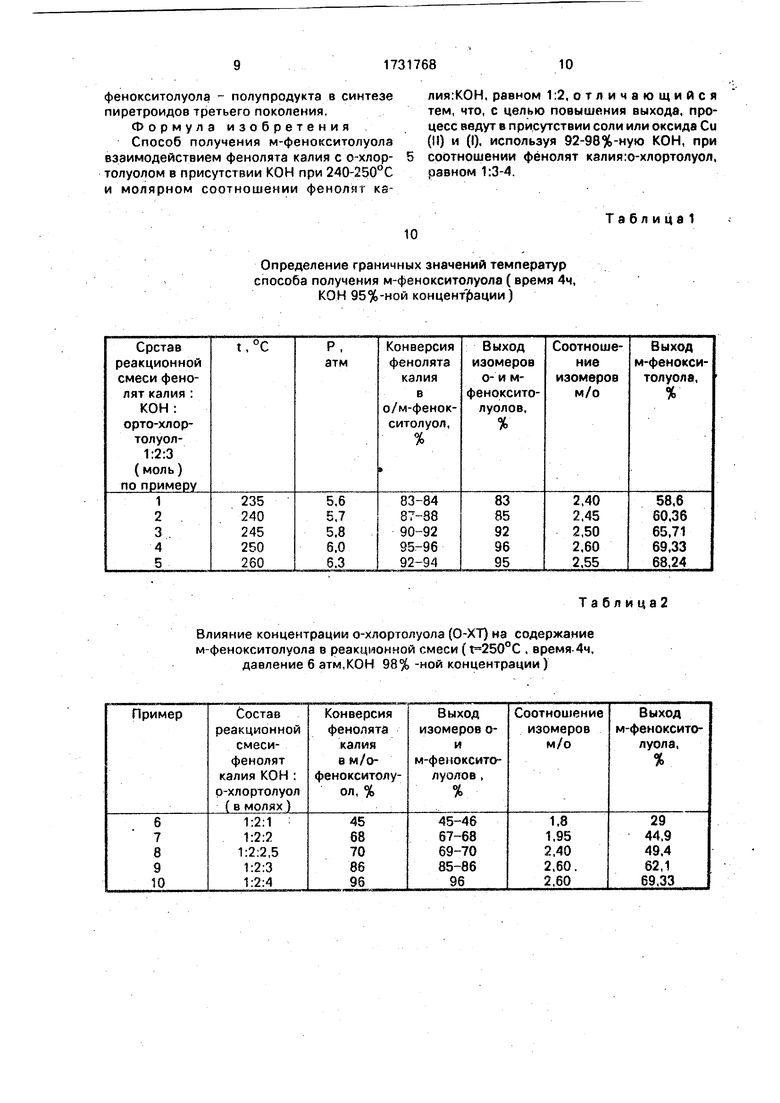
Аналогично были проведены синтезы при граничных температурах 240, 245, 250 и 260°С. Полученные результаты представлены в табл.1 (примеры 1-5).
Пример 6. В автоклав из нержавеющей стали емкостью70 мл помещают 12,65 г (0,1 М) фенолята лития, 9,6 (0,4 М) гидроксида лития, 12,65 г (0,1 М) о-хлортолуо а и 0,4 г хлорида меди (I). Нагревают при встряхивании и 250°С в течение 4 ч. Охлаждают и обрабатывают как в примере 1. Содержание м-фенокситолуола в продукте-сырце 10%.
Пример 7. В автоклав из нержавеющей стали емкостью 70 мл помещают 5,81 г (0,05 М} фенолята натрия, 6 г (0,15 М) гидроксида натрия, 18,93 г (0,15 М) о-хлортолуола и 0,4 г хлорида меди (I). Автоклав нагревают при встряхивании и 250°С в течение 4 ч. Охлаждают, обрабатывают и анализируют как в примере 1.
Содержание м-фенокситолуола в продукте-сырце 25%.
Аналогичные данные были получены в присутствии оксида меди (II), ацетата меди, основного карбоната меди.
В щелочной среде соединения меди восстанавливаются до металлической меди, которая в момент выделения образует тонкодисперсную взвесь с большой поверхностью контакта. В таком состоянии медь оказывает селективное действие на процесс конденсации, направляет в сторону предпочтительного образования м-изоме- ра.
Известны примеры использования соединений меди в качестве катализатора реакции Ульмана. Однако, как было обнаружено, только в присутствии сильного основания гидроксида калия при мольном соотношении реагентов фенолят калия:гидроксид калия:ор- то-хлортолуола 1:2:3-4 медь в момент выделения оказывает направленное действие процесс идет в сторону предпочтительного образования м-фенокситолуола.
Предварительно были исследованы граничные значения количества гидроксида ка- 5 лия, отличные от выбранных 2 молей. Уменьшение концентрации гидроксида калия до 1 моля на 1 моль фенолята калия резко снижает выход м-фенокситолуола почти в 2 раза. В таких условиях не генери0 руется в достаточном количестве промежуточный активный бензиновый интермедиат и поэтому процесс не эффективен.
Увеличение концентрации гидроксида калия более 2 молей экономически не выгод5 но, так как гидроксид калия дорог, а использование хлорида калия, выделенного в качестве побочного продукта, проблематично. Кроме того, применение избытка (свыше 2 молей) гидроксида калия приводит к уве0 личению выхода побочных продуктов таких как изомерные дитолиловые эфиры, которые трудно отделяются от м-фенокситолуола из-за близости температур кипения. Как видно из табл.1, снижение темпе5 ратуры до 235°С при равном времени нагревания приводит к уменьшению содержания м-фенокситолуола в реакционной смеси до 40-41% (пример 1, табл.1).
Повышение температуры до 260°С на0 правляет процесс в сторону образования значительных количеств продуктов конденсации, осмоления в среднем до 30%. Поэтому оптимальной температурой для данного процесса является 250°С.
5 Кроме того, были проведены исследования по определению влияния концентрации о-хлортолуола на содержание м-фенокситолуола в продуктах, конденсации. Количество молей о-хлортолуола изменяли от 1 до 4.
О Полученные данные представлены в табл.2 (примеры 6-10).
Как видно из табл.2, применение 1 моля о-хлортолуола при прочих равных условиях снижает содержание м-фенокситолуола в
5 реакционной смеси до 29% (пример 6). Повышение концентрации о-хлортолуола до 2- 2,5 молей заметно повышает содержание м-фенокситолуола в реакционной смеси до 44-49%. При концентрации о-хлортолуола,
0 равной 3-4 моля на 1 моль фенолята калия, выход метафенокситолуола составляет 62,1- 69,3% (примерЭ и 10). Поэтому оптимальной концентрацией о-хлортолуола была выбрана концентрация 3-4 моля о-хлортолуола на
5 1 моль фенолята калия.
Таким образом, описанные условия проведения процесса конденсации фенола, о-хлортолуола в присутствии гидроксида калия 98%-ной концентрации и соединений
меди позволяют получить м-фенокситолуол с выходом 62-69%.
Известно, что феноляты щелочных металлов термически не устойчивы при 350- 450°С; продуктами разложения являются метан, оксид углерода, водород, которые, очевидно, и создают давление в автоклаве по известному способу. Кроме того, для фенолятов щелочных металлов в жестких условиях в силу своего химического строения наряду с образованием простых эфиров возможны реакции арилирования. Поэтому выход м-фенокситолуола в известном способе меньше, а количество побочных продуктов больше.
На прохождение .процесса конденсации фенолята калия и о-хлортолуола существенное значение оказывает концентрация гид- роксида калия.
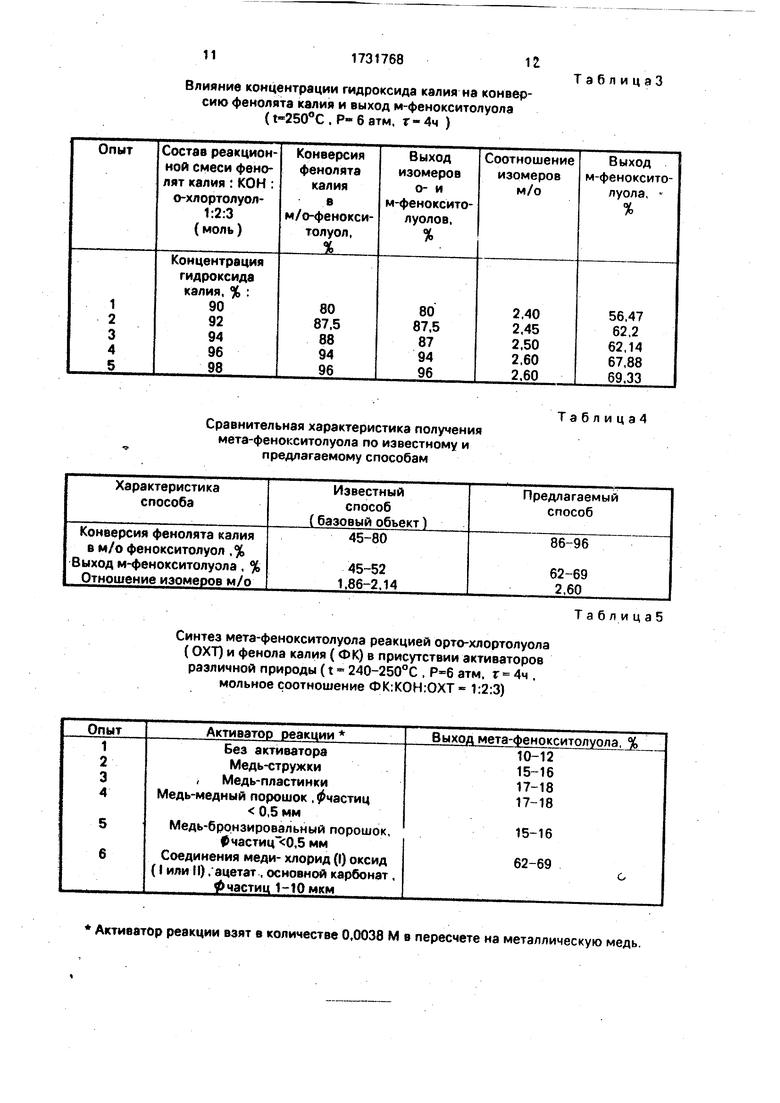
Проведен ряд исследований по изучению влияния концентрации гидроксида калия на конверсию фенолята калия и выход м-фенокситолуола. Полученные данные представлены в табл.3.
Из дйнных табл.3 следует, что наилучший выход м-фенокситолуола был получен на 92-98%-ном гидроксиде калия. Поэтому оптимальной концентрацией для получения м-фенокситолуола является концентрация гидроксида калия, равная 92-98%.
Как показали исследования в присутствии гидроксида калия (85%-ной чистоты) и выдержанных граничных параметрах известного способа (пример 5 и 6) м-фенокситолуол выделен с выходом 50-52% при отношении изомеров м/о, равном 1,86 (по аналогии с примером 5 известного способа), и смеси орто-, мета-фенокситолуолов 43- 45% при отношении м/о, равном 2,14 (по аналогии с примером б известного способа).
Воспроизведение известного способа при 240-250°С без активатора процесса соединения медь + гидроксид калия (95%) позволило получить мета-фенокситолуол с выходом 15-20% и только введение соединения меди в присутствии гидроксида калия (95%) позволяет создать такой активатор реакции, который обеспечивает направление реакции в сторону предпочтительного образования мета-фенокситолуола. Полученные данные приведены в табл.4.
Как видно из табл.4, снижение температуры на 10CM40°C и проведение процесса в присутствии активатора реакции позволяет улучшить процесс, повысить выход целевого продукта.
Проведение процесса конденсации в присутствии медных стружек, медных пластин, порошка меди и бронзировал ьной меди (медной бронзы) в граничных параметрах
температуры и состава не привело к положительному результату. Поэтому применение такого приема как совместное соединение меди и гидроксида калия (95%ной концентрации) позволяет повысить выход мета-фенокситолуола до 70%, а по известному способу не превышает 50%, при этом часть продукта порядка 15-20% при 350-400°С осмоляется (известный способ).
0 Такая совокупность соединения меди и гидроксида кг ия при 240-250°С обеспечивает высокоэффективный катализ,
Механизм действия катализатора-активатора основан на образовании тонкодис5 персной меди в момент восстановления последней из ее соединений. В таком состоянии медь обладает большой поверхностью контакта и развивает общую поверхность до 5-6 м2.
0 Для подтверждения этого механизма процесса активации, проведен ряд синтезов по получению мета-фенокситолуола в присутствии активаторов различной природы (табл.5),
6 Как видно из данных табл.5, только коллоидные частицы меди, образованные из со- единений меди в щелочной среде, активируют процесс конденсации и позволяют значительно (в 4-5 раз) увеличить вы0 ход мета-фенокситолуола по сравнению с другими активаторами, Как известно, один из двух методов получения дисперсионных систем конденсационный, основанный на химической реакции, ведущей к образова5 нию нерастворимых веществ дисперсного порядка. При этом поверхность катализатора, а следовательно поверхность контакта повышается в 500-1000 раз.
Медные стружки и другие формы меди в
0 щелочной среде не оказывают такого каталитического воздействия.
Процесс в присутствии металла-меди не интенсифицируется, выход целевого продукта не достигает 15-18%.
5 Что касается других гидроксидов щелочных металлов (натрия и лития), то процесс конденсации при 240-250°С практически не проходит (табл.2, примеры 6,7).
0 Гидроксид калия (95%-ной концентрации) как сильное основание генерирует ин- термедиат дегидротолуол, который в присутствии коллоидной меди вступает в реакцию с фенолятом калия с образованием
5 м-фенокситолуола. Гидроксиды лития и натрия уступают по силе гидроксиду калия, поэтому выход з присутствии указанных гидроксидов не превышает 10-25%.
Предлагаемый способ упрощает организацию промышленного производства мфенокситолуола - полупродукта в синтезе пиретроидов третьего поколения. Формула изобретения Способ получения м-фенокситолуолз взаимодействием фенолята калия с о-хлор- толуолом в присутствии КОН при 240-250°С и молярном соотношении фенолят KSлиягКОН, равном 1:2, отличающийся тем, что, с целью повышения выхода, процесс ведут в присутствии соли или оксида Си (II) и (I). используя 92-98%-ную КОН, при соотношении фенолят калияю-хлортолуол, равном 1:3-4.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2,4-дихлорфеноксиуксусной кислоты | 2020 |
|
RU2757739C1 |
| Способ получения 2,4-дихлорфеноксиуксусной кислоты | 2018 |
|
RU2684114C1 |
| Способ получения виниловых эфиров аминофенолов | 2016 |
|
RU2640808C1 |
| Способ получения хлотолуолов | 1977 |
|
SU658123A1 |
| Способ получения гексаарилоксициклотрифосфазенов | 1990 |
|
SU1761759A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАМЕТИЛЬНЫХ ПРОИЗВОДНЫХ ДИФЕНИЛОВОГО ЭФИРА | 2016 |
|
RU2643519C1 |
| ВОДНЫЙ ЖИДКИЙ СОСТАВ С НИЗКОЙ ТЕМПЕРАТУРОЙ ЗАМЕРЗАНИЯ, СОДЕРЖАЩИЙ ФЕНОЛЯТЫ, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ, ВОДНАЯ СУСПЕНЗИЯ ИЛИ ДИСПЕРСИЯ, ВКЛЮЧАЮЩАЯ СОСТАВ | 2001 |
|
RU2298543C2 |
| Способ получения динитропроизводных дифениловых и трифениловых эфиров | 2017 |
|
RU2671581C1 |
| Способ получения фенола и с @ -с @ -алкенилфенола | 1979 |
|
SU971089A3 |
| СПОСОБ ПОЛУЧЕНИЯ БИСФЕНОЛА-А | 1991 |
|
RU2060984C1 |
Изобретение касается получения диари- ловых эфиров, в частности получения м-фе- нокситолуола, который м.б. использован в качестве полупродукта при синтезе пиретроидных инсектицидов. Цель - повышение выхода целевого продукта. Для этого фенолят калия в присутствии 92-98%-ного КОН подвергают взаимодействию с о-хлортолуо- лом при молярном соотношении реагентов соответственно 1:2:(3-4) в поисутствии соли или оксида Си (II) или (I) при 240-250°С.В этих условиях повышают выход целевого продукта до 69,3% при соотношении м- и о-изомеров 1:2,6. 5 табл. VI СА О 00
Определение граничных значений температур
способа получения м-фенокситолуола (время 4ч,
КОН 95%-ной концентрации)
Влияние концентрации о-хлортолуола (0-ХТ) на содержание
м-фенокситолуола в реакционной смеси (t 250°C , время-4ч,
давление б атмЖОН 98% -ной концентрации)
10
Та б л и ца 1
Таблица2
11
Влияние концентрации гидроксида калия на конверсию фенолята калия и выход м-фенокситолуола (t-250°C . Р- 6 атм, г-4ч )
Сравнительная характеристика получения
мета-фенокситолуола по известному и
предлагаемому способам
Синтез мета-фенокситолуола реакцией орто-хлортолуола
(ОХТ) и фенола калия (ФК) в присутствии активаторов
различной природы (t - 240-250°С , Р-6 атм, г 4ч ,
мольное соотношение ФК:КОН:ОХТ - 1:2:3)
1731768
12
ТаблицаЗ
Таблица4
Таблицаб
| Корнилов М.Ю | |||
| и др | |||
| Способы получения и свойства фенвалерата/ МНИИТЭХИМ, 1984 | |||
| РАБОЧИЙ ОРГАН РОТОРНОГО РЫХЛИТЕЛЯ | 2010 |
|
RU2460263C1 |
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| Шахтный подъемник | 1983 |
|
SU1191409A2 |
| Веникодробильный станок | 1921 |
|
SU53A1 |
| КОЛЬЦЕВОЙ СЧЕТЧИК НА ДВУХТАКТНЫХ ФЕРРИТ-ДИОДНЫХ ЭЛЕМЕНТАХ С ЦИФРОВОЙ ИНДИКАЦИЕЙ | 0 |
|
SU291341A1 |
| Акцептованная заявка ФРГ № 2932093 , кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| Способ запрессовки не выдержавших гидравлической пробы отливок | 1923 |
|
SU51A1 |
| Патент Англии N° 1579151, С 2 С, 1979 | |||
| Патент СШ AN 4377712, С07С41/16, 1981 | |||
| Турова Н.Н | |||
| и др | |||
| Спиртовые производные щелочных и щелочноземельных металлов | |||
| - Успехи химии, 1965, 34, № 3, с.385-433 | |||
| кл кл | |||
Авторы
Даты
1992-05-07—Публикация
1990-01-22—Подача