карбонил (он м.б. замещен галогеном, ме- токсикарбонилом). Ci-Сг-алкил (он м.б. замещен С2 Сз-алкоксикарбонилом), которые, как гербициды могут быть использованы в
сельском хозяйстве. Цель - создание новых
активных и малотоксичных веществ. Их синтез ведут реакцией соответствующего тиазоноамина с фенилизоцианатом в присутствии брома при охлаждении. 3





























| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ТИОУРЕИДОБЕНЗОЛА | 1969 |
|
SU453831A3 |
| СОЮЭНАЯ Iш^тш^'^ш.'^'т^Ш | 1972 |
|
SU341202A1 |
| Гербицидная композиция (ее варианты) | 1985 |
|
SU1706370A3 |
| Способ получения гетероциклических соединений | 1982 |
|
SU1075974A3 |
| Способ получения производных акриловой кислоты и их стереоизомеров | 1985 |
|
SU1819259A3 |
| ПРОИЗВОДНЫЕ АМИНА ИЛИ ИХ СОЛИ И ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1991 |
|
RU2038352C1 |
| ПРИМЕНЕНИЕ ТИАЗОЛИДИНДИОНОВ ДЛЯ ПРЕДОТВРАЩЕНИЯ ИЛИ ОТДАЛЕНИЯ НАСТУПЛЕНИЯ ИНСУЛИННЕЗАВИСИМОГО САХАРНОГО ДИАБЕТА (NIDDM) | 1994 |
|
RU2195282C2 |
| ПЕСТИЦИДЫ | 1994 |
|
RU2142938C1 |
| ЗАМЕЩЕННЫЕ 3-ФЕНИЛ-5-АЛКОКСИ-1,3,4-ОКСАДИАЗОЛ-2-ОНЫ И ИХ ПРИМЕНЕНИЕ ДЛЯ ИНГИБИРОВАНИЯ ГОРМОНОЧУВСТВИТЕЛЬНОЙ ЛИПАЗЫ | 2001 |
|
RU2281283C2 |
| Способ получения производных 2,3-диаминоакрилонитрила или их солей (его варианты) | 1988 |
|
SU1630610A3 |
Изобретение касается производных ти- адиазола, в частности получения соединений общей ф-лы Г1(В Г2 N. yvV ч где fc- 0. S, NRi, CR2R3 при Ri-СНз. C2H5. CeHs, R2-R3-H, ОН, -ОС(0)-СНз, - С(0)ОСНз, -C(OhOC2H5; n и n - H, СНз; гз и и - Н, С1-С4-алкил, фенил, СеНзСЬ. п-СНз- СбН4, CH2-S-CH3. СН2-0-СНз, СН2-0-изо- R (равны или различны) - галоген, N02. CN.-OR4, -CfOhORs; -C(O)-NR6R7. -С(ОКбН5, -С- NRg-ORa, -NRioRio, С1-С2-алкилт ю, замещенный карбокси- илиС1-Сз-ал- коксикэрбонилом, Ci-Сз- а л кил, замещенный галогеном. ОН, CN. метокси или фенилом, ме- тилфенилэтоксикарбонилом, пропаргилокси- карбонилацетилоксигруппой -P(OXOC2Hs)z. С2-алкенилом он м.б. замещен -C(0)-ORii при Rn-H. Na, С1-С -алкил, пропаргил ; п- 1-5: , хиноксалинил. замещенный хлором, пиридил, тиаэолил, замещенный хлором и метиламином, тетрагидропиранил, -P(S) ОСНз или 0-C2Hs 2, S(0)2R12 при RU- СНз, метилфенил, -C(0)-NRi3Ri4 при Rn и Ri4 - Н или С1 С2-алкил: С1 С2-алкил, замещенный галогеном или CN; циклопропил, фенил (он м.б. замещен галогеном, N02, CN, СНз или метокси); ацетилокси, триметилси- лил, изоксалил, замещенный СНз: оксадиа- золил (он м.б. замещен Ci-Cs-алкилом), пиразолил, пиридил или -C(0)ORis, C(0)- NRiSRi7, -C(0)-Ri8; -C(R2o) - N-ORig, -QR21. при , Na, Ci-Сз-алкилиденамино, ал- лил, Сз С5-алкинил, фенил, Ci-Сю-алкил, замещенный галогеном: Ci-Сз-алкокси-, С2 Сз-алкенилокси, бензилокси, фенил, замещенный метокси, триметилсилилом, ци- анометилтио, феноксиаллилтио, бензилтио, фенилтио, С1-С2-алкоксикарбонил, меток- сикарбонилметилтио , фурил, изоксазолил, замещенный метилом; Rie и RI Н, этокси, аллилокси, циклогексилкарбамоил, алкил (он м.б. замещен Ci-Сз-алкоксифени- лом), С-|-С2-алкоксикарбонил, аллил, пропаргил, циклогексил, фенил; Rie-СНз, фенил, морфолино; Rig-H. аллил, ацетил (он м.б. замещен галогеном); R2Q-CH3. фенил. RH2; R21-H, С1-С2-алкил (он м.б. замещен фенилом, метокси, фенокси). С1-С2-алкокси- карбонил, винил, фенил (он м.б. замещен галогеном, N02, метокси, СНз, СРз, метилен- диокси), нафтил, пиридил (он м.б. замещен СНз, метилкарбамоилом); Q - 0, S (0)m при т 0 или 1-2; Rs-H, Na, Сз-алкилидена- мино, Ci-Cs-алкил (он м.б. замещен цикло- пропилом, С1-С4-алкоксикарбонилом, ме- токси, фенокси, фенилтио, триметилсилил или -0-1(СН2)я р-ОСНз при q 1-3, р - 2-7. Сз-С4-алкенил (он м.б. замещен Ci-Сз-ал- коксикарбонилом), пропаргил (он м.б. замещен фенилом); Re и Ry-H, Ci-Сз-алкил. пропаргил, этокси; Ra-Н, С1-С2-алкил (ои м.б. замещен С1-С2-алкоксикарбонилом); Rg-H. СНз; Rio- H, пропаргил, С1-С2-алкил 4 4 О 00 00 4 CJ

Изобретение относится к способу получения производных тиадиазола общей формулы:
в которой
t
E-0-.-S-N-; -Сk.
при этом Rt-СНз. C2Hs, CeHs,
,OH, ОСОСНз,-СГ .У
ЧОСНз СхН5
п и Г2-Н, СНз;
гз и Г4-Н, С1 С4-алкил, CeHs, СбНзС 2, п-СбН4-СНз, -CH2SCH3, -СНаОСНз, -СНа- 0-СзН7-1;
R - одинаковые или разные и выбраны из группы, содержащей Hal - галоген, N02, CM, OR
C-O-KS .. -с о
N, UK4. , г
-o-bs ° R6.
N -C NOR8R7
ч
Rio RID
СсН
6П5
V N:
или С1-С2-алкилтио, замещенный карбокси или Ci-Сз-алкоксикарбонилом, или Ci-Сз-алкил, замещенный галогеном, окси. циано, метокси, фенилом, метилфени- лэтоксикарбонилом, пропаргилоксикарбо- нилацетилокси или группой ° ос2н5
ос,н,
С2-алкенилом, который может быть замещен группой COORn, где RH - водород или натрий, Си-Ст-алкил или пропаргил, при этом п - 1-5 - целое число;
R4 - водород, хиноксалинил, замещенный хлором, пиридил, триазолил, замещенный хлором и метиламином, тет- рагидропиранил или группы
|1хОСН3(С2Н5)
H OCH3IC2H5) S02R12, где Ri2 - метил или метилфенил,
х , где R13 и R14-водород или
О Ц ЧС1-С2-алкил, С1 С12-алкил, замещенный галогеном или циано, циклопропил, галоциклопропил, фенил, который может быть замещен галогеном, нитро, циано, метилом или метокси, ацетилокси, триметилсилил, изоксазолил, замещенный метилом, оксади- азолил, который может быть замещен CiСз-алкилом, пиразолил, пиридил или группы
т---К:
- Г -D L rsio
II18
О
C-NORt9 ,QR21
20
5
0
5
0
5
где Ris водород, натрий, Ci-Сз-алкилиде- намино, аллил, Сз-Сб-злкинил, фенил или Ci-Сю-алкил, замещенный галогеном, Ci- Сз-алкокси, С2-Сз-алкенилокси, бензилокси и ли фенил, замещенный метокси, три- метилсилилом,циано, метилтио, фенок- сиаллилтио, бензилтио или фенилтио, С1-С2-алкоксикарбонил, метоксикарбонил- тилтио, фурил, изоксазолил, замещенный метилом;
Ri6 и Ri - водород, этокси, аллилокси, циклогексилкарбамоил, С1-С4-алкил, который может быть замещен Ci-Сз-алкоксифе- нилом, С1-С2-алкоксикарбонил, аллил, пропаргил, циклогексил или фенил;
RIB - метил, фенил или морфолино;
Rig - водород, аллил или ацетил, который может быть замещен галогеном;
R20- метил, фенил или амино;
R21 - водород, Ст-С2-алкил. который может быть замещен фенилом, метокси или фенокси, С1-С2-алкоксикарбонил, винил, фенил, который может быть замещен галогеном, нитро, метокси, метилом, трифторме- тилом или метилендиокси, нафтил, пиридил,
который может быть замещен метилом или метил карбамоилом:
Q - кислород или S(0)m. где т-0.1 или 2;
Rs водород или натрий, Сз-алкилиде- намино или d-Ce-алкил, который может быть замещен циклопропилом, С1-С4-ал- коксикарбонилом, метокси, фенокси, фе- нилтио, триметилсилил или группа -0-(CH2)q- pOCH3, где q - 1-3 - целое число, Р - 2-7 - целое число; Сз-Сд-алкенил, который может быть замещен Ci-Сз-алкок- сикарбонилом, или пропаргил, который может быть замещен фенилом;
Re и R каждый - водород, Ct-Сз-алкил, пропаргил или этокси;
RB - водород или С1-С2-алкил, который может быть замещен С1-С2-алкоксикарбо- нилом;
Rg - водород или метил,
Rio - водород, пропаргил, С1-С2-алкил- карбонил, который может быть замещен га- логеном, метоксикарбонилом или С1-С2-алкил, который может быть замещен С2-Сз-алкоксикарбонилом.
Эти соединения могут найти примене- ние в гербицидных композициях в качестве активного компонента.
Цель изобретения - получение новых производных тиадиаэола, обладающих высокой эффективностью гербицидного дей- ствия и высокой степенью безопасности для , млекопитающих животных.
Химическая структура полученного соединения определяется с помощью спектра ядерного магнитного резонанса (ЯМР), масс-спектра и инфракрасного (И К) спектра.
П р и м е р 1. 3-{5-Ацетонилокси-4-хлор- 2-фторфенилимино)-5,6-дигидро-6,6-диме- тил-ЗН-тиазол 2,3-С11,2,4 тиадиазол (соединение № 228)
С1
Вг,
ОСН2ССН3
ОСН2ССН3
о
1,5 г 2-амино-5,5-диметил-2-тиазолина растворяют в 15 мл дихлорида метилена. В этот раствор вводят по каплям с одновре- менным перемешиванием при 0°С раствор 3,0 г 2-фтор-4-хлор-5-ацетонилоксифенили- зотиоцианата в 15 мл дихлорида метилена. После перемешивания в течение 1 ч в реакционный раствор вводят 0,72 г пиридина и
в этот раствор при охлаждении льдом вводят по каплям раствор 1,7 г брома в 10 мл дихлорида метилена. Реакционный раствор дополнительно перемешивают в течение 30 мин, после чего данный раствор промывают 30 мл воды, 30 мл 5%-ного раствора NaOH и 30 мл воды в указанной последовательности. Слой дихлорида метилена высушивают над безводным сульфатом магния. Этот же слой фильтруют и затем концентрируют. Остаточный продукт концентрирования очищают в хроматографической колонке с силикагелем и в результате получают 2,5 г соединения. Т.пл. 107-108°С.
П р и м е р 2.3- 4-Хлор-2-фтор-5-(1-эток- сикарбонилэтокси)фенилимино}-5.6-дигид- ро-6-метил-ЗН-оксазол 2,3-С11,2,4 тиадиа - зол (соединение 355).
Г
+
сн
OCH-COOC2HS ChU
ОСН-СООС2Н5 СН3
9,60 г 4-хлор-2-фтор-5-(1-этоксикарбо- нилэтокси)-фенилизотиоцианата растворяют в 100 мл хлороформа. Затем раствор охлаждают до -10°С и вводят в него 3,80 г 5-метил-2-амино-2-оксазолина. Реакционный раствор перемешивают в течение 5 ч при 0°С и затем в него вводят по каплям раствор 5,06 г брома в 30 мл хлороформа при температуре от -10 до 0°С. После прекращения этого ввода по каплям реакционный раствор промывают 50 мл водного раствора 1 н. NaOH, затем 50 мл воды и высушивают над безводным сульфатом магния. После фильтрации сульфата магния флороформ отгоняют в вакууме. Остаточный продукт очищают в хроматографической колонке и в результате получают 10,04 г продукта (по26 - 1.5870).
ПримерЗ. 3- 4-Хлор-5-(1-Цианоэток- си)-2-фторфенилимино -6-метил-5,6.7. 7а-тетрагидро-ЗН-пиррол 2,1-С11,2,4)тиади. азол (соединение 583).
«
OCHCN СН3
№
СН, NH2
НИ
OCHCN
П р и м е р 4. 3- 4-Хлор-5-{1-этоксикарбо- нмлэтокси}-2-фторфенилиминоЗ-5,6-дигидро -7-метил-З Н-имидазо 2,1-C11.2,4 тиадиазол (соединение 671)
N
ОС
F t SCN4O
СН,
СН:
13v,t 13
1,56 г бромгидрата 2-амино-3-метил-1- имидазолина суспендируют в 10 мл хлороформа. В эту суспензию затем вводят по каплям при охлаждении льдом раствор 0,37 г едкого натра в 2 мл воды. После охлаждения до -15°С в реакционный раствор вводят по каплям раствор 2,31 г 2-фтор-4-хлор-5-(1- этоксикарбонилэтокси)фенилизотиоциана- та в 10 мл хлороформа. После перемешивания в течение 1 ч при -15°С в реакционный раствор снова вводят по каплям раствор 1,2 г брома в 10 мл хлороформа. После перемешивания еще в течение 1 ч реакционный
Степень повреждения
(Свежий вес в необработанной делянке) - (Свежий вес в обработанной делянке)
Свежий вес в необработанной делянке
раствор промывают 30 мл воды и хлороформный слой высушивают над безводным , сульфатом магния, после чего его концентрируют. Остаточный продукт концентрирования очищают в хроматографической колонке с силикагелем и в результате получают 1,48 г продукта. Т.пл. 75-78°С.
Предлагаемые соединения, которые могут быть получены аналогичным способом,
приведены в табл.1.
Данные соединения обладают наивысшей гербицидной активностью и могут вноситься непосредственно в почву при обработке растений в предвсходовый период роста или на листву при обработке в послевсходовый период роста, или же они могут быть смешаны непосредственно с почвой. Соединения могут наноситься на почву или на листву растений в количестве 1 г
или более на 10 ар.
Испытание 1. Испытание на рисовом поле Падди.
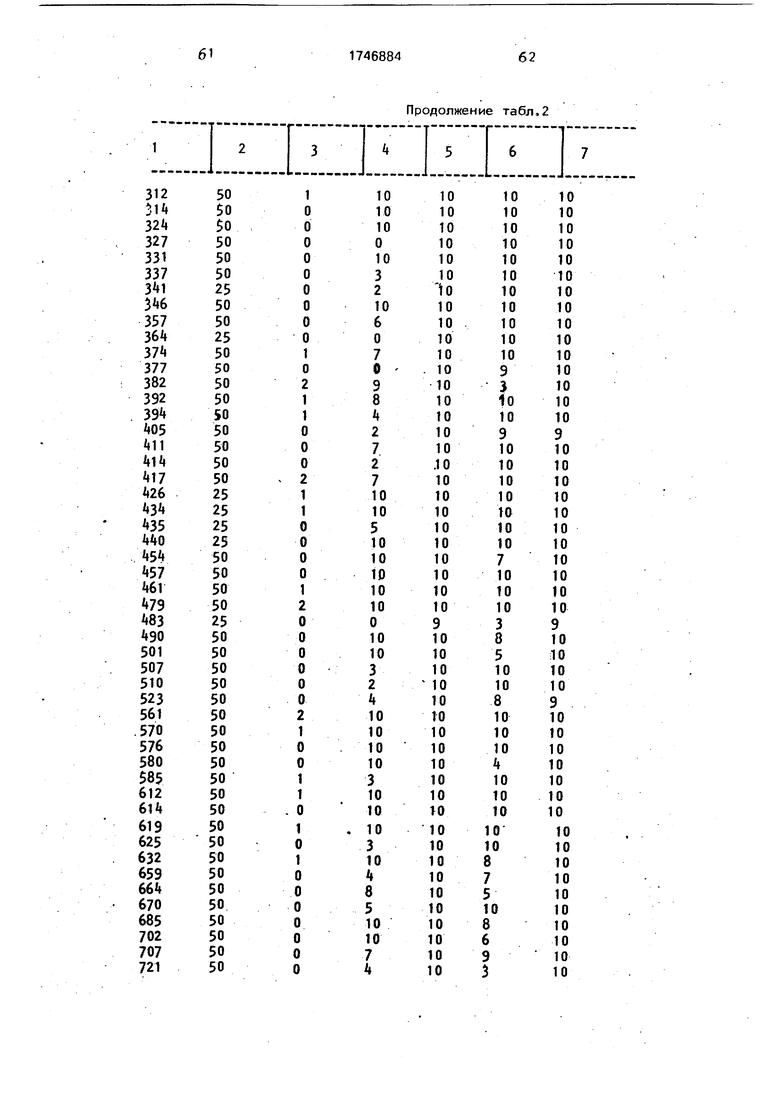
Семена проса петушьего (Echlnochloa crus-galli), сорняка ряски (Monochorla vaginalis), камыша озерного (Sclrpus Hotarui) и мелкоцветной умбреллы (Cyperus difformis) высаживают в пластмассовых горшках на глубине 0,2-0,5 см (горшки высотой 15 см и диаметром 14 см), в которых содержится почва рисового поля Падди, и высаживают два рисовых растения (разновидности Nihonbare) на стадии появления 2-3 листьев. же вводят гранулы каж- дого из предлагаемых соединений, -дозами, указанными в табл.2. Горшки выдерживаются в теплице.
Через 3 нед после обработки определяют степень повреждения каждого растения и дают оценку этого повреждения в единицах шкалы 0-10, которые имеют следующие значения:
Индекс Степень повреждения,
ОО
220-29
440-49
660-69
880-89
10100
Индексы 1,3, 5, и 9 означают промежуточную степень повреждения в пределах между 0 и 2, 2 и 4, 4 и 6, 6 и 8, 8 и 10 соответственно,
Результаты приведены в табл.2.
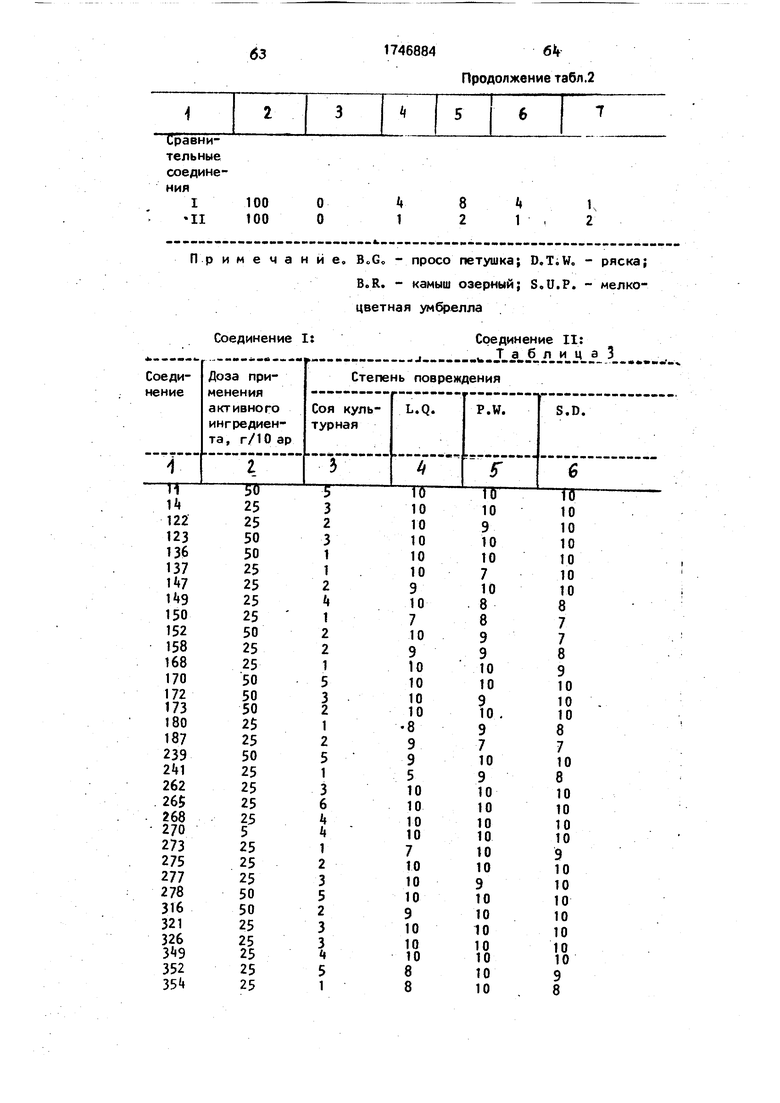
Испытание 2, Испытание с обработкой в послевсходовый период роста.
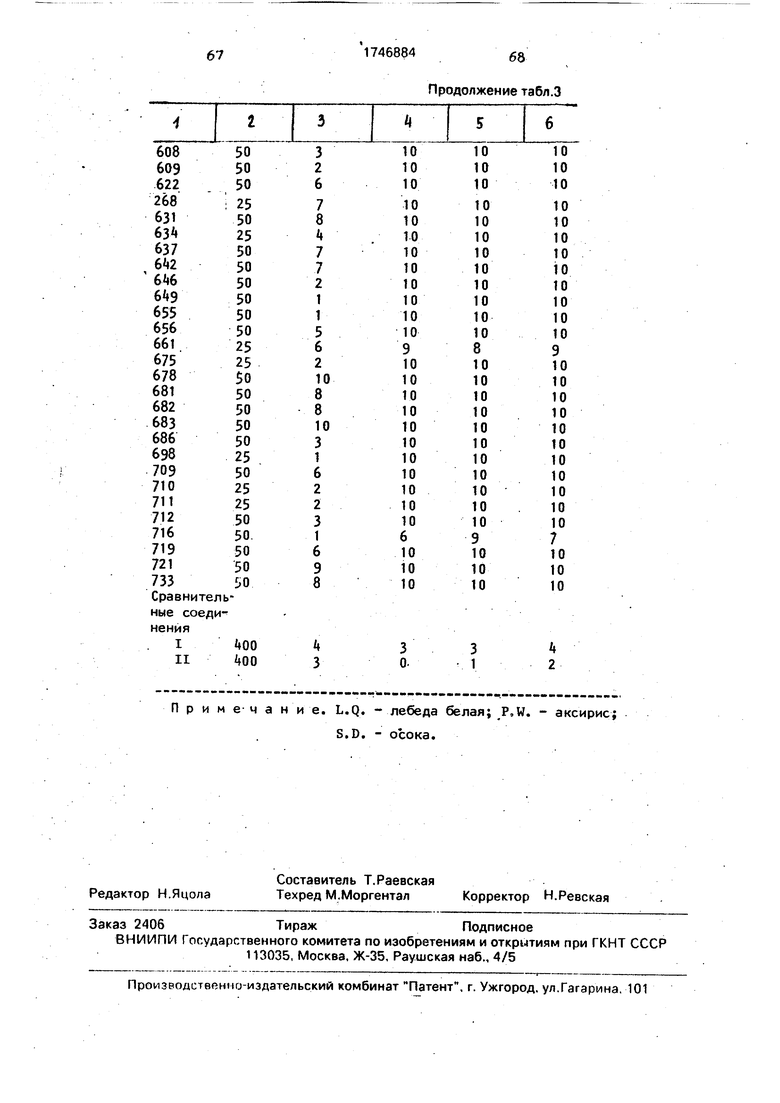
Семена лебеды белой (Chenopodlum album), аксириса (Amaranthus retroflexus), осоки (Cyperum microcrla) и сои культурной высаживают в глиняных горшках (высотой 12 см и диаметром 16 см), содержащих суг- нилистую почву, и выращивают в теплице. После того как растения достигают высоты 3-10 См, на листву этих растений распыляют с помощью микрораспылителя водную суспензию, полученную путем разбавления эмульсионного концентрата водой до определенной концентрации (500 ч./млн), доза распыления составляет 100 1/10. Через 3 нед после обработки определяют степень повреждения каждого растения и оценивают эту степень повреждения в той же шкале, что указана в табл.1. Результаты испытания представлены в табл.3.
Формула изобретения
Способ получения производных тиади- азола общей формулы
где
Rt R2 i iz E-o-,-s-N-;-C«3
где Ri-СНз, CaHs. CeHs; o
R2-R3-H, ОН, ОСОСНз.-С
ПИГ2-Н, СНз; OCHj1 OC2H5i
гз и Г4-Н, С1-С4-алкил, CeHs, CeHaCIa,
п-СеН4-СНз, -СНаЗСНз, -СНаОСНз. -СНаО-СзНт-1;
R - одинаковые или разные и выбраны
из группы, содержащей Hal - галоген, N02,
CN.OR4.r-0-Rr . .0
-г ,-и.
I,OR4.C-0-RS, -#0 „
6CVN
0Н7
-С4н5
К9
-N;
-Rio
или С1-С2-алкилтио. замещенный карбокси или Ci-Сз-алкоксикарбони- лом, или Ci-Сз-алкил, замещенный галогеном, окси, циано, метокси, фенилом, метилфенилэтоксикарбонилом, пропарги- локсикарбонилацетилокси или группой
мхОС2Н5 х
°С2Н5
С2-алкенилом, который может быть замещен группой COORn, где Rn - водород или натрий, С1-С -алкил или лропаргил, при этом п 1-5 - целое число;
R4 - водород, хиноксалинил, замещенный хлором, пиридил, триазолил, замещенный хлором и метиламином, тетрагидропиранил или группы
и/ОСН3(С2Н5)
Хосн3{с2н«о
S02R12, где Ri2 - метил или метилфенил. -rxi/R«
Г
Ч
где Ria и Ri4 водород или С Са-алкил, С1 С12-алкил, замещенный галогеном или
циано, циклопропил, галоциклопропил, фенил, который может быть замещен галогеном, нитро, циано, метилом или метокси, ацетилокси, триметилсилил, изоксазолил, замещенный метилом, оксадиазолил, который может быть замещен Ci-Cs-алкилом, пиразолил, пиридил или группы
-S-°R« ;
°о R
-c NORt9; 41
Чо.
S R16 0
где Ris - водород, натрий, Ci-Сз-алкилиде- намино, аллил, Сз С5-алкинил, фенил или Ci-Сю-алкил, замещенный галогеном, Ci- Сз-алкокси, С2 Сз-алкенилокси, бензилокси или фенил, замещенный метокси, триметилсилилом, цианометилтио, феноксиаллилтио, бензилтио или фенилтио, С1-С2-алкоксикар- бонил, метоксикарбонилметилтио, фурил, изоксазолил, замещенный метилом;
Ri6 и Ri - водород, этокси, аллилокси,
циклогексилкарбамоил, С1-С4-алкил, который может быть замещен Ci-Сз-алкоксифе- нилом, С1-С2-алкоксикарбонил. аллил, пропаргил, циклогексил или фенил; Ria - метил, фенил или морфолино;
Rio - водород, аллил или ацетил, который может быть замещен галогеном; R20 - метил, фенил или амино; R21 - водород. С1-С2-алкил, который может быть замещен фенилом, метокси или фенокси, С1-С2-алкоксикарбонил, винил,
фенил, который может быть замещен гало- ге ном, нитро, метокси, метилом, трифторме- тилом или метилендиокси, нафтил, пиридил, который может быть замещен метилом или метилкарбамоилом;
Q - кислород или S(0)m, где m 0,1 или 2;
RS - водород или натрий, Сз-алкилиде- намино или Ci-Ce-алкил, который может быть замещен циклопропилом. С1 С4-ал- коксикарбонилом, метокси, фенокси, фе- нилтио, триметилсилил или группа -О-{СН2)ч- рОСНз, где q 1-3 - целое число, Р 2-7 - целое число, Сз С4-алкенил, который может быть замещен Ci-Сз-алкок- сикарбонилом, или пропаргил, который может быть замещен фенилом;
Re и R каждый - водород, Ci-Сз-алкил, пропаргил или этокси;
Re - водород или С1 С2-алкил. который может быть замещен С1-С2-алкоксикарбо- нилом;
Rg - водород или метил;
Rio - водород, пропаргил, С1-С2-алкил- карбонил, который может быть замещен галогеном, метоксикарбонилом, или Ci-C2- алкил, который может быть замещен алкоксикарбонилом. отличающийся тем, что соединение общей формулы
&
где имеют указанные значения,
подвергают взаимодействию с соединением общей формулы
10
SCNWn
где R имеет указанные значения, в присутствии брома при охлаждении. Приоритет по признакам:
г, о1 r24-Npj V
где Hal - галоид;
R4 - С1 С12-алкил, галоидалкил, ri и Г2 - водород или метил; гз и Г4 - С1-С4-алкил; Ј - кислород или сера
Таблица 1
Продолжение табл.1
17
1746884
18
Продолжение табл.
160- - - 161- - - 162SS 6,6-{СН
г
163- - - 164- -
6-CH
6,6-(СН,)г
167
168
4-Cl, 5-OCHCOO CjH,-M3o) CH7
4-Cl, 5-ОСНСООСНСгН
СИ, CH, 4-Cl, S-OCHCOOCHCOOCjHj.
CH, CHj optical isomer)
4-Cl, 5-ОСНСООСН.СЁСН I
CHj
43-44
С 1,5777
124-128
n 1.5670 111-113
5-OaiCOOCH,C:CH
I
CH,
81-83
nЈw-1,5971
,5713
n 1,5784
Продолжение табл. I
288
п .it, - Продолжений табл.1
-«yv О-сн
124-125
305
306
5 6,6-(CH.,)2
307
6-СИ,
6-CH,
fr--c,Hr
6-CH,
2-F, 4-CV, 5-OC-CONHCH. I3
CH,
147-145
CH3 4-Cl, 5-0-C-COOH
Ч
4-Cl, 5-ОСНСОК-(Ну
62-65
68-71
CH, CON№- i
4-C1, 5-OC,jHir 4-C1, ,.-иэо 4-C1. 5-OCjH7 4-C1. 4-C1, 5-OCHC :CH
SHT
4-C1, 5-OCIIC I
c,n 4-Br, 5-OCHCH
Kf np - 1.5442
n& - 1,5872 n«i. |,5891 n 1,5942 n« « 1,6010
n 1,5680
4-C1, 5-OCHCOOCzHf
С,Ну 4-Cl, 5-OCHOOOCUjjC I CH
C2HS
71-73
4-Cl. 5-ОСНСООСНгСН«СН2
VH
L2«5
68-70
1,5770
Продолжение табл.1
Продопмнис табл.1
33
174688434
Продолжение табл.1
35
40 6-CjH,-
174688436
Продолжение табл.1
78-85
Продолжение тавп.1
Продолжение табл.1
Продолжение табл. I
Продолжение тябл.1
49
1746884
SO
Продолжение табл,1
51
174688452
Продолжение табл.1
53
- -,«.
СИ,
2-F, -С1, 5-СООСНСООСН,
I 3
сн.
1746884
54
Продолжение табл.
-сна- 6-сн,
Г«3 2-F.4-C1, 5-ОСС ЈСН
CHj 2-F, 4-CI, 5-ОСН,СООСгН4045-50
Продолжение табл.I
(2Н,«), 3,2-3,6 (1Н,ш),
Продолжение табл,2
бз
Примечание. В„Go - просо петушка; D.T.W, - ряска;
B.R. - камыш озерный; S.U.P. - мелкоцветная умбрелла
Соединение I:
25 25 50 50 25 25 25 25 50 25 25 50 50 50 25 25 50 25 25 25
25 5
25 25 25 50 50 25 25 25 25 25
3 2
3 1 1 2 Ц 1 2 2 1 5
3 2
1 2 5
1
3 6 k Ц
1
2 3 5 2
3
ц
5 1
17468846k
Продолжение табл.2
Соединение II: ТаблицаЗ
10 10 10 10 10 9 10 7
10 9 10 10 10 10 8 9 9 5
10 10 10 10
10
10
0
10
0 10
10
9
10
10
7
10
8
8
9
9
10
10
9 10
9
7
10
9
10
10
10
10
10
10
9 10 10 10
10 10
10 10
10
10
10
10
10
10
8
7
7
8
9
10
10
10
8
7
10
8
10
10
10
10
9
10
10
10
10
10
10
10
9 8
Примечание. L.Q. - лебеда белая; P,W. - аксирис;
S.D. - осока.
Продолжение табл.3
| Гетероциклические соединения./Под ред | |||
| Эльдерфильда | |||
| Приводный механизм в судовой турбинной установке с зубчатой передачей | 1925 |
|
SU1965A1 |
Авторы
Даты
1992-07-07—Публикация
1986-01-27—Подача