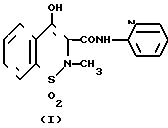
Изобретение относится к химии гетероциклических соединений, а именно к усовершенствованному способу получения N-(2-пиридил)-2-метил-4-гидрокси-2Н-1,2-бензотиазин-3-карбоксамид-1,1-диокси да формулы I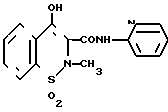 которое широко используется в медицине в качестве высокоэффективного нестероидного препарата, обладающего противовоспалительным, жаропонижающим и болеутоляющим действием.
которое широко используется в медицине в качестве высокоэффективного нестероидного препарата, обладающего противовоспалительным, жаропонижающим и болеутоляющим действием.
Известен способ получения N-(5-метил-3-оксазолил)-4-гидрокси-2-метил-2Н-1,2-бензо- тиазин-3-карбоксамид-1,1-диоксида взаимодействием этил-4-гидрокси-2-метил-2Н-1,2-бензотиазин-3-карбоксилат-1,1-диоксида с 5-метил-3-аминоизоксазолом при кипячении в ксилоле в аппарате Сокслета в присутствии молекулярных сил Linde 4 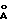 (1,5 мас.доли) в течение 24 ч. Выход целевого продукта составляет 69% [1].
(1,5 мас.доли) в течение 24 ч. Выход целевого продукта составляет 69% [1].
Также известен способ получения N-(2-пиридил)4-гидрокси-2-метил-2Н-1,2-бензо- тиазин-3-карбоксамид-1,1-диоксида, основанный на реакции этил-4-гидрокси-2-метил-2Н-1,2-бензотиазин-3-карбоксилат-1,1- -диоксида с 2-аминопиридилмагнийбромидом в среде тетрагидрофуран-ксилол при 100оС в токе инертного газа с последующим гидролизом интермедиата 1 N HCl. Выход сырого продукта достигает 50% [2].
Недостатками описанных способов являются: по способу [1] реакция осуществляется в присутствии дорогостоящих молекулярных сит Linde. Отсутствие молекулярных сил отечественного производства не позволяет использовать этот метод для промышленного получения соединения I. К недостаткам способа [2] относятся необходимость дополнительной стадии (получение реактива Гриньяра и далее магнийорганического производного 2-аминопиридина) проведения процесса, использование металлического магния и легковоспламеняющегося тетрагидрофурана в качестве растворителя обуславливает огнеопасность процесса, что затрудняет реализацию этого способа в промышленности.
К недостаткам последнего способа относится также необходимость исключения влаги, проведение процесса в инертной атмосфере, наличие дополнительной стадии гидролиза магнийорганического комплекса и низкий выход целевого продукта.
Известен способ получения соединения I заключающийся в кипячении с обратным холодильником эквимольных количеств 2 -метил-4-гидрокси-2,6-диметил-2Н-1,2-бензотиазин-3-карбоксилат-1,1-диоксида и 2-аминопиридина в токе инертного газа в течение 18 ч с азеотропной отгонкой смеси ксилол + метанол. Выход неочищенного целевого продукта составляет 61% [3].
Недостатками прототипа являются низкий выход целевого продукта, осуществление реакции в инертной атмосфере, большой расход сухого ксилола.
Целью изобретения является повышение выхода целевого продукта и упрощение технологии процесса.
Поставленная цель достигается тем, что взаимодействие 2-аминопиридина (III) с этил-4-гидрокси-2-метил-2Н-1,2-бензотиазин-3-карбоксилат-1,1-диоксидом (II) осуществляют в аппарате Сокслета, содержащем безводный хлорид кальция. Реакцию проводят в среде абсолютного ксилола при температуре кипения растворителя 140оС при соотношении II : III : CаCl2, равном 1:1:0,5-1.
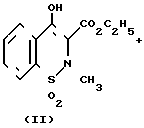
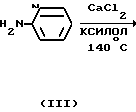
 Реакция завершается в течение 10 ч с выходом целевого продукта I 91% (т.пл. 197-200оС). После перекристаллизации из ксилола соединение I выделяют с выходом 75% (т. пл. 199-201оС). Хлорид кальция легко регенерируется прокаливанием, что дает возможность его многократного использования.
Реакция завершается в течение 10 ч с выходом целевого продукта I 91% (т.пл. 197-200оС). После перекристаллизации из ксилола соединение I выделяют с выходом 75% (т. пл. 199-201оС). Хлорид кальция легко регенерируется прокаливанием, что дает возможность его многократного использования.
П р и м е р 1. В литровую одногорлую колбу помещают 27,8 г (0,098 моль) этил-4-гидроксил-2-метил-2Н-1,2-бензотиазин-3- карбоксилат-1,1-диоксида (II), 9,2 г (0,098 моль) 2-аминопиридина (III) и 0,5 л безводного ксилола. Колбу соединяют с аппаратом Сокслета, в который помещают 5,44 г (0,049 моль) свежепрокаленного до 300оС хлорида кальция (марки ч.). Смесь нагревают до кипения растворителя (140оС) в течение 10 ч. Горячий раствор отфильтровывают. Выпавшие кристаллы отделяют, промывают холодным гексаном. Получают 29,4 г (91%) N-(2-пиридил)-2-метил-4-гидрокси-2Н-1,2-бензотиазин 3-карбоксамид-1,1-диоксида, т.пл. 197-200оС. После перекристаллизации из ксилола выделяют 24,4 г (75%) соединения I, т.пл. 199-201оС, по литературным данным [4] т.пл. 198-201оС.
Найдено,%: C 54,63; H 4,03; N 12,93; S 9,67.
C17H17N3O4S
Вычислено, %: С 54,37; Н 3,95; N 12,68; S 9,67.
ИК-спектр ( ν, KBr, см-1): 1520 (C=C), 1630 (С=О), 3390 (ОН, NH).
Спектр ПМР (CDCl3, δ): 13,03 (с, ОН), 7,71 (м, Ph, 2-Py), 2,93 (с, Ме).
П р и м е р 2. В литровую колбу помещают 47 г (0,17 моль) этил-4-гидрокси-2-метил-2Н-1,2-бензотиазин-3-карбоксилат-1,1-ди- оксида, 16 г (0,17 моль) 2-аминопиридина и 600 мл безводного ксилола. Колбу соединяют с аппаратом Сокслета в который помещают 19 г CaCl2 (0,17 моль). Реакционную смесь нагревают при 140оС в течение 10 ч. После обработки, аналогичной примеру 1, выделяют 45 г (80%) N-(2-пиридил)-4-гидрокси-2-метил-2Н-1,2-бензотиазин-3-карбо- ксамид-1,1-диоксида (I), т.пл. 198-200оС.
П р и м е р 3. В 0,5-литровую колбу помещают 14,1 г (0,05 моль) этил-4-гидрокси-2-метил-2Н-1,2-бензотиазин-3-карбо- ксилат-1,1-диоксида, 4,7 г (0,05 моль) 2-аминопиридина и 300 мл безводного ксилола. Колбу соединяют с аппаратом Сокслета, в который помещают 1,7 г (0,015 моль) СаСl2. Реакционную смесь нагревают в течение 18 ч при 140оС. После обработки, аналогичной примеру 1, выделяют 12,5 г (75%) соединения I т.пл. 197,5-200оC.
П р и м е р 4. Смесь 5 г (0,018 моль) этил-4-гидрокси-2-метил-2Н-1,2-бензотиаз- ин-3-карбоксилат-1,1-диоксида, 1,7 г (0,018 моль) 2-аминопиридина и 300 мл безводного ксилола нагревают с обратным холодильником в течение 30 ч. Выделяют 3,4 г (58%) продукта I коричневого цвета. После перекристаллизации из толуола получают 1,9 г (35%) соединения I, т.пл. 197-199оС.
Использование: в качестве противовоспалительного, жаропонижающего и болеутоляющего средства в медицине. Сущность изобретения: Продукт: N-(2-пиридил)-2-метил-4-гидрокси-2Н-1,2 -бензотиазин-3-карбоксамид-1,1-диоксид. Т. пл. 199 - 201°С, выход 75 - 80%. Реагент 1: этил-4-гидрокси-2-метил-2Н-1,2-бензотиазин-3-карбоксилат-1,1-диоксид. Реагент 2: 2-аминопиридин. Условия реакции: в среде ксилола при кипячении в присутствии безводного хлорида кальция взятого в молярном соотношении к реагенту 1 1:0,5 1,0. 1 п.ф-лы.
СПОСОБ ПОЛУЧЕНИЯ N-(2-ПИРИДИЛ)-2-МЕТИЛ-4-ГИДРОКСИ-2Н-1,2-БЕНЗОТИАЗИН-3-КАРБОКСАМИД-1,1-ДИОКСИ ДА формулы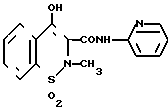
путем взаимодействия эквимольных количеств производного 2-метил-4-гидрокси-2H-1,2-бензотиазин-3-карбоновой кислоты 1,1-диоксида и 2-аминопиридина в среде ксилола при кипячении, отличающийся тем, что, с целью повышения выхода целевого продукта и упрощения процесса, в качестве производного 2-метил-4-гидрокси-2H-1,2-бензотиазин-3-карбоновой кислоты 1,1-диоксида используют этиловый эфир и процесс проводят в присутствии безводного хлорида кальция, взятого в мольном соотношении к эфиру 1 : 0,5 - 1,0 соответственно.
| Патент США N 4551525, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1994-07-30—Публикация
1990-09-10—Подача