Изобретение относится к получению ал- килфенолов, в частности смеси 2,6- и 2,4- ксиленолов.
Ксиленолы находят широкое применение в различных органических синтезах для получения гербицидов, пластификаторов, стабилизаторов, душистых веществ, смол, лекарственных препаратов и т. д. Так, 2,6- ксиленол применяют как сырье для производства нового вида термостойких пластмасс - полифениленоксида, отличающийся хорошими диэлектрическими характеристиками и устойчивостью к действию кислот, щелочей и перегретого пара, 2,4- ксиленол находит применение в синтезе витамина Е и химических средств защиты растений. Он широко применяется в медицине, животноводстве.
Наряду с индивидуальными ксиленола- ми применяется и смесь изомеров ксилено- ла для получения полупродукта в синтезе мономеров, пестицидов, витаминов, негорючих функциональных жидкостей и растворителей для эмалей, наносимых на электропровода.
Ресурсы ксиленолов в каменноугольной смоле в несколько раз меньше потребностей в этом сырье. Поэтому во всех развитых странах организованы производства синтетических ксиленолов.
Имеется сообщение о реакции алкили- . рования фенола или о-крезола метанолом в присутствии различных катализаторов. Отмечается, что основными продуктами алки- лирования являются о-метилфенолы, в частности о-крезол и 2.6-ксиленол. В большинстве случаев в условиях алкилирования фенола или о-крезола почти отсутствуют п- изомеры. в частности 2 4-ксиленол. Реакцию алкилирования фенола метанолом в присутствии 2,6-ксиленола и воды изучали при температуре 440-500° С над катализатором, содержащим Мд МдСОз. Мд(ОН)а, .содержащие2,5% МпОидо 10% связующего полипропиленоксида. Полученный катг- лизат при 500° С содержит 27,5%
VI VI
00
о
2.6-ксиленола, 1.6% 2/1 ксиленола. 42.5% о крезола, а также 4,6-мезитол. Процесс пригоден для синтеза о-крезола и2,6-ксиле- нола. Недостатком способа является низкий выход 2,4-ксиленола, высокая температура реакции, приводящая к газификации метанола, а также побочное превращение 2,6-ксиленола в результате реакции его трансметилирования.
В литературе имеются некоторые сообщения о получении 2,6-ксиленолэ на основе о-крезола и метанола с незначительным содержанием других изомеров, в частности 2,4-ксиленола.
Реакцию алкилирования о-крезола метанолом изучали в присутствии у- при широком интервале температур (170-430° С). Установлено, что при низких температурах (200-270° С) основными продуктами реакции являются о-метиланизол и 2,6-ксиле- нол, суммарный выход которых ближе к 100%. С ростом температуры в алкилатах рэстут выходы других изомеров ксиленрла, в частности 2,4-, 2,3-, 2,5-изомеры. Одновременно наблюдается рост в алкилатах содержания три- и полиметилфенолов. Полученная сложная смесь метилфенолов не пригодна для дальнейшей переработки алкилита для получения 2,6- и 2,4-ксилено- лов, максимальный выход которых составляет соответственно 42,2% (при т-320° С и 19,4% (при т-ре 430° С). Наличие в алкилатах значительных количеств п- и м-крезолов (до 11%), а также 2,3- (до 9,9%), 2,5- (до 10%) -ксиленолови полиметилфенолов (до 11,3%) намного усложняют технологию процесса при значительных отходах производства.
Известен способ непрерывного алкилирования фенолов метиловым спиртом и ди- метиловым.эфиром в жидкой фазе в присутствии галогенидов цинка, хрома, и небольшого количества соляной и броми- стоводородной кислоты при температуре 175-250° С и давлении 0,5-6,0 МПа (лучше 3 МПа). Сообщается, что в присутствии катализатора HBr H20 при 230° С полученный алкилат содержит 54% о-, 22,7% п-крезолов и до 40% высших алкилфенолов, в частности 2,4-ксиленола (11,6%), 2,6-ксиленола (7,0%) и др.
Недостатком указанных способов является высокое давление, низкая селективность процесса по конкретным изомерам крезолов и ксиленолов и быстрая коррозия аппаратуры.
В качестве прототипа принят способ получения ксиленолов алкилирования о- крезола метанолом при температуре 320- 400° С. объемной скорости подачи сырья 0,3-0,9 , молярном соотношении о-крезол:метанол - 2-1:1-2 в присутствии водорода. В качестве катализатора используют синтетические Р-мордениты, содержащие 0,1-5,0 мас.% никеля и 25% А120з в качестве
связующего компонента. При температуре 380° С, объемной скорости подачи сырья 0,5 ч , молярном соотношении о-крезол:мета- нол 1:1 выхода 2,6- и 2,4-ксиленолов соответственно равны 69,8 и 17,5% при
0 конверсии о-крезола 40,2%. В указанных условиях в алкилате присутствуют также другие изомеры ксиленолов (до 2,2%), 2,4.6- мезитол (6,0%) и полиметилфенолы (1.3%), что снижает селективность реакции по 2,65 и 2,4-ксиленолам.
Данные каталитические системы менее стабильны в реакции алкилирования о-крезола метанолом и позволяют синтезировать преимущественно 2,6-ксиленол, выход ко0 торого в смеси двух изомеров достигает до 80%.
Таким образом, недостатком прототипа является низкий выход 2,6- и 2,4-ксиленолов, малое количество 2,4-ксиленола в сме5 си двух изомеров, нестабильная работа катализатора и невысокая селективность процесса.
Целью изобретения является устранение недостатков прототипа, а именно увели0 чение выхода целевых продуктов в селективности процесса, а также повышение стабильности работы катализатора,
Указанная цель достигается путем алкилирования о-крезола при температуре 3305 400° С, объемной скорости подачи сырья 0,3-1,0 , молярном соотношении о-кре- зол:метанол 0,5-1,5:1 в присутствии водорода на синтетическом Н-морденитном катализаторе, модифицированным никелем
0 и сульфатом хрома (Щ) следующего состава, мас.%:
NI0.1-5
Сг2(504)з0,1-0,5
н-Моденит (5Ю2:А120з 45) 69,5-78,8
5 А120з20,0-25,0
Предлагаемый способ осуществляется следующим образом.
Алкилирование о-крезола метанолом проводится на лабораторной установке про0 точного типа. В реактор загружается 100см3 катализатора, скорость подачи сырьевой смеси о-крезола и метилового спирта регулировалась насосом в пределах 0,3-1,0 , а водорода ротаметром. Из реактора пары
5 реакционной смеси, проходя холодильник, конденсируются и поступают в сепаратор, где жидкие продукты отделяются от газообразных, которые, проходя адсорбер и газовые часы, поступают в газометр. Температура реактора регулируется и контролируется с помощью потенциометра, Жидкие продукты реакции исследуются с помощью ГЖХ и ИК спектроскопии. Хрома- тографические анализы проводились на хроматографе хром-5 с колонкой 3,6 м, заполненной хромосорбом W, пропитанным 18% диметилфталатом. Скорость газа носителя гелия 80 мл/мин,температура колонки 130° С. Идентификация пиков хроматог- рамм проводится введением эталонных углеводородов в исследуемых продуктах с последующим снятием хроматограммы образца. Относительная погрешность при анализе не превышает 3-5.0%. Результаты проведенных опытов показаны на примерах 1-7.
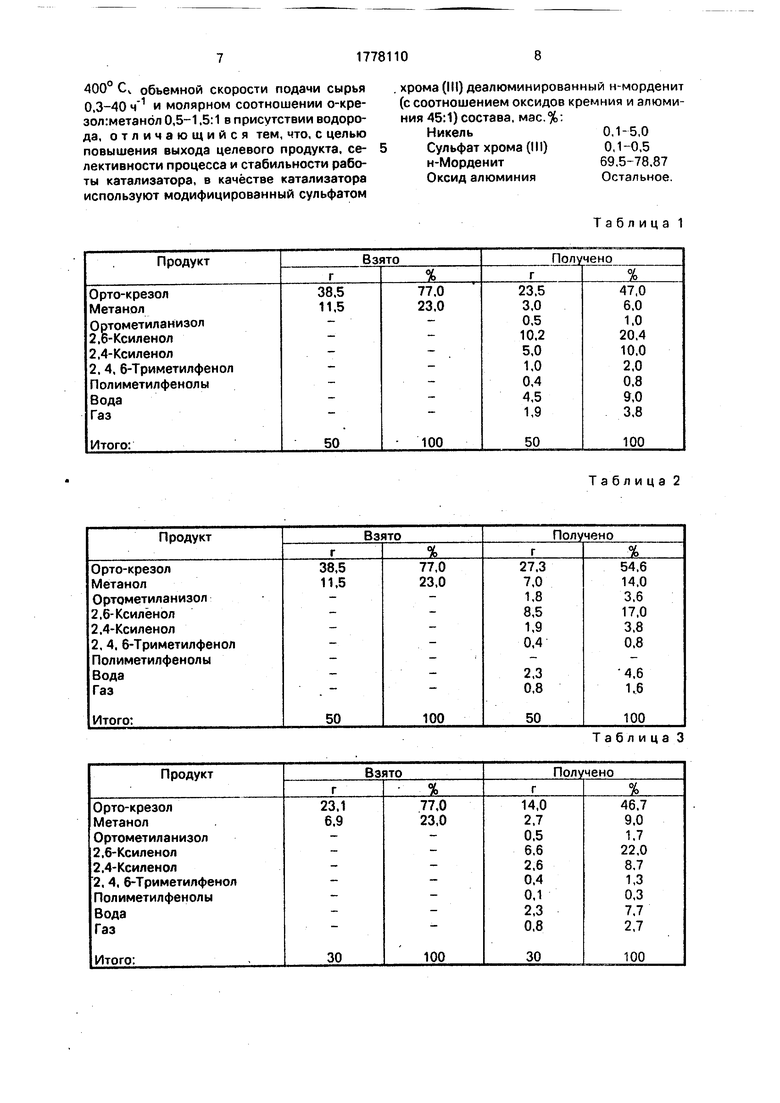
Пример 1. Смесь 38,5 г о-крезола и 11,5 г метанола пропускают над таблетиро- ванным катализатором состава, мас.%: 1,0 Ni, 0,2% Сг2(5См)з. 75% Н-морденита (ЗЮ2:А120з 45) и 23,8% А120з с обьемной скоростью 0,5 ч , при температуре 370° С, мольном соотношении о-крезол:метанол 1:1. Расход водорода 850 л на 1 л катализатора в чос (850 л /л.кат ч).
Полученный катэлизат подвергают ректификации и хроматографическому анализу и получают 23,5 i непрореагировавшего о- крезола, 0,5 г метиланизола. 10,2 г 2,6-кси- ленола, 5,0 г 2 ,4-ксиленола, 1,0 г 2,4,6-триметилфенола, 0,4 г лолиметилфе- нола, 3,0 г непревращенного метанола, 4,5 г воды и 1,9 г газообразных продуктов. Выход 2,6- и 2,4-ксиленолов соответственно составляет 60,3 и 29,6%. Суммарный выход 2,4- и 2,6-ксиленолов на пропущенный о- крезол равен 35,1%. Конерсия о-крезола 39,0%. Конверсия метанола 73,0%.
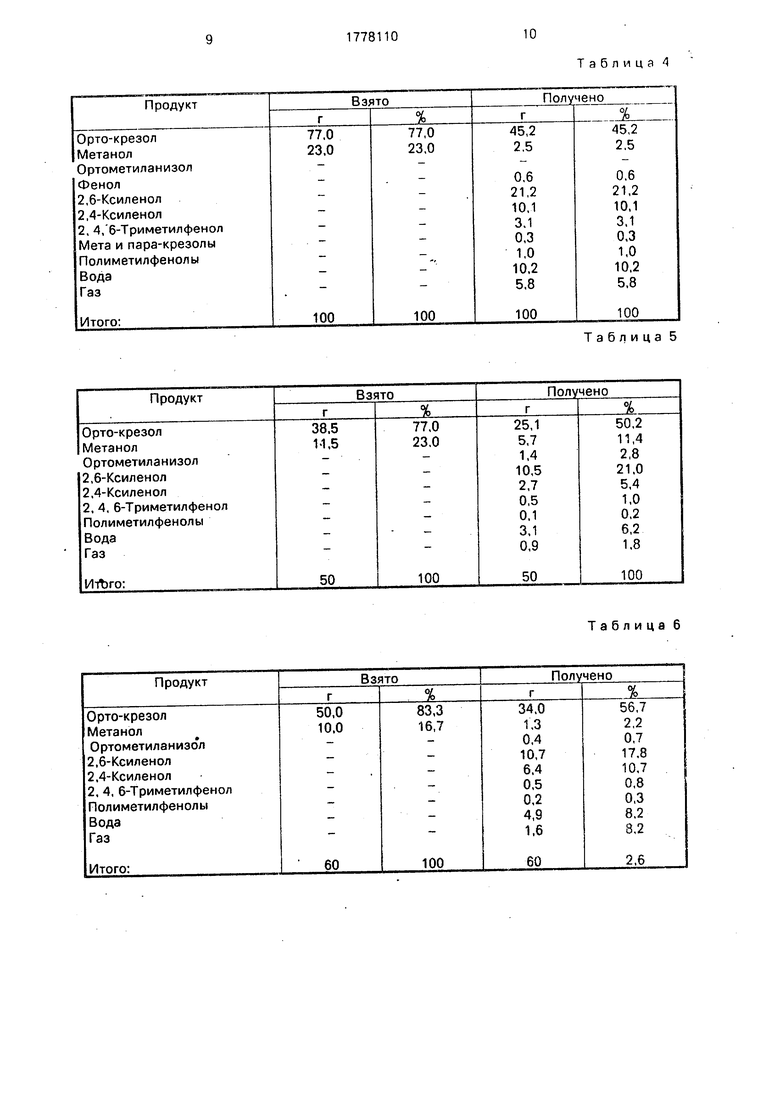
Примеры 1-7. Осуществляют согласно примеру 1 за исключением условий и результатов, приведенных в табл. 1-7 соответственно.
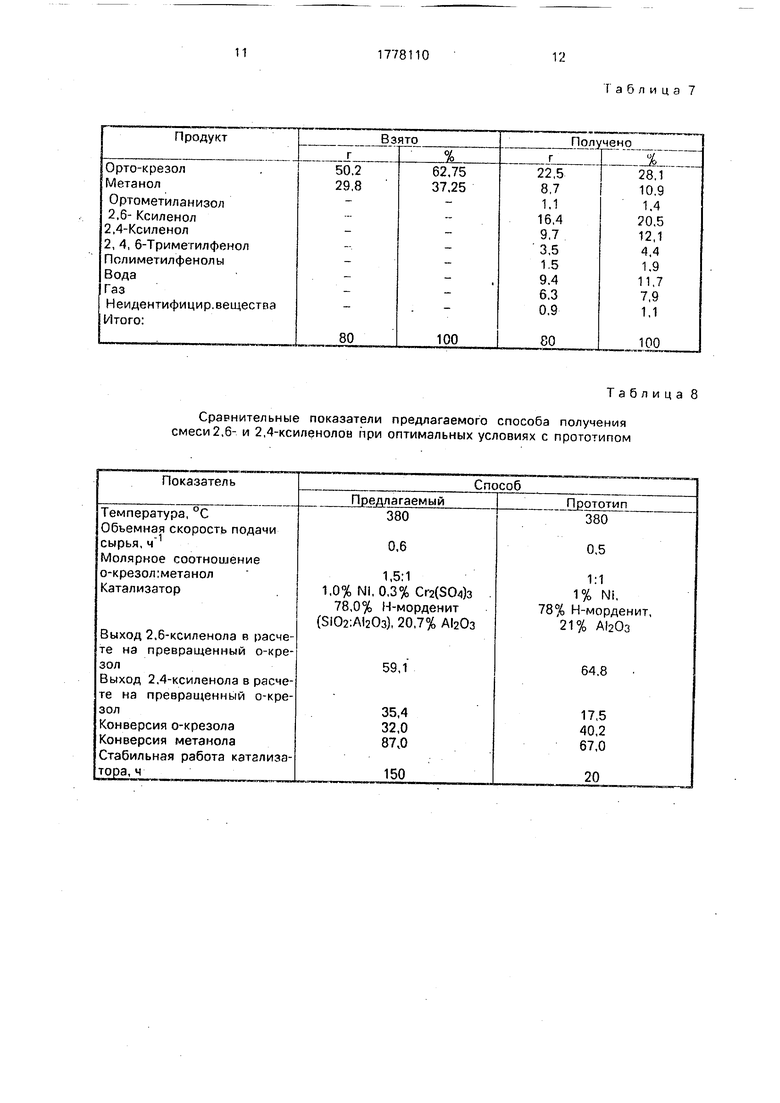
Сравнительные показатели предлагаемого способа получения 2,6- и 2,4-ксиленолов при оптимальных условиях с выбранным прототипом показаны в табл, 8,
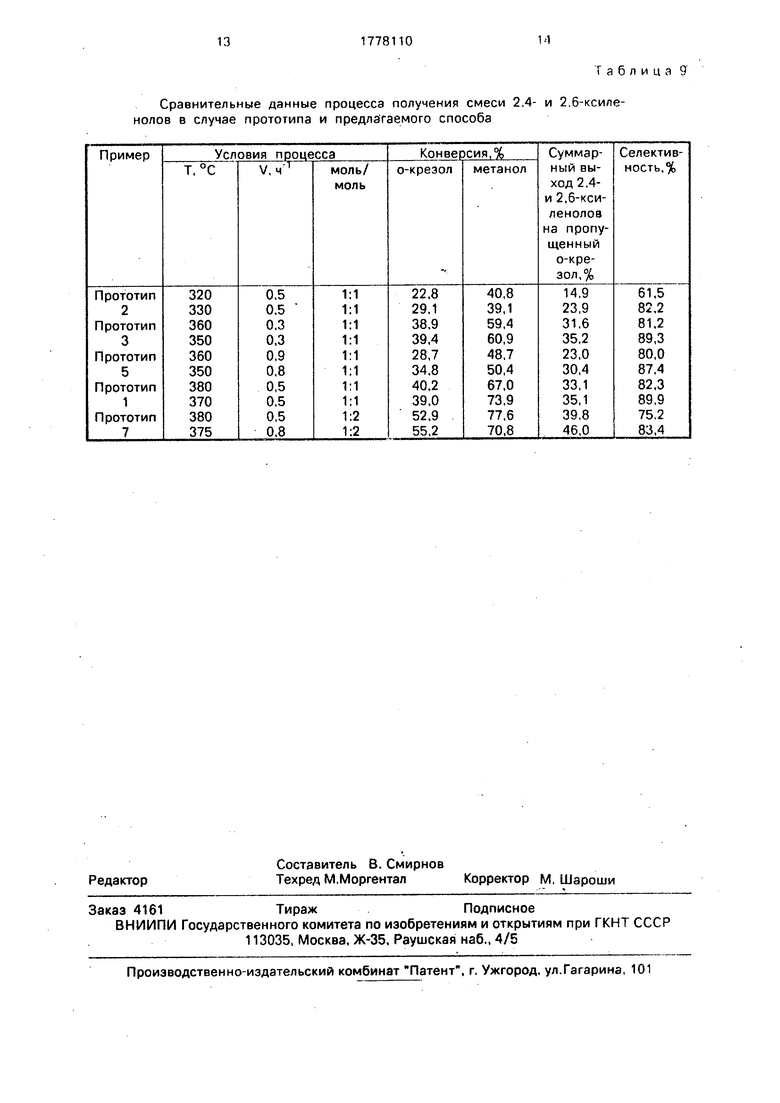
Кроме того, для полного представления о преимуществе предложенного способа в табл. 9 представлены все данные, в том числе по конверсии о-крезола и метанола, суммарный выход 2,6- и 2.4-ксиленолов в расчете на пропущенный и на превращенный о-крезол. Как видно, в близких условиях (температура, объемная скорость, мольное соотношение) показатели предложенного способа выше, чем в случае прототипа. При этом необходимо отметить, что в прототипе приводится суммарный выход 2,4- и 2,5-кси- ленолов (кроме 2,6-изомерэ), а в предлагаемом способе только 2,4-ксиленола. т. е. в
. алкилзтах полностью отсутствует 2,5-изо- мер. Следовательно, приведенные данные в табл. Q по выходу и селективности в случае прототипа несколько завышены. Несмотря и на это, предложенный способ превосходит прототип по суммарному выходу 2,6- и 2,4-кс.иленолов в расчете на пропущенный и нз превращенный о-крезол, а также по стабильности работы каталисатора. При этом в
0 смеси изомеров ксиленола выход 2,4-диме- тилфеиола растет почти в два раза.
Отсутствие в алкилате других изомеров ксиленола намного упрощает технологию его дальнейшей переработки.
5 Таким образом, предложенный процесс является высокоселективным, не требует дорогого сырья, сверхособого технологического оформления и может рекомендован для производства 2,6- и 2,4-ксиленолов.
0Выхода 2.6- и 2,4-ксипенстов п расчете
на превращенный о-крезо/. соответственно
равны 67,2 и 15,0%. Конверсия о-крезола
29,1 %, Конверсия метанола 39,1 %. Суммар. ный выход 2,6- и 2,4-ксиленолов на пропу5 щенный о-крезол равен 23,9%.
Выхода 2,6- и 2,4-ксиленолов в расчете на превращенный о-крезол соответственно раины 64,1 и 25,2%. Конверсия о-крезола 39,4%. Конверсия метанола 60,9%. Суммар0 ный выход 2,6- и 2,4-ксиленолоп на пропущенный о-крезол равен 35,2%.
Выхода 2,6- и 2,4-ксиленолов в расчете на превращенный о-крезол соответственно равны 59,1 и 28.1%. Конверсия о-крезола
5 41,3%. Конверсия метанола 89,1 %. Суммарный выход 2,6- и 2,4-ксиленолов на пропущенный о-крезол равен 36,0%.
Выхода 2,6- и 2.4-ксиленолов в расчете на превращенный о-крезол соответственно
0 равны 69,5 и 17.9--%. Конверсия о-крезола 34,8%. Конверсия метанспз 50,4%. Суммарный выход 2,6- и 2,4-ксиленолов на пропущенный о-крезол равен 30.4%.
Выхода 2,6- и 2,4-ксиленолов в расчете
5 на превращенный о-крезол соответственно равны 59,1 и 35,4%. Конверсия о-крезола - 32,0%. Конверсия метанола 87 0%. Суммарный выход 2,6- и 2,4-ксиленопов на пропущенный о-крсоол равен 30.2%.
0Выхода 2,6- и 2,л-ксиленолов в расчете
на превращенный о-крезол соответственно равны 52,4 и 31,0%. Конверсия о-крезола 55,2%. Конверсия метанола 70,87о. Суммарный выход 2,6- и 2,4-ксиленолов на пропу5 щенный о-крезол равен 46,0%.
Формула изобретения Способ получения смеси 2,6- и 2.4-ксиленолов путем алкилирования о-крезола метанолом в присутствии катализаюра - морденита. содержащего никель, при 330400° Cv объемной скорости подачи сырья 0,3-40 и молярном соотношении о-кре- зол:метанол 0,5-1.5:1 в присутствии водорода, отличающийся тем, что, с целью повышения выхода целевого продукта, селективности процесса и стабильности работы катализатора, в качестве катализатора используют модифицированный сульфатом
. хрома (III) деалюминированный н-морденит (с соотношением оксидов кремния и алюминия 45:1) состава, мас.%:
Никель0,1-5,0
Сульфат хрома (III)0,1-0,5
н-Морденит69.5-78,87
Оксид алюминияОстальное.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения крезолов | 1989 |
|
SU1721043A1 |
| СПОСОБ ПОЛУЧЕНИЯ О-КРЕЗОЛА И 2,6-КСИЛЕНОЛА | 1993 |
|
RU2043330C1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ О-АЛКИЛФЕНОЛОВ | 2002 |
|
RU2256644C1 |
| Способ получения орто-метилзамещенных фенолов | 1973 |
|
SU461092A1 |
| СПОСОБ ПОЛУЧЕНИЯ 0-КРЕЗОЛА И 2,6-КСИЛЕНОЛА | 1970 |
|
SU273208A1 |
| СПОСОБ ПОЛУЧЕНИЯ о-КРЕЗОЛА И 2,6-КСИЛЕНОЛА | 1969 |
|
SU255290A1 |
| СПОСОБ ПОЛУЧЕНИЯ о-МЕТИЛЗА.(\\ЕЩЕКНЫХ ФЕНОЛОВ | 1967 |
|
SU200515A1 |
| Способ получения крезолов | 1988 |
|
SU1595833A1 |
| Способ получения метилпроизводных фенола | 1989 |
|
SU1671655A1 |
| Способ получения метилфенолов | 1981 |
|
SU1004342A1 |
Область использования: основной органический синтез получение полупродуктов. Сущность изобретения: продукт 2,6- и 2,4ксиленолы БФС С 8 Н 100. Реагент 1: метанол. БФ СН40. Реагент 2: 0-крезол БФ . Катализатор, модифицированный никелем и сульфатом хрома деалюминиро- . ванный морденит состава, мас.%: никель 0,1-5; сульфат хрома 0,1-0,5; Н-морденит (соотношение оксидов, кремния и алюминия 45-1) 69,5-76,8; оксид алюминия - остальное до 100%. Условия реакции: температура 330-400° С. объемная скорость подачи сырья 0,3-1.0 ч , молярное соотношение о-крезол:метанол 0,5-1,5:1, присутствует водород. Выход 23,9-46%. Селективность 82,2-95,3%. 2 табл.
Таблица 1
Таблица 2
Таблица 3
Таблица 4
Таблица 5
Таблица 6
Сравнительные показатели предлагаемого способа получения смеси 2,6- и 2,4-ксиленолов при оптимальных условиях с прототипом
Показатель
Температура, °С
Объемная скорость подачи
сырья,
Молярное соотношение
о-крезол:метанол
Катализатор
Выход 2.6-ксиленола в расчете на превращенный о-кре- зол
Выход 2,4-ксиленола в расчете на превращенный о-кре- зол
Конверсия о-крезола Конверсия метанола Стабильная работа катализатора, ч
Таблица 7
Таблица 8
Способ
Предлагаемый
Прототип
380 0.5
1:1
1% NI.
78% Н-морденит, 21%
59,1
17,5 40,2 67,0
20
Сравнительные данные процесса получения смеси 2.4- и 2,6-ксиле- нолов в случае прототипа и предлагаемого способа
Таблица 9
| Ахмедов В.М | |||
| и др | |||
| - Журн | |||
| прикладной химии, 1987, т | |||
| Способ получения молочной кислоты | 1922 |
|
SU60A1 |
| Коллектор для пароперегревателей в жаровых трубках | 1921 |
|
SU1431A1 |
Авторы
Даты
1992-11-30—Публикация
1990-03-01—Подача