Изобретение относится к усовершенствованному способу получения пироглута- милсодержащих субстратов, которые находят применение в медицинской биологической химии.
Известно несколько способов синтеза n-нитроанилидов пироглутамилсодержа- щих субстратов. Их получают конденсацией пироглутамилпептида с п-нитроанилидом аминокислоты.
Известен способ получения пироглута- милпептидов методом активированных эфи- ровсиспользованием
пентафторфенилового или М-оксисукцини- мидного эфиров. Конденсация пироглутамилпептида с п-нитроанилидом аминокислоты проведена с N.N -дициклогексилкарбодиимидом, иногда в присутствии одного эквивалента М-оксисукциними- да.
Известны ферментативные способы получения n-нитроанилидов пироглутамил- содержащих субстратов путем конденсации фрагментов с использованием химотрипси- на и термолизина.
Эти способы не позволяют получать продукты с достаточно высоким выходом, они не удобны для использования в промышленности при крупномасштабных производствах и требуют дорогостоящих реактивов.
Известны способы получения пироглу- тамилсодержащих ферментных субстратов путем конденсации Вос-замещенной L-пиviсо
ю ю
0
роглутаминовой кислоты с п-нитроанили- дом в присутствии конденсирующего агента (ДЦК) при 0°С с последующей выдержкой при комнатной температуре.
Недостаток известного способа состоит в том, что в нем используют защищенную по аминогруппе пироглутаминовую кислоту, дициклогексилкарбодиимид (сильный аллерген), кроме того при осуществлении известногоспособатребуетсядополнительная стадия - отщепление защитной группы. Выход целевого продукта невысок и составляет-ч.17%.
Недостатком известных способов является использование в синтезе М-защищен- ных производных пироглутаминовой кислоты.
Цель описываемого способа - повышение выхода пироглутамилсодержащих ферментных субстратов и упрощение процесса
Поставленная цель достигается описываемым способом, в котором хлоран- гидрид 1-пироглутаминовой кислоты полученный непосредственно перед введением в реакцию обработкой 1-пироглутаминовой кислоты пятихлористым фосфором при температуре -5 - 10°С в абсолютном хлорированном углеводороде, вводят во взаимодействие с азотсодержащим ароматическим нитросоединением
формулы A-NH- J -N02 , где , L-Phe,
L-Phe-L-Ala, L-Alaa-L-Ala-L-Leu и процесс ведут в присутствии основания с последующей выдержкой в течение 16 часов, предпочтительно при в качестве основания использовать избыточное количество п-нитроанилида.
Способ осуществляют следующим образом.
Индивидуальность полученных соединений установлена методом ТХС на пластинках Silufol в системах, этанол-н-бутанол-вода 1:4:1 (А); пиридин- н-бутанол-вода-уксусная кислота 20:30:12:6(5); н-бутанол-уксусная кислота- вода 200-35:70 (В).
К суспензии 18,1 г (87 ммоль) пентахло- рида фосфора в 150 мл абсолютного хлорированного углеводорода (метиленхлорид, хлороформ) порциями добавляют 10,2 г (79 ммоль) L-пироглутаминовой кислоты, под- дё ржйвая т е мпературу реакционной смеси -5-10°С При данной температуре переме- шибйют еще 1 ч. Растворителе обсасывают. Прибавляют 79 ммоль n-нитроанилида аминокислоты или пептида, или п-нитроанили- на и 79 ммоль основания х (триэтиламин пиридин, N-метилморфолин) в абсолютном
неполярном растворителе (тетрагидрофу- ран, диоксан). Прибавление ведет при температуре -5-10°С, затем перемешивают 2 ч при той же температуре, и оставляют на
16-20 ч при температуре 18-20°С. Раствори- тельупаривают в вакууме водоструйного насоса (температура бани 40°С), остаток обрабатывают 1 н. раствором соляной кислоты, отфильтровывают и на фильтре промывают водой. При перекристаллизации из спирта получают соответственный пироглу- тамилсубстрат.
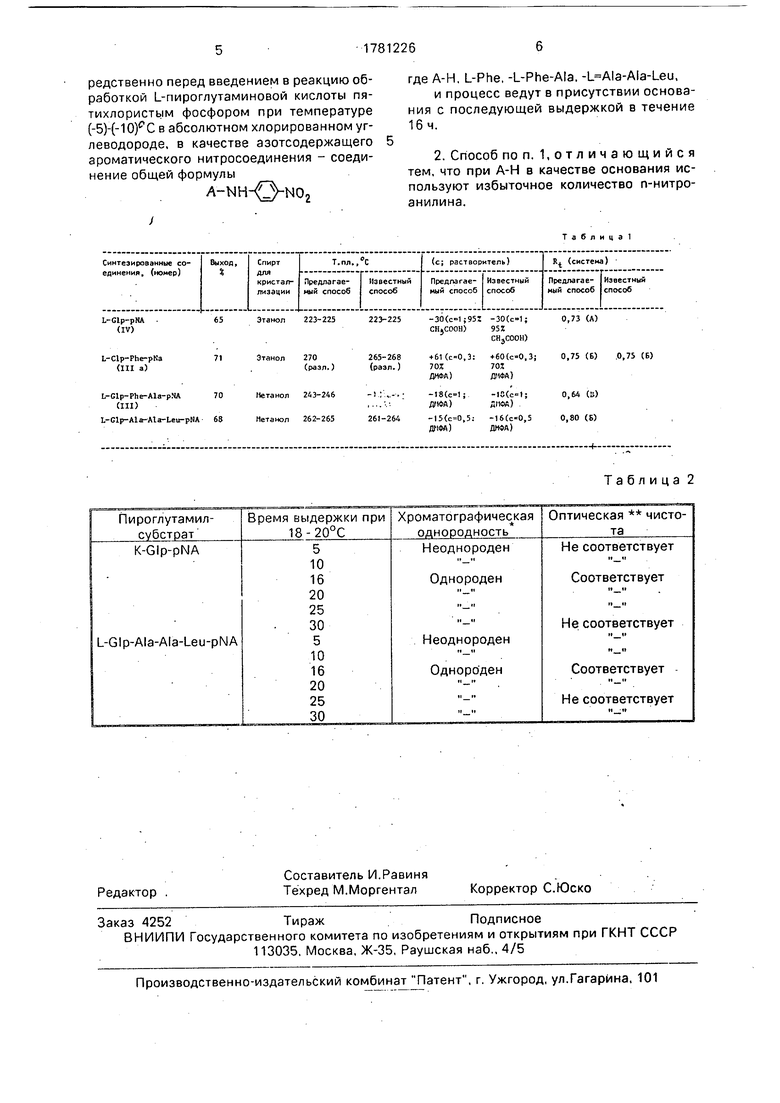
Выходы и свойства полученных соединений даны в табл.1.
При использовании п-нитроанилина
для синтеза п-нитроанилина L-пироглутаминовой кислоты прибавление основания не требуется
По сравнению с известными способами
получения пироглутамилсодержащих ферментных субстратов преимущество предложенного способа характеризуется тем, что по одной общей унифицированной схеме можно синтезировать любой представитель
класса пироглутамилсодержащих ферментных субстратов. Это позволяет провести синтез выше названных соединений в одинаковых технологических условиях.
Кроме того, предложенный способ позволяет исключить работу с сильным аллергеном МЫ-дициклогексилкарбодиимидом, который используется в известных способах для конденсации пироглутамилпептида с п- питроанилидом аминокислоты,
Для осуществления предложенного способа не требуется дефицитные и дорогостоящие сЬерментные препараты (химотрип- син, термолизин), которые используются в известных способах для синтеза препаративных количеств некоторых пироглутамил- пептидов.
Формула изобретения 1 Способ получения пироглутамилсодержащих субстратов общей формулы
L-CCp-NRNO-,
где R-H, L-Phe-, -L-Phe-Ala, -L-Ala-Ala-Leu, путем взаимодействия производного Lпироглутаминовой кислоты с соответствующим азотсодержащим ароматическим , нигросоединением в абсолютном неполяр- ; ном органическом растворителе при пониженной температуре с последующей
выдержкой при комнатной температуре, о т- личающийся тем, что, с целью упрощения процесса и повышения выхода, в качестве производного L-пироглутаминовой кислоты используют хлорангидрид L-пиро- глутаминовой кислоты, полученный непосредственно перед введением в реакцию обработкой L-пироглутаминовой кислоты пя- тихлористым фосфором при температуре (-БН-Ю С в абсолютном хлорированном углеводороде, в качестве азотсодержащего ароматического нитросоединения - соединение общей формулы
А-МН- 3 М02
где А-Н. L-Phe, -L-Phe-Ala. -L Ala-Ala-Leu,
и процесс ведут в присутствии основания с последующей выдержкой в течение 16ч.
2. Способ по п. 1,отличающийся тем, что при А-Н в качестве основания используют избыточное количество п-нитро- анилина.

| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИДНЫЕ СУБСТРАТЫ ЦИСТЕИНОВЫХ ПЕПТИДАЗ СЕМЕЙСТВА ПАПАИНА | 2018 |
|
RU2717689C2 |
| @ -Нитроанилиды пироглутамилсодержащих пептидов в качестве субстратов сериновых протеиназ | 1980 |
|
SU1025091A1 |
| Способ получения трипептидов | 1980 |
|
SU1277904A3 |
| Способ получения пептидов | 1976 |
|
SU668594A3 |
| СПОСОБ ПОЛУЧЕНИЯ НОНАПЕПТИДЭТИЛАМИДА | 1995 |
|
RU2086561C1 |
| Способ получения пептидов | 1970 |
|
SU439967A1 |
| Способ получения производных борсодержащих пептидов | 1988 |
|
SU1807988A3 |
| ПРОИЗВОДНЫЕ БОРСОДЕРЖАЩИХ ПЕПТИДОВ | 1991 |
|
RU2017749C1 |
| Способ ферментативного получения пептидов | 1980 |
|
SU1378785A3 |
| Способ получения полипептидов или их солей | 1977 |
|
SU910116A3 |
Использование: в медицинской и биологической химии. Сущность: способ получе- ния пироглутамилсодержащих ферментных субстратов общей формулы: L-GLp-MR-C CH-C-N02 СН СН-СН где R-H, -Phe, -Phe-Ala, -Ala-Ala-Leu. Реагент 1: хлорангидрид L-пироглутаминовой кислоты, полученный непосредственно перед введением в реакцию обработкой L-пироглутаминовой кислоты пятихлористым фосфором при температуре -5-10°С в абсолютном хлорированном углеводороде: . Реагент 2: RNH-C-CH-C-N(2 сн сн-сн Процесс ведут в присутствии основания с последующей выдержкой в течение 16 ч. Предпочтительно при получении соединений I, где , в качестве основания используют избыточное количество n-нитроанилина. Выход 70-95%. 1 з.п. ф-лы, 2 табл. со С
Таблица
Таблица 2
| @ -Нитроанилиды пироглутамилсодержащих пептидов в качестве субстратов сериновых протеиназ | 1980 |
|
SU1025091A1 |
| кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| @ -Нитроанилид @ -пироглутамил- @ -фенилаланил- @ -аланина-хромогенный субстрат тиоловых протеиназ | 1984 |
|
SU1198082A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Fujiwaka К | |||
| и др | |||
| New chromogenic and Fluorogenlc substrats for Pyrrolidonyl Peptidase | |||
| -J.Biochem | |||
| Чугунный экономайзер с вертикально-расположенными трубами с поперечными ребрами | 1911 |
|
SU1978A1 |
Авторы
Даты
1992-12-15—Публикация
1990-02-05—Подача