Изобретение относится к новым производным триазиноиндола, конкретнее к N-(2-гидроксиэтил)амиду (1,2,4-триазино[5,6-b]индолил-3-тио)уксусной кислоты формулы I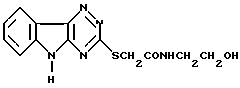
обладающему противогипоксической активностью и восстанавливающему функциональную электрическую активность мозга (соединение I).
Известны производные 1,2,4-триазино[5,6-b] индола, обладающие противогипоксической активностью, однако их эффективность в отношении восстановления угнетенной электрической активности мозга не выявлена.
Из этих соединений наиболее активен гидрохлорид 3-(3-диметиламинопропилтио)-1,2,4-триазина[5,6-b]индола (соединение II) и 3-(пиперидинокарбонилметилтио)-1,2,4-триазино[5,6-b] индол (соединение III). Последнее соединение обладает противогипоксической активностью и защищает от острого токсического отека легких.
Цель изобретения новое производное триазиноиндола, обладающее преимуществами при защите от гипоксии по сравнению со структурным аналогом и восстанавливающее угнетенную электрическую активность мозга.
Поставленная цель достигается синтезом соединения I.
П р и м е р. К раствору 6,07 г (30 ммоль) 3-меркапто-1,2,4-триазино[5,6-b] индола в 33 мл 1н.водного раствора едкого натра прибавляют при интенсивном перемешивании раствор 4,54 г (33 ммоль) N-(2-гидроксиэтил)-α-хлорацетамида в 10 мл воды. После добавления около половины указанного раствора образуется желеобразная масса вишневого цвета. Реакционную массу оставляют на ночь, размешивают с 50 мл воды, осадок отфильтровывают, промывают водой (2х30 мл), охлажденным до 0oC спиртом (2х15 мл) и сушат при 60oC. Получают 6 г (66%) предлагаемого соединения в виде желтых кристаллов. Вещество очищают перекристаллизацией из смеси диметилформамида с изобутиловым спиртом, 1:2,4 об. (85 мл/г). Выход при перекристаллизации 67% (выход перекристаллизационного вещества по отношению к исходному меркаптопроизводному 44,2% ), получают 4,2 г светло-желтых кристаллов с т.пл. 226oC. Вещество однородно по данным ТСХ на силуфоле УФ-254, элюент этиловый спирт 3%-ный водный аммиак, 10:0,5 по объему, Rf0,69.
Строение вещества подтверждено данными элементного анализа и спектрами.
УФ-спектр в спирте, lмакс, нм lgε: 204 (4,46), 222 (4,39), 265 (4,58), 344 (4,21). Положение и интенсивность двух длинноволновых полос поглощения характерно для S-алкильных и S-аминоалкильных производных триазиноиндола.
ИК-спектр в суспензии в вазелиновом масле, n, см-1: 1650 (С=О) полоса "Амид-I", 1542 (NH) полоса "Амид-II", 1290, 765, 625 (C-N) полосы "Амид-III".
Найдено, C 50,91, H 4,12, N 23,02, S 10,49.
C13H13N5O2S.
Вычислено, C 51,48, H 4,32, N 23,09, S 10,57.
Изучение противогипоксической активности заявляемого соединения в сравнении с прототипом.
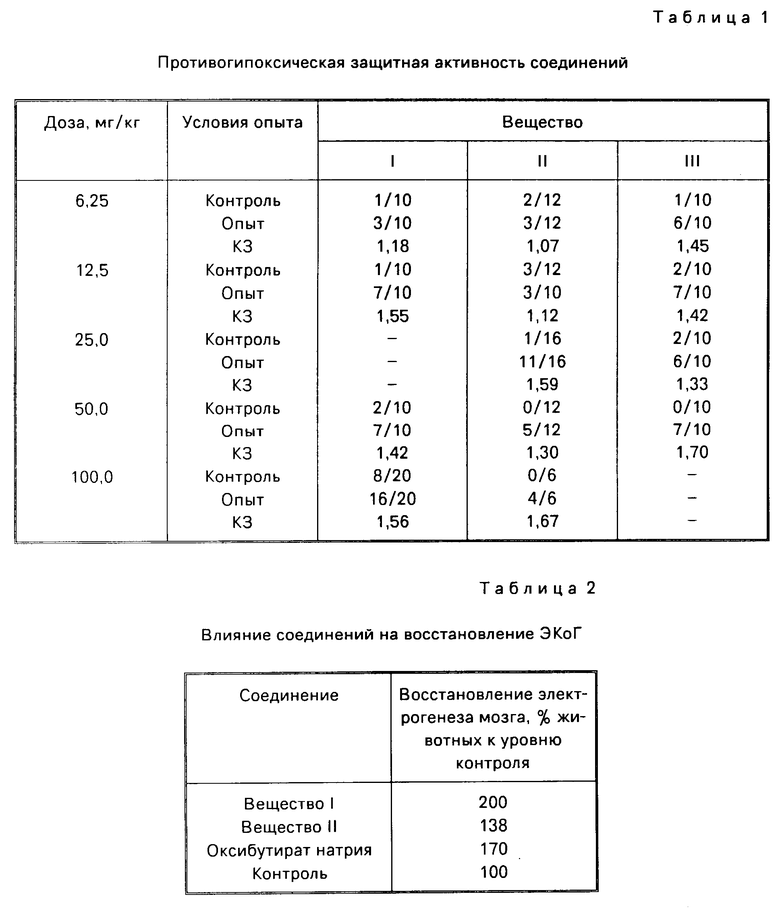
Опыты ставились на белых мышах-самцах обычных кондиций, которым вводили внутрибрюшинно за 40 60 мин до опыта водную суспензию соединения I, стабилизированную твином-85, или водный раствор соединенния-аналога II и III. Контрольным животным вводили тем же путем растворитель в том же объеме. В процессе эксперимента животных "поднимали" в барокамере на высоту 9,5 км и удерживали там 45 мин (Пастушенков Л.В. 1966). Учитывалось число погибших и выживших животных в контроле и опыте. На основании этих данных рассчитывался коэффициент защиты (КЗ) (Ильченко И.Д. и др. 1987). Результаты опытов представлены в табл.1.
В табл.1 в строках "Контроль" и "Опыт" в числителе число выживших животных, в знаменателе число животных, взятых в опыт. Для значений опыта для всех трех препаратов точным методом Фишера с использованием четырехпольной таблицы показано, что достоверные отличия в активности при Р 0,05 в пользу соединения I существуют только в дозе 12,5 мг/кг. В остальных дозах различия статистически несущественны. Различия в активности вещества 1 в дозах 12,5, 50 и 100 мг/кг были несущественны. Следовательно, максимальная эффективная доза составила 12,5 мг/кг. Для аналогов (соединений II и III) эта доза была равна 100 и 50 мг/кг соответственно. Различия в активности всех трех веществ в максимальных эффективных дозах также несущественны. Следовательно, вещество I не уступает аналогам, но эффективнее в меньшей дозе 12,5 мг/кг. Главным показателем при сравнении противогипоксической активности в данном случае является терапевтический индекс (см. ниже).
Изучение способности восстанавливать электрическую активность мозга в сравнении со структурным аналогом-соединением II и аналогом по действию - оксибутиратом натрия.
Нарушения электрической функциональной активности мозга воспроизводили у крыс путем отключения спонтанного дыхания с помощью миорелаксанта - Д-тубокурарина (0,5 мг/кг внутрибрюшинно). У животных регистрировали электрокортикограмму (ЭКоГ). Препараты вводили внутрибрюшинно в дозе 50 мг/кг за 1 ч до опыта, в каждом опыте использовали по 10 крыс. Через 30 с после исчезновения ЭКоГ животным проводили искусственную вентиляцию легких и регистрировали максимальные величины восстановления ЭКоГ. Средние результаты испытаний для соединения I, II и оксибутирата натрия представлены в табл.2. Для аналога по структуре III в этих опытах активность не была выявлена.
В табл.2 за 100% принято количество животных с восстановленным электрогенезом мозга в контроле. Достоверными при Р≅0,05 были отличия между контролем и соединением I, контролем и оксибутиратом натрия, и между соединениями I и II. Различия между контролем и соединением II были недостоверны. Новое соединение I превосходит аналог II и оксибутират натрия по способности восстанавливать электрическую активность мозга.
Острая токсичность соединения I и аналогов II и III определялась по методу Прозоровского В.Б. и др. (1978). ЛД50 для соединения I была равна 1850 мг/кг, для соединения II 560 мг/кг, для соединения III 4500 мг/кг. Соответственно терапевтический индекс для противогипоксического действия, равный отношению ЛД50 к максимальной терапевтической дозе, для вещества I составил 148,0, а для аналогов II и III 5,6 и 90,0 соответственно.
Таким образом, новое вещество I превосходит структурные аналоги II и III по способности восстанавливать электрическую активность мозга и по терапевтической широте антигипоксического действия.
Сущность изобретения: продукт: N-(2-гидроксиэтил)-амид (1,2,4-триазино[5,6-b]индолил-3-тио)уксусной кислоты формулы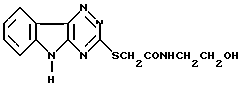
БФ: C13H13N5O2S; выход 67%, т.пл. 226oC. Реагент 1: 3-меркапто-1,2,4-триазино[5,6-b] индол, реагент 2: N-(2-гидроксиэтил)-α-хлорацетамид. Условия реакции: в среде водного раствора едкого натра. 2 табл.
N-(2-Гидроксиэтил)-амид(1,2,4-триазино[5,6-b] индолил-3-тио)-уксусной кислоты формулы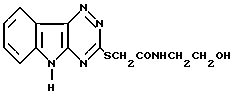
обладающий противогипоксической активностью и восстанавливающий функциональную электрическую активность мозга.
| ГИДРОХЛОРИД 3-(3-ДИМЕТИЛАМИНОПРОПИЛТИО)-1,2,4-ТРИАЗИНО [5,6-B]ИНДОЛА, ОБЛАДАЮЩИЙ ПРОТИВОГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 1989 |
|
SU1598431A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| 3-(ПИПЕРИДИНОКАРБОНИЛМЕТИЛТИО)-1,2,4-ТРИАЗИНО [5,6-B] ИНДОЛ, ОБЛАДАЮЩИЙ ПРОТИВОГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ И ЗАЩИЩАЮЩИЙ ОТ ОСТРОГО ТОКСИЧЕСКОГО ОТЕКА ЛЕГКИХ | 1989 |
|
SU1681504A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1996-09-10—Публикация
1991-02-11—Подача