ел С


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОДНОВРЕМЕННОГО ОПРЕДЕЛЕНИЯ КЛЕТОК С РЕЦЕПТОРАМИ К БИОЛОГИЧЕСКИ АКТИВНЫМ ВЕЩЕСТВАМ И ИХ ПОПУЛЯЦИОННОЙ ПРИНАДЛЕЖНОСТИ | 1994 |
|
RU2081418C1 |
| СПОСОБ ДИАГНОСТИКИ АТОПИЧЕСКИХ АЛЛЕРГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 1991 |
|
RU2026551C1 |
| Способ диагностики силикотуберкулеза | 1986 |
|
SU1442919A1 |
| Способ определения адекватных физических нагрузок у спортсменов | 1984 |
|
SU1246009A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДИФФЕРЕНЦИРОВКИ T-, B-, NK-ЛИМФОЦИТОВ В МАЗКАХ КРОВИ ЖИВОТНЫХ И ПТИЦ | 2000 |
|
RU2192638C2 |
| Способ диагностики туберкулеза | 1987 |
|
SU1527593A1 |
| Способ определения е-розеткообразующих клеток | 1979 |
|
SU862919A1 |
| Способ определения функциональной активности Т-лимфоцитов-супрессоров | 1989 |
|
SU1702316A1 |
| СПОСОБ ИММУНОДИАГНОСТИКИ ИНФЕКЦИЙ | 1996 |
|
RU2136000C1 |
| Способ первичного скрининга химических соединений на иммуномодулирующую активность | 1989 |
|
SU1704084A1 |
Использование: в медицине, а именно в иммунологии. Сущность изобретения: один из фиксированных эритроцитарных реагентов предварительно окрашивают 0,1%-ным раствором одного из красителей (ализариновый желтый, амйдочер- ный, хризоидин, зозин натрия, эритрозин, кристаллвиолет), окрашенные эритроциты отмывают, используют вместе с неокрашенным эритроцитарным реагентом в розеткообразовании, приготовленный затем мазок фиксируют в ацетоне в течение 4,9-5,1 мин при комнатной температуре. Способ дает возможность дифференцировать лимфоциты и моноциты между собой и мононуклеары каждого, из этих типов по двум маркерам одновременно. 4 табл.
Изобретение относится к медицине, а именно к иммунологии.
Идентификация лейкоцитов, особенно лимфоцитов, по их мембранным рецепторам и антигенам - одна из важнейших задач экспериментальной и клинической иммунологии.
Цель изобретения - повышение точности идентификации субпопуляций лимфоцитов.
Способ осуществляют следующим образом. Смешивают равные объемы 5-25% взвеси фиксированных эритроцитов и 0,1 %- ного раствора красителя. Смесь выдерживают в кипящей водяной бане в течение 60-90 мин, Окрашенные эритроциты трехкратно отмывают забуференным, рН 7,2 0,85%-ным раствором хлорида натрия/Технология этого этапа соответствует способу прототипа, но в качестве красителя используют один из перечисленных выше красителей. Проводят смешанное розеткообразование в общепринятом режиме с применением двух эритроцитарных реагентов - неокрашенного и предварительно окрашенного. Затем готовят мазок, который фиксируют химически чистым ацетоном в течение 4,9-5,1 мин, при комнатной температуре (15-25°С), Фиксированный мазок окрашивают по Романов- скому-Гимза. Окрашенный эритроцитарный реагент под микроскопом имеет фиолетовую окраску (при использовании всех перечисленных, кроме хризоидина, красителей) или желтую (при использовании хризоидина) окраску. Другой эритроцитарный реагент (неокрашенный) имеет красный цвет, а
00
ho
N
чэ со
розово-фиолетовые моноциты и лимфоциты различаются морфологически. Возможны следующие варианты маркирования розет- кообразующих клеток: лимфоцит не связал оба эритроцитарных реагента (количество связанных лимфоцитом эритроцитов каждого из реагентов не превышает двух) - такой лимфоцит не имеет ни одного из двух определяемых маркеров; лимфоцит связал не менее трех эритроцитов неокрашенного реагента (для маркера 1) и не более двух эритроцитов окрашенного реагента (для маркера 2) - такой лимфоцит имеет маркер 1 и не имеет маркера 2; лимфоцит связал не более двух эритроцитов неокрашенного реагента и не менее трех эритроцитов окрашенного реагента - такой лимфоцит имеет маркер 2 и не имеет маркера 1; лимфоцит связал не менее трех эритроцитов каждого из двух реагентов (неокрашенного и окрашенного) - такой лимфоцит имеет оба маркера.
Сходными с прототипом признаками являются: 1. Применение для идентификации путем смешанного розеткообразования одного из предварительно окрашенных эритрОцитарных реагентов. 2. Условия окраски эрйтроцитарного реагента.
Существенным отличительным признаком является применение других красителей для предварительной окраски фиксированных эритроцитов и другого способа фиксации мазка, что обеспечивает возможность визуальной дифференциации в мазке разных эритроцитарных реагентов в розетках и морфологической дифференциации лимфоцитов и моноцитов.
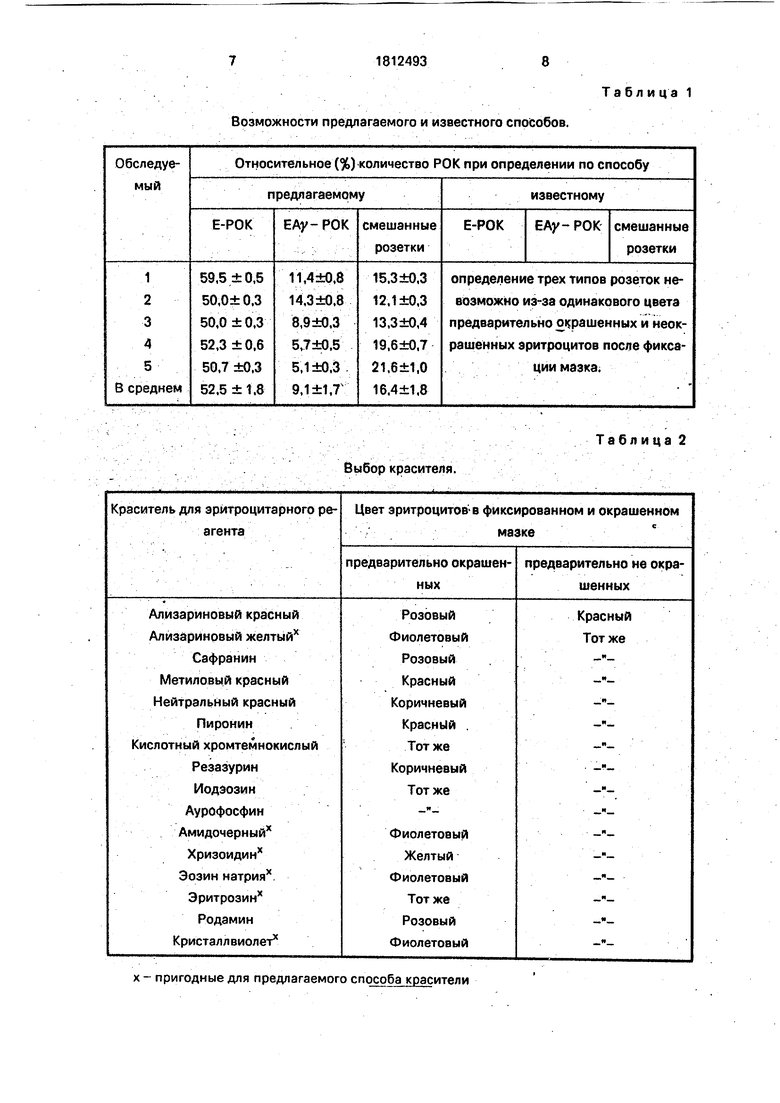
Пример 1. Сравнение предлагаемого и известного способов. По предлагаемому способу: а) окрашивают бараньи фиксированные ацетальдегидом эритроциты амидочерным (или любым другим из перечисленных красителей) путем смешивания равных объемов 10% взвеси эритроцитов и 0,1% раствора красителя, выдерживают смесь при периодическом встряхивании в течение 60 мин е кипящей водяной бане, отмывают эритроциты забу- ференным (рН 7,2)0,85% раствором хлорида натрия (режим этого этапа - как в известном способе). 6) готовят смесь эритроцитарных реагентов для розеткообразования, соединяя равные объемы взвесей окрашенный эритроцитов барака и эритроцитов быка, сенсибилизированных антителами, каждая из которых содержит 2,4 х 108 клеток в 1 мл. в) соединяют полученную смесь и взвесь выделенных лимфомононук- «леаров, содержащую 2 х 106 клеток в 1 мл, в равных объемах. Полученную смесь выдерживают 5 мин при 37°С, центрифугируют 5 мин при 1000 об/мин и дополнительно инкубируют 1 ч при 4°С) готовят мазок, сушат его при комнатной температуре и фиксируют в ацетоне в течение 5 мин при комнатной температуре, д) после высушивания мазка его окрашивают по РомановскомуТимза и под микроскопом подсчитывают содержание моно- и смешанных розеток. Опыт проведен при обследовании 5 доноров.
Предварительное осуществление способа точно по описанию прототипа (учет в камере Горяева) не позволило дифференцировать лимфоциты и моноциты. Поэтому
способ прототипа, с целью обеспечения дифференциации лимфоцитов и моноцитов, использован в варианте учета розеткообразования в мазке. На этапе а) фиксированные ацетальдегидом бараньи эритроциты окрашивают 0,1%-ным раствором генцианвио-; лета, на этапе г) мазок фиксируют 96° метанолом. Остальные этапы выполняют - как описано выше. Способ применен при обследовании тех же 5 доноров. Полученные результаты приведены в табл. 1.
Определение розеток для каждого обследуемого при применении предложенного и известного способов проводили раздельным подсчетом 7 сотен лимфоцитов.
По известному способу дифференциация розеток с Е бар. и ЕА в мазке невозможна, эти эритроциты одинаково окрашены в розовый цвет, поэтому нельзя определить, какой реагент связан. По предлагаемому
способу удалось, благодаря возможности четкой дифференциации Е бар. и ЕА, определить специфические моно- и смешанные (двойные) розеткообразуЮщие лимфоциты. П р и м е р 2. Выбор красителя для
предварительного окрашивания эритроцитов, Фиксированные эритроциты окрашива- ли одним из следующих красителей: ализариновый красный, ализариновый желтый, метиловый красный, нейтральный
красный, кислотный хромтемнокислый, ре- зазурин, иодэозин, аурофосфин, амидочер- ный, хризоидин, зозин натрия, родамин, кристаллвиолет. Все этапы выполняли - как описано в примере 1 для предлагаемого
способа. Результаты приведены в табл. 2.
Видно, что из использованных красителей четкое отличие окраски двух эритроци- тарных реагентов - предварительно окрашенного и не окрашенного of еспечива- ют: ализариновый желтый, амидочерный, хризоидин, зозин натрия, эритрозин, кристаллвиолет.
Пример 3. Выбор способа фиксации мазка.
Фиксированные ацетальдегидом эритроциты барана окрашивали (отдельные порции) каждым из следующих красителей: ализариновый желтый, амидочерный, хри- зоидин, эозин натрия, эритрозин, кристалл- виолет - как описано в примере 1 для предлагаемого способа.
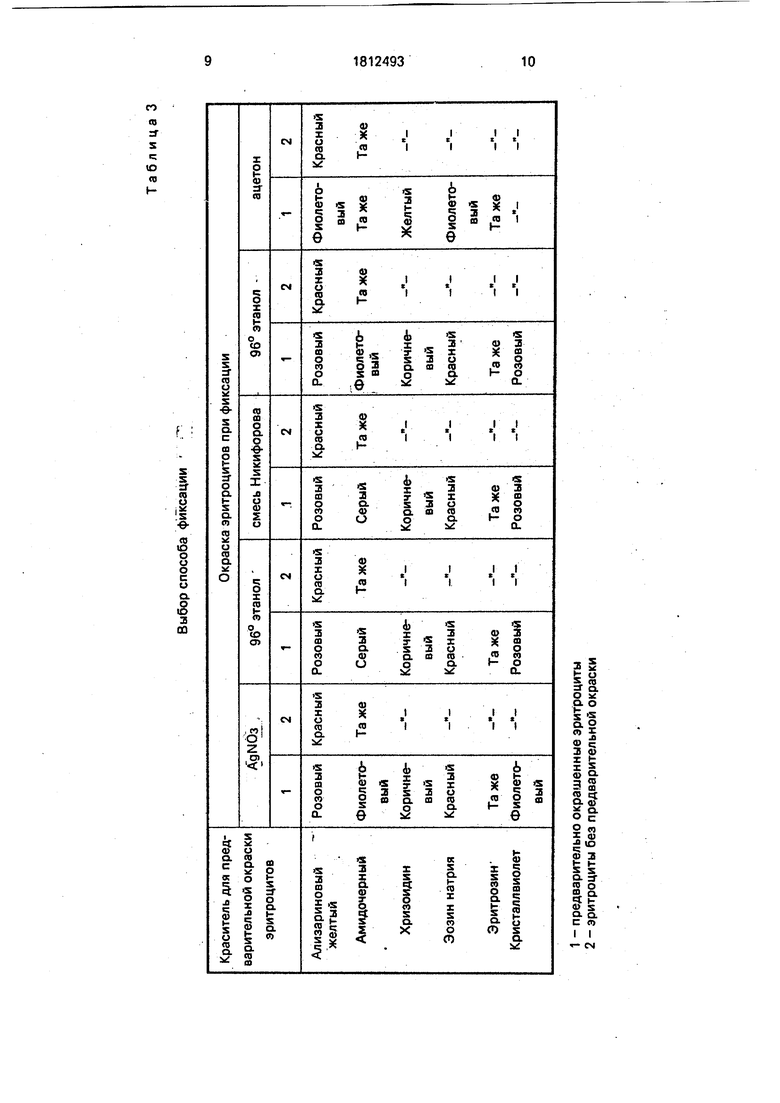
Фиксацию мазка осуществляли одним из следующих методов: 10% раствор АдМОз (10 мин), 96° этанол (30 мин), смесь Никифорова (30 мин), 96° метанол (15 мин), ацетон (5 мин). Все остальные этапы выполнены - как в примере 1 для предлагаемого способа. Результаты приведены в табл. 3. Видно, что отличие в мазке двух эритроцитарных реагентов (окрашенных и не окрашенных предварительно) обеспечивают, в зависимости от использованного для предварительной окраски красителя, разные фиксаторы. Но наиболее четкие и для большего числа красителей результаты получены при фиксации мазков ацетоном. Видно, что при фиксации мазков 96° метанолом эффективной по четкому различию цвета оказалась только предварительная окраска эритроцитов ами- дочерным. При фиксации мазков ацетоном столь же эффективна предварительная окраска эритроцитов любым из б использованных в этом примере красителей, С учетом высокой токсичности метанола и возможности более широкого выбора красителей для предварительной окраски эритроцитов при фиксации мазков ацетоном методом выбора при фиксации мазков является обработка их ацетоном. Преимуществом такой фиксации является одинаковая для большинства подобранных красителей окраска в мазке предварительно окрашенного эритроцитарного реагента.
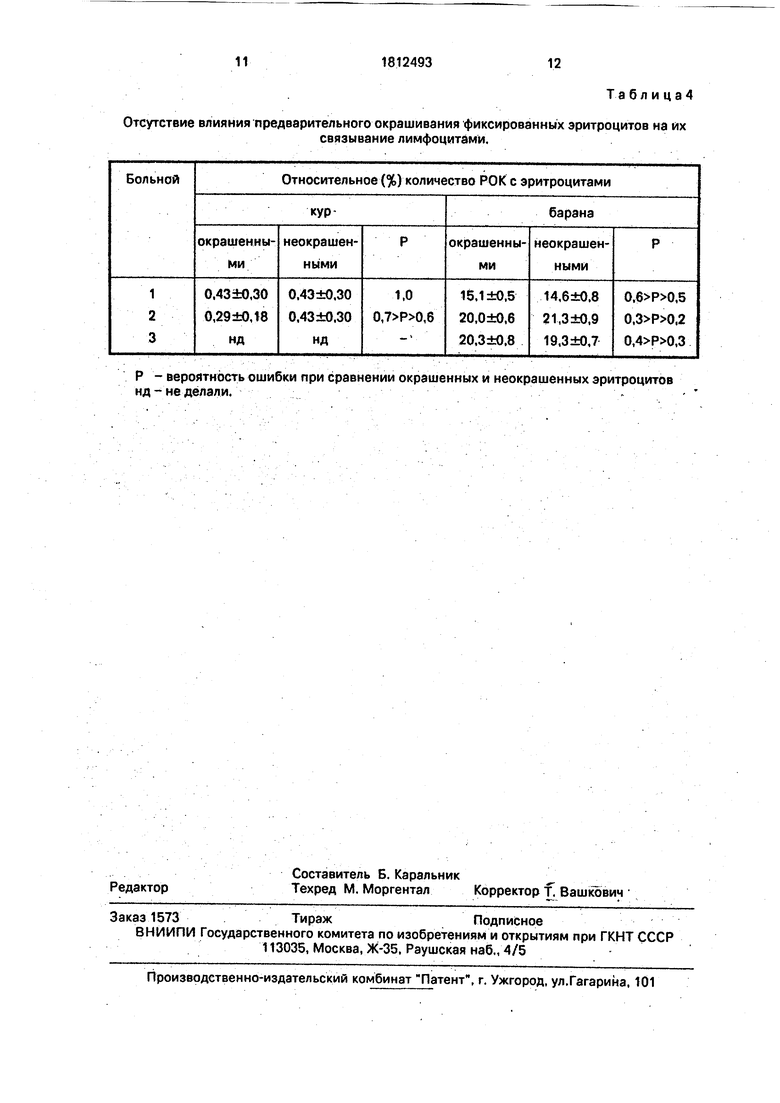
П р и м е р 5. Проверка специфичности адгезии окрашенных эритроцитов. Важно проверить, влияет ли предварительная окраска фиксированных ацетальдегидом эритроцитов на их адгезионную способность в розеткообразовании. Проверку осуществляли, используя фиксированные ацетальдегидом эритроциты кур, практически лишенные адгезивных свойств, и такие же эритроциты барана, активно участвующие в спонтанном розеткообразовании. При исследовании мононуклеаров больных оценивали влияние предварительного окрашивания этих эритроцитов кристаллвиоле- том на их связывание лимфоцитами (таб. 4). . Видно, что предварительная окраска фиксированных эритроцитов не изменила их адгезивных свойств (не увеличила и не
снизила). Следовательно, специфичность розеткообразования с окрашенными по предлагаемому способу эритроцитами сохраняется.
5П р и м е р б. Вы.бор длительности фиксации мазка ацетоном. Предлагаемый способ осуществляли как в примере 3, при использовании красителя кристаллвиолета и различной длительности фиксации мазков
0 ацетоном - 1, 3, 5 и 10 мин. Точность регистрации экспозиции при фиксации ±5-6 с. Получены следующие результаты. Фиксация мазков в течение 1-3 мин не обеспечивает четкой цветовой дифференциации
5 неокрашенных и предварительно окрашенных эритроцитов. Фиксация мазков в течение 10 мин приводит к разрушению некоторых мононуклеаров.
Следовательно, оптимальной длитель0 ностью фиксации мазков является 5 мин, а с учетом точности регистрации экспозиции 5,0 ±0.1 мин.
Таким образом, разработан способ идентификации субпопуляций лимфоцитов
5 смешанным розеткообразованием с эрит- роцитарными реагентами, позволяющий использовать эритроциты, не различающиеся морфологически. Способ может быть использован для идентификации лимфоци0 тов по наличию двух различных маркеров, например, по рецептору к эритроцитам барана и Fc фрагменту IgG, или по антигенсвязывающему рецептору и рецептору к эритроцитам барана и т.п. Кро5 метбго, поскольку учет розеткообразования. выполняется в мазке, а предлагаемый способ позволяет четко дифференцировать лимфоциты и моноциты по морфологии, предлагаемый способ обеспечивает диффе0 ренциацию различных розеткообразующих мононуклеаров.
Ф о р м у л а и з о б р ете н и я Способ идентификации субпопуляций лимфоцитов путем проведения реакции ро5 зеткообразования с окрашенными и неокрашенными эритроцитами барана с последующим микроскопическим исследо- . ванием полученных препаратов, отличающийся тем, что, с целью повышения
0 точности способа, окраску эритроцитов осуществляют 0,1 %-ным раствором или ализаринового желтого, или амидочерного, или хризоидина. или эозина натрия, или эритро- зина, или кристаллвиолета, а микроскопиче5 ское исследование проводят на мазке, фиксированным в ацетоне в течение 4,9-5,1 мин при 15-25°С.
Возможности предлагаемого и известного способов.
Выбор красителя.
Краситель для эрйтроцитарного реагента
Ализариновый красный Ализариновый желтыйх
Сафранин
Метиловый красный Нейтральный красный
Пиронин
ислотный хромтемнокислый
Резазурин
Иодэозин
Аурофосфин
Амидочерный
Хризоидин
Эозин натрия.
Эритрозин
Родамин Кристаллвиолет
х - пригодные для предлагаемого способа красители
Таблица 1
Таблица 2
Цвет эритроцитов-в фиксированном и окрашенном
мазке
предварительно окрашенных
предварительно не окрашенных
Красный Тот же
-
«
1 - предварительно окрашенные эритроциты
2 - эритроциты без предварительной окраски
Выбор способа фиксации
Та бл и ц а 4
Отсутствие влияния предварительного окрашивания фиксированных эритроцитов на их
связывание лимфоцитами.
Р - вероятность ошибки при сравнении окрашенных и неокрашенных эритроцитов нд-не делали.
| Цой И.Г | |||
| и др | |||
| Стабилизированный диагностикум для идентификации Т-суп- рессоров методом комбинированного ро- зеткообразования | |||
| Лабораторное дело, 1987, № 12, с | |||
| Автоматическое устройство для укладывания досок с торфинами, поступающими с торфяного пресса на канатный транспортер | 1923 |
|
SU919A1 |
Авторы
Даты
1993-04-30—Публикация
1991-01-11—Подача