Изобретение относится к новому производному пиперидона-4, а именно к 1-(3-бутоксипропил)-4-оксопиперидину формулы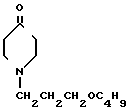 являющемуся промежуточным соединением в синтезе гидрохлорида 1-(3-бутоксипропил)-4-фенил-4-пропионилоксипиперидина, обладающего анальгетической активностью.
являющемуся промежуточным соединением в синтезе гидрохлорида 1-(3-бутоксипропил)-4-фенил-4-пропионилоксипиперидина, обладающего анальгетической активностью.
Целью изобретения является поиск новых соединений в ряду производных пиперидина, являющихся промежуточными соединениями для синтеза веществ, обладающих более высокой анальгетической активностью, чем структурный аналог.
П р и м е р 1. 1-(3-Бутоксипропил)-4-оксопиперидин (1).
Смесь 176,9 г (150 мл, 1,143 моль) 3-бутоксипропиламина и 197,2 г (206,5 мл, 2,29 моль) метилакрилата в 250 мл метанола перемешивают при 65-70оС в течение 3,5 ч, упаривают растворитель, остаток перегоняют в вакууме. Получают 302,1 (87,1% от теоретического) 3-бутоксипропил-бис-(метоксикарбонилэтил) амина (диэфир) с т.кип. 176-178оС/4 мм рт.ст. nD20 1,4446.
В трехгорлую круглодонную колбу, снабженную мешалкой, термометром и капельной воронкой, помещают 230 мл метанола и при постоянном перемешивании добавляют порциями 28,92 г (1,26 моль) мелко нарезанного металлического натрия. После полного растворения натрия к раствору добавляют 337 мл толуола и доводят температуру до 70-80оС. Затем прикапывают 302,1 г (0,995 моль) диэфира со скоростью отгонки азеотропной смеси толуола с метанолом. Аэеотроп отгоняют до тех пор, пока температура смеси не достигнет 90-95оС. Затем прекращают отгонку, смесь нагревают еще в течение 30 мин. К охлажденному раствору приливают 300 мл соляной кислоты (1:1) и 200 мл концентрированной соляной кислоты. Разделяют слои, водный слой представляют собой солянокислый раствор гидрохлорида 1-(3-бутоксипропил)-3-карбометокси-4-оксопиперидина. Последний подвергают омылению и декарбоксилированию кипячением раствора в течение 2,5 ч до полного отсутствия окрашенной реакции на 3%-ный раствор хлорного железа. После окончания реакции охлажденный раствор подщелачивают насыщенным раствором NaOH до рН 9-10. Продукт экстрагируют бензолом. Упаривают бензол, остаток перегоняют в вакууме и получают 123,7 г (58,2% от теоретического) 1-(3-бутоксипропил)-4-оксопиперидина (1) с т.кип.99-101оС/ мм рт.ст. nD20 1,4630.
Найдено, C 67,54; H 10,82; N 6,73.
C12H23NO3.
Вычислено, C 67,57; H 10,87; N 6,57.
ИК-спектр, ν, см-1 (раствор в ССl4, 10-1 моль/л): 1120, 1203 (С-О), 1735 (С О).
П р и м е р 2. Гидрохлорид 1-(3-бутоксипропил)-4-фенил-4-пропионилоксипипе- ридина.
В трехгорлую круглодонную колбу помещают 1,26 г (0,18 моль) мелко нарезанного металлического лития в 150 мл абсолютного эфира, при постоянном перемешивании в токе аргона добавляют по каплям 7,8 мл (0,075 моль) бромбензола в 100 мл абсолютного эфира. При этом наблюдается разогревание. Смесь перемешивают в токе аргона 1 ч при комнатной температуре и 1 ч при 35-40oС. Затем к охлажденному раствору прикапывают 10,7 г (0,05 моль) 1-(3-бутоксипропил)-4-оксопиперидина (1) в 50 мл эфира, перемешивают 1 ч при комнатной температуре и 1 ч при 35-40оС. Раствор охлаждают и прикапывают 5,2 мл (0,06 моль) хлористого пропионила в 50 мл эфира. К реакционной смеси добавляют 50 мл воды, подкисляют HСl до рН 3-4, при этом наблюдается образование осадка. Осадок отфильтровывают, растворяют в воде и подще- лачивают раствором NaOH до рН 9-10 и продукт многократно экстрагируют бензолом. Бензольный экстракт сушат MgSO4. Осушитель отфильтровывают, частично упаривают растворитель к оставшемуся раствору добавляют 10,4 мл (0,12 моль) хлористого пропионила и смесь выдерживают в течение 2,5 ч при 50-60оС. Выпавший осадок отфильтровывают из изопропанола. Получают 13,63 г (71% от теоретического) гидрохлорида 1-(3-бутоксипропил)-4-фенил-4-пропионилоксипиперидина с т.пл.159-161оС.
Найдено, C 65,83; H 8,32; Cl 9,25.
C21H34NO3Cl
Вычислено, C 65,69; H 8,93; Cl 9,23.
ИК-спектр (в таблетке с KCl) ν, см-1: 1110, 1140, 1200 (С-О), 1750 (С=0 сл.эфирн.).
П р и м е р 3. Исследование фармакологической активности.
Гидрохлорид 1-(3-бутоксипропил)-4-фенил-4-пропионилоксипиперидина под шифром АВ-101 испытан на анальгетическую активность.
В опытах на белых мышах при внутрибрюшинном введении определяли приблизительную острую токсичность и с дозы 1/5 от ЛД50 исследовали влияние АВ-101 на порог болевой чувствительности при электрическом раздражении хвоста мыши.
Подробное исследование токсических и анальгетических свойств АВ-101 проводили в сравнении с промедолом в опытах на крысах при подкожном введении. Болевое раздражение наносили крысам путем дозированного сжатия кончика хвоста (механическое раздражение. Сангайло А.К. 1958 г). Подсчитывали эффективные дозы (ЭД50) и индекс широты фармакологического действия (ЛД50/ЭД50). Оценивали два параметра анальгезии: "достаточная" (повышение порога 2 в раза и более) и "полная" анальгезия (отсутствие реакции на боль при сдавливании хвоста 100 мм рт.ст.).
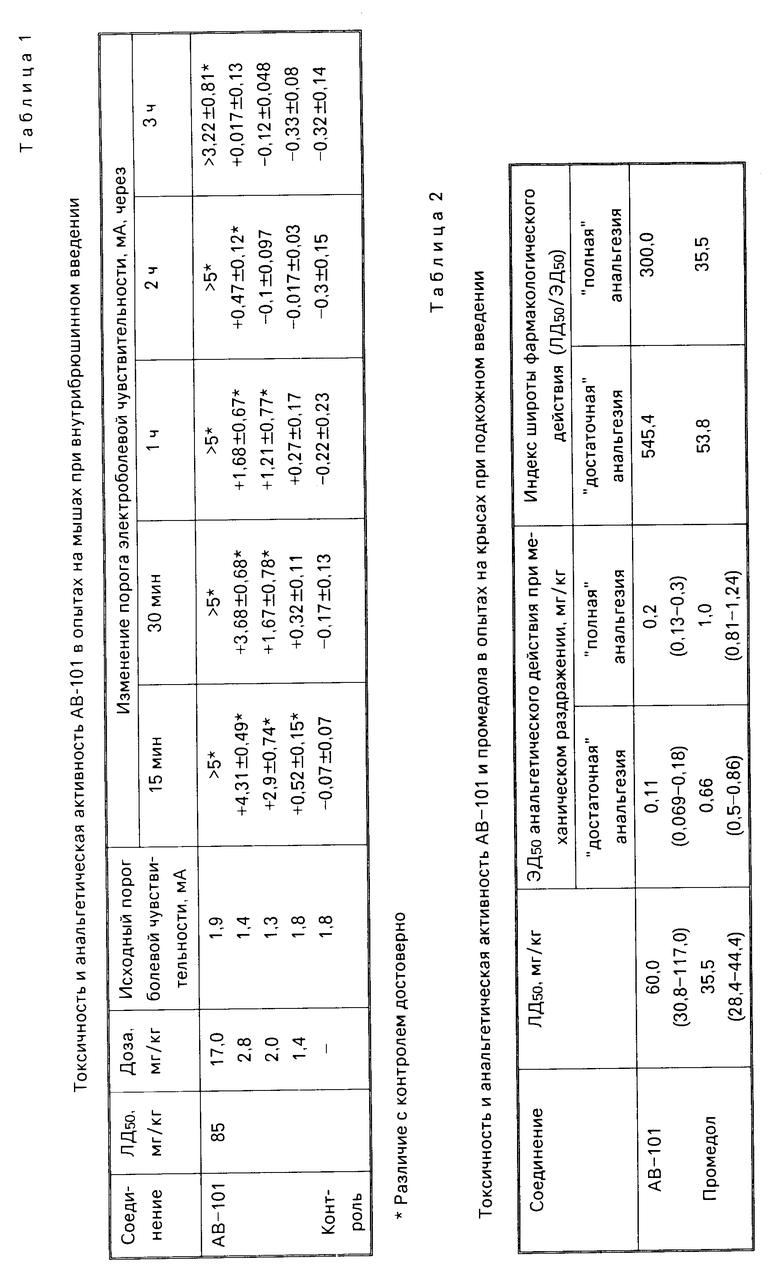
Полученные экспериментальные данные свидетельствуют о том, что в опытах на мышах АВ-101 сохраняет отчетливое обезболивающее действие при снижении дозы до 1/60 от ЛД50 (табл.1).
Сравнение токсических и анальгетических свойств соединения АВ-101 и промедола в опытах на крысах показало, что острая суточная токсичность АВ-101 меньше, чем у промедола, а по обезболивающему действию АВ-101 значительно активнее промедола (cм. табл. 2). Так, по "достаточной" анальгезии АВ-101 превосходит промедол в 6 раз, а по "полной" анальгезии в 5 раз. Широта фармакологического действия АВ-101 в 8-10 раз больше, чем промедола.
Таким образом, соединение 1 является промежуточным соединением для синтеза гидрохлорида 1-(3-бутоксипропил)-4-фенил-4-пропионилоксипиперидина, обладающего более высокой анальгетической активностью, чем промедол, при меньшей токсичности. АВ-101 может найти применение в медицине в качестве обезболивающего средства.
Использование: в качестве промежуточного соединения в синтезе гидрохлорида 1-(3-бутоксипропил)-4-фенил-4-пропионилоксипиперидина, обладающего анальгетической активностью. Сущность изобретения: продукт - 1-(3-бутоксипропил)-4-оксипиперидин. Реагент 1: 3-бутоксипропил-бис-(2-метоксикарбонилэтил)амин. Реагент 2: мотилат натрия. Условия реакции: циклизация в толуоле при 90 95°С. 2 табл.
1-(3-Бутоксипропил)-4-оксопиперидин формулы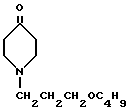
в качестве промежуточного соединения в синтезе гидрохлорида 1-(3-бутоксипропил)-4-фенил-4-пропионилоксипипередина, обладающего анальгетической активностью.
| Машковский М.Д | |||
| Лекарственные средства | |||
| М.: Медицина, 1986, т.1, с.173. |
Авторы
Даты
1995-07-09—Публикация
1991-01-28—Подача