Изобретение относится к биотехнологии, касается способа получения биологиче: ски активных веществ, например, ферментов, таких как щелочная фосфатаза, экстрагированных из ракообразных( arthropodes), особенно из креветок.
Преимущество способа, согласно данному изобретению, состоит в том, что биоактивные соединения можно выделить из исходного сырья, т.е. из ракообразных посредством обычной экстракции водой так, что биоактивные соединения присутствуют в растворенном состоянии, это означает, что компоненты могут быть выделены путем концентрирования, экстракции и фильтрации для удаления примесей.
Другое преимущество способа, согласно настоящему изобретению состоит в возможности работать с весьма незначительной потерей активности биоактивных компонентов, приводящей в результате к возможности выделения из рассола
основного количества биоактивных компонентов.
Дальнейшее преимущество упомянутого изобретения-заключается в возможности экстракции ценных в коммерческом отношении продуктов из продуктов, являющихся отходами, которые иначе требовали бы обработки для устранения загрязнения окружающей среды.
Дополнительное преимущество состоит в сохранении питательной ценности ракообразных.
Соответственно изобретению ценные вещества выделяют из свежего или консервированного сырья, состоящего из ракообразных, преимущественно из креветок, а такжеиз их частей продуктов, с применением воды.
Экстрагированный рассол обрабатывают соответственно данному изобретению в независимом порядке с применением одной или нескольких следующих стадий одЁ
00
со
00
fe
ON
CJ
некратно или многократно: очистка, кон- центрирование, экстракция и/или удаление желательных веществ, далее выделение и возможная стандартизация и стабилизация очищенных биоактивных веществ.
Консервированный исходный материал может быть доступным или в замороженном состояний (в блоках или в индивидуальном виде), химически консервированным, например, в рассоле, консервированным посредством ферментации, силосования, сушки, облучения или добавления консервирующих средств.
Экстракцию соответственно изобретению можно осуществлять при использовании растворителя на основе воды, особенно чистой или очищенной воды при температуре в пределах 0-100°С,.и рН в пределах 1-14 в зависимости от выделяемого продукта.. Наиболее благоприятные температура и рН составляет, соответственно 15°С и рН 8,1.
Операции по очистке включают прежде всего предварительное, грубое фильтрование первичного экстрагированного рассола для удаления нерастворимого материала в виде частиц, например, путем фильтрования или центрифугирования для получения неочищенного экстракта, далее происходят тонкую очистку биологически активных компонентов с применением хро- матографических методов, таких как ионообменная хроматография, афинная хроматография, гельфильтрация, или же подобные им. Выбор метода должен зависеть от конкретных биологических и физико-химических признаков индивидуальных макромолекул.
Коллоидный материал можно удалить из исходного сырья посредством добавления средства, способствующего фильтрова- нию, такого как поликатионы или полианионы на основе полиакриламида, также путем экстракции и/или фильтрования при образовании окончательного экстракта.
Стадии способа согласно изобретению включают концентрирование неочищенного экстракта и окончательного экстракта, которое может быть осуществлено, например, мембранным фильтрованием (поперечное фильтрование) или концентрированием при пониженном давлении. Полезно повторять операции концентрирования несколько раз во время процесса выделения и концентрировать вещества в 1-50 раз на каждой стадии.
Для получения стандартизованных биоактивных продуктов желаемой концентрации и активности, окончательный экстракт можно, например, обработать посредством
диафильтрации/ультрафильтрации и, в случае необходимости, провести дополнительную операцию хромэтографирования.
Окончательный продукт может быть доступен в твердом или жидком виде. Стабилизацию очищенногожидкого биоактивного продукта можно осуществлять посредством замораживания или добавления, например, солей, кислот и/или основания (для установ0 ления рН) или других обычно применяемых стабилизаторов. Продукт можно превратить в твердое состояние посредством обычно используемых процессов высушивания таких, например, как высушка вымораживани5. ем.
Для изготовления продукта с желаемой активностью на 1 г вещества обычно добавляют пригодный для применения материал, служащий разбавителем или носителем.
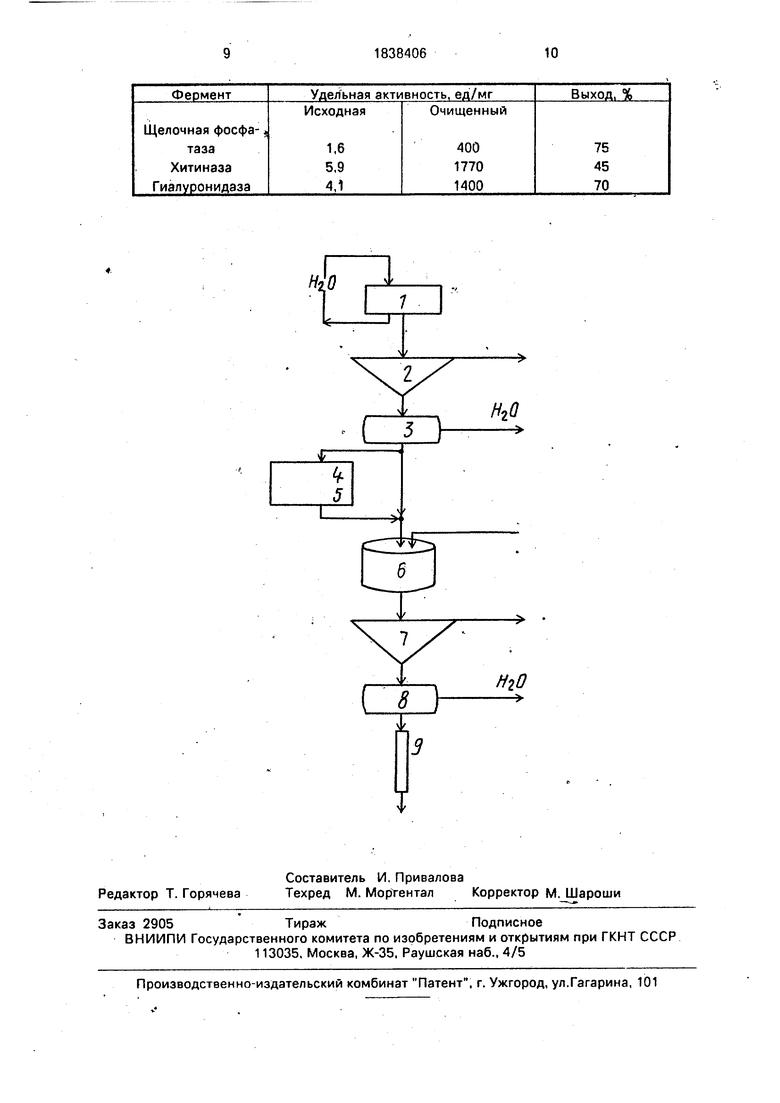
0 Предлагаемый способ поясняется чертежом. Блок замороженных свежих креветок экстрагируют (1) по меньшей мере 8 ч водой (рН 8,1, температура 15°С). Полученный экстракт обрабатывают путем грубого
5 фильтрования (2), например, на вращающемся сите с отверстием 0,5 мм. Экстракт концентрируют (3) В 10 раз в,Јистеме поперечного (cross-flow) фильтрования. Если необходимо или желательно, экстракт может
0 быть заморожен или высушен с помощью замораживания для промежуточного хранения (4).
Если экстракт замораживают, то перед дальнейшей обработкой его следует размо5 розить или растворить, установить требуемую температуру (5). Материал в виде частиц осаждают в резервуаре (6) посредством добавления флокулирующего средства, например, пликатиона на основе полиакри0 ламида при концентрации 0,1 г/л экстракта. Далее материал фильтруют (7) на фильтр- прессе. Осветленный фильтрат концентрируют (8) в 10.раз в поперечной системе фильтрования. Фермент связывают с 10 л
5 Q-сефарозы в колонке (9), имеющей площадь поверхности 500 см , при скорости 8 л/ч. Колонку уравновешивают трис-HCI буфером (рН 7,2:1 мМ хлорида магния). Целевые ферменты элюируют из колонки
0 трис-HCI буфером с добавлением 0,1-0,5 моля хлорида натрия.
П р и м е р 1. Щелочная фосфатаза из креветок (Pandalus borealis) 12 т креветок экстрагируют 2500 л воды 8 ч при рН 8,1 и
5 температуре 15°С. Общее содержание протеина в экстракте составило около 2,5 мг протеина/мл. Уровень щелочной фосфата- зы в данном экстракте составил приблизительно 2,5 единицы на 1 мг протеина. Метод измерения соответствует стандартному методу, при котором измеряют скорость гидролиза n-нитрофенилфосфата в диэтанола- миновом буфере при 37°С. Экстракт подвергают грубому фильтрованию с применением вращающегося сита. (Ротосито) с отверстиями 0,5 мм.
Фильтрат концентрируют & 10 раз посредством ультрафильтрации в системе с поперечной фильтрацией, представляющей собой блок из полых полисульфоновых волокон, с пропусканием молекул до 10000 дальтон. Такая концентрация достигается без существенной утрать) активности (менее 10%). Объем после упомянутого концен- трирования составил около 250 л.
Коллоидные частицы удаляют из концентрированного экстракта путем прямой фильтрации после добавления поликатиона на основе полиакриламида. Применяют около 0,1 г поликатиона на 1 л экстракта. После флокуллирования и фильтрации фло- кул.пированных частиц с применением рамного фильтра, окончательный экстракт дополнительно концентрируют. Второе концентрирование производят в 10 раз в системе поперечной фильтрации, состоящей из блока полых полисульфоновых волокон с пропусканием молекул до 10000 дальтон. Объем после этого последнего кон- центрирования составляет приблизительно 20л,
Щелочную фосфатазу связывают с 10 л Q-сефарозы (непрерывный поток) в колонке с площадью поверхности приблизительно 500 см , со скоростью 8 л/ч, Колонку уравновешивают трис-HCI буфером (при рН 7,2, 1 мМ хлорида магния). Нежелательные протеины элюируют трис-HCI буфером (рН 7,2, 1 мМ хлорида магния), Нежелательные протеины элюируют трис-HCI буфером (рН 7,2, 1 мМ хлорида магния), к которому добавлено 0,25 мл хлорида натрия. Щелочную фосфатазу элюируют упомянутым буфером, к которому добавлено 0,4 моля хлорида натрия. Элюат, содержащий щелочную фосфатазу, концентрируют до требуемой целевой концентрации и после этого диафильтруют с использованием 0,03-молярного триэта- ноламиннового буфера (рН 7,6, 3-моля хлорида натрия, 0,001 моля хлорида цинка).
П р и м е р 2. Гиалуронидаза из креве- JOK (Pandalus borealis) 12 т креветок экстрагируют 2500 л воды 8 часов при рН 8,1 и температуре 15°С. Общее содержание протеина в данном экстракте составляет приблизительно 2,5 мг/мл. Уровень гиалуронидазы измеряют по сокращению мутности при инкубировании с гиалуроно- вой кислотой и добавлении альбумина. Экстракт подвергают грубому фильтрованию
на вращающемся сите с отверстиями д уа- метром 0,5 мм, фильтрат концентрируют приблизительно в 10 раз посредством ультрафильтрации в системе с поперечной филь- 5 трацией, состоящей из блока полых полисульфоновых волокон с пропусканием молекул до 10000 дальтон. После этой стадии концентрации не происходит существенного снижения активности.
0 Окончательный объем продукта на данной стадии равен 250 л.
Коллоидальные частицы удаляют из концентрированного экстракта путем прямой фильтрации после добавления поликэ5 тиона на основе полиакриламида. Применяют приблизительно 0,1 г фильтрующего средства на 1 л экстракта. После фло- кулирования и удаления частиц на фильтр-прессе, фильтрат концентрируют
0 еще в 10 раз в системе поперечной фильтрации, состоящей из блока полисульфоновых полых волокон с пропусканием молекул до 10000 дальтон. Окончательный объем после упомянутого концентрирования составляет
5 приблизительного л,
Гиалуронидазу связывают приблизительно с 10 л G-сефарозы (непрерывный поток) в колонке с площадью поверхности 500 м , со скоростью 8 л/ч. Колонку уравнове0 шивают трис-HCI буфером (рН 7,2, 1.ммоль хлорида магния). Гуалоуродиназу элюируют трис-HCI буфером (рН 7,2, 1 ммоль хлорида магния), к которому добавлено 0,25 моля хлорида натрия.
5 Элюат, содержащий гуалоруонидазу, доводят до требуемой окончательной концентрации, затем высушивают посредством вымораживания.
П р и м е р 3. Хитиназа из креветок
0 (Pandalus borealis).
12т креветок экстрагируют 2500 л воды при рН 8,1 и температуре 15°С. Общее содержание протеина в этом экстракте составляет приблизительно 2,5 мг протеина в
5 1 мл. Уровень хитиназы в данном экстракте равен приблизительно 6-8 единицам/мг протеина. Хитиназу измеряют как свободный N-ацетил-глюкозамин после разложения коллоидного хитина хитиназой и
0 N-ацетил-глюкозаминидазой,
Экстракт подвергают грубому фильтрованию на вращающемся сите с отверстиями 0,5 мм. Фильтрат концентрируют приблизительно в 10 раз путем ультрафиль5 трования с блока из полых полисульфоновых волокон с пропусканием молекул до 10000 дальтон. Потеря активности этой стадии фильтрования невелика. Объем после упомянутого концентрирования составляет приблизительно 250 л.
Коллоидные частицы удаляют из концентрированного экстракта путем прямой фильтрации после добавления поликатиона на основе полиэкриламида.
На 1 л экстракта берут 0,1 г вспомогательного вещества, способствующего фильтрованию, После флокуллиропания и удаления частиц на фильтр-прессе, фильтрат концентрируют еще в 10 раз в системе поперечного фильтрования из полых пол- исульфоновых волокон с пропусканием молекул до 100000 дальтон. Окончательный объем после упомянутого концентрирова- ния составляет приблизительно 20 л.
Хитиназу связывают с 10 л Q-сефарозы (быстрый поток) в колонке с площадью поверхности 500 м2 со скоростью 8 л/ч. Колонку уравновешивают трис-НС буфером (рН 7,2,1 ммоль хлорида магния). Хитиназу элю- ируют трис-HCI буфером (рН 7,1, 1 ммоль хлорида магния) с использованием солевого градиента в пределах от 0,1 до 0,5 моля хлорида натрия. Элюат, содержащий хити- назу, концентрируют до требуемой окончательной концентрации, затем высушивают вымораживанием.
В следующей таблице заявитель приводит данные удельной активности первоначально и после выделения из колонки с Q-сефарозой ферментов согласно примерам. Выход приведен в процентах содержания фермента в исходном водном материале.
После нескольких повторов стадий фильтрации, концентрирования и очистки удельная активность щелочной фосфатазы в конечном счете доводится до 2200 ед/мг.
Как следует из изложенного выше, удельная активность, достигнутая для щелочной фосфатазы, является высокой, что указывает на получение очень чистого продукта. Хитиназа экстрагируется с колонки с Q-сефарозой при градиенте концентраций от 0,1 до 0.,5 М NaCI, в то время, как щелочная фосфатаза и гиалуронидаза выходят при 0,4 М и 0,25 М NaCI соответственно.
Следовательно, хитиназа выявляется в обеих фракциях, содержащих гиалуронида- зу и щелочную фосфатазу, но главная фракция хитиназы выделяется выше 0,4 М NaCI. Это, естественно, является объяснением довольно низкому выходу (в %) хитиназы в указанной таблице по сравнению с другими
ферментами. Фракции, собранные для гиа- луронидазы и щелочной фосфатазы, содержат хитиназу, но их дополнительно очищают с помощью афинной хроматогра- фии, благодаря чему достигается разделение разных ферментов.
Таким образом, получают высокочистые ферментные продукты.
Фор мула изобретения
1. Способ получения биологически активных компонентов, преимущественно ферментов, предусматривающий извлечение целевого продукта из ракообразных
(Crustacea, phylum Arthropodes) и его очистку с использованием ионообменной хрома- тографии, отличающийся тем, что извлечение целевого продукта осуществляют путем экстрагирования целых ракообразных и/или целых их частей водой при температуре в пределах 1-35°С, предпочтительнее в пределах 10-25°С, в течение 1-12 ч, предпочтительно, 8ч, и в дополнение к ионообменному хроматографированию
эккстракт очищают фильтрованием, центрифугированием или хроматографией, кон- центрированием и/или удалением нежелательных веществ, выделением, стандартизацией и стабилизацией концентрированных биоактивных компонентов.
2. Способ по п. 1, о т л и ч а ю щ и и с я тем, что экстрагируют креветки, особенно блок свежезамороженных креветок посредством их размораживания водой.
3. Способ по п. 1, о т л и ч а ю щ и и с я тем, что очистку экстракта проводят путем грубой фильтрации на вращающемся сите с отверстиями 0,5 мм с последующим концен- трированием в 1-20 раз, предпочтительно в
10 раз, в поперечно-продольной фильтровальной системе, добавлением в концентрат поликатиона на основе полиакриламида в концентрации 0,05-0,15 г/л экстракта, предпочтительно 0,1 г/л, фильтрованием на
5 фильтр-прессе, концентрированием в 1-50 раз, предпочтительно в 10 раз, в поперечно- продольной системе и ионообменной хроматографией на колонке.
0 4. Способ поп, 1,отличающийся тем, что перед очисткой экстракт хранят в замороженном илилиофильно высушенном состоянии.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выделения ДНК-полимеразы TRU из биомассы бактерий микроорганизма JнеRмUS RUвеR ВКМ 1258 | 1988 |
|
SU1701112A3 |
| Способ получения простатической кислой фосфатазы | 1990 |
|
SU1747488A1 |
| СПОСОБ ОЧИСТКИ ТРОМБИНОПОДОБНОЙ ПРОТЕАЗЫ ИЗ ЗМЕИНОГО ЯДА | 1997 |
|
RU2186849C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТАТИВНОГО КОМПЛЕКСНОГО ПРЕПАРАТА, ОБЛАДАЮЩЕГО КОЛЛАГЕНАЗНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2412997C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЛАЦЕНТАРНОГО ПРОТЕИНА | 1991 |
|
RU2007420C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЛАЦЕНТАРНОГО ПРОТЕИНА | 1991 |
|
RU2007418C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЛАЦЕНТАРНОГО ПРОТЕИНА | 1991 |
|
RU2007419C1 |
| Способ получения гибридного полипептида, содержащего НВ @ А @ | 1988 |
|
SU1746887A3 |
| Способ получения щелочной фосфатазы | 1988 |
|
SU1576563A1 |
| СТАБИЛИЗАТОР ДЛЯ ГИАЛУРОНИДАЗЫ И ЖИДКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ГИАЛУРОНИДАЗУ | 2013 |
|
RU2647835C2 |
Использование: биотехнология, может быть использовано в биохимии и клинической химии. Сущность изобретения: осуществляют выделение щелочной фосфатазы, гиалуронидазы и хитиназы из ракообразных, преимущественно креветок, путем экстракции целых ракообразных и/или целых их частей водой при 1-35°С в течение 1-12 ч, обработкой полученного экстракта центрифугированием или фильтрацией, очисткой, экстракцией и удалением нежелательных веществ. 3 з.п. ф-лы, 1 ил.

| Сотр | |||
| Biochem, Physlol | |||
| v | |||
| Капельная масленка с постоянным уровнем масла | 0 |
|
SU80A1 |
| Physio, Lool | |||
| v | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| Gates B.I | |||
| and Trevis (.Purification and characterization of Carboxypeptidases A and В from the White Shrimp Penques Setiferus Biochemistry, 1973, 1, Nk 10, p | |||
| Ролик для электрической проводки | 1924 |
|
SU1867A1 |
Авторы
Даты
1993-08-30—Публикация
1989-10-23—Подача