Известен способ получения бифункциональных силоксаноБЫх олигомеров линейного строения, имеющих на концах гидроксильные груниы, нутем взаимодействия циклических органосилоксанов с минеральными кислотами при нагревании.
Предложенный способ заключается в том, что раскрытие циклов в органоциклосилоксанах идет в результате взаимодействия их с ангидридами карбоновых или перфторкарбоновых кислот. Это дает возможность получить бифункциональные силоксановые олигомеры линейного строения с активными концевыми ацилокси (перфторацилокси) группами.
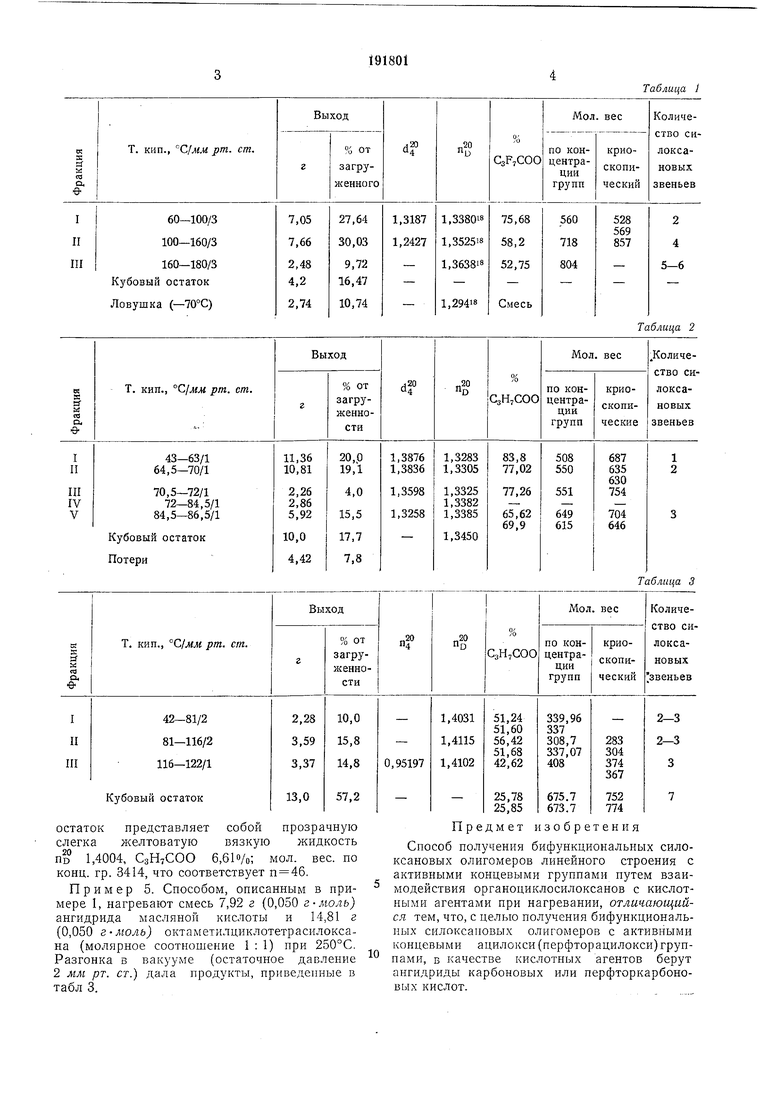
Пример 1. Смесь 14,84 г (0,036 г-моль) ангидрида гептафтормасляной кислоты и 10,66 г (0,036 г-моль) октаметилциклотетрасилоксана (молярное соотношение 1:1) нагревают в запаянной стеклянной ампуле емкостью 100 мл при 230°С в течение 24 час. Фракции, полученные в результате разгонки смеси продуктов реакции в вакууме, приведены в табл. 1.
Пример 2. В условиях, описанных в примере I, нагревают 3,12 г (0,0076 г-моль) ангидрида геитафтормасляной кислоты и 19,88 г (0,067 г-моль) октаметилциклотетрасилоксана (молярное соотношение 1:9). При попытке расфракционировать реакционную смесь в вакууме (2 мм рт. ст.) ири темиературе бани
250°С отогнан 0,91 г (4,75о/о загруженного) непрореагировавшего октаметилциклотетрасилоксана (по 1,3960; мол. вес криоск. 285,2). Кубовый остаток 20,3 г. Прозрачная желтоватая вязкая жидкость, по 1,4004; мол вес. по конц. гр. 3840, что соответствует п 46.
Пример 3. В условиях, описанных в примере I, нагревают 0,62 г (0,00151 г моль) ангидрида гептафтормасляной кислоты и 22,20 г (0,07485 г моль) октаметилциклотетрасилоксана (молярное соотношение 1 : 50). После отгонки в описанных в примере 2 условиях
1ос .. 20
1,85 3 октаметилциклотетрасилоксана (по 1,3969; мол. вес. криоск. 295,6), кубовый остаток 16,13 г - малоподвижная прозрачная желтоватая жидкость. По 1,4051; мол. вес. по концентрации групп 19700, что соответствует п 260. Полученные фракции прпведены в табл. 2.
Пример 4. В условиях, описанных в примере 1, нагревают смесь 1,48 г (0,07 г-моль) ангидрида трифторуксусной кислоты и 20,73 г (0,07 г-.ноль) октаметилциклотетрасилоксана (молярное соотношение 1 : 10) при 210°С. После отгонки при остаточном давлении
Таблица 2
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЭПОКСИДНЫХ БЛОК-ОЛИГОМЁТШ" | 1972 |
|
SU328134A1 |
| Способ получения ацилоксисилоксановых олигомеров | 1976 |
|
SU763377A1 |
| ПРОИЗВОДНОЕ АЛКЕНИЛСУКЦИНИМИДА КАК ДИСПЕРГИРУЮЩАЯ ПРИСАДКА К КОМПОЗИЦИОННЫМ СМАЗОЧНЫМ МАСЛАМ, СУКЦИНИРОВАННЫЙ ОЛИГОМЕР ПРОПИЛЕНА КАК ПРОМЕЖУТОЧНЫЙ ПРОДУКТ ДЛЯ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО АЛКЕНИЛСУКЦИНИМИДА И СМАЗОЧНАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2042665C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННОЙ ФЕНОЛФОРМАЛЬДЕГИДНОЙ РЕЗОЛЬНОЙ СМОЛЫ | 1973 |
|
SU376403A1 |
| Способ получения гидрохлорида сложного метилового эфира @ -L-аспартил-L-фенилаланина | 1990 |
|
SU1834892A3 |
| Способ получения хлорсодержащих органосилоксанов | 1972 |
|
SU455600A1 |
| Способ получения олигомеров пиперилена | 1973 |
|
SU449070A1 |
| СПОСОБ ПОЛУЧЕНИЯ СИЛОКСАНОВЫХ ОЛИГОМЕРОВ | 1968 |
|
SU220502A1 |
| Способ получения хлорсилоксановых олигомеров | 1977 |
|
SU696034A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-БУТИЛ-1-ОЛОВ | 1971 |
|
SU422134A3 |

Таблица 3
Даты
1967-01-01—Публикация