Изобретение относится к области -получения веществ, обладающих фунгииидными свойствами.
3-Фенилкарбамоил-1,3,4-оксадиазоло;;ы-2 - эффективное средство против паразитов, вызывающих поражение листьев яблони, картофеля и табака.
Предложено получение З-фенилкарбамоил1,3,4-оксадиазолонов-2 общей формулы
N j-CONH-,
вЛ о
1де R-атом водорода или алкильнып, арильный, аралкильный, гетероциклический, циановый, алкилоксильный, алкилтиоловый, алкилоксиалкиль)1ый, алкилтиоалкильный, алкилоксикарбонильный, алкилкарбамоильный, алкансульфонильный, алкансульфонилалкильлый радикал, у которых алкильные радикалы и алкильные части других радикалов содержат от I до 6 атомов углерода, фенильиый радикал
или фенильный радикал, замещенный одним или нecкoльки rн радикалами из числа следующих: атомы галоида, алкильный, алкенильиый, алкило,ксильный, алкенилоксильный, алкилтиоловый, алкенилтиоловый, трифторметильный, циановый или диалкиламиновый радикал, где алкильные радикалы и алкильные части других радикалов имеют от 1 до 6 углеродных атомов, а алкеиильные ради-калы и алкенильные части других радикалов имеют от 2 до 6 атомов углерода.
Способ заключается в том, что изоцианат общей формулы
15
NCO
где/ у имеет вышеуказанное значение,
RI 1 одзергают взаимодействию с 1,3,4-оксадиазо25 ло;|ОМ -2 общей формулы
N-N
где R имеет вышеуказанное значение, в среде безводного-бензола в присутствии триэтиламииа.
Пример 1. К раствору 12,8г 5-пропил-1,3,4оксадиазолона-2 в 80 еж- безводного бензола добавляют 3 1капли метиламина, затем в течение 5 мин раствор 11, фенилизоцианата в 20 см безводного бензола. Температура повышается При этом до 32° С. Раствор нагревают в течение 2 час с обратным холодильником,затем охлаждают до 20° С. После удаления бензола нутем перегонки под вакуумом получают 24 г 3-фенилкарбамоил-5-прапил-,3,4-0(ксадиазолона-2. После иерекрнсталлизации из циклогексака т. нл. 97° С.
Исходный 5-нропил-1,3,4-оксадиазолон-2 (т. кип. ) получают но способу Дорнова и BpyHKCJia действием фосгена на бутирилтидразин.
Пример 2. Смесь 5 г 5-метил-1,3,4-оксадиазолона-2 и 8, г 4-диметиламинофенилизоцианата в 50 см безводного бензола нагревают в течение 2 час с обратным холодильником в присутствии 3 капель триэтиламина. Смесь охлаждают до 20° С; образующийся осадок отжимают, 1промывают бензолом и сушат. Таким нутем получают 12,5 г (4-диметиламинофенил)-3-карбамоил-5-метил-1,3,4 - оксадиазолона-2. После перекристаллизации из 1,2-дихлорэтана т. нл. 202° С.
Пример 3. К раствору 14,2 г 5-г/;ег-бутил1,3,4-оксадиазолона-2 в 80 см сухого бензола добавляют Б течение 5 мин раствор 14,9 г 4-метоксифенилизоцианата в 20 огз сухого бензола в присутствии 3 1Капель триэтиламина. Раствор леремешивают в течение 4 час при температуре окружающей среды, после чего растворитель отгоняют под вакуумом. Получают 30 г {4-метоксифенил)-3-карбамоил-5грег-бутил-1,3,4-оксадиазолона-2. После лере«ристаллизации из смеси цнклогексана и бензола т. .ил. 118° С.
Аналогично получают ряд соединений, поKa3a;;iujx а таб,пице.
Т а б л и ц а


Предмет ;; з о 5 р е т е ini я
Способ получения 3-фе1П1Лкарбамоил-,3,4оксадиазолонов-2 общей формулы N-N-COiiH -С Н-4 О (килтиоловый, алкилоксиалкильиый, алкилтиоалкильный, алкилоксикарбонильный, алкилкарбамоильный, алкансульфоиильный, алкансульфонилалкильный радикал, у которых алкильные радикалы и алккльные част.и
других радикалов содержат от 1 6 атомов углерода, а
фенильный радикал или фенильный радикал, замещенный одним или несколькими радикалами из числа следующих: атомы галоида, алкильный, алкенильный, алкилоксильный, алкенилоксильный алкилтиоловый, алкенилтиолоаый,трифторметильный,
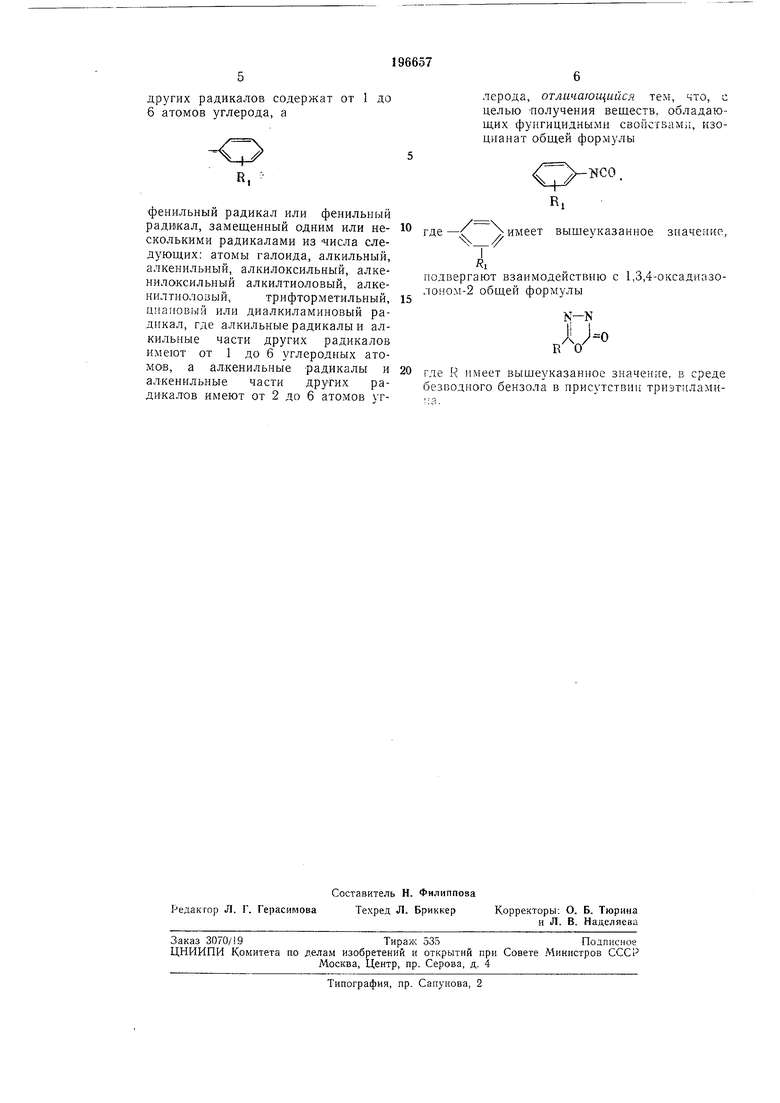
циагювый или диалкиламиновый радикал, где алкильные радикалы и алкильные части других радикалов имеют от 1 до 6 углеродных атомов, а ал,кенильные -радикалы и алкенильные части других радикалов имеют от 2 до 6 атомов углерода, отличающийся тем, что, с целью Получения веществ, обладающих фунгицидными свойствам, изоцианат общей формулы
КСО
RI
где-( /имеет выщеуказанное значение,
Y
подвергают взаимодействию с 1,3,4-оксадиазолоном-2 общей формулы
N-N
nVгде К имеет выщеуказанное значение, в среде безводного бензола в присутствии триэтилами
Даты
1967-01-01—Публикация