Изобретение относится к области получения ртутноорганических соединений, которые могут представить интерес как биологически активные вещества.
Предложен способ получения ди- и тризамещенных ртутноорганических производных изоциануровой кислоты формулы
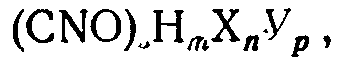
где X - заместитель азота PHg, в котором
R - одновалентный алкиловый, ариловый или алкилариловый радикал;
У - одновалентный радикал -SCCl3, -(СН2)x-СН2ОН, -СН2-СН=СН2, -(СН2)2-CN, - (CH2)3NH2 или - (СН2)2СООН;
x - число, максимально равное 3;
m - 0 или 1;
n - 1, 2 или 3;
p - 3 - m - n.
Способ заключается в том, что замещенную или незамещенную изоциануровую кислоту подвергают взаимодействию с ртутноорганическими галогенидами RHgHal в водной среде с примесью растворителя ртутноорганических галогенидов, смешивающегося с водой, или с ртутноорганическими гидроокисями в среде безводного органического растворителя, способного полностью или частично растворять оба компонента реакции. Реакцию проводят при температуре 50-100°С, рН среды поддерживают от 6 до 14.
Пример 1. В 550 см3 воды, содержащей 50 см3 диметилформамида, перемешивая, вводят 12,9 г циануровой кислоты и поднимают температуру до 90°С; рН реакционной смеси доводят до 9 и сохраняют его на этом уровне, вводя 30%-ный раствор гидроокиси натрия, одновременно и постоянно добавляя 79,5 г хлорида этилртути в течение 1 час.
В конце реакции массу, содержащую суспендированный продукт, охлаждают до 20°С, потом фильтруют ее и получают 81,2 г трисизоцианурата этиловой ртути. Выход 99,5%.
Результаты элементарного анализа следующие.
Вычислено, %: С 13,1; Н2 1,8; N2 5,3; Hg 73 8.
Найдено, %: С 13,2. Н2 1,9; N2 5,2; Hg 73,9.
Пример 2. Чтобы в промышленных масштабах получать продукт согласно примеру 1, в движущийся и нагретый до 75°С реакционный сосуд одновременно и беспрерывно подают 219 кг/час суспензии циануровой кислоты, содержащей 3% циануровой кислоты, в воде, 175,6 кг/час раствора, содержащего 40,6 кг хлорида этиловой ртути в 135 кг этанола и 20,83 кг/час 30%-ного раствора гидроокиси натрия, чтобы рН оставался около 9. Так как реакция длится приблизительно 30 мин, то подачу регулируют таким образом, чтобы время пребывания в аппарате составляло приблизительно 60 мин.
После фильтрования продукт сушат, перегоняют фильтрат для регенерирования растворителя, который подают опять в реакционный цикл, и выделяют остаточную, содержащую хлорид натрия, воду.
В этих условиях получение 1 т в день трисизоцианурата этиловой ртути требует общего расхода 158 г циануровой кислоты, 975 кг хлорида этиловой ртути и 150 кг гидроокиси натрия, причем в конце процесса регенерируют растворитель и возвращают его опять в реакционный цикл.
Пример 3. Поступая, как в примере 1, но с ограничением подачи хлорида этиловой ртути на 53 кг, после фильтрования получают 58,4 г бисизоцианурата этиловой ртути. Выход 99,7%.
Получаемый продукт практически чист, как видно из результатов элементарного анализа.
Вычислено, %: С 14,25; Н2 1,91; N2 7,18; Hg 68,5.
Найдено, %: С 14,3; Н2 1,87; N2 7,16; Hg 68,4.
Пример 4. Если при тех же самых условиях 58,6 г получаемого согласно примеру 3 продукта подвергают реакции с 31,3 г хлорида фениловой ртути, то получают 85,5 г изоцианурата 1,5-диэтилртуть-3-фенилртути.
Вычислено, %: С 18,1; Н 1,7; N 4,9; Hg 69,7.
Найдено, %: С 18,05; Н 1,6; N 4,9; Hg 69,5.
Пример 5. К 1000 мл водноспиртового раствора, который содержит 100 мл этанола на каждый литр, прибавляют 25,8 г циануровой кислоты и нагревают до 75°С. В эту среду постоянно подают 125,2 г хлорида фениловой ртути, причем рН путем автоматической подачи щелочного раствора поддерживают равным 9. После охлаждения и фильтрования получают 135,3 г практически чистого бисизоцианурата фениловой ртути. Выход продукта 99,2%.
Пример 6. Поступая, как в предыдущих примерах, из 12,9 г циануровой кислоты, суспендированной в смеси 500 см3 воды и 50 см3 диметилформамида, нагретой до 80°С, и 72,6 г хлорида нафтиловой ртути получают 71,9 г бисизоцианурата нафтиловой ртути (выход 99%).
Элементарный анализ продукта реакции дает следующие средние результаты.
Вычислено: %: С 35,1; Н2 1,85: N2 5,25; Hg 51,1.
Найдено, %: С 35,3; Н2 1,92; N2 5,36; Hg 51,2.
Пример 7. В раствор 12,9 г циануровой кислоты в 100 см3 диметилформамида, поддерживаемый при температуре 70±5°С, подают раствор 74 г гидроокиси этиловой ртути в 150 см3 этанола. Реакция продолжается 3 час и после охлаждения, фильтрования и сушки получают 79,8 г триеиаоцианурата этиловой ртути той же чистоты, что и продукта, описанного в примере 1. Выход 97%.
Пример 8. Если работают в условиях предыдущего примера и замещают гидроокись этилртути 88,5 г гидроокиси фенилртути, получают 92,5 г изоцианурата трифениловой ртути с выходом 96,5%.
Вычислено, %: С 26,1; Н2 1,7; N2 4,4; Hg 62,5.
Найдено, %: С 26,3; Н2 1,6; N 4,4; Hg 62,7.
Пример 9. 219 г N-бисоксиэтилизоцианурата растворяют в 1 л диметилформамида и добавляют, перемешивая, 1 л метанола, содержащего 294,5 г гидроокиси фениловой ртути. Реакционную среду нагревают до 75°С в течение 3 час, охлаждают и после фильтрации получают 482 г 1,5-оксиэтил-3-фенилртутьизоцианурата. Общий выход 97,5%.
Вычислено, о/0; С 31,4; Н2 3,05; N2 8,5; Hg 40,4.
Найдено, %: С 31,6; Н2 3,1; N2 8,5; Hg 40,6.
Пример 10. В раствор из 42,8 г бис-(N-трихлорметилтио)-изоциануровой кислоты в 200 см3 хлороформа, перемешивая, вводят 24,65 г гидроокиси этиловой ртути и нагревают 3 час с флегмой при 60°С. После охлаждения, фильтрования и сушки получают 64,3 г изоцианурата 1,3-(трихлорметилтио)-5-этилртути.
Вычислено, %: С 12,5; Н2 0,8; Cl 32,3; N2 6,3; S 9,6; Hg 30,6.
Найдено, %: С 12,8; Н2 0,8; Cl 32,4; N2 6,4; S 9,7; Hg 30,5.
Пример 11. Согласно способу примера 1 из раствора, содержащего 21,7 г N-1,3-бис-оксиэтилизоциануровой кислоты в 500 см3 воды и 50 см3 диметилформамида, в который постоянно подают 25,1 г хлорида метиловой ртути, причем поддерживают температуру 90°С и рН 9, по истечении 60 мин реакции получают 41,6 г изоцианурата и N-1,3-окси-этил-5-метиловой ртути. Выход 96,5%.
Вычислено, %: С 22,1; Н2 3,0; N2 9,9; Hg 46,5.
Найдено, %: С 22,2; Н2 3,0; N2 9,7; Hg 46,4.
Пример 12. Изготовляют 43,1 г N-1,3-диалил-5-этилртутьизоцианурата с выходом 98,5%, подвергая взаимодействию в условиях, описанных в примере 1, 20,9 г 1,3-N-диаллилизоцианурата с 26,5 г хлорида этиловой ртути в присутствии 50 см3 воды и 50 см3 диметилформамида.
Способ получения ди- и тризамещенных ртутноорганических производных изоциануровой кислоты формулы
(CNO3)HmXnУp,
где X - RHg, в котором R представляет одновалентный алкиловый, ариловый или алкилариловый радикал;
У - представляет радикал -SCCl3, -(СН2)x-СН2ОН, -СН2-СН=СН2, -(СН2)2-CN, -(CH2)3NH2 или -(СН2)2СООН;
x - число, максимально равное 3;
m - 0 или 1;
n - 1, 2 или 3;
p - 3 - m - n,
отличающийся тем, что замещенную или незамещенную изоциануровую кислоту подвергают взаимодействию с ртутноорганическим галогенидом RHgHal (R имеет вышеуказанные значения) в водной среде с примесью смешивающегося с ней органического растворителя или с ртутноорганической гидроокисью в безводном органическом растворителе при температуре 50-100°С и рН от 6 до 14.
Авторы
Даты
1968-07-10—Публикация
1966-08-27—Подача