Изобретение относится к области получения соединений, которые могут найти применение в фармацевтической промышленности.
Предлагаемый способ получения 6-[5′-(низший) алкил-3′-фенилизотиазол-4′-карбоксамидо]-пенициллановой кислоты общей формулы
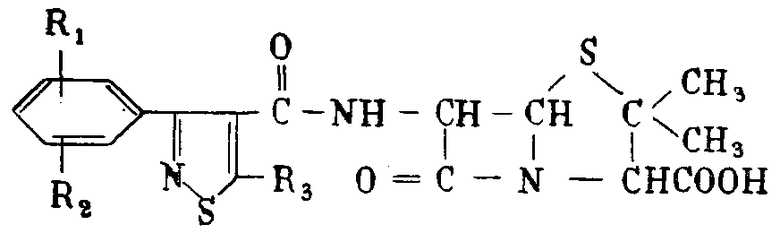
где R1 - водород, хлорметил или трифлуорометил, R2 - водород, хлор- или трифлуорометил, флуорометилсульфонил, нитро-, низший алкил или низший алкоксил; R3 - низший алкил, заключается во взаимодействии 6-амино-пенициллановой кислоты с хлорангидридами или со смешанным ангидридом кислоты общей формулы

где R1, R2, R3 имеют вышеуказанные значения.
Пример 1. Натрий-6-(5-метил-3-фенилизотиазол-4-карбоксамидо)-пенициллинат. Раствор из 3,2 г (0,0136 моль) 5-мегил-3-фенилизотиазол-4-карбонилхлорида в 5 мл хлористого метилена добавляют в течение 2 мин в быстро размешиваемый раствор из 3 г (0,0138 моль) аминопенициллановой кислоты и 3 г (0,03 моль) триэтиламина в 50 мл хлористого метилена при температуре 5-10°С. Реакционную смесь размешивают 1 час при 15°С, после чего извлекают тремя порциями воды по 50 мл каждая. Скомбинированные водные экстракты промывают двумя порциями эфира по 50 мл каждая, чередуя с 100 мл этилового эфира уксусной кислоты. Состав смеси регулируют до показателя 2 концентрации водородных ионов 10%-ной хлористоводородной кислотой. Слой этилового эфира уксусной кислоты отделяют, после чего водный слой снова извлекают двумя 100-мл порциями этилового эфира уксусной кислоты. Скомбинированные вытяжки этилового эфира уксусной кислоты промывают 50 мл воды, сушат сульфатом натрия, фильтруют (50 добавочных мл этилового эфира употребляют для промывки сосуда и фильтра) и обрабатывают с 4 мл 39%-ного раствора 2-этилгексаната натрия в метилизобутилкетоне. Прозрачный раствор выпаривают до объема около 200 мл и отделившиеся тонкие игольчатые кристаллы натрия -6-(5-метил-3-фенилизотиазол-4-карбоксамидо)-пенициллината (I) собирают фильтрованием. Второй выход (II) получается при добавлении к фильтрату сухого эфира.
Для вещества I: 1,97 г (33%); т. пл. 184-190°С (разложение).
Для II: 0,38 г (6%); т. пл. 180-190°С (разложение).
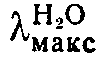 266,5 ммк (Е 11,200).
266,5 ммк (Е 11,200). 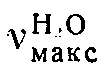 1780, 1665, 1615, 1540, 1410, 1330 см-1
1780, 1665, 1615, 1540, 1410, 1330 см-1
Вычислено для C19H18N3O4S2Na·Н2O, %: С 49,88; Н 4,11; N 9,19.
Найдено, %: С 50,31; 49,69; Н 4,91; 4,61; N 9,02; 9,23.
Пример 2. 6-(3-n-Хлорфенил-5-метилизотиазол-4-карбоксамидо)-пеницилланат натрия. В постоянно размешиваемый раствор из 600 мг (2,8 ммоль) 6-аминопенициллановой кислоты (6-АРА), 700 мг (8 ммоль) двууглекислого натрия, 45 мл воды и 50 мл ацетона вводят по каплям раствор из 620 мг (2,28 ммоль) 3-n-хлорфенил-5-метилизотиазол-4-хлорокиси углерода в 20 мл сухого ацетона при температуре от 0 до до 2°С. Реакционную смесь размешивают и течение 15 мин при 10-15°С, промывают дважды 100 мл порциями эфира и между ними порцией из 100 мл уксусноэтилового эфира и регулируют до показателя концентрации водородных ионов 2 разбавленной хлористоводородной кислотой, вводимой при размешивании и температуре 2°С. По отделении органического слоя водный слой дважды извлекают 50 мл порциями уксусноэтилового эфира. Комбинированные вытяжки уксусноэтилового эфира дважды промывают 50 мл порциями воды и сушат безводным сернокислым натрием. Фильтрат концентрируют до объема около 50 мл при температуре в 30°С и уменьшенном давлении. Концентрат обрабатывают 1,2 мл 39%-ного 2-этилгексаната натрия (SEH). Очистка сосуда в течение 30 мин приводит к кристаллизации. Кристаллы 6-(3-n-хлорфенил-5-метилизотиазол-4-карбоксамидо)-пеницилланата натрия собирают фильтрованием, промывают уксусноэтиловым эфиром и высушивают в вакууме фосфорным ангидридом. Выход 870 мг (80%); т. пл. 192-197°С (разложение).
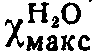 268 ммк (14,000).
268 ммк (14,000).
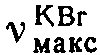 770, 1635, 1605, 1405 см-1.
770, 1635, 1605, 1405 см-1.
Вычислено для C19H17ClN3O4S2Na·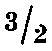 Н2O8, %: С 45,56; Н 4,02; N 8,39.
Н2O8, %: С 45,56; Н 4,02; N 8,39.
Найдено, %: С 45,64; 45,68; Н 4,02; 4,19; N 8,88; 8,73.
Пример 3. 6-(5-Метил-3-м-нитрофенилизотиазол-4-карбоксамидо)-пеницилланат натрия. К постоянно размешиваемому раствору из 700 мг (3,24 ммоль) 6-АРА, 800 мг (9,5 ммоль) двууглекислого натрия, 25 мл воды и 25 мл ацетона примешивают по каплям 820 мг (2,9 мл) 5-метил-3-м-нитрофенилизотиазол-5-хлорокиси углерода в 30 мл сухого бензола при температуре от 0 до 5°С. Реакционную смесь размешивают в течение 30 мин при 10°С, дважды промывают 100 мл порциями эфира, покрывают 100 мл порциями эфира, 100 мл уксусноэтилового эфира и регулируют разбавленной хлористоводородной кислотой при 5°С до показателя концентрации водородных ионов 2. Органический слой отделяют и водный слой дважды извлекают 50 мл порциями уксусноэтилового эфира. Оба комбинированных экстракта уксусноэтилового эфира дважды промывают 50 мл воды и сушат безводным сернокислым натрием. Фильтрат концентрирован при 30°С и уменьшенном давлении до объема 50 мл, после чего концентрат обрабатывают 1,4 мг 39%-ного SEH и размешивают в течение 3 час при комнатной температуре. Отделенный продукт, 6-(5-метил-3-м-нитрофенилизотиазол-4-карбоксамидо)-пеницилланат натрия, собирают фильтрованием, промывают уксусноэтиловым эфиром и сушат в вакууме фосфорным ангидридом. Выход 950 мг (67%); т. пл. 220-225°С (разложение).
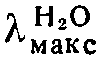 265 ммк (ε 19,300).
265 ммк (ε 19,300).
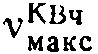 1760, 1625, 1600, 1400 см-1.
1760, 1625, 1600, 1400 см-1.
Вычислено для C19H17N4O6S2Na·2Н2O, %: С 43,85; Н 4,07; N 10,77.
Найдено, %: С 43,76; Н 3,57; 3,49; N 11,36, 11,43.
Пример 4. 6-(3-о-Хлорфенил-5-метилизотиазол-4-карбоксамидо)-пеницилланат натрия. К постоянно размешиваемой смеси из 2,5 г (0,0115 моль) 6-АРА, 2,9 г (0,034 моль) двууглекислого натрия, 80 мл воды и 50 мл ацетона прибавляют по каплям раствор из 2,55 г (0,0094 моль) 3-о-хлорфенил-5-метилизотиазол-4-хлорокиси углерода в 30 мл сухого ацетона при 5°С. Размешивание продолжают еще в течение 30 мин при температуре 10-15°С. Реакционную смесь дважды промывают 100 мл порциями эфира и одной порцией из 100 мл уксусноэтилового эфира и регулируют разбавленной хлористоводородной кислотой при 5°С до показателя концентрации водородных ионов 2. По отделении слоя уксусного эфира слой воды извлекают двумя 50 мл порциями уксусноэтилового эфира. Комбинированные экстракты уксусноэтилового эфира промывают водой, сушат безводным сернокислым натрием и выпаривают до  своего объема. Концентрат обрабатывают 35%-ным SEH и дал кристаллический осадок 6-(3-о-хлорфенил-5-метилизотиазол-4-карбоксамидо)-пеницилланат натрия, собранный фильтрованием. При промывании ацетоном преципитат проявляет тенденцию к растворению в растворителе.
своего объема. Концентрат обрабатывают 35%-ным SEH и дал кристаллический осадок 6-(3-о-хлорфенил-5-метилизотиазол-4-карбоксамидо)-пеницилланат натрия, собранный фильтрованием. При промывании ацетоном преципитат проявляет тенденцию к растворению в растворителе.
Остаточный преципитат В (1,3 г) промывают уксусноэтиловым эфиром.
С другой строны, к ацетоновому раствору, содержащему часть образца, добавляют пять объемов этилового эфира. Полученный раствор слегка концентрируют и получают 1,6 г 6-(3-о-хлорфенил-5-метилизотиазол-4-карбоксамидо)-пеницилланата натрия в кристаллах (А). Кристаллизационные формы образцов А и В отличаются друг от друга инфракрасным спектром, но их микробиологические процессы почти одинаковы.
Образец «В» также перекристаллизовывают ацетоном и уксусноэтиловым эфиром, получая 0,6 г кристаллов, инфракрасный спектр которых идентичен спектру образца «А». Общий выход 2,2 г (50%).
Для «В» т. пл. 182-188°С (разложение),
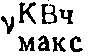 1760, 1650, 1595, 1530, 1405 см-1
1760, 1650, 1595, 1530, 1405 см-1
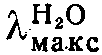 258 ммк (ε 9,100).
258 ммк (ε 9,100).
Для «А» т. пл. 182-188°С (разложение).
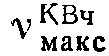 3530, 3370, 1765, 1650, 1600, 1510, 1480, 1410 см-1
3530, 3370, 1765, 1650, 1600, 1510, 1480, 1410 см-1
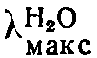 257,5 ммк (ε 9,400).
257,5 ммк (ε 9,400).
Вычислено для C19H17ClN3O4S2Na·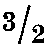 Н2О, %: С 45,55; Н 4,02; N 8,39.
Н2О, %: С 45,55; Н 4,02; N 8,39.
Найдено, %: С 45,31; 45,66; Н 3,83; 4,16; N 8,45; 8,95.
Пример 5. 6-(3-n-Метоксифенил-5-метилизотиазол-4-карбоксамидо)-пеницилланат натрия. В постоянно размешиваемый раствор из 2,6 г (0,012 моль) 6-АРА и 3 г (0,036 моль) двууглекислого натрия в 80 мл воды вводят по каплям при 5°С раствор из 2,9 г (0,011 моль) 3-метоксифенил-5-метилизотиазол-4-хлорокиси углерода в 30 мл сухого ацетона. Смесь размешивают 30 мин при 15°С и промывают двумя 100 мл порциями эфира, после чего промывную жидкость удаляют. Реакционную смесь охлаждают до 5°С, смешивают с 100 мл уксусноэтилового эфира и регулируют до показателя концентрации водородных ионов 2, разбавленной хлористоводородной кислотой при энергичном размешивании.
Отделяют органический слой, водный пласт извлекают двумя порциями уксусноэтилового эфира по 50 мл. Скомбинированные экстракты уксусноэтилового эфира промывают водой и сушат безводным сернокислым натрием. Фильтрат обрабатывают 5 мл 35%-ного раствора SEH и концентрируют под уменьшенным давлением при температуре ниже 40°С. Отделившийся осадок 6-(3-n-метоксифенил-5-метилизотиазол-4-карбоксамидо)-пеницилланата натрия собирают фильтрованием, промывают уксусноэтиловым эфиром и сушат в вакууме пятиокисью фосфора. Выход 2,6 г (52%), т. пл. 160-165°С.
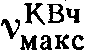 1780, 1655, 1610, 1400 см-1.
1780, 1655, 1610, 1400 см-1.
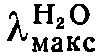 278 ммк (ε 12,900).
278 ммк (ε 12,900).
Вычислено для C20H20N3O5S2Na, %: С 51,16; Н 4,29; N 8,95.
Найдено, %: С 50,90; 50,90; Н 4,70; 4,70; N 7,91; 8,12.
Пример 6. 6-[3-(2,4-дихлорфенил)-5-метилизотиазол-4-карбоксамидо]-пеницилланат натрия. К постоянно размешиваемому раствору из 0,86 г (0,004 моль) 6-аминопенициллановой кислоты, 1 г (0,012 моль) двууглекислого натрия, 40 мл воды и 25 мл ацетона добавляют раствор 1,1 г (0,0036 моль) 3-(2,4-дихлорофенил)-5-метилизотиазол-4-хлорокиси углерода в 15 мл сухого ацетона при 5°С. Реакционную смесь размешивают в течение 1 час при 5°С, промывают двумя порциями эфира по 100 мл, покрывают 100 мл уксусноэтилового эфира и регулируют до показателя концентрации водородных ионов 2 100%-ным раствором хлористоводородной кислоты при 5°С. Пласт уксусноэтилового эфира отделяют, а слой воды извлекают двумя порциями по 40 мл уксусноэтилового эфира. Скомбинированные экстракты уксусноэтилового эфира промывают двумя порциями воды по 20 мл и сушат безводным сернокислым натрием. Фильтрат выпаривают до 50 мл объема при температуре ниже 40°С и под уменьшенным давлением. Концентрат обрабатывают 1,7 мл 35%-ного раствора SEH, а затем 100 мл n-гексана, что дает 6-[3-(2,4-дихлорофенил)-5-метилизотиазол-4-карбоксамидо]-пеницилланат натрия, собранный фильтрованием и высушенный в вакууме пятиокисью фосфора. Выход 1,64 г (89%); т. пл. 170-175°С.
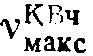 1765, 1640, 1600, 1400 см-1.
1765, 1640, 1600, 1400 см-1.
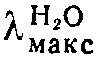 258 ммк (ε 9,400).
258 ммк (ε 9,400).
Вычислено для C19H16Cl2N3O4S2Na, %: С 44,89; Н 3,17; N 8,27.
Найдено, %: С 46,14; 46,28; Н 4,06; 4,14; N 7,23; 7,02.
Пример 7. 6-(3-м-Аминофенил-5-метилизотиазол-4-карбоксамидо)-пеницилланат натрия. К непрестанно размешиваемому раствору из 1,8 г (0,0083 моль) 6-АРА, 2,8 г (0,33 моль) двууглекислого натрия, 50 мл воды и 30 мл ацетона примешивают по каплям 2,2 г (0,0076 моль) 3-(м-аминофенил)-5-метил-4-хлорокиси углерода в 20 мл сухого ацетона при 5°С. Реакционную смесь размешивают в течение 15 мин при 15°С, промывают двумя порциями эфира по 100 мл и регулируют 10%-ной хлористоводородной кислотой до показателя концентрации водородных ионов 4 для отделения окрашенного в желтовато-коричневый цвет осадка, содержащего свободную 6-(3-м-аминофенил)-5-метилизотиазол-4-карбоксамидо)-пенициллановую кислоту.
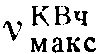 1780, 1720 (коротк.), 1650, 1520 см-1
1780, 1720 (коротк.), 1650, 1520 см-1
Осадок удаляют фильтрованием. Фильтрат прослаивают 100 мл уксусноэтилового эфира и регулируют 10%-ной хлористоводородной кислотой до показателя концентрации водородных ионов 2. Слой уксусноэтилового эфира отделяют, а водянистый слой извлекают двумя порциями уксусноэтилового эфира по 50 мл.
Скомбинированные вытяжки уксусноэтилового эфира промывают двумя порциями воды по 50 мл, сушат безводным сернокислым натрием и концентрируют до 100 мл объема при пониженном давлении и при температуре ниже 40°С.
Концентрат обрабатывают 4 мл 35%-ного раствора SEH, что дает 6-[3-(м-аминофенил)-5-метилизотиазол-4-карбоксамидо]-пеницилланат натрия, собранный фильтрацией, промытый уксусноэтиловым эфиром и высушенный в вакууме пятиокисью фосбора. Выход 1,38 г (40%); т. пл. 25-30°С.
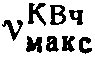 1760, 1655, 1600, 1400 см-1
1760, 1655, 1600, 1400 см-1
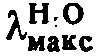 250 ммк (ε 10,500).
250 ммк (ε 10,500).
Вычислено для C19H19N4O4S2Na·5Н2O, %: С 41,95; Н 5,37; N 10,30.
Найдено, %: С 41,34; 41,10; Н 4,65, 4,65; N 8,89; 8,99.
Пример 8. 6-(3-м-Хлорфенил-5-метилизотиазол-4-карбоксамидо)-пеницилланат натрия. Аналогично готовят 3-м-хлорфенил-5-метилизотиазол-4-карбоновую кислоту (т. пл. 148-147°С), которую превращают в ее ангидрид (т. кип.137-139°С), в свою очередь, реагировавший с 6-аминопенициллановой кислотой, что дает 6-(3-м-хлорфенил-5-метилизотиазол-4-карбоксамидо)-пенициллинат натрия, плавящийся при 213-218°С с разложением.
Вычислено для C19H17ClN3O4S2Na·1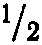 Н2O, %: С 45,55; Н 4,25; N 8,39.
Н2O, %: С 45,55; Н 4,25; N 8,39.
Найдено, %: С 45,37; 45,47; Н 4,33; 4,22; N 8,46; 8,66.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных имидазола или их солей | 1975 |
|
SU552027A3 |
| Способ получения производных имидазо (1,5-а) /1,4/- диазепина или их солей | 1976 |
|
SU730308A3 |
| Способ получения фосфорорганических производных изотиазола | 1973 |
|
SU489336A3 |
| Способ получения карбоксипроизводных 6-аминопенициллановой кислоты или их солей | 1971 |
|
SU527138A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНИЦИЛЛИНА | 1969 |
|
SU240565A1 |
| Способ получения сложных эфиров @ -аминопенициллинов или их кислотно-аддитивных солей | 1973 |
|
SU1153830A3 |
| СПОСОБ ПОЛУЧЕНИЯ-)-а-АМИНО-п- | 1971 |
|
SU309520A1 |
| Способ получения производных имидазо/1,5-а//1,4/диазепина или их солей | 1977 |
|
SU725563A3 |
| СПОСОБ ПОЛУЧЕНИЯ б-(а-АЗИДОФТОРФЕНИЛЛЦЕТАМИДО)- -ПЕНИЦИЛЛАНОВОЙ КИСЛОТЫ | 1972 |
|
SU333764A1 |
| Способ получения производных диазепина или их 5-окисей, или их солей | 1974 |
|
SU552028A3 |
Способ получения 6-[5′-(низший) алкил-3′-фенилизотиазол-4′-карбоксамидо]-пенициллановых кислот общей формулы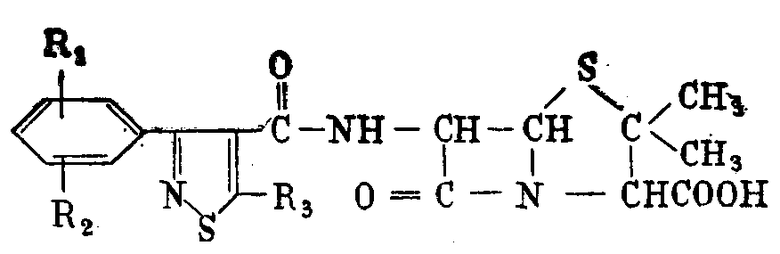
где R1 - водород, хлорметил или трифлуорометил,
R2 - водород, хлоро- или труфлуорометил, флуорометилсульфонил, нитро-, низший алкил или низший алкоксил,
R3 - низший алкил,
отличающийся тем, что 6-аминопенициллановую кислоту подвергают взаимодействию с хлорангидридом или со смешанным ангидридом кислоты общей формулы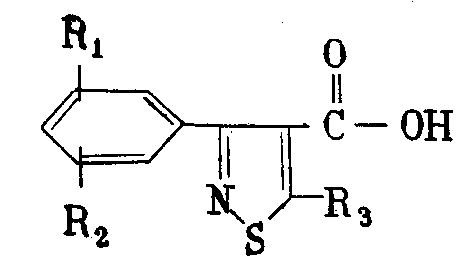
где R1, R2, R3 имеют вышеуказанные значения.
Авторы
Даты
1968-12-08—Публикация
1966-07-28—Подача