Изобретение относится к получению новых производных цефалоспорина, которые могут найти применение в фармацевтической промышленности. Известен способ получения сложных эфиров дезацетоксицефалоспорина нагреванием сложного эфира сульфоокиси пенициллина при 80--150°С в растворителе, содержащем третичпый амид карбоновой кислоты, в присутствии сульфокислоты, с одновременным удалением воды из реакционной массы. Продукты выделяют известным способом. Хотя выход дезацетоксицефалоспорановых эфиров наиболее высокий по сравнению с выходом указанных эфиров, получаемых известными рапее способами, однако и в этих условиях образуются некоторые количества побочных продуктов. Предлагается опособ получения 3-окси-З-метил-7-аминоцефалоспоринов общей формулы S .HN-pY Х .A он Где R - водород, группа Hz , группа, защищающая аминогруппу, такая, как трифенилМетил, карбоксикарбонил,бензилоксикарбонил, аллилоксикарбонил,циклопентилоксикарбонил, предпочтительноацильная группа общей формулы )т- lO)z-(CH2)n-GOгде ш - О-4, п- 1-4, z - О или 1, причем когда г - О, группы (СН2)т и (СП2)п соединены между собой в цепь, фенильное ядро ацильной группы может быть замещено ia фтор, хлор, бром, йод, оксигруппу, Ci-Сз-алкил, Ci-Са-оксиалкил, нитро, циано или трифторметил; один или два атома водорода в группах (СН2)т или (СН2)п могут быть замещены метилом; R - водород, атом щелочного металла, остаток четвертичного аммония, эфирная группах (СП2)т или (СН2)п могут быть замепый заряд. Примером ацильных групп могут служить фенилацетил, феноксиацетил, фенилгептаноил, феноксиизопропионил, бензилоксиацетил, фенилпропионил, фенилбутирил, 3-метилфенилбутирил, 4-пропилбензилацетил, бензилоксиацетил, фенилэтоксипропионил, фенилбутоксибутирил, 3-фторфеноксиацетил, 3-оксифенилацетил, 4-бромфенилпропионил, 4-йодфенил3
ацетил, 2-хлорбеизилоксипропионил, феиил2,2-дпметилацетил, 4-нитрофенилацетил, 3-цианофеиилпропионил, трифторметилфеноксиаиетил.
Эфирная группа представляет собой одну из известных групп, легко омыляемых с помощью разбавленного водного раствора щелочЕ трифторуксусной кислоты, уксусной кислоты -л порошка цинка или нутем восстановления в присутствии подходящего катализатора, такого, как палладий, платина или родий на подходящем носителе, например на угле, сульфате бария или алюминия. Предпочтительными эфирными группами являются С4 - Сб-трет-алкил, Cs - Су-грёт-алкенил, Cs - Су-грет-алкинил, такие, как трег-бутил, грет-пентил, 1,1-диметил-2-проненил, 1,1-диметил-2-пентинил, 2,2,2-трихлорэтил, бензил, 3или 4-меток€ибензил, 3- или 4-нитрО|бензил, фталимидометил, сукцинимидометил, -CHaR группа, где R - Cj - Се-алканоил, бензоил, толуоил, фе:ноил или фуроил, или бензгидрил.
Способ заключается в том, что сульфоксид пенициллановой кислоты или ее эфира нагревают при 80-150°С в присутствии серной или сульфаминовой кислоты или их водорастворимых эфиров или солей и в присутствии по крайней мере около 10 об. % грет-карбоксамида общей формулы
/-0
Кз
в которой RI - водород и каждый Rs и Rs - алкил, фенил, толил, или ксилил, причем Rs и Rs вместе должны содержать 14 атомов углерода;
или по крайней мере один из Ri, R2 и Rs - алкил и не более, чем два из Ri, R2 и Ra - фенил, толил, ксилил, причем Ri, Rs и Rs вместе содержат около 18 атомов углерода; или Ri - водород или алкил, Ra и Rs вместе с атомом азота, с которым они связаны, образуют моноциклическое кольцо с насыщенными связями, которое содержит 4-6 атомов углерода, причем кольцо может также содержать кислород, а RI, R2 и Rs вместе содержат не более 12 атомов углерода;
или R и R2 вместе с амидной группой -С (О)-N, к которой они присоединены, образуют насыщенное карбонильное соединение, содержащее моноциклическое кольцо с 4-6 атомами углерода, Rs - алкил, фенил, толил или ксилил и R, Rs и Rs вместе должны содержать не более 14 атомов углерода.
Примерами трет-карбоксамидов могут быть:
М,Ы-диметил-, N,N-диэтил-, Ы,Ы-диизопроПИЛ-, Ы,К-дибутнл-, N,N-дипeнтил-, N-метилN-этил-, N-мeтил-N-фeнил-, Н-этил-М-(1г-толил)-, М-пропил-1Ч-(3,5-днметилфенил)-, N,Nдифенил-, Ы,М-бис-(4-метилфенил)-, N-(3,5диметил) -N-метил-, К,К-бис- (2,4-диметилфенил)формамиды;
,Ы-диметил-, Ы,-диэтил- и Ы,М-диизопропилацетамиды, N,N-димeтилпpoпиoнaмид, N,Nдибутилацетамид, Ы,Ы-ди-грет-бутилацетамид, N,N - диэтилпропионамид, N,N - дипентилпропионамид, Ы,К-диметилдеканоамид, N,N-димeтилбензамид, Ы,Ы-диэтилбензамид, Ы,Ы-дипропил-./и-толуамид, М,К-дибзтил-/г-толуамид, К-фенил-М - метилацетамид, N- (п - толил) -Nэтилацетамид, N- (3,5-диметилфенил) -N-метилпропионамид, N,N-димeтил-3,5 - диметилбензамид, М,М-дибутил-4-зтилбензамид, К,Ы-дифенилацетамид, N-(3-мeтилфeнил)-N - этилбензамид, 1,М-бис-(6-метилфенил) - пропионамид, К,К-бис-{7-метилфенил) -пропионамид, N,Nбис- (3,5-диметилфенил) -пропионамид;
(З-формилпиперидин, N - ацетилпирролидин, N-пропионилморфолин, Ы-ацетил-4,5-диметилпирролидин, N-бутаноилпиперидин, N-ацетил6-метилпиперидин;
1 -метил-2-пирролидон, 1 -фенил-2-пирролидон, 1-бутил-2-пиперидон, 1-(.л«-толил)-2-пиперидоп, -этил-2-пиперидон, I-(3,5-диметилфенил)-2-пиперидон, 1-метил-2-пиперидон, 1-фенил-2-пиперидон, 1-пропил-2-пиперидон, 1-изопропил-2-гомопиперидон, М-этил-2 - гомопиперидон.
Однако чаще всего используют диметилацетамид, дкметилформамид и М-метил-2-пирролидон.
Продукты выделяют известным способом в свободном виде или в виде соли с наиболее высоким выходом, чем во всех известных способах.
Продолжительность реакции 24 час. При использовании предпочтительных растворителей и реагентов высокий выход целевого продукта достигается в течение 5-14 час. Концентрация сульфоксида пенициллановой кислоты или ее эфира в смеси, содержащей трет-карбоксамид и инертный растворитель (объемное отнощение 3:5-5:3) составляет 1-20 вес. %. Соотнощение между растворителями и концентрацией сульфоксида пенициллина зависит от характера грег-карбоксамида и инертного растворителя, температуры реакции и ее продолжительности. Из грет-карбоксамидов лучще всего использовать N,N-димeтилaцeтaмид, который может оказывать влияние на ход реакции.
Из солей и эфиров серной и сульфаминовой кислот могут быть использованы соли щелочных металлов, таких, как литий, натрий, калий и рубидий (однако соли лития и рубидия очень дороги), соли щелочноземельных металлов, таких, как магний и кальций, неполные и полные эфиры с Ci - Co-спиртами, например диметилсульфат, диэтилсульфат, дипропилсульфат. Однако проще и удобнее использовать свободные кислоты.
3-Окси-З-метил - 7 - аминоцефалоспорановые соединения выделяют известными методами. Обычно реакционную смесь концентрируют в вакууме, остаток растворяют в подходящем растворителе, например в хлорированном углеводороде, таком, как метиленхлорид, хлороформ, четыреххлористый углерод, в спирте
Ci - Сб, таком, как метанол, изопропанол, или в углеводороде, таком, как бензол, толуол, ксилол, гептан, экстрагируют разбавленной кислотой, отгоняют остаток трет-карбоксамида и перекристаллизовывают.
Концентрация серной или сульфаминовой кислоты, их солей и эфиров зависит от нрироды взятой кислоты, концентрации сульфоксида эфира пенициллина, или пенама, используемой системы растворителей, времени реакции. Обычно молярное соотношение между сульфоксидом пенициллина и кислотой составляет 1:1-50:1, между сульфоксидом эфира пенициллина и кислотой 5:1-15:1.
Сульфоксид пенициллаиовой кислоты, или пенам, ее соли или эфиры в подкисленном растворителе нагревают при 80-150°С. В этих условиях происходит прямая перегрупнировка сульфоксида пенициллина в 3-окси-З-метил7-аминоцефамовые соедииения. При использовании Гуоет-карбоксамида в качестве растворителя процесс лучше вести при 90-130°С в течеиие 2-24 час.
грет-Карбоксамид быть использован в качестве растворителя, однако для нолучения продукта с Оптимальным выходом лучше разбавлять трег-карбаксамид инертным органическим растворителем, таким, как углеводороды, особенно СБ - Сд-алканы .и Сб - Cs-apoматические углеводорды, галоидуглеводороды, содержащие 1-6 атомов углерода и 1-4 атома хлора или брома, а также их простые и сложйые эфиры, Нитрилы и т. д. Примерами подходящих разбавителей являются пентан, гексан, гептан, бензол, толуол, ксилол, метиленхлорид, хлороформ, четыреххлор-истый углерод, 1,2-дихлорэтан, метилэтилкетон, метилизобутилкетон, этилацетат, изопрапилацетат, н-пролилацетат, диацетат нролиленгликоля, ацетонитрил, нронионитрил, диаксаи.
Соединения формулы 1, в которых R - водород, могут быть получены в результате перегруппировки сульфоксида пенициллина, который полностью превращается в 3-окси-З-метил-7-ациламидоцефам-4-карбоновую кислоту или ее эфир под действием пятихлористого фосфора в присутствии эквивалентного количества третичного амина, например пиридина, с последующей обработкой низшим спиртом, например метанолом, и затем водой для отщепления 7-ацильной группы. Примерами таких соединений являются 3-окси-З-метил7-аминоцефам-4-карбоновая кислота и третбутил-3-окси-З-метил - 7-аминоцефам-4-карбоксилат. Эти соединения могут быть выделены из реакционной смеси известными способами, например в виде соли с Се - С12-сульфокислотой, которая легко отделяется от органических растворителей. Полученные 7-аминосоединения могут быть также в форме внутренних или цвиттер-ионных солей при 4-карбоксильной группе (в которой R - заряд аниона).
В тех случаях, когда R - Нг , второй водород находится в карбоксиле. Такие соединения также могут существовать в виде солей с сильными кислотами (рКа не менее 4), такими, как соляная, серная, ортофосфорная, азотная, йодистая, надхлорноватая кислоты и им подобные.
В качестве исходных соединений можно использовать также 6-аминопенам-З-карбоновую кислоту, например 6-аминоненициллановую кислоту (6-АПК), и ее эфиры, напри.мер 2,2,2трихлорэтил - 6 - амвно - 2,2 - диметилпенам - 3 карбоксилат, по лучше исходить из пенама, в котором аминогруппа защищена.
Примером соединений формулы I (в скобках названы сульфоксиды, из которых оии могут быть получены) могут служить:
трет - бутил-3 - ожси - 3-метил - 7-(феНилацетатамидо) -цефам-4-карбоксилат (грет-бутиловый эфир фенилметилпенициллинсульфоксида); Г ,Г- диметил-2 - пропинил - 3-окси-метил7-(4-нитрофеиилацетамидо)-цефам - 4-карбоксилат(Г ,1 -диметил-2 - пропиниловый эфир 4-нитрофенилметилпенициллинсульфоксида);
2,2,2 -трихлорэтил - 3-окси-3-метил-7-(октанонламидо)-цефам - 4-карбоксилат(2,2,2трихлорэтиловый эфир гептилпенициллинсульфокснда);
4 -1Нитробензил-3 - окси-3-метил - 7-(2-,2-диметилфенилацетамидо)-цефам - 4-карбоксилат (4 -нитробензилоБый эфир 2,2-диметилфенилпенициллинсульфоксида);
т/7ет-бутил - 3-окси-З - метил-7-(5- бутоксикарбониламиноадипоиламидо) - цефам - 4-карбоксилат (грет-бутиловый эфир N-бутоксикарбоКСил (защищенный) - пенищиллии - N-сульфоксида);
3-окси -3-метил -7 - (феноксиацетамидо-цефам-4-карбоновая кислота (феноксиметилпенициллинсульфоксид); 3-окси-З - метил-7- (2тиенилацетамидо)-цефам-4-карбоновая кислота (тиенилметилпенициллинсульфоксид).
Соли соединений формулы I получают при обработке кислот основанием или основной солью, например гидроокисью натрия или калия, ацетатом натрия или калия, карбонатом
калия, гидроокисью аммония или триалкиламином, например триметиламином или триэтиламииом, образующим соответствующие
аммониевые или аминные соли.
3-Окси-З-метил - 7-аминоцефалоспорановые
соединения могут быть использованы для получения соединений, содержащих Дз-цефамцефалоспорановое ядро. Например, перемешивая 15 мин одно из 3-окси-З-метилцефамовых соединений со смесью уксусного ангидрида и
М,Ы-диметилацетамида на масляной бане при 100-110°С, пол чают с хорошим выходом соО7ветствующие 3-метил-Дз-цефамовые соединения. Например, г/зег-бутил-3-окси-З-метил7-(феноксиацетамидо)-цефам - 4-карбоксилат
Б результате реакции элиминирования образует соответствующий эфир трет-бутил-З-метил7-(феноксиацетамидо)-Аз-цефам - 4-карбоксилат, который используется в синтезе известного цефалоспоранового антибиотика-цефалексина 7(В-а - амшюфенилацетамидо)-3 - метилАЗ-цефам-4-карбоновая кислота из феноксиметилпенициллииа. В этом синтезе феноксиацетильную группу в 3-метил-Аз-цефемовом эфире обрабатывают пятихлористым фосфором и пиридином, хлорированный продукт обрабатывают метанолом и затем водой, образовавшийся 7-амино - 3 - метил-ДЗ-цефамовый зфир, который может быть выделен, например, в виде соли п-толуолсульфоновой кислоты, переацилиругот Ы-запдии1енной сс-аминофенилуксусной кислотой, удаляют N-защитную и эфирную группу и получают цефалексин.
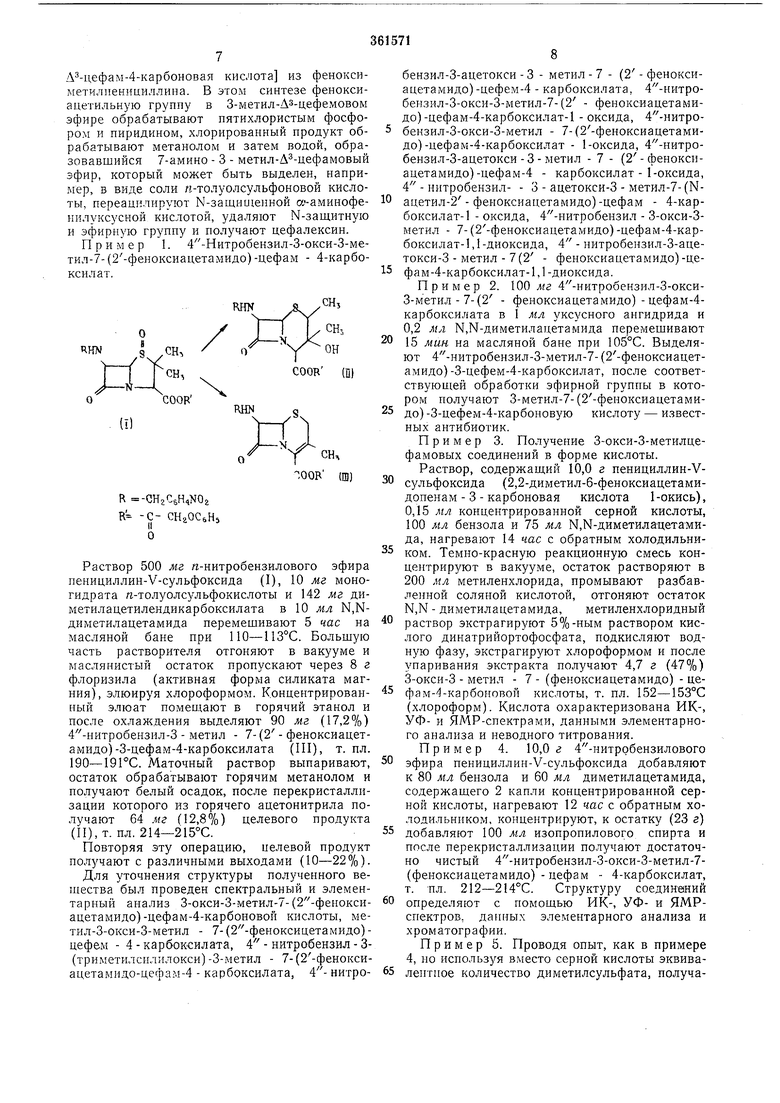
Пример 1. 4 -Нитробензил-3-окси-3-метил-7-(2-феноксиацетамидо)-цефам - 4-карбоксилат.
RHN
(I)
/
сн,
.ООВ (Ш)
R -CH2C5H N02 R -С- CHaOC Hs О
Раствор 500 мг я-нитробензилового эфира пенициллин-У-сульфоксида (I), 10 мг моногидрата г-толуолсульфокислоты и 142 мг диметилацетилендикарбоксилата в 10 ил N,Nдиметилацетамида перемешивают 5 час на масляной бане при ПО-113°С. Большую часть растворителя отгоняют в вакууме и маслянистый остаток пропускают через 8 г флоризила (активная форма силиката магния), элюируя хлороформом. Концентрированный элюат помеидают в горячий этанол и после охлал дения выделяют 90 мг (17,2%) 4 -нитробензил-3 - метил - 7-(2- феноксиацетамидо)-3-цефам-4-карбоксилата (III), т. пл. 190-191 0. Маточный раствор выпаривают, остаток обрабатывают горячим метанолом и получают белый осадок, после перекристаллизации которого из горячего ацетонитрила получают 64 мг (12,8%) целевого продукта (11),т. пл. 214-215°С.
Повторяя эту операцию, целевой продукт получают с различными выходами (10-22%).
Для уточнения структуры полученного вешества был проведен спектральный и элементарный анализ 3-окси-3-метил-7-(2 -феноксиацетамидо)-цефам-4-карбоновой кислоты, метил-3-окси-З-метил - 7-(2 -феноксицетамидо)цефем - 4-карбоксилата, 4 - нитробензил - 3(триметилснлнлокси)-3-метил - 7-(2-феноксиацетамидо-цефам-4 - карбоксилата, нитробензил-3-ацетокси - 3 - метил-7 - (2- феноксиацетамидо)-цефем-4 - карбоксилата, 4 -нитробензил-3-окси-3-метил-7-(2 - феноксиацетамидо)-цефам-4-карбоксилат-1 -оксида, 4 -нитробензил-3-окси-З-метил - 7-(2-феноксиацетамидо)-дефам-4-карбоксилат - 1-оксида, 4 -нитробензил-3-ацетокси-3-метил - 7 - (2-фенокснацетамидо)-цефам-4 - карбоксилат - 1-оксида, 4 - нитробензил- - 3 - ацетокси-3 - метил-7-(Мацетил-2- феноксиацетамидо)-цефам - 4-карбоксилат-1 -оксида, 4 -нитробензил - 3-окси-Зметил - 7-(2-феноксиацетамидо)-цефам-4-карбоксилат-1,1-диоксида, 4 - нитробензил-3-ацетокси-3 - метил - 7(2 - феноксиацетамидо)-цефам-4-карбоксилат-1,1-диоксида.
Пример 2. 100 мг 4 -нитробензил-3-окси3-метил - 7-(2 - феноксиацетамидо)-цефам-4карбоксилата в 1 мл уксусного ангидрида и 0,2 мл М,М-диметилацетамида перемешивают
15 мин на масляной бане при 105°С. Выделяют 4 -нитробензил-3-метил-7- (2-феноксиацетамидо)-3-цефем-4-карбоксилат, после соответствующей обработки эфирной группы в котором получают 3-метил-7-(2-феноксиацетамидо)-3-цефем-4-карбоновую кислоту - известных антибиотик.
Пример 3. Получение 3-окси-З-метилцефамовых соединений в форме кислоты. Раствор, содержащий 10,0 г пенициллин-Vсульфоксида (2,2-диметил-6-феноксиацетамидопенам - 3 - карбоновая кислота 1-окись), 0,15 мл концентрированной серной кислоты, 100 мл бензола и 75 мл Ы,М-диметилацетамида, нагревают 14 час с обратным холодильником. Темно-красную реакционную смесь концентрируют в вакууме, остаток растворяют в 200 мл метиленхлорида, промывают разбавленной соляной кислотой, отгоняют остаток N,N - диметилацетамида, метиленхлоридный
раствор экстрагируют 5%-ным раствором кислого динатрийортофосфата, подкисляют водную фазу, экстрагируют хлороформом и после упаривания экстракта получают 4,7 г (47%) 3-окси-З - метил - 7 - (феноксиацетамидо) - цефам-4-карбоновой кислоты, т. пл. 152-153°С (хлороформ). Кислота охарактеризована ИК-, УФ- и ЯМР-спектрами, данными элементарного анализа и неводного титрования. Пример 4. 10,0 г 4 -нитробензилового
эфира пенициллин-У-сульфоксида добавляют к 80 мл бензола и 60 мл диметилацетамида, содержащего 2 капли концентрированной серной кислоты, нагревают 12 час с обратным холодильником, концентрируют, к остатку (23 г)
добавляют 100 мл изопропилового спирта и после перекристаллизации получают достаточно чистый 4 -нитробензил-3-окси-3-метил-7(феноксиацетамидо) - цефам - 4-карбоксилат, т. -нл. 212-214°С. Структуру соединений
определяют с помощью ИК-, УФ- и ЯМРспектров, дарптых элементарного анализа и хроматографии.
Пример 5. Проводя опыт, как в примере 4, но используя вместо серной кислоты эквивалептиое количество диметилсульфата, получают 4 -нитробензил-3-окси-3-метил-7- (феноксиацетамидо)-цефам-4-карбоксилат, т. пл. 208- .
Пример 6. 10,0 г 4-11Итробензилового эфира пенициллин-У-сульфоксида, 0,194 г сульфаминовой кислоты в 112 мл бензола и 88 мл диметилацетамида иеремешивают и нагревают 14 час с обратным холодильником, выдерживают 3 час при комнатной температуре, отгоняют растворители в вакууме, остаток обрабатывают ксилолом и концентрируют в вакууме. Полученный продукт обрабатывают .хлороформом, отфильтровывают и получают 3,91 г (40,5%) продукта, т. пл. 211-212°С, индентифицированного, как в примере 1, и отнесенного к соединению формулы II в том же примере.
Пример 7. Смесь 2,5 г 4-нитробензилового эфира пенициллин-У-сульфоксида, 0,07 г бисульфата калия в 28 мл бензола и 22 мл диметилацетамида нагревают с обратным холодильником до окончания реакции (около 18 час), концентрируют сначала в вакууме и затем после образования азеотропа с ксилолом. 4 -Нитробензил-3 - окси-3-метил-7-(феноксиацетамидо) -цефам-4-карбоксилат перекристаллизовывают из хлороформа. Выход 1,02 г (41%), т. ил. 211-213°С. Т. пл. смешанной пробы с заведомо известным образцом 211 - 213°С.
Пример 8. Проводят опыт, как в примере 4, но используют 2,2,2-трихлорэтиловый эфир пенициллин-У-сульфоксида в смеси с бензолом и диметилацетамидом, содернсащим концентрированную серную кислоту в качестве подкисляющего агента. После нагрева с обратным холодильником и соответствующей обработки реакционной массы получают 2,2,2 -трихлорэтил-3 - окси - 3-метил - 7- (фенилацетамидо)-цефам-4-карбоксилат, который используется в качестве промежуточного продукта в синтезе дезацетоксицефалоспорановых антибиотиков, например цефалексина.
Пример 9. Проводят синтез, как в примере 4, но заменяют 4-нитробензиловый эфир пенициллин-У-сульфоксида на т/7е7-бутил-2,2-диметил - 6-(2,2 - диметилфенилацетамидо) - пенам-З-карбоксилат-1-окись и получают трегбутил-3-окси-З-метил - 7-(2,2 - диметилфенилацетамидо) -цефам-4-карбоксилат, используемый в качестве промежуточного продукта в синтезе дезацетоксицефалоспорановых антибиотиков.
Пример 10. Повторяя пример 4, но используя вместо эфира пенициллин-У-сульфоксида 1, 1 -диметил-2 -пропинил-2,2-диметил6-(2-тиенилацетамидо) - пенам - 4 - карбоксилат-1-окись, получают Г , l -димeтил-2-пpoпинил-3-oкcи - 3-метил - 7-(2 - тиенилацетамидо)-цефам-4-карбоксилат, который используется в качестве промежуточного продукта в синтезе дезацетоксицефалоспорановых антибиотиков, таких, как З-метил-7- (2-тиенилацетамидо)-Аз-цефам-4-карбоновая кислота.
Пример И. В сухой бензол, содержащий
28 ммоль сухого пиридина, загружают 7,8 ммоль 4 -метаксибанзил-3-окси-3-метил7-(феноксиацетамидо)-цефам - 4 - карбоксилатп, который получают нагреванием 4 -метоксибензилового эфира пенициллин-У -сульфоксида в диметилацетамиде при 90-110°С в течение 6 час в присутствии серной кислоты в качестве катализатора. Полученный раствор нагревают до 50-60°С, перемешивают при
этой температуре в течение 1 час в атмосфере азота, с 28 ммоль пятихлористого фосфора, охлаждают и обрабатывают метанолом. Выдержав несколько часов при комнатной температуре, выпаривают основное количество
растворителей при температуре 50°С под давлением, остаток (рП около 1,8) обрабатывают смесью воды и тетрагидрофурана (отношение остатка к объему смеси растворителей 1:1). Через 2 чох тетрагидрофуран отгоняют,
водный остаток перемешивают с этил ацетатом и подщелачивают едким натром до рН 6,5-7. Этилацетатный слой, содержащий сырой 4 -метоксибензил-3-окси - З-метил-7 - аминоцефам-4-карбоксилат, обрабатывают 8 ммоль
4 - толуолсульфокислоты, отфильтровывают 4 -метоксибензил - З-окси-З-метил-7 - аминоцефам-4-карбо ксилат-д-толуоЛсульфонат, обработкой которого смесью этилацетат - вода при рН 7 можно выделить чистый 4 -метоксибензил-З-окси-3 - метил-7 - аминоцефам - 1-карбоксилат, используемый в качестве промежуточного продукта в синтезе цефалексина. Ацилированием аминоэфира Ы-(г;Оег-бутоксикарбонил) -D-a-фенилглицином при нагревании до
105°С в присутствии смешанных ангидридов, М,Ы-диметилацетамида, содержащего уксусный ангидрид, и затем обработкой полученного продукта ангидридом трифторуксусной кислоты в течение 15 мин получают З-метил-7-(Dа-аминофенилацетамидо)-Д -цефам - 4-карбояовую кислоту (цефалексин). Этот антибиотик может применяться парэнтерально или предпочтительно орально в количестве 50-500 мг 1-4 раза в день.
Пример 12. Проводят опыт, как в примере 3, феноксиметилпенициллинсульфоксид смещивают с М,М-диметилацетамидом, бензолом и эквивалентным количеством сульфаминовой кислоты, нагревают 14 час, концентрируют, очищают, как описано выше, и получают 3-окси-З-метил - 7-(феноксиацетамидо) -цефам-4-карбоновую кислоту.
Предмет изобретения
1. Способ получения З-окси-З-метил-7-аминоцефалоспоринов общей формулы
.он,
он
соов
где R - водород, группа , группа, защи65 щающая аминогруппу, такая, как трнфенилметил, карбоксикарбонил, бензилоксикарбонил, аллилок1СИкар1бонил, циклапентилокшкарбонил, предпочтительно ацильная группа общей формулы (CHaU-10, - (СНг)п-СОгде ш - О-4, п - О-4, z - О или 1, причем когда Z - О, метиленовые группы (СН2)т и (СН2)п соединены в цепь; фенильное ядро ацильной группы может быть замещено на фтор, хлор, бром, йод, ОКСИ-, нитро-, цианогруппы, Ci - Сз-алкил, Ci - С2-оксиалкил, трифторметил; R-сложноэфирная группа, такая, как 2,2,2-трихлорэтил, €4 - Се-г/оет-алкил, GS - Су-грег-алкенил, Сз - Сг-грет-алкинил, бензил, нитробвнзил, метоксибензил, фталим.идометил, сукцинимидометил, бе нзгидрил или -CHaR, где - G6-aлкalHoил, бензоил, толуоил, фаноил или фуроил, или R - водород, атом щелочного металла, или если R - группа Н, отрицательный заряд, отличающийся тем, что сульфоксид пенициллановой кислоты или ее эфира нагревают при 80-150°G в присутствии серной или сульфаминовой кислоты или их водорастворимых солей или эфиров и в присутствии по крайней мере 10 об. % грег-карбоксамида общей формулы в которой RI - водород и каждый Ra и Ra - алкил, фенил, толил или ксилил, причем R2 и R:) вместе должны содержать 14 атомов углерода;или по крайней мере один из Ri, Rs и Rj - алкил и не более, чем два из Ri, R2 и Rs - фенил, толил, ксилил, причем Ri, R2 и Rs вместе содержат около 18 атомов углерода; или RI - водород или алкил, а Ra и Rs вместе с атомом азота, к которому они присоединены, образуют; моноциклическое кольцо с насыщенными связями, которое содержит 4-6 атомов углерода, причем кольцо может также содерл ать кислород, а Ri, R2 и Rs вместе содержат не более 12 атомов углерода; или RI и Ra вместе с амидной группой -G(0)-N-, с которой они связаны, образуют насыщенное карбонильное соединение, содержащее моноциклическое кольцо с 4-6 атомами углерода, Rs - алкил, фенил, толил или ксилил и RI, R2 и RS вместе должны содержать не более 14 атомов углерода, с последующим выделением продуктов в свободном виде или в виде соли известным способом. 2.Gnoco6 по п. 1, отличающийся тем, что процесс ведут в растворителе, например в бензоле. 3.Gnoco6 по п. 1, отличающийся тем, что в качестве грет-карбоксамида используют Ы,М-диметилацетамид.






Авторы
Даты
1973-01-01—Публикация