Изобретение относится к способам получения антибиотиков сельскохозяйственного назначения, преимущественно антибиотиков, .применяемых для защиты возделываемых растений от фитопатогенных грибов.
Известен способ получения антибиотика вентурицидина А (АА368), при осуществлении которого в качестве гриба-цродуцента берут штаммы N.C.I.В. 9198, N.C.I.В. 9199 и N.C.I.В. 9200 Streptomyces aureofaciens.
Предлагается способ получения антибиотиков вентурицидина В и (или) вентурицидина X, нри котором в качестве гриба-нродуцента берут штамм S. aureofaciens NRRL 3399 (National Regional Research Laboratory USDA).
, хранится также пол названием Тй 342 в лабораториях фирмы-заявителя, а также депонирован в Микробиологическом институте при университете в Тюбингене (Швейцария).
Штамм выделяют ,из образца почвы, .взятого в окрестностях Козусса (Гвинея). По видовым признакам см. HiJtter et al. Arch. f. Mikrobie, 39, 173 (1961) он принадлежит к виду S. aureofaciens Duggar, 1948.
Основные характерные признаки штамма NRRL 3399:
2споры эллипсоидной формы, размером (0,6- 0,9) X (0,8-1,4) мк, с гладкой поверхностью;
воздушный мицелий вначале беловатого цвета, позднее - от коричнево-серого до золотисто-серого;
цепочки спор разветвлены моноподиально в форме открытых, свободных спиралей в 4-6 витков;
на питательной среде, содержащей пептон, меланиновидный пигмент не появляется.
Оптимальная температура роста для штамма колеблется от 33 до , в то время как у других представителей вида S. aureofaciens она колеблется от 27 до 30°С. Помимо антпбиотпков вентурициднна X п В вид S. aureofaciens продуцирует известный антибиотик вентзфицидин (антибиотик АЛ 368, см. DAS 1 184458), который в дальнейшем будет называться «вентурицидином А. Антибиотики могут быть разделены, например, распределением по Craigy и (или) хроматографией на селикагеле. Возможно также вентурицидин А перевести в вентурицидин В.
Способ получения антибиотиков вентурицидина X и (или) В заключается в следующем. Культуру S. aureofaciens NRRL 3399, дающую вентурицидин X и (нли) вентурицидин В, выращивают в аэробных условиях в водном
растворе, содержащем источники углерода и азота, а также неорганические соли, пока раствор не нокажет существенного антибиотического действия. Затем выделяют вентурицидин X и (или) В и по желанию полученный также вентурицидин А переводят в вентурицидин В. Полученные антибиотики можно перевести в их производные.
В качестве источников углерода и азота можно использовать глюкозу, сахарозу, фруктозу, крахмал, маннит и аминокислоты, например глицнн, пентиды, протеины и их продукты расщенления, например пептон или триптон, мясные экстракты, водную вытяжку из зерна (кукуруза, ншеница), дистнлляционные остатки нри получении алкоголя, дрожжи, семена (особенно растений ранса, сои и хлопчатника), аммониевые соли и нитраты. Из неорганических солей питательный раствор может содержать хлориды, карбонаты, сульфаты, нитраты, фосфаты щелочных и щелочноземельных металлов, магния, цинка, марганца и железа.
Культуру ведут в аэробных условиях при взбалтывании или перемещивании с воздухом или кислородом в специальных сосудах или ферментатерах. Более всего подходит температура 27-37°С. Культуральная жидкость показывает существенное антибактериальное действие в среднем через 24 час.
Культивируют преимущественно в несколько стадий: сначала готовят жидкую питательную среду, которую затем инокулируют. Сначала, нанример, переинокулируют споровый мицелий, полученный после двухнедельного выращивания на твердной питательной среде, в жидкую питательную среду и дают ему расти еще 48 час. Антибиотики из культурного фильтрата выделяют известными способами с учетом их химических, физических и биологических свойств.
Для проверки действия антибиотиков в отдельпых стадиях изолирования, а также и в культурной среде очень хорощим тест-организмом является Botrytis cinerea. Гифы этого микроорганизма морфологически сильно изменяются под действием антибиотиков (сильное разветвление, начиная от определенной точки, так что возникают метелкообразные формы).
Этот тест проводят, например, в виде диффузии на пластинках следующим образом.
В середине солодоагаровых пластинок в кругообразную нлощадь диаметром 5 мм инокулируют В. cinerea, и эти нластинки подвергают в течение двух-трех дней инкубации при 24°С. За это время мицелий развивается до 20--30 мм. Раствор контролируемого вещества наносят посредством фильтровых кружков диаметром 6 мм на расстоянии приблизительно 5 мм от края мицелия. После этого нластинки подвергают инкубации в течение 24- 36 час при температуре 24°С. В активных растворах наблюдается морфологическое изме.чение на расстоянии до 24 мм от фильтровых
кружков. Растворы концентрацией 10 мкг1А л антибиотиков дают еще заметно измененные гифы.
Антибиотик вентурицидин X не является гликозидом, в отличие от вентурицидинов А и В, которые являются гликозидами 2-дезокси-О-рамнозы (вентурицидин В) или соответственно 3-о-карбаминил-2-дезокси-О-рамнозы (вентурицидин А). Он не содержит сахара и не является идентичным также с агликоном вентурицидина А и В (СзвНеоОа). Вентурицидин X до сих пор получали не в виде кристаллического вещества, а в виде однородного аморфного порошка при тонкослойной хроматографии. Это жирорастворимое, нейтральное, бесцветное вещество, растворимое, между прочим, в метаноле, этаноле, ацетоне, этнлацетате, хлороформе и метиленхлориде.
Элементарный анализ, %: С 66,35; Н 9,18; О 24,90.
Мол. В. (осмометричеокий метод на основании паров в, метиленхлориде) равен 701. Эти данные соответствуютбрутто-формуле
CsgHsiOi, (мол. в. 709; С 66,077о; Н 9,10%; О 24,83%) и CsgHciOio (мол. в. 692; С 67,60%; Н 9,31%; О 23,09%). б1,5° ( в хлороформе).
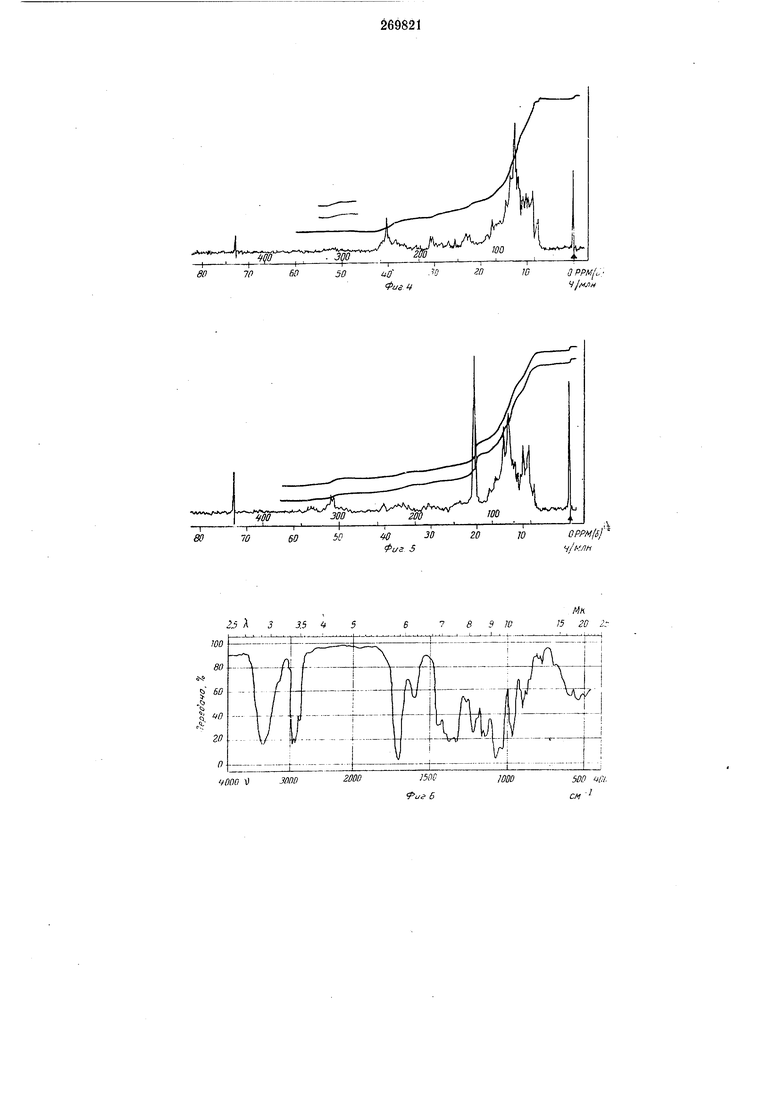
IR-спектр в бромистом калие показывает ленты при 3480, 2965, 2942, 2875, 1702, 1643, 1452, 1382, 1300 (плечо), 1279, 1232, 1222, 1184, 1169 (плечо), 1129, 1095, 1052, 984, 910, 880, 870, 850, 780, 752, 718 сл-i (см. фиг. 1). NMRспектр в дейтерохлороформе, 60 МС, изображен на фиг. 2.
Ультрафиолетовый спектр в чистом спирте указывает следующие максимальные данные л 220 нм (lege 4,47; плечо); нм (Ieg8 4,50); i 232,5 нм (,47); нм (iegs 4,25); . 295 нм (,53, плечо).
При тонкослойном хроматографировании на селикагеле (агент текучести этилацетат) значение Rf равно 0,80, т. е. на много выще, чем у вентурицидинов А и В (вентурицидин А 0,49; вентурицидин В 0,41).
При гидрировании вентурицидина X на угле палладия в метаноле поглощается приблизительно 2 моль водорода. Тетрагидровентурицидин X образует бесцветные кристаллы с т. нл. 156-157°С. Элементарный анализ, %: С 67,39; 67,11; П 9,91; 9,89; мол. в. 765 (оомометрический метод при использовании паров в этилацетате). Этим данным соответствует брутто-формула CgHcgO;., (вычислено С 67,21%; Н 9,84%; мол. в. 697). Вероятная брутто-фор. мула вентурицидина X CsgneiOio.
Вращение тетрагидронроизводного ajgfg - 48,5° (с 0,968% в хлороформе).
Ультрафиолетовый спектр в чистом спирте показывает максимальные значения при л 212 нм (,88) и /.275 нм (Ieg8 2,20). чо), 2960, 2940, 2875, 1732, 1708, 1697, 1625, 1457, 1411, 1395, 1381, 1370, 1339, 1270, 1242, 1225, 1215, 1190, 1170 (плечо), 1133, 1089, 1052 (плечо), 1029, 1011, 989, 933, 908, 882, 849, 839, 808, 796, 773, 746, 729, 695, 593, слгп (см. фиг. 3). NMR-cneKxp в СОСЬ тетрагидровентурицидина X.показан па фиг. 4. Вентурицидин X и его тетрагидропропзводное возможпо ацилировать обыкповепны.м способом, например, при помощи галогенидов кислот и особенно галоге11ангидридов, например, таких алифатических, аралифатических, ароматических или гетероциклических карбоновых кислот (особенно низших л ирных кислот), как уксусная кислота. При ацетилировании тетрагидровентурицидина X получают производное ацетилена в виде бесцветного масла. Инфракрасиый спектр этого соединения в дейтерохлороформе показан на фиг. 5. IR-спектр в хлороформе показывает ленты при 3460, 1733, 1705 (плечо), 1457 н 1370 слг i. NMD-спектр в CDCls показывает сигналы нри 6 2,02 ррт (s, ЗН); 2,08 ррт (s, са. 9Н). (Здесь и далее сокран1,ение ррт обозначается Ч/1 млн). При кислом метанолизе получают приблизительно пять продуктов реакции, из которых три хроматографически в чистой форме в виде бесцветных масел. Метилгликозиды при этом не получаются. NMR-сиектры продуктов показывают ОСНз-сигиалы, которые могут возникнуть из метанолиза одного из лактоновых колед. На наличие (макроциклического) лактонового кольца указывает также соответствующий -СОО-СН группе сигпал 6 5,0 ррт, который встречается в негидрированном и гидрированном вентурицнднне X. Три остальных сигнала в этой области, которые показывает только негндрированный продукт, иринадлежат к атомам водорода в местах двойной связи. Сиигулет при б 2,5 ррт (фиг. 2) должен находится в С-метиловой группе, так как этот сигнал отсутствует в спектре гидрированного продукта тоже. В связи с ультрафиолетовым спектром, который соответствует одиому конъюгированному диену, можно счнтать одну нз частичных формул I а и I б частью структуры Помимо этой диеновой системы имеется еще одна неконъюгированная кетогрупиа (плечо при приблизительно 295 нм в ультрафиолетовом спектре вентурицидина X и при приблизительно 275 нм в гидрированном продукте). Из NMR-епектров выводят примерно Ш метилосродного скелета, похожего на классические макролиды эритномицинового типа. Для вентурицидина А предлагается фор.мула C.i3H7iN6i2. Структура соединения не выяснена. В связи с исследованием нового антибиогика вентурицидииа В выяснены структуры частичных фрагментов вентурицидина В. Для ве1ггурицидина В из анализов выводится формула С оНтоОц. Таким образом, вентурицидин В на CONH меньше вентурицидина А. На основании инфракрасного спектра (фиг. 6 и 8) можно предполагать, что вентурицидин А является сложным эфиром карбамииовой кислоты вентурицид на В, так как максимум при 1605 см 1 у вентурнцидина В отсутствует. Это подтвери дается также и тем, что вентурицидин В дает три-о-ацетилпроизводное, в то время как вентурнцидин А лишь ди-о-ацетилцроизводное. Это предположение подтверждено получением из вентурицидина А и В по одному сахарообразмому продукту расщепления и выяснением их взаимоотношения и построения. Вентурнцидин .- при метанолизе с кисЛСТ11ЫМ катализатором ирн .мягких условиях среди нрочего дает кристаллический метилгликозид CsHisNOs (I). Посредством гидролиза с гидроокисью оария отщеилена кароамоиловая группа и получен метилгликозидС-НмО (И) дидезоксигексозы. Из N.MR-спектра для метилгликозида CgHisKOs выводят следующее построение При этом распределение отдельных сигналов поддерживается расценлением спина (см. пример 1). Сигнал при б 4,86 ррт относится к протону в третьей позиции. Его .химическое с.мещенне соответствует смещению водорода около ацнлокснгрупны. К атому водорода Н-4 должен быть отнесен сигнал при б 3,21 ррт. При С-4, таки.м образом, должна быть свободная гидроксильная группа, в то время как карбамоиловый остаток у С-3. Сигнал Н-1 (б 4,73 ррт) двойной доблет с малой постоянной сцепления Jle,,8 CpS И Jle,2a 1,5 CpS. ОтСЮда вывод Тт, с одной стороны, экваториальное положенне Н-1, с другой стороны, - позицию 2СН2-группы, которая также вытекает пз расцепления спина. Постоянные сцепления J2, 11,5 cps, Лз,4 9 cps и J4,5 9 cps доказывают осевое ноложение атомов водорода при С-3, С-4 и С-5. Дублет при 6 1,33 для одной СНа-СН-группы показывает, что соединение - 6-дезоксисахар. Продукт расщепления из вентурицидина А, таки.м образом, является З-о-карба.моли-2-дезоксирамнозой. Гидтйлгликозит а-метил-2-дезокси-В-рамнозид C7Hi4O4 построения II:R CH3 III:R H То же соединение нолучают при метанолизе вентурицидина В. При гидролизе II получают свободный сахар III, который показывает в воде оптическое вращение а + 19,9° (окончательная величина через 90 мин). Агликон вентурицидина А и В в чистом виде еще не получен. На основании тонкослойнохроматографической реакции и NMR-cneKTpOB предполагают, что оба антибиотика содерлсат одинаковый агликон. Вентурицидин В и вентурицидин X обладают хорошим антимикробным, в частности фитопатогенным, действием, более эффективным, чем у вентурицидина А. В табл. 1 дан спектр действия вентурицидина А, В и X в разных концентрациях на различные грибы на диффузионных пластинах (диаметр пропитанных раствором антибиотиков фильтровых кружков 6 мм). Цифры в скобках означают неполное торможение, черточки - эксперимент не был проведен. Табл. 1 указывает также, что антибиотики при проверенных максимальных концентрациях (10 мг/мл)) не действуют на Saccharomyces cerevisiae. Это имеет значение для применения Ёентурицидина X и (или) В в качестве фунгицидов в виноградниках. Остатки органических фунгицидов, применяемых в виноградниках, в урожае исчисляются в 10 ррт. Однако количество, равное 3-5 ррт, уже тормозит брожение (Vegeler и. Geelanener, Zeitschr. fui Obst- und Weinbau, 103, 494-504, 1967). Так как граница действия вентурицидииа X и В на дрожжи лежит намного выше, рекомендуется применять их в качестве фунгицидов в виноградниках. При борьбе с фитопатогенными гирами, например Aspergillus niger, Alternaria tennis, Botrytis cinerea, Cercospora melonis, Didymella Lycopersici, Fusarium nivale, Glemerella cingulata, Helminthosporium avenae usf. и др., антибиотики можно применять в виде жидких средств (растворы, взвеси или эмульсии), или в твердой форме (грануляты, порошкообразные и распыляемые средства). Для получения непосредственно легкорасиыляемых растворов антибиотиков берут, например, фракции минеральных масел от высокого до среднего диапазона кипения: дизельное масло или керосин, масло каменноугольной смолы и растительные или животные масла, а также углеводороды, такие как алкилированные нафталины, тетрагидронафтадин, в некоторых случаях при употреблении смесей ксилолов циклогексанолов, кетонов, далее хлорированные углеводороды, как трихлорэтан и тетрахлорэтан, трихлорэтилен или тритетрахлорбензол. Успешно используют органические растворители с т. кии. выше 100°С. Водные формы антибиотиков готовят из эмульсионных концентратов, паст или смачивающихся порошков. В качестве эмульгаторов и дисперсионных средств употребляются нейоногенные продукты, например продукты конденсации алифатических спиртов, аминов или карбоновых кислот, с длинноцепочечным остатком СИ с 10-20 атомами углерода с окисью этилена, продукт конденсации октадецилалкоголя и 25-30 моль окиси этилена, или продукт конденсации жирной кислоты сои и 30 моль окиси этилена, или продукт конденсации технического олеиламина и 15 моль окиси этилена, или продукт конденсации додецилмеркаптана и 12 моль окиси этилена. Из анионактивных эмульгаторов, которые можно употреблять, следует упомянуть натриевую соль додецилового сложного эфира серной кислоты, натриевую соль додецилового сложного эфира бензолсульфоновой кислоты, калиевую или триэтаноламиновую соль олеиновой или абиетиновой кислоты, или смесей этих кислот, или натриевую соль петролсульфонной кислоты. В качестве катионактивных дисперсионных средств можно употреблять четвертичные аммонийные соединения, например цетилпиридинийбромид или диоксиэтилбензилдодециаламмониумхлорид. Для изготовления порошков и распыляемых средств в качестве твердной основы могут быть использованы тальк, каолин, бентонит, углекислый кальций, фосфорнокислый кальций, а также уголь, пробочная мелочь, древесная мука и другие вещества растительного происхождения. Препараты изготовляют и в виде грануляторов. Добавлением веществ, улучшающих прилипаемость, стойкость к смыванию, распределяемость и внедряемость в другую среду, можно расширить сферу применения препаратов. Добавлять можно жирные кислоты, смолу, клей, казеин или альгинаты. Пример 1. 300 мл питательного раствора, содержащего 20 г соевой муки (с полным содержанием жиров) и 20 г маннита на 1 л, величину рН которого перед стерилизацией доводят раствором гидроокиси калия до 7,5, заливают в колбу Эрленмейера, стерилизуют, охлаждают и инокулируют бактериальной культурой S. aureofaciens NRRL 3399. Затем суспензию инкубируют при 27°С, непрерывно взбалтывая на машине. Через примерно 48 час
культуру переносят в соотношении I : 10 в питательный раствор того же состава, залитый в ферментационное устройство. Инкубирование проводят снова при 27°С и интенсивном продувании воздуха в течение 24 час. Для контроля активности культур на всех этапах работы проводят тест на В. cinerea.
S. aureofaciens NRRL 3399 выращивают по описанному способу в питательном растворе, содержащем 20 г солодового экстракта (содержание твердых веществ примерно 50%), 20 г сухой кукурузной барды (Distillers solubles), 5 г хлористого натрия и 1 г азотнокислого натрия на 1 л.
S. aureofaciens NRRL 3399 выращивают по описанному способу в питательном растворе, содержащем 20 г сухой кукурузной барды, 20 г лактозы, 5 г хлорнстого патрия и 1 г азотнокислого натрия на 1 л.
S. aureofaciens NRRL 3399 выращивают по описанному способу в питательном растворе, содержащем 10 г глюкозы, 5 г пептона, 3 г мясного экстракта, 5 г хлористого натрия и 10 г углекислого кальция на 1 л. Величину рН устанавливают до стерилизации гидроокисью калия до 7,2.
Когда культура начнет проявлять сильное антибактериальное действие, ее о.хлаждают и фильтруют под давлением с добавлением вещества, облегчающего фильтрацию, например Hyfle-Supercel. Фильтрат экстрагируют дважды при том же значении рН (нримерно 7,5- 7,8) половинным количеством этилацетата; при этом вещества, действующие как антибиотики, переходят в этилацетат. Значительные количества антибиотика находятся также в остатке на фильтре. Они извлекаются оттуда многократным экстрагированием метанолом. Метанольные вытяжки выпаривают до небольшого объема в вакууме, разбавляют водой и затем многократно экстрагируют этилацетатом. После выпаривания этилацетатных экстрактов из фильтрата культуры и остатков на фильтре получают из 100 л культурного раствора маслянистый остаток в количестве 80-100 г.
40 г этого остатка иредвар.ительно очищают посредством распределения по Craigy по 190 ступеням. Применяемая при этом система растворителей содержит на .4,25 л четыреххлористого углерода 0,75 л хлороформа, 4 л метанола и 1 л воды. Вентурицидин А, В и X накопляется в ступенях 75-130 (максимально в ступени 100). Эти фракции объединяют и выпаривают досуха в вакууме. Получают 25 г бледно-желтого порошка. 21 г этого вещества распределяют с той же системой растворителей по 600 ступеням. Вентурицидин находится в ступенях 265-396. Выпариванием в вакууме из ступеней 265-308 получают 5,1 г вентурицидина В и X, из ступеней 309-328 - 5,4 г вентурицидина В и ХХА, а из ступеней 329- 396-10,1 г вентурицидина А и X. Вещества дают в тонкослойной хроматограмме на селикагеле 254 (готовые плитки фирмы Мерк) с
этилацетатом в качестве агента текучести еледующие значения Rf (пятна проявлены опрыскиванием концентрированной серной кислотой и нагреванием до 140°С): веитурицидин А
0,49; Вентурицидин В 0,41; Вентурицидин X 0,80. Три смеси хроматографируют на колонках селикагеля фирмы хМерк. Из остатка от вынаривания фракции 329-396 при хроматоррафировании на 250 г селикагеля (Мерк) и
элюировапня 1,5 л смеси хлороформа и этилацетата (1:1) получают 1,85 г вентурицидина X в виде желтоватого аморфного порошка с характеристиками, указанными в общей части описания.
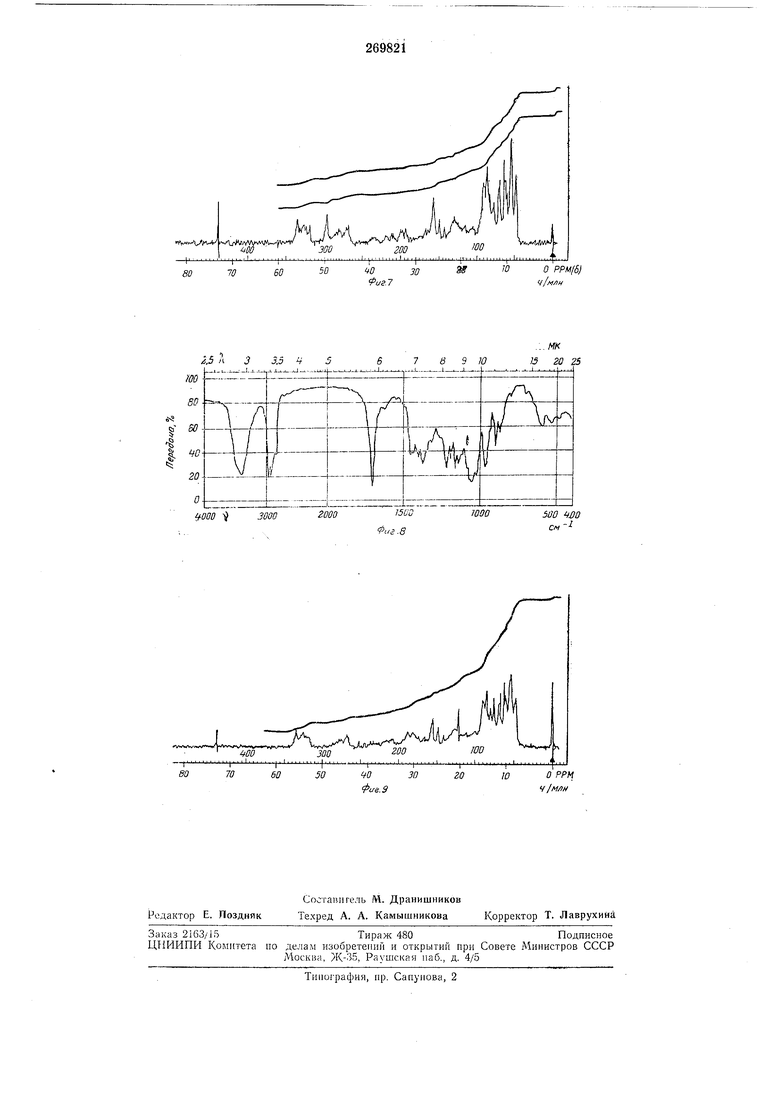
Вслед за тем остаток фракции 329-396 элюируют 1 л этилацетата. При этом кристаллизацией из хлороформэфира получают 5,27 г вентурицидина А в виде бесцветных кристаллов с т. пл. , -М19° (концентрация 0,5 в .хлороформе). Спектр IR к Квг (на фиг. 6). Спектр NMR (60 МНг) в CDC1.3 на фиг. 7.
П р и .м е р 2. 3 г вентурицидина X гидрируют в 150 мл метанола с 750 мг 100%-ного палладия на угле в атмосфере водорода. Через 2 час гидрирование ирекращается. Поглощено 237 л;л водорода (20°С, 725 мм рт. ст.), что соответствует примерно 2 моль. Катализатор отфильтровывают, раствор выпаривают и остаток хроматографируют на 30 г селнкагеля. Этилацетатом элюируют 2,56 г тетрагидропроизводного вентурицидина X в виде бесцветного вепдества, кристаллизующегося при смачивании эфиром. Свойства соединения указаiibi в общей части описания.
Пример 3. 100 мг тетрагидровентурицидина X подвергают реакции с 2 мл ангидрида уксусной кислоты и 2 мл пиридина в течение G час при ком атной температуре. Затем раст Ор выпаривают насухо. Хроматографированием на силикагеле (10 г) со смесью хлороформа с этилацетатом (4:1) в качестве элюциоииого средства иолучают 84 лг бесцветного .масла. Свойства этого продукта ацетилировапня тетрагидровеитурицидина X указаны в общей части описания.
Пример 4. 4,31 г остатка от выпаривания фракции 265-308 примера 1 хроматографируют на 350 г селикагеля. Смесью хлороформа и этилацетата (1 : 1) элюируют 1,76 г вентурицидина X. Элюируя этилацетатом, получают 1,23 г хроматографически однородного веитурицидина В. Переосаждением из смеси этилацетата с петролейцым эфиром получают
вещество в виде бесцветного порошка с т. пл.
145-149 С; + 100° (концентрация 0,847
в хлороформе). Спектр IR в бромисто.м калие
на фиг. 8, спектр NMR в CDCls на фиг. 9.
Вычислено, %: С 67,16; Н 9,40; мол. в 751;
С,2П-эО11.
Найдено, %: С 66,86; Н 9,29; мол. в 733. Молекулярный вес определяют осмометрически по давлению в метиленхлориде. П р и м е р 5. 200 мг вентурицидина В аце13
собой, описанным в примере 1 для вентурицидина А. Сырой три-о-ацетилвентурицидин В очищают хроматографией на селикагеле и элюируют этилацетатом. Получают аморфный бесцветный порошок с т. нл. . Спектр NMR в CDCU показывает между прочим сигналы при ,99 ррт (s,3H); 2,01 ррт (S, ЗН) и 2,02 ррт (s, ЗН). Вычислено, %: С 65,73; Н 8,73;
C48H7«Oi4.
Найдено, %: С 65,92; Н 8,54.
Пример 6. 100 мг вентурицидина X растворяют в 1 мл этилцеллосольва, содержащем 10% тритон , и доливают дистиллированной водой до 1 л. Раствором опрыскивают виноградные лозы, например, для борьбы с инфекцией В. cinerea.
Участки опытного виноградника после опрыскивания суспензией второй генерации серой гнили четырехкратно опрыскивают вышеуказанным раствором через промежутки времени в 14 дней. При сравнении с контрольными
14
участками, не подвергавшимися действию раствора, устаповлено хорошее действие раствора против В. cinerea.
Пример 7. Испытуемый раствр билогически активного вещества готовят растворением 10% вентурицидппа В в этилцеллосольве, содержаще.м 10% тритона Х 100, и разбавлеписм дистиллированной водой до требуемой концентрации.
.Молодые листья примерно одинаковой величины саженцев лозы сорта «рислинг сильванер опрыскивают испытуемым раствором и раскладывают для просушки. Другую партию листьев кладут на 48 час в раствор активного
вещества. Обработанные таким образом листья инфицируют водной суспензией конидий В. cinerea и инкубируют при комнатной температуре во влажной ка.мере. По пстечении четырех суток на глаз онредсляют поверхность
листа, изменившую окраску вследствие инфекции возбудителем. Результаты приведены в табл. 2, приче.м в качестве эталона взят 50%ный препарат оксихлорида меди.
Таблица 2






| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения антибиотического комплекса а-28086 | 1975 |
|
SU576966A3 |
| Способ получения антибиотиков | 1967 |
|
SU528883A3 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА А204 | 1971 |
|
SU296323A1 |
| Способ получения антибиотика G-6302 | 1978 |
|
SU1003761A3 |
| Способ получения антибиотического комплекса | 1976 |
|
SU584800A3 |
| Способ получения производных изоксазола | 1986 |
|
SU1493106A3 |
| Способ получения метаболита "а 27 106 | 1974 |
|
SU539538A3 |
| Способ получения баумицина а и в | 1977 |
|
SU867318A3 |
| Способ получения антибиотика | 1978 |
|
SU738517A3 |
| КОНДЕНСИРОВАННОЕ ИНДОЛЬНОЕ ПРОИЗВОДНОЕ ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ АКТИВНОСТЬ АНТАГОНИСТА 5-НТ*004-РЕЦЕПТОРА | 1993 |
|
RU2104279C1 |


Пример 8. Готовят 0,1%-ный водный раствор вентурицидина X, которым профилактически один раз опрыскивают выращенные в теплице растения риса. Через два дня после опрыскивания растения инфицируют суспензией конидий Poricularia oryral и через семь дней осматривают для установления степени поражения грибками. По сравнению с контрольными растениями, не подвергавшимися опрыскиванию, растения иоражаются грибками лишь на 15%.
Предмет изобретения
вептурицидина X, в качестве гриба-нродуцента берут .птамм S. aureofaciens NRRL 3399 (National Regional Research Laboratory USDA).
по Graigy в системе растворителей, содерл ащей четыреххлорнстый углерод, .хлороформ, метанол, воду.
да V 3000
8070
г.5 л J 3,5 f 5
4000 V 000 °°
15 20 25
см 500 Ш
О PPM/SJ
10 Ч
woo 500 WO
fue 3 8. Способ по пп. I-7, отличающийся тем, что вентурицидин X или продукт его гидрироваыия ацетилируют,
25 3 3.5 f
WO
что 1)30DD
о
OPPM/S
80
80
70
О PPM/S}
Ч/M/IM
500 fJJO
0 PPM Ч/МЛН

Авторы
Даты
1970-01-01—Публикация