Изобретение относится к получению нового ряда замещенных у,у-л.илакто11ов дикарбоновых кислот, которые могут найти применение в синтетической химии и фармацевтической промышленности.
Известные соединения .ТДИлактонов, имеющие либо спиро-, либо сларенное бицикли iecKoe строение
/°Vo
°t
-R
R-1
R-Д
-R
получают при гидробромировании, например, диаллилмалонового эфира.
По предлагаемому способу у.ТД лактоны общей формулы
X
HsCgOOC C
СООСгНз
пли
f/
С
10 где R-Ci-Со-алкил или бензил;
X и Y -водород, или X -водород, Y -
метил, или X - метил, Y - хлор,
получают при взаимодействии тетраэтилового
15 эфира 1,6-диалкилгексен-3-тетракарбоновой-1, 1,6,6 кислоты или диэтилового эфира 2,7-диалкилоктен-4-дикарбоновой-1,8 кислоты с бромом в среде четыреххлористого углерода или хлороформа при температуре не выше
20 10°С, преимущественно О-5°С, с последующим выделением целевого продукта известными приемами. Выход до 88%.
Схема реакции
COOC.HSСООСгНд
,1I ,Вгг
R (;-СИ,-СХ СУ-СНг-С-Н -г:г,
(jti, ь J иСООС Н
гП5
С- СИ г- СЛВт-CYBr-CHa- C-R
СООС,Н
2 5
R НлС.ООС пример 1. В колбу, охлаждаемую льдом с солью до -5°С, помещают смесь 10,2 г (0,0199 моль) тетраэтилового эфира 1,6-днизоамилгексен-3-тетр акар боковой-1,1,6,6 кислоты и 50 мл ecu и при перемешивании прикапывают смесь 3,5 г (0,022 моль) брома в 50 мл ecu с такой скоростью, чтобы температура была О-5°С. По окончании прикапывания (около 0,5 час избыток брома обесцвечивают раствором тиосульфата натрия. Маслянистый слой отделяют, водный - экстрагируют эфиром, От экстракта и маслянистого слоя в вакууме, создаваемом водоструйным насосом, отгоняют растворители, остаток фракционируют в глубоком вакууме. Получают 8 г (88% от теории) у, -1 :лла}. 2,7-диизоамил-2,7-дикарбэтокси - 4,5-диоксиоктандикарбоновой-1,8 кислоты, т. кип. 240-246°С/ 1,4685; df 1,0925; /2,5 мм рт. ст., Найдено, %: С 63,77; Н 8,25; MR C24H3sOg. Вычислено, %: С 63,44; Н 8,37; MRn 115,28. При титровании 0,1280 г спиртового раствора у,у-л11лактона 2,7-диизоамил-2,7-дикарбэтокси-4,5-диоксиоктандикарбоновой-1,8 кислоты на холоду затрачено 0,1 мл 0,LY NaOn,
СрОСгНз i . -гСгНзВг
СООСгНэ
X Y
О о R f N;
Таблица 1 а при нагревании 5,8 мл 0,N NaOH, т. е. основность О и 2,05 соответственно. В ИК-спектре иолученного лактона обнаружены интенсивные полосы поглощения при 1728 и 1768 слг-. В табл. 1-3 приведены константы соединений, 1Л1еющих различные значения R. Пример 2. Аналогично примеру 1 бромироваиием 21,4 г (0,05 г-моль) тетраэтилового эфира 1,6-диэтилгексен-3-тетракарбоновой-1,1, 6,6 кислоты получают 15,9 г (86% от теории) у,7-дилактоиа 2,7-диэтил-2,7-дикарбэтокси-4,5диоксноктандикарбоновой-1,8 кислоты, т. кип. 230°С/3 мм рт. ст.; 1,4700; df 1,1694. Пайдено, С 57,91; П 7,24; MRp 88,27. CisnseOs. Вычислено, %: С 58,37; Н 7,03; MRr, 87,56. Основность на холоду и при нагревании О и 2,2 соответственно. Пример 3. Подобно примеру 1 из 24,2 г (0,05 моль) тетраэтилового эфира 1,6-дибутилгексеи-З-тетракарбоиовой-1,1,6,6 кислоты получают 18,1 г (85% от теории) 2,7-дибутил,6-дикарбэтокси-4,5 - диоксиоктандикарбоновой-1,8 кислоты, т. кип. 260-2QS°C/5 мм рт. ст. ,4713; df 1,1183.
Таблица 2

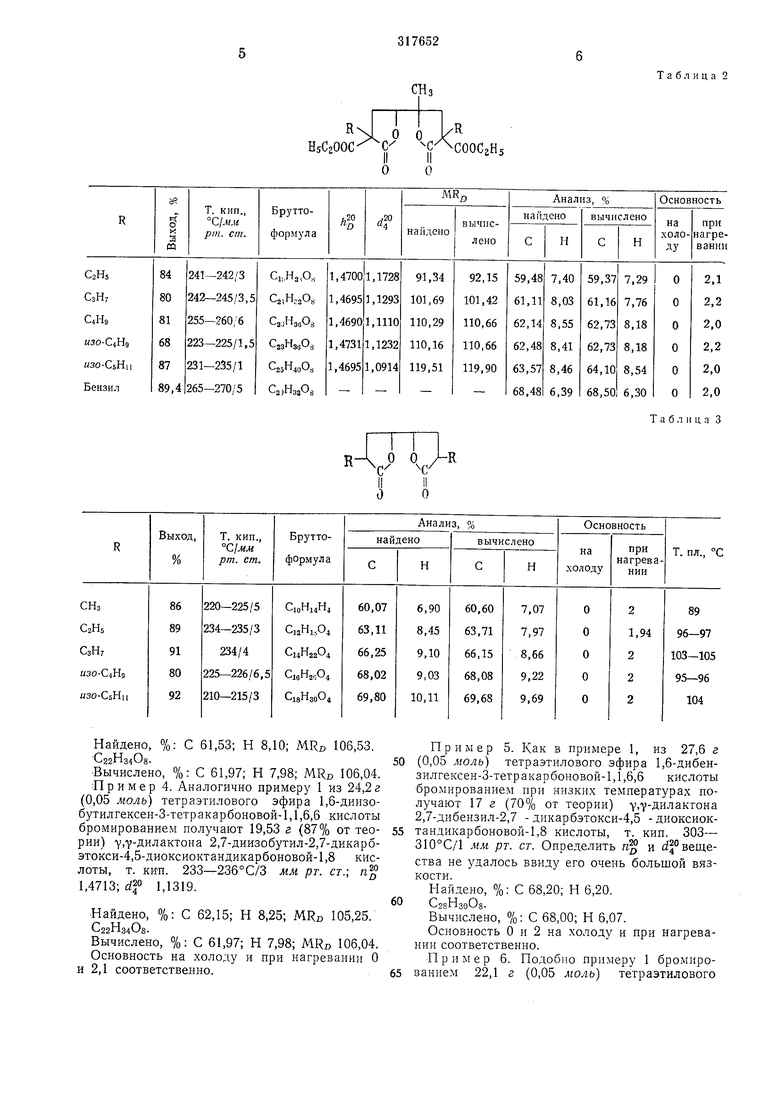



Найдено, %: С 61,53; Н 8,10; MRo 106,53. С22Нз4О8. Вычислено, %: С 61,97; Н 7,98; MRo 106,04. Пример 4. Аналогично примеру 1 из 24,2г (0,05 моль) тетраэтилового эфира 1,6-диизобутилгексен-З-тетракарбоновой-1,1,6,6 кислоты бромированием получают 19,53 г (87% от теории) Y.V-ДИлактона 2,7-диизобутил-2,7-дикарбэтокси-4,5-диоксиоктандикарбоновой-1,8 кислоты, т. кип. 233-236°С/3 мм рг. ст.; 1,4713; df 1,1319. Найдено, %: С 62,15; Н 8,25; MR 105,25. С22Нз4О8. Вычислено, %: С 61,97; Н 7,98; MRo 106,04. Основность на холоду и при нагревании О и 2,1 соответственно.
Т а б л II ц а 3
-R
0 О С С 50 55 60 Пример 5. Как в примере 1, из 27,6 г (0,05 моль) тетраэтилового эфира 1,6-дибензилгексен-3-тетр акарбоновой-1,1,6,6 кислоты бромированием при низких температурах получают 17 г (70% от теории) Y VДилaктoнa 2,7-дибензил-2,7 - дикарбэтокси-4,5 -диоксиоктандикарбоновой-1,8 кислоты, т. кип. 303- 310°С/1 мм рт. ст. Определить п и df вещества не удалось ввиду его очень большой вязкости. Найдено, %: С 68,20; Н 6,20. СгвНзоОзВычислено, %: С 68,00; Н 6,07. Основность О и 2 на холоду и при нагревании соответственно. эфира 1,6-диэтил-З-метил гексеп-3-тетр акар боновой-1,1,6,6 кислоты 8 г брома (0,05 АЮЛЬ} в хлороформе или CCLi иолучают 16,13 г (84% от теории) 2,7-диэтнл-2,7-Л11карбэтокси-4-метил-4,5- диоксиоктапдикарбоновой-1,8 кислоты, т. кип. 241-242°С/ /3 .K.w рт. ст.; 1,4700; df 1,1728. Найдено, %: С 59,48; Н 7,40; МНд 91,34. CigHgsOs. Вычислено, %: С 59,37; Н 7,29; MR« 92,15. Основность на холоду и при нагревании О и 2,1 соответственно. Пример 7. Как в нрнмере 1, бромироваиием 23,5 г (0,05 моль) тетраэтилового эфира 1,6-диПропил-З-метилгексен-З-тетракарбоновой-1,1,6,6 кнслоты получают 16,5 г (80% от теории) Y 7 -i T i on3 2,7-дннропил-2,7-дикарбэтокси-4-метил-4,5 - диоксиоктандикарбоновой-1,8 кислоты, т. кип. 242-245°С/3,5 мм рт. ст.; «20 1,4695; df 1,1293. Найдено, %: С 61,11; Н 8,03; MRo 101,69. C2lH3208. Вычислено, %: С 61,16; Н 7,76; MRi, 101.42. Основность о и 2,2 на холоду н при иагрсвании соответственно. Пример 8. Лналог 1чно прнмеру 1 из 24,9 г (0,05 моль тетраэтилового эфира 1,6дибутил-3-метилгексен-З-тетракарбоновой - 1, 1,6,6 кислоты получают 17,82 г (81% от теории) чТДил2ктона 2,7-дибутил-2,7-дикарбэтокси - 4 - метил - 4,5 - дпоксиоктандикарбоновой-1,8 кислоты, т. кип. 255-260°С;6 мм рт. ст.; «I 1,4690; df 1,1110. Найдено, %: С 62,34; Н 8,55; MRz, 110,29. / ТТ РЧ Вь1числено, %: С 62,73; Н 8,18; MRn 110,66. Основность о и 1,98. Пример 9. Подобно примеру 1 из 24,9 г (0,05 моль тетраэтилового эфира 1,6-диизобутил-3-метилгексен -З-тетракарбоновой-1,1,6,6 кислоты получают 15 г (68% от теории) VV дилактона 2,7-диизобутил-2,7-дикарбэтокси-4метил-4,5-диоксиоктандикарбоновой-1,8 кислоты, т. кип. 223-225°С/1,5 мм рт. ст.; 1,4731; df 1,1232. Найдено, %: С 62,48; Н 8,41; MRi, 110,16. С2зНзв08. Вычислено, %: С 62,73; Н 8,18; MRn 110,66. Основность о и 2,1 на холоду и при нагревании соответственно. Пример 10. Как в примере 1, из 26,3 г (0,05 моль тетраэтилового эфира 1,6-диизоамил-3-метилгексен-З-тетракарбоновой -1,1,6,6 кислоты получают 20,35 г (87% от теории) у, Дилактона 2,7-диизоамнл-2,7-дикарбэтокси4-метил-4,5-диоксиоктандикарбоновой-1,8 кислоты, т. кин. 231-235°С/1 мм рт. ст.; п 1,4695; df 1,0914. С25Н4о08. Найдено, %: С 63,57; Н 8,46; MRo 119,51. Основность о и 2,3 на холоду и при нагревании соответственно. Пример 11. Подобно примеру 1 из 50,5 г (0,1 г-моль) тетраэтилового эфира 1,6-дипропил-З-хлор-4-метилгексен-З - тетракарбоновой кислоты получают 40,2 г (90% от теории) Y, -дилактона 2,7-дииронил-2,7-дикарбэтокси. 4 - хлор-5 - метил - 4,5 - диоксиоктандикарбоновой-1,8 кислоты, т. кип. 222-223°С/3 ММ рт. ст.; 1,4707; df 1,1445. Найдено, %: С. 56,83; Н 7,35; С 7,38; MR л 108,84. C2iH3i08Cl. Вычислено, %: С 56,44; Н 6,94; С1 7,95; MRn 106,29. Основность на холоду и нри нагревании О и 2,2 соответственно. Пример 12. Бромированием 28,4 г (0,1 моль диэтилового эфира 2,7-диметилоктен-4-дикарбоновой-1,8 кнслоты при (-10) - (-5) °С в среде CCU с последующей обработкой, как в примере 1, выделяют 19,4 г (86% от теории) у,у-дилактоиа 2,7-диметпл-4,5-диоксиоктандикарбоновой-1,8 кислоты, т. кип. 225-228°С/5 мм рт. ст., который закристалллзопывается в -процессе перегонки. Т. ил. 89°С (из спирта). Найдено, %: С 60,07; Н 6,90. CioHi4O4. Вычислено, %; С 60,60; Н 7,07. Основность на холоду и при нагревании О и 2,17 соответственно. Пример 13. При бромировании 31,2 г (0,1 моль диэтилового эфира 2,7-диэтилоктен-4-дикарбоновой-1,8 кислоты получают 22,6 г (89% от теории) .7-Дилактона 2,7-диэтил-4,5-диоксиоктандикарбоновой-1,8 кислоты, т. кип. 234-235°С/3 мм рт. ст.; 1,4770; df 1,1241. Найдено, %; С 64,20; Н 8,60; MRn 56,54. Вычислено, %: С 63,71; Н 7,97; MR/j 56,79. Основность на холоду и при пагреваиии О и 1,94. Пример 14. Бромированием 36,8 а (0,1 моль диэтилового эфира 2,7-диизобутилоктен-4-дикарбоновой-1,8 кислоты получают 24,8 г (80% от теории) УТ Дилактона 2,7-диизобутил - 4,5 -диоксиоктандикарбоновой -1,8 кислоты, т. кип. 225°С/6,5 мм рт. ст., который сразу закристаллизовывается. Т. пл. 125- 127°С (из спирта). Найдено, %: С 68,02; Н 9,03. С1бН2бО4. Вычислено, %: С 68,08; Н 9,22. Основность на холоду и при нагревании О и 2,0 соответственно. Пример 15. Согласно примеру 1 из 39,6 г (0,1 моль диэтилового эфира 2,7-диизоамилктен-4-дикарбоновой-1,8 кислоты получают 1,1 г (92% от теории) 7ТДилактона 2,7-дизоамил-4,5-диоксиоктандикарбоновой-1,8 кисоты, т. кнп. 211-214°С/2 мм рт. ст., который акристаллизовывается в кристаллы с т. пл. 107°С (из спирта). Основность на хол при нагревании О и 2,0 соответственно. Найдено, %: С 69,50; ,Н 10,00. С18НзоО4. Вычислено, %: С 69,68; Н 9,68. Предмет изобретения Способ получения замещенных у.-дил нов дикарбоновых кислот общей формул НбСгООС и« ОО -Сб-алкил или бензил; ХиУ - водород или X - водород, Y - метил, или X - метил, Y - хлор, отличающийся тем, что соответствующие замещенные тетраэтиловые зфиры 1,6-диалкилгексен-З-тетракарбоновой-1,1,6,6 кислоты или диэтиловые эфиры 2,7-диалкилоктен-4-дикарбоновой-1,8 кислоты обрабатывают бромом в среде четыреххлористого углерода или хлороформа при температуре не выше 10°С с последующим выделением целевого продукта известными приемами,
Даты
1971-01-01—Публикация