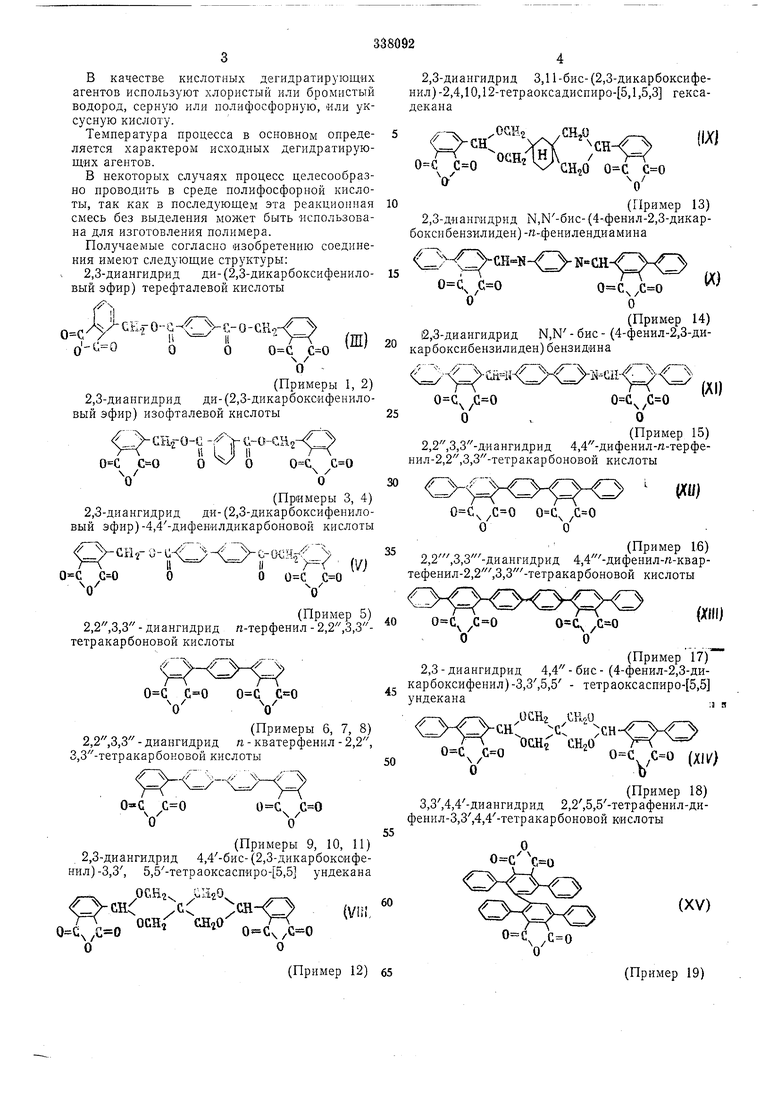
Изобретение касается способа получения новых диангидридов ароматических тетракарбоновых кислот, которые могут найти применение в полимерной промышленности. Получаемые согласно изобретению соединения имеют следующие структурные формулы:где А - фенилен, нафтилен, дифенилен, диметилдйфенилен, дифениленоксид, дифениленметан или одна из следующих групп: -сн ™ в ;ш,OCHj- CHgO -СНг-0-С-В-С-0-СН2- , R - атом углерода или четырехвалентный 1,1,3,3-радикал циклогексана, циклогенсан-5-ола или циклогексан-5-она; В -мета-, пара- фенилен, нафтилен или 4,4-дифенилен; Г - фенилен, нафтилен, дифенилен, диметилдифенилен, дифениленоксид, дифениленметан;DI - фенил; DZ - фенйл или нафтил. Способ заключается в том, что соответствущие диангидриды, содержащие эндо-оксоциклогексеновые систе.мы и имеющие следующие структурные формулы: -А /А/ // о о 0000 где А, Б, DI и D2 - аналогичны указанным значениям, подвергают кислотной дегидратации с последующим выделением целевого продукта известными приемами. В качестве кислотных дегидратирующих агентов используют хлористый или бромистый водород, серную или полифосфорную, «ли уксусную кислоту. Температура процесса в основном опреде- 5 ляется характером исходных дегидратирующих агентов. В некоторых случаях процесс целесообразно проводить в среде полифосфорной кнслоты, так как в последующем эта реакционная 10 смесь без выделения может быть использована для изготовления полимера. Получаемые согласно изобретению соединения имеют следующие структуры: 2,3-диангидрид ди-(2,3-дикарбоксифенило- 15 вый эфир) терефталевой кислоты -GE.fO-C- i li /тгг) iu/ 20 V (Примеры 1, 2) 2,3-диангидрид ди- (2,3-дикарбокоифениловый эфир) изофталевой кислоты25
С-О-СНгЧ
о
(Примеры 3, 4)
2,3-диангидрид ди- (2,3-дикарбоксифениловый эфир)-4,4-дифен«лдикарбоновой кислоты f VCH,-O-U C-0€Hf S . y-t,ri9 VJ .-С о (Пример 5) 2,2,3,3 -диангидрид л-терфенил-2,,3 тетракарбоновой кислоты С-0 о (Примеры 6, 7, 8) 2,2,3,3 - диангидрид п - кватерфенил - 2,2, 3,3 -тетракарбоновой кислоты
О С
О
(Примеры 9, 10, 11)
2,3-диангидрид 4,4-бис-(2,3-дикарбокоифенил)-3,3, 5,5-тетраоксаспиро- 5,5 ундекана
/СНг СНгО
( /сС /ш
(Vl.l
° о-с;,, оо
(Пример 15)
2,2,3, ангидрид 4,4 -дифенил-л-терфенил-2,2,3,3 -тетракарбоновой кислоты
V4
(Пример 18)
3,3,4,4-диангидрид 2,2,5,5-тетрафенил-дифенил-3,3,4,4-тетракарбоновой кислоты
(XV) 2,3-диангидрид 3,11-бис-(2,3-дикарбоксифел)-2,4,10,12-тетраоксадиспиро- 5,1,5,3 гексаканас оНо (Пример 13) 2,3-диангидрид N,N-биc-(4-фeнил-2,3-дикapкснбензилиден)-п-фенилендиамина Г- (X) , о (Пример 14) е,3-диангидрид М,Ы-бис-(4-фенил-2,3-дирбоксибензилиден)бензидина ... VtMi о (Пример 16) 2,2,3,3 -диалгидрид 4,4 -дифенил-п-кварефенил-2,2,3,3 -тетракарбоновой кислоты о (Пример 17) 2,3 - диангидрид 4,4 - бис - (4-фенил-2,3-диарбоксифенил)-3,3,5,5 - тетраоксаспИро- 5,5 ндекана х;-А ч СКоО I -O-CR: У -сн- V Л OCHf СНгО . (xii/) Ъ
Пример 1. 2 ммоль (1,04 г) 2,3-диангидрида ди-(2,3 - дикарбокси-1,4-оксо-5-циклогексенилового эфира) терефталевой кислоты в 170 мл ледяной уксусной кислоты обрабатывают током сухого хлористого водорода при 100°С в течение 12 час. Растворитель удаляют в вакууме, продукт перекрксталлизовывают из этилацетата, и получают 72% (0,7 г) 2,2-диаигидрида ди- (2,3-дикарбоксифенилового эфира) терефталевой кислоты, т. пл. 216- 217°С, кислотное число 457 (рассчитано 460). Найдено: С 64,2; Н 3,18; рассчитано для СгаНиОю; С 64,1 ;Н 2,98.
Пример 2. К2 ммоль (1,04 г) 2,3-Д1иаигидрида ди-(2,3-дикарбокси-1,4-оксо-5-циклогексенилового эфира) терефталевой кислоты в 130 мл ледяной уксусной кислоты добавляют 4 капли концентрированной серной кислоты и перемешивают 62 час при 20°С. Продукт высаживают в воду, промывают на фильтре, и после перекристаллизации из этилацетата получают 80% (0,778 г) 2,3-диангидрила ди-(2,3дикарбоксифенилового эфира) терефталевой кислоты.
Пример 3. 2 ммоль : (1,04 г) 2,3-диа1Нгидрида ди-(2,3-дикарбокси-1,4-оксо-5-циклог-ексенилового эфира) изофталевой кислоты в 40 мл полифосфорной кислоты перемешивают 72 час при 30-40°С. Продукт высаживают в воду, промывают водой до нейтральной реакции и перекристаллизовывают из этилацетата. Получают 54% (0,525 г) 2,3-диангидрида ди(2,3-дикарбоксифенилового эфира) изофталевой кислоты, т. пл. 187-189°С, кислотное число 446 (рассчитано 460). Найдено: С 63,84; Н 3,12; рассчитано для С.сНмОю; С 64,1; Н 2,98.
Пример 4. 2 ммоль (1,04 г 2,3-диангидрида ди - (2,3 - дикapбoкcи-l,4-oкco-5-циклoгeкceнилoвoгo эфира) изофталевой кислоты обрабатывают по методике примера 1 и получают 76% (0,738 г) 2,3-диангидрида ди-(2,3-дикарбоксифенилового эфира) изофталевой кислоты.
Пример 5. 1,68 ммоль (1 г) 2,3-диангидрида ди- (2,3-дикар бокси-1,4-оксо-5-ик; логекоенилового эфира) -4,4-дифенилдикарбоновой кислоты обрабатывают по меттике примера 2 и получают 68% (0,638 г) 2,3-диангидрида ди- (2,3-дикарбоксифен«лового эфира) -4,4-дифеэилдикарбоновой кислоты, т. пл. 218-219°С, кислотное число 392 (рассчитано 399). Найдено: С 68,3; Н 3,40; рассчитано для C-.c..Oio: С 68,3; Н 3,21.
|Пр1Имер 6. Б ммоль (2,03 г) 2,3-диангидрида 1,4-ди-(2,3-дикарбокси-1,4-оксоц11клогексен-б-ил) бензола, 42 мл концентрированной соляной кислоты, 345 мл ледяной уксусной кислоты нагревают 48 час при 100°С. Растворитель удаляют в вакууме, и продукт хроматографируют на нейтральной окиси алюминия в тетрагидрофуране и получают 62% (1,17 г) диангидрида «-терфенил-2,2,3,3 -тетракарбоновой кислоты, т. пл. 300°С. Кислотное число: найдено 584, рассчитано 605. Найдено
С 70,62; Н 3,03; рассчитано для C92HioO6: С71,4;-Н2,71.
Пример 7. 5 ммоль (2,03 г) 2,3-диангидрида 1,4-ди-(2,3-дикарбокси-1,4-оксоциклогексен-5-ил) бензола, 167 мл ледяной уксусной кислоты в присутствии 2 капель концентрированной серной кислоты перемешивают 24 час при 20°С. Раствор высаживают в эфир, и продукт хроматографируют на нейтральной окиси алюминия в тетрагидрофуране, и получают 74% (1,36 г) диангидрида п-терфеиил-2,2, 3,3 -тетракарбоновой кислоты.
Пример 8. 2 ммоль (0,812 г) 2,3-диангидрида 1,4-ди(2,3-дикарбокси-1,4-оксоциклогексен-5-ил) бензола в 75 мл 116%-ной полифосфорной кислоты перемешивают 5 дней при 40-50°С. Раствор высаживают в воду, осадок отфильтровывают, растворяют в 5% КОН, фильтруют и высаживают 5%-ной HCI. После
нагревания (4 час) при 100°С в уксусном ангидриде получают 56% (0,41 г) диаигидрида п-терфенил-2,2,3,3 -тетракарбоновой кислоты. Пример 9. 2 ммоль (0,944 г) 2,3-диангидрида 4,4-ди-(2,3-дикарбокси-1,4-оксоциклогексен-5-ил) дифенила обрабатывают по методике примера 6, и получают 47% (0,42 г) диангидрида /г-кватерфенил-2,2,3,3 -тетракарбоновой кислоты, т. пл. 300°С. Кислотное число: найдено 492, рассчитано 503. Найдено
С 75,0; Н 3,51; рассчитано для CoeHj-tOe: С 75,3; Н 3,14.
Пример 10. 2 мм.оль (0,944 г) 2,3-диангидрида 4,4-ди-(2,3-дикар бокси-1,4-оКСоциклогексен-5-ил) дифенила обрабатывают по методике примера 7 и получают 53% (0,47 г) диангидрида п-кватерфенил - 2,2,3,3 - тетракарбоновой кислоты.
Пример 11. 2 ммоль (0,944 г) 2,3-диангидрида 4,4-ди-(2,3-дикарбокси-1,4-оксоциклогексен-5-ил) дифенила обрабатывают по методике примера 8, и получают 67% (0,696 г) диангидрида п-кватерфенил-2,2,3,3 -тетракарбоновой кислоты.
Пример 12. 2 ммоль (0,96 г) 2,3-диангидрида 4,4-бис-(2,3-дикарбокси-1,4-оксоциклогексен-5-ил) -3,3,5,5-тетраоксаспиро- 5,5 ундекана в 100 мл ледяной уксусной кислоты обрабатывают сухим хлористым водородом при 100°С в течение 16 час. Раствор высаживают в эфир, и продукт перекристаллизовывают из метанола с активированным углем. Получают 51% (0,454 г) 4,4-бис-(2,3-дикарбоксифенил)-3,3,5,5-тетраоксаспиро- 5,5 ундекан-2,3 диангидрида, т. ил. 284-286°С. Кислотное число 490 (рассчитано 495). Найдено С 61,3; Н 3,51; рассчитано C sHisOio: С 61,0; Н 3,40.
Пример 13. 2 ммоль (1,12 г) 2,3-диангидрида 3,11 -бис- (2,3-дика рбокси-1,4-оксоциклогексен-5 - ил) - 2,4,10,12 - тетраоксадиспиро 5,1,5,3 гексадекана нагревают в 75 мл 116%ной полифосфорной кислоты 4 дня при 30- 40°С. Раствор выливают в воду, осадок промывают, и после перекристаллизации из этада 3,11-бис-(2,3-дикарбоксифенил) - 2,4,10,12тетраоксадиспиро- 5,1,5,3 гексадекана, т. пл. 261-262°С, кислотное число 430 (рассчитано 430). Найдено С 64,42; Н 4,74; рассчитано для C28H24Oio: С 64,6; Н 4,63. Пример 14. 2 ммоль (1,24 г) 2,3-дианг«дрида Ы,М-бис-(4-фенил-2,3-дикарбокси-1,4-оксоциклогексен-5-илиден) . га-фенилендиамина растворяют в 170 мл ледяной уксусной кислоты, добавляют 21 мл концентрированной соляной кислоты и нагревают 48 час при 100°С. Растворитель удаляют в вакууме, и продукт перекристаллизовывают из ацетонитрила. Получают 72% (0,825 г) 2,3-диангидрида N,Nбис - (4-фенил-2,3-дикарбокоибензилйден) - пфенилендиамина, не плавится до 300°С. Кислотное число 372 (рассчитано 389), найдено С 74,5; Н 3,56; N 5,12; рассчитано для С.збНгоМгОб: С 75,0; Н 3,48; N 4,87. Пример 15. I ммоль (1,37 г) М,М-бис-(4фенил-2,3-дикарбокси - 1,4 - оксоциклогексен5-илиден)-бензидин-2,3-диангидрида растворяют в 180 мл ледяной уксусной кислоты, добавляют 8 капель концентрированной серной кислоты, и реакционную смесь перемешивают 56 час при 20°С. Продукт выливают в 0,5 л воды, осадок отфильтровывают, промывают водой и перекристаллизовывают из ацетонитрила. Получают 64% (0,855 г) N,N-6HC-(4-cbeнил-2,3-дикарбоксибензилиден) - бензидин-2,3диангидрида, не плавится до 300°С. Кислотное число 342 (рассчитано 348). Найдено С 77,0; Н 3,52; N 4,47; оассчитано для C4oH24N2Ofi: С 77,2; 3,73; N 4,35. Пример 16. ммолъ (2,7931 2,3-диангидрида 1,4-ди-(4-фенил-2,3-дикарбокси-1,4-оксоц«клогекс€н-5-ил) бензола растворяют в 400 мл ледяной уксусной кислоты и при 100°С пропускают газообразный бромистый водород в течение 12 час. Растворитель удаляют в вакууме, и продукт перекристаллизовывают из ацетилацетона. Получают 78% (2.04 г) диангидрида 4,4 -дифенил-а-терфенил-2.2.3.3 -тетракарбоновой кислоты, т. пл. 300°С, кислотное число 432 (рассчитано 429). Найдено С 77,8; Н 3,58; рассчитано для Сз4Н18Об: С 78,2; Н 3,45. Пример 17. 2 ммоль (1.268 г) 2,3-диангидрида 4,4-ди - (4-фенил-2,3-дикарбокси-1,4оксоциклогексен-5-ил) дифенила в 40 мл 116%-ной полифосфорной кислоты перемешивают 5 дней при 20°С. Раствор вливают в воду, осадок отфильтровывают, промывают водой и перекристаллизовывают из ацетилацетона. Получают 51% (0,603 г) диангидрида 4,4 -дифенил-п-кватерфецил - 2,2.3,3--тетрякарбоцовой кислоты, т. пл. 300°С, кислотное число 384 (рассчитано 375). Найдено С 79,2; Н 3,82; рассчитано для С,)оН22Об: С 80,3; Н 3,68. Пример 18. К 2 ммоль (1,28 г) 2,3-диацгидрида 4,4-бис-(4-фенил-2,3-дикарбокси-1,4оксоциклогексен-5-ил) - 3,3,5,5-тетраоксаспиро- 5,5 ундекана в 100 мл ледяной уксусной кислоты прибавляют 4 капли концентрирован ной серной кислоты, выдерживают 7 дней при 20°С, растворитель удаляют в вакууме, и продукт перекристаллизовывают из ацетона. Получают 71,8% (0,86 г) 2,3-диангидрида 4,4бис-(4-фенил-2,3-дикарбоксифенил) - 3,3,5,5тетраоксаспиро- 5,5 ундекана, т. пл. 212°С, кислотное число 370 (рассчитано 372), найдено С 69,2; Н 4,13; рассчитано для Сз5Н24О|о: С 69,6; Н 3,98. Пример 19. 1 ммоль (1,268 г) 2,2,5,5тетрафенил - 3,3,4,4 - тетракарбокси-1,1-дициклогексен - 1-ил-3,3,4,4-диангидрида обрабатывают по методике примера 16, и после перекристаллизации из ацетилацетона получают 51% (0,603 г) диангидрида 2,2,5,5-тетрафенил-дифенил-3,3,4,4-тетракарбоновой кислоты, т. пл. 284-286°С, кислотное число 362 (рассчитано 375). Найдено С 80,15; Н 3,84. Рассчитано для С4оН220б: С 80,3; Н 3,68. Предмет изобретения 1. Способ получения диангидридов ароматических тетракарбоновых кислот общих форМУЛили где А - фенилен, нафтилгн, дифенилен, диметилдифенилен, дифениленоксид, дифениленметан или одна из следующих групп: ОСНг.СНгО. -п/ - гтт . / ftv,,. UH t ОСИ СН20 -СНгО-С-В-С-О-СН - . БCH N-Г-N CH- или любые значения А; R - атом углерода или четырехвалентный 1,1,3,3-радикал циклогексана, циклогексан-5-ола или циклогексан-5-она; В-мета-, пара- фенилен, нафтилен или 4,4-дифенилен; Г-фенилец, нафтилен, дифенилеи, диметилдифенилен, дифениленоксид, дифениленметан;DI - фенил; D2 - фенил или нафтил, отличающийся тем, что соответствующие диангидриды, содержащие эндо-оксоциклогексеновые системы и имеющие следующие структурные формулы: 9 - V / т. TV О V г О „ X, у, ,-с .. или 0 л 1оП-ОС /О 00 000 о А Т ие// Y г Д л. хЯч 10 о о о 00 О 10 где А, Б, DI и D2 - аналоличны указанным значениям, подвергают кислотной дегидратации с последующим выделением целевого продукта известными приемами. 2. Способ по п. 1, отличающийся тем, что кислотную дегидратацию ведут в присутствии ледяной уксусной кислоты, концентрированной серной кислоты, газообразных хлористого или бромистого водорода или полифосфорной кислоты, 


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИАНГИДРИДОВ АРИЛЗАМЕЩЕННЫХ | 1972 |
|
SU336981A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОЦИКЛИЧЕСКИХ ПОЛИМЕРОВ | 1971 |
|
SU299169A1 |
| Полимеризационноспособные ароматические олигоимиды и способ их получения | 1975 |
|
SU584014A1 |
| Способ получения полиэфиримидов | 1974 |
|
SU1181553A3 |
| ССОРЗависимый от патента № — Заявлено 22.11.1968 (J6 J219895/23-5)Приоритет 25.11.1967, № 2794/67, ШвейцарияОпубликовано 12.111.1973. Бюллетень № ИДата опубликования описания 17.V.1973М. Кл. С ftSg 20/32УДК 678.675(058.8) | 1973 |
|
SU373951A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИИМИДОВ | 1968 |
|
SU231437A1 |
| Полимеризационноспособные олигоимиды и способ их получения | 1975 |
|
SU550836A1 |
| ЭЛЕКТРОФОТОГРАФИЧЕСКИЙ МАТЕРИАЛ | 1984 |
|
SU1190780A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАНГИДРИДА 4,4´-БИНАФТИЛ-1,1´,8,8´-ТЕТРАКАРБОНОВОЙ КИСЛОТЫ ИЗ ГАЛОГЕНАЦЕНАФТЕНОВ | 2017 |
|
RU2671579C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОДЕРЖАЩИХ ИМИДНЫЕ ГРУППЫ ПЕНОПЛАСТОВ | 2013 |
|
RU2643818C2 |



Даты
1972-01-01—Публикация