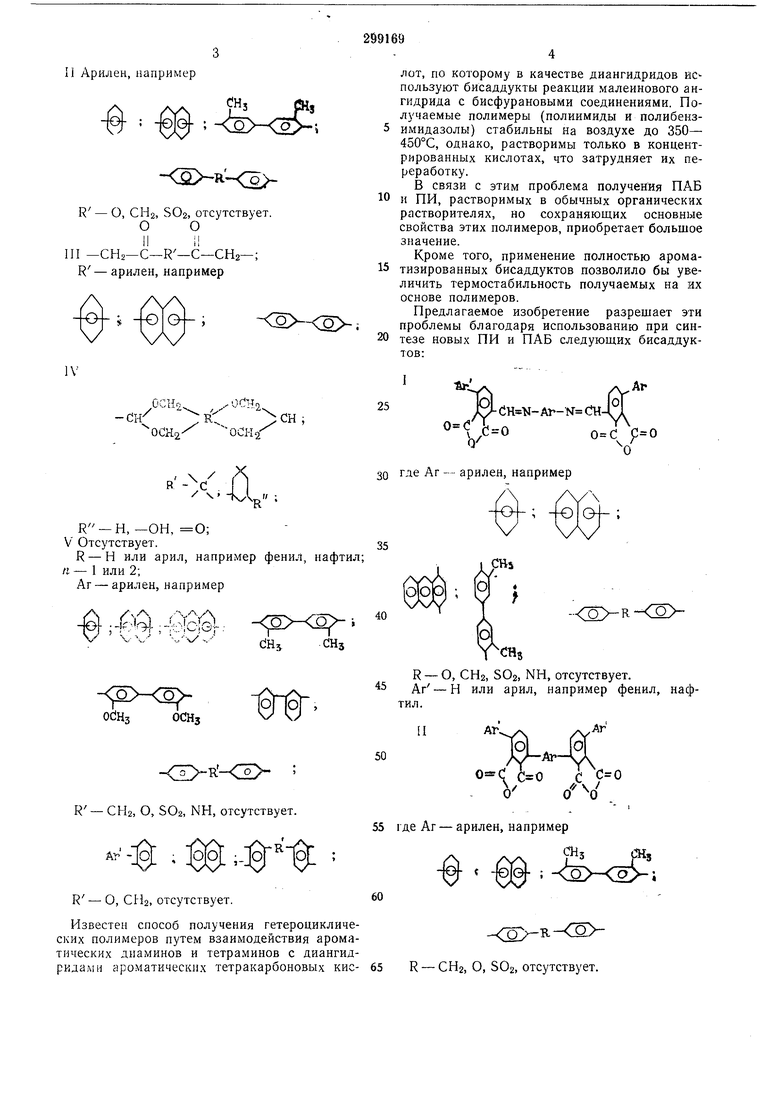
Изобретение относится к технике получения не описанных ранее термостабильных гетероииклических полимеров имидной и ароилеябисбензимидазольной, а также смешанной имидоаронлензбензимидазольной структур, имеющих общие формулы
о Rn
гII /
М-
-l-Ai-N
Uл
ПОЛИМИДЫ (ПИ);
10
- ПОЛИ (ароиленбисбензимидазолы) (ПАБ);
О Rn Rrt
1-Аг-М С М
п
- сополимер имйдоароиленбензимидальной структуры (ПМБ), где М означает: I -CH N-R-N CH-;
R - арилен, например.
,бн.
- S -R-сн
; оТо О
20
R -OiCHa, SOa, NH, отсутствует.
i Арилен, например
- О, СНг, SO2, отсутствует. ОО
IIII
III -СНг-С-R-С-GHz-; R - арилен, например
.
лот, по которому в качестве диангидридов ИС пользуют бисаддукты реакции малеинового ангидрида с бисфурановыми соединениями. Получаемые полимеры (полиимиды и полибензимидазолы) стабильны на воздухе до 350- 450°С, однако, растворимы только в концентрированных кислотах, что затрудняет их переработку. В связи с этим проблема получения ПАБ
и ПИ, растворимых в обычных органических
растворителях, но сохраняющих основные
свойства этих нолимеров, приобретает большое
значение.
Кроме того, применение полностью ароматизированных бисаддуктов позволило бы увеличить термостабильность получаемых на их основе полимеров.
Предлагаемое изобретение разрешает эти проблемы благодаря использованию при синтезе новых ПИ и ПАБ следующих бисаддуктов:
IV
. OCHf
,ОСНо,
СН
ОСН2- 001-12
/
R -С
/ Ч
R
R -а -ОН, О; V Отсутствует.
R-Н или арил, например фенил, п - 1 или 2;
Аг - арилен, например
-& ,т ;4Щ
ч/х-s,-... ч/ .
dHj снз
1
.Аг
-C;H N-A -N CH°1у - О.С
30 где Аг -- арилен, например
тОСНз
R - СЬЬ, О, SOa, NH, отсутствует.
,
00 ..о
R - О, СН2, SO2, NH, отсутствует. 45 Аг - Н или арил, например фенил, нафтил.
II
55 где Аг - арилен, например
Нз Известен способ получения гетероциклических полимеров путем взаимодействия ароматических диаминов и тетраминов с диангидридами ароматических тетракарбоновых кис- 65 R - СН2, О, ЗОг, отсутствует.
Ar - Н или арил, например фенил, нафтил.
Ill
,
СНдОС- Af- СОСН2
с о
арилен, например
IV
V /
где 1 с , -ОН, 0;
JB /
Аг - Н или арил, например фенил, нафтил.
10
15 То1 ../ сне н4.° )сЛ ОСН / ОГН Г 2 ОгС nHaN-Ar-№ О d по( АгХ С с/ Оо 2) форполимер подвергается 20 А внутримолекулярной циклизации с выделением воды: где Аг - фенил. Процесс формирования структуры полимеров включает две стадии: 1) образуется форполимер - полиамидокис) образуется форполимер - полиамидокислота (ПАК) или полиаминоамидокислота (ПААК); температура 20-80°С, растворители - диметилформамид, диметилсульфоксид: r-NH-C-Ar -d-NH4С ПАК) HOni-yVnnu О, II(ПААК) -4Г /NH-c C-NH О. NH2 СООН CiOOHH2NJ i t NHo fnm






| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИАНГИДРИДОВ АРОМАТИЧЕСКИХ ТЕТРАКАРБОНОВЫХ КИСЛОТ | 1972 |
|
SU338092A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАНГИДРИДОВ АРИЛЗАМЕЩЕННЫХ | 1972 |
|
SU336981A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛ ИБЕН;5ИЛ\ИДАЗОЛОВ | 1971 |
|
SU312857A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИПИРОЛДИОНПИРОМЕЛЛИТИМИДА | 1966 |
|
SU214803A1 |
| Способ получения полиамидобензимидазолов | 1985 |
|
SU1381948A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИИМИДОАЗОПИРРОЛОНОВ | 1970 |
|
SU268645A1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ i иИБ^И^СГ | 1971 |
|
SU299520A1 |
| ЗАМЕЩЕННЫЕ 4-ФЕНИЛАЗОФТАЛОНИТРИЛЫ И ПОЛИМЕРЫ С НЕЛИНЕЙНЫМИ ОПТИЧЕСКИМИ СВОЙСТВАМИ, СОДЕРЖАЩИЕ ЭТИ ФРАГМЕНТЫ В БОКОВОЙ И ОСНОВНОЙ ЦЕПИ ПОЛИМЕРА | 2007 |
|
RU2369597C2 |
| ВПТБ | 1973 |
|
SU397526A1 |
| Способ получения полибензимидазолимидов | 1973 |
|
SU502912A1 |

О
1 ч .С-Ж4- MH-c;
Аг:/ Jn
Hood соон
.
Введение в полимеры спирановых и сложноэфирных группировок между участками сопряжения обусловливает их растворимость в крезолах, фенолах, пиридине и т. п. растворителях. Сложноэфирные связи являются наиболее слабыми, однако, введение имидазопирролоновых структур в макромолекулу повышает термостабильность полимера по срав и
-fAr-N/SA/ r N-l ПИ)
L г-/ f/ -JT
(ПАБ)
нению с известными полиэфирами на 50- 70°С.
Полимеры с объемными боковыми заместителями (фенильными или нафтильными) имеют высокую термостабильность - температура
начала разложения в пределах 470-500°С, что лишь на 5-10% ниже соответствующих незамешенных аналогов, и в то же время обладают растворимостью в диметилформамиде, диметилсульфооксиде, лг-крезоле и т. п. растворителях, из которых они способны образовывать пленки.
Полимеры, полученные по предлагаемохсу способу, могут применяться в качестве пленок, волокон, пенопластов, прессрвочных изделий, покрытий, связующего для .слоистых пластиков и т. п.
Получают также полимеры смешанной имид;0 -nH2N-Ar-NH2+n Аг и имида.: опирролоновой структуры путем конденсации указанных выше бас-продуктов СО;смесью ароматических ди- и тетраминов.
Этот способ позволяет снизить расход дорогостояш:их тетраминов путем использования довольно доступных диаминов. Количество вводимого диамина варьируется от 5 до 95% от общей загрузки.
Таким образом, получают сополимеры по следующей схеме:
HoNNHo
а NH,
В-л «
У
-шд.
Af-NH-C
ноо
COQh HjW
2n
Rn Rn
Rn RI, 0
iN-Ar-
- сополимер; где Аг -
АгR CH2, О, отсутствует; ArloT,
, О, отсутствует.
Дальнейшая модификация свойств ПАБ и ПИ достигается синтезом полимеров при использовании бисаддуктов совместно с диангидридами нафталинтетракарбоновой, пиромеллитовой, бензофенонтетракарбоновой, дифенилоксидтетракарбоновой и других кислот.
Этот метод позволяет варьировать термические, абляционные и электрические свойства. Соотношение диангидридов изменяется от 0,01 : 1 до 1 : 0,01.
В качестве второго компонента для синтеза ПАБ используют 3,3-диаминобензидин,
3,3,4,4-тетраминодифенилметан, 3,3,4,4-тетрамииодифениловый эфир, 1,4,5,6-тетраминонафталин, 1,2,4,5-тетраминобензол, а также их
солянокислые соли.
В синтезе ПИ используют следующие диамины: фенилендиамины, бензидин, 3,3-диаминодифенил-4,4-диаминодифениловый эфир, 4,4-диаминодифениламин, диаминонафталины,
1,4-диаминоантрацен, а также их солянокислые соли.
Структура синтезированных полимеров идентифицирована по элементарному составу и
изучению их ИК-спектров. При переходе от ПАК или ПААК к циклизованным полимерам исчезают полосы поглощения, характерные для ОН и NH связей при 2900 и 3400 CM-I, появляются полосы третичного азота при 1565 и
1380 см-, исчезает поглощение амидного карбонила при 1665 см-, появляется интенсивное поглощение С О группы при 1780 см-. Подобные изменения отмечены для известных ПИ и ПАБ, а также для модельных соединеНИИ.
Термостойкость получаемых ПИ и ПАВ повышается благодаря ароматизации бисаддуктов до или в процессе поликонденсации. В последнем случае поликонденсацию проводят в
среде полифосфорной кислоты.
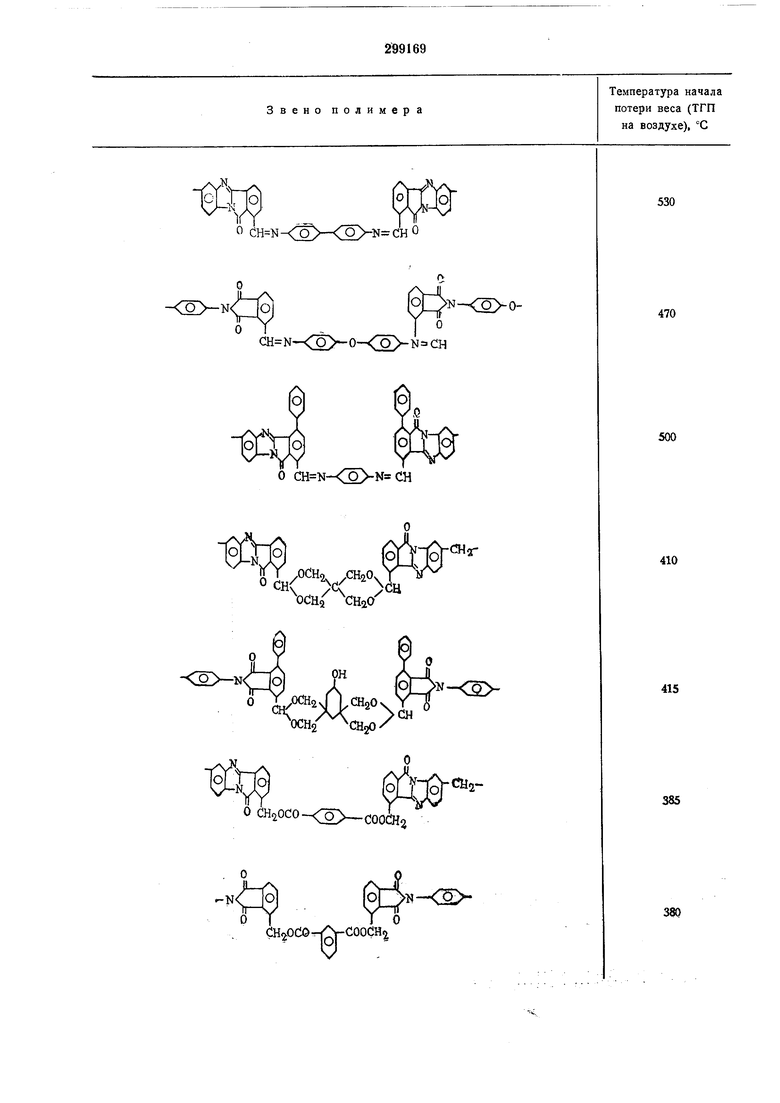
Данные о термостойкости полученных полимеров приведены в таблице.
Звено полимера
Температура начала
потери веса (ТГП
на воздухе), °С
530
СН
4 |о| S o470
500
о По
5 г оси, СН.О
ОСЕ( снао ЬсШаО ° оснг снзо/
о CH oco-xfo
, о
- ч/ Чх |Г
о тТо
CH OCO-r gj-COOCH
СНг
410 о
CHj385
-СООСНз
(380.
Звено полимера
Продолжен ч е
Температура начала
потери веса (ТГП
на воздухе), °С
470
460
510
480
460 О tiSl о Г 101 сн №ко |я а:13
Пример 1.5 ммоль I
;АГ---Н)
и 5 ммоль свободного основания 3,3,4,4-тетраминодифенилметана в 70 мл диметилсульфоксида (ДМСО) нагревают 18 час в атмосфере аргона при 75°С. Раствор высаживают в абсолютный метанол, осадок отфильтровывают, промывают метанолом и сушат при 60°С в вакууме 10 мм рт. ст. Получают 78% ПАЛК
CH N-N CH
299169
14
Для ПИ (с исходными Аг и Аг) выход 58%, т)-:0,24.
Найдено, %: С 73,2; Н 3,42; N 8,54.
Рассчитано для С42Н24М4Об, %: С 74,11; 74,11; Н 3,55; N 8,23.
П р и м е р 4. 5 ммоль I
, .)
И 5 ммоль солянокислой соли бензидина получают по методике примера 2. Для ПИ (с исходными Аг и Аг) выход 64%, ,23.
Найдено, %: С 76,3; Н 4,22; N 8,84.
Рассчитано для C42H24N4O4, %: С 77,7; Н 3,73; N 8,64.
Пример 5. К5 ммоль I
-; )
Найдено, %: С 66,3; Н 5,03; N 12,94.
Рассчитано для Сз7Нз2МбОб, %: С 67,6; Н 4,87; N 12,8.
Термообработка ПААК при 300°С в вакууме 10-5 Мм рт. ст. приводит к ПАБ, выход 94%.
Найдено, %: С 76,9; Н 3,14; N 14,87.
Рассчитано для CsyHjgNgOs, %: С 76,5; Н 3,44; N 14,5.
Характеристическая вязкость ,34.
Пример 2. 5 ммоль I
(Аг
в 30 мл ДМСО за 2 час при 65°С добавляют 4,95 ммоль 3,3,4,4-тетраминодифенилметана в 20 мл ДМСО в токе аргона и нагревают смесь 18 час. Продукт высаживают в абсолютный метанол, промывают и получают ПААК (с исходными Аг и Аг), выход 86%, in 0,28.
Найдено. %: С 72,6; Н 4,96; N 9,27.
Рассчитано для C55H4oN6O6, %: С 73,14; Н 4,8; N 9,15.
П.агреванием ПААК при 300°С в вакууме 10- мм рт. ст. получают ПАБ, вы.ход 96%, ,34.
Найдено, %: С 79,8; Н 3,74; N 10,8.
Рассчитано для С55Нз21 бО2, %: С 77,6; Н 3,55; N 10,6.
Пример 6. Из 5 ммоль I
и 5 ммоль тетрахлоргидрата диаминобензидина в 50 мл ПФК нагревают 16 час при 200°С в токе аргона. Охлажденный до 90°С раствор высаживают в воду, осадок промывают на фильтре горячей водой, раствором углекислого аммония и снова водой до нейтральной реакции. После термообработки по методике примера 1 получают ПАБ (с исходным Аг и Аг), выход 92%.
Найдено, %: С 78,98; Н 3,51; N 13,62.
Рассчитано для С42Н22НбО2, %: С 78,49; Н 3,45; N 13,08. ,44.
Пример 3. 5 ммоль 1 ) и 5 ммоль 4,4-диаминодифенилового эфира обрабатывают по методике примера 1 и получают ПАК (с исходными Аг и Аг), выход 72%, ,18.
(Аг -jAv Ph)
и тетрахлорида 3,3-диаминобензидина по методике примера 2 получают ПАБ (с исходными Аг и Аг), выход 79%, ,44.
Найдено, %: С 79,8; Н 4,02; N 10,34.
Рассчитано для С54НзоНбО2, %: С 81,6; Н 3,78; N 10,58.
П р и м е р 7. 10 ммоль П и 10 ммоль 3,3,4,4-тетраминодифенилового эфира обрабатывают по методике примера 1, получают ПААК (с исходными Аг и Аг), выход 72%, ,38. Найдено, %: С 67,2; Н 4,42; N 9,24. Рассчитано для C34H24N4O7, %: С 68,0; Н 4,0: N 9,34. 1516Найдено, %: С 78,1; Н 3,17; N 10,87.Найдено, %: С 73,9; Н 4,62; N 3,56.
Рассчитано для Сз4Н1бМ4Оз, %: С 77,3;НРассчитано для CsoHssNjOg, %: С 74,1; Н
3,03; N 10,6.4,7; N 3,46.
Пр им ер 8. 10 ммоль IIПример 13. Из 5 ммоль IV и 10 ммоль тетрахлоргидрата диаминобензидина обрабатывают по методике примера 2 и получают НАБ (с исходными Аг и Аг), выход 000/ r,nfi9 Н°айдено f С 81 1- Н 3 34- N 8 РяссчитанГлля С ЛпМ.а о г 81 f Н ,4 мпТч oa2oiN402. /0. С 81,е, П 0,-t, i ,ОО. Прим ер 9. Из 5 ммоль II . ( А/, Н) и 5 ммоль солянжислой соли «-(};енилс: диамина плоучают по методике 2 ПИ, выход bo/0, nj ,, . ,„ .., . „о Наидено, %: С 822; Н 4 16; N 4,32 Рассчитано для С48НзоН2О4, %: С 82,5; Н 4,3; N 4,01. Примерю. 2 моль II Сн сн ili I 30 ( Ах нафтип и 2 ммоль солянокислого 3,3-диаминобензидина обрабатывают по методике примера 2 и по-35 лучают ПАБ (с исходными Аг и Аг), выход 83%, л 0,28. Найдено, %: С 84,8; Н 4,34; N 6.52. Рассчитано для Сб2НзбМ40г, %: С 85,7; Н 4,15; N 6,45.40 Пример 11. 10 ммоль IV , / ( , ) , ..-с д. и 10 ммоль 1,4,5,6-тетраминонафталина обрабатьшают по методике примера 1 и получают ПААК, выход 72/о, Tij-0,49. Найдено, %:C604;H5,52;N9,15 Рассчитано для СззН28Н401о, %: С 61,8; НCQ 4ОО. м о 7С ,38, N8,75. После термообработки ПААК получают соответствующий ПАБ, выход 98%,, ,76. Найдено, %: С 69,3; Н 3,8; N 10,4. Рассчитано для C33H2oN4O6, %: С 69,7; Н 3,52; N 9,85. При мер 12. Из 5 ммоль IV ,/ (Т1 М ) /ч 60 ОН
299169 20 ( ) .. i г. ч г | тетрахлоргидрата 1,2,4 5-тетрамиыобензола по методике примера 2 получают «7%, h 0,93. Найдено, %: С 74,3; К 3,18; N 7,68. Рассчитано для С4бН25Н4О7, %: С 74,1; Н т ОС. М 7 Ц9 .do, IN /,йл П р и м е р 14. 10 MMO.ib III -.() j „„g. свободного основания З.З-диаминобензидина обрабатывают по методике при. j получают ПААК, выход 72%, TI :о 39 х, А /и, L и Найдено, %: С 67,14; Н 4,62; N 8,51. Рассчитано для Сз8Н28Ы4О8, %: С 68,4; Н 4,15; N 8,33. После термообработки ПААК дает соответствующий ПАБ, выход 79%, ,49. Найдено, %: С 76,4; Н 3,72; N 9,48. Рассчитано для C38H2oN4O4, %: С 76,5; Н 3,35; N 9,38. П р им ер 15. Из 10 ммоль III (.О ) JQ солянокислого толидина по методике примера 1 получают ПИ, выход 88%, hi 0,38. Найдено, %: С 75,75; Н 4,18; N 4,59. Рассчитано для С4оН2бН2Об, %: С 76,1; Н 4 13-N4 45 пример 16. Из 2 ммоль V и 2 ммоль 3,3,4,4-тетраминодифенилового эфира по ме примера 1 получают ПААК, выход йЯо/„ О LlJ Jt JНайдено, %: С 65,15; Н 6,45; N9,34. Рассчитано для C32H36N4O7, %: С 65,3; Н 6 12-N 9 52 термообработка ПААК дает ПАБ, выход 97% Найдено, %: С 75,1; Н 5,03; N 10,68. Рассчитано для C32H28N4O3, %: С 74,4; Н 5,42; N 10,8. Пример 17. Из 2 ммоль V и 2 ммоль солянокислого 3,3-диаминобензидина по методике примера 2 получают ПАБ, выход 84%, ,72. Пример 18. Из 2 ммоль V и 2 ммоль солянокислого бензидина по методике примера 2 получают ПИ, выход 92%, т Найдено, %: С 75,7; Н 5,61; N 5,69. Рассчитано для Сз2ПзоН2О4, %: С 5,92Уы б .ЬзГ .92- N 5 БЯ. Пример 19. 0,25 ммоль (0,53 г) 3,3-диами1 i р п 1V1 с р 1 о/. U, нобензидина, 0,25 ммоль (0,5 г) 4,4-диаминонобензидина, 0,25 MIV TTHfhPHMnnnnrn аЛнпя в 23,7 МЛ диметилацетдифенилового эфира J„ атмосфере амида нагревают в аргона до 75°С и к реакционной смеси добавляют 0,5 ммоль I S Ar Ph) и продолжают нагревание 18 час. Далее по методике примера 1 получили ПААК и ПАК, выход 79%, ,25. После дегидратации форполимера получают сополимер смешанной имидной и имидазопирролоновой структуры, выход 84%, ,32. Пример 20. 0,1 ммоль тетрахлоргидрата 3,3-диаминобензидина, 0,4 ммоль солянокислого бензидина и 0,5 ммоль И П р и м е р 24. 0,1 ммоль I (Аг ) , 0,4 ммоль диангидрида 1,4,5,8-нафталинтетракарбоновой кислоты и 0,5 ммоль тетрахлоргидрата 3,3-диаминобензидина обрабатывают по методике примера 2 и получают соответствующий поли (ароиленбисбензимидазол), выход 86%, Ы 1,2. Предмет изобретения 1. Способ получения гетероциклических полимеров путем взаимодействия ароматических диаминов и(или) тетраминов с диангидридами ароматических тетракарбоповых кислот, отличающийся тем, что, с целью расширения ассортимента термостабильных полимеров, в качестве диангидридов используют ароматизованные бисаддукты реакции малеинового ангидрида с бисфурановыми соединениями общей формулы:
- Al- ,
обрабатывают по методике примера 2 и получают сополимер имидной и имидазопирролоновой структуры с выходом 72%, т)0,18. Пример 21. 0,48 ммоль тетрахлоргидрата 3,3-диаминобензидина, 0,02 ммоль солянокислого бензидина и 0,5 ммоль II
i .)
(АгС О
0
30
или
35
обрабатывают по методике примера 2 и получают соответствующий сополимер, выход 83%, л 0,42.
Пр имер 22. 0,4 ммоль I45
(Ar -;АГ н) 0,1 ммоль диангидрида 1,4,5,8-нафталинтетракарбоновой кислоты и 0,5 ммоль тетрахлоргидрата 3,3-диаминонафталина обрабатывают по методике примера 2 и получают поли(ароиленбисбензимидазол), выход 87%, ,74. Пример 23. 0,25 ммоль I
; )
(AY 0,25 ммоль диангидрида
или
ОСЕ./CH2U.
R:; н-СН
ОСН2СН2,0 3,34,4-тетраминодигде А - арилен, например фенилен, нафтилен, дифенилен, 3,3-диметилдифенилен, дифениленметан, дифениленоксид, дифениленсульОО||| фон или СНгО-С-В-С-О-СНа-, 19 R - атом углерода или четырехвалентный 1,1,3,3-радикал циклогексанола-5- или циклогексанона-5;Г -арилен, например фенилен, нафтилен, антрилен, дифенилен, диметилдифенилен, ди-5 фениленметан, дифениленоксид, дифениленсульфон, дифениленамин;ч Д1 - фенил, Д2 - арил. 20 2. Способ по п. 1, отличающийся тем, что в реакционную систему вводят смесь ароматизированного бисаддукта и диангидрида тетракарбоновой кислоты, выбранной из групиы, состоящей из пиромеллитовой 1,4,5,8-нафталинтетракарбоновой, 3,4,9,10-перилентетракарбоновой, 3,3,4,4-бензофенонтетракарбоновой, 3,3,4,4-дифенилоксидтетракарбоновой кислот.

Авторы
Даты
1971-01-01—Публикация