Изобретение касается способа получения сложных эфиров, имеющих ненасыщенную связь в спиртовом алкиле и находящих различное применение в полимерной промышленности.
Известен промышленный способ получения аллиловых эфиров карбоновых кислот, например диаллилфталата, путем этерификацин соответствующей кислоты и аллиловых спиртов при нагревании в присутствии кислых катализаторов, например серной кислоты, /г-толуолсульфокислоты, и азеотропного агента - ароматического углеводорода или диаллилового эфира,-в значительной мере подавляющего этерификад-ию исходного спирта в простой эфир.
Иногда процесс этерификации проводят в атмосфере сернистого ангидрида. Это позволяет облегчить очистку получаемого эфира, поскольку предупреждается образование окрашенных примесей, появляющихся вследствие протекания побочных реакций.
Целевой эфир выделяют обработкой реакционной массы раствором щелочи или соды (для нейтрализации кислого катализатора и моноэфиров, если в качестве исходной кислоты берут дикарбоновую кислоту) с последующими сепарацией, фильтрованием, высушиванием и ректификацией.
Как видно, в известном способе применяют сложную переработку реакционной смеси для выделения целевого эфира.
С целью упрощения процесса предлагается проводить переэтерификацию аллилацетата и метилового или этилового эфира соответствующей кислоты в присутствии алкоголятов металлов I-III групп периодической системы или их смеси, или комплексных солей алкоголятов металлов при температуре не выше температуры кипения реакционной смеси. Этот способ исключает длительную переработку реакционной массы. Целевой эфир выделяют путем его отгонки или другим подходящим приемом непосредственно из реакционной смеси. Получаемые эфиры не содержат как металлосодержащих соединений, так и других примесей, придающих нежелательную окраску.
После отгонки целевого эфира от катализатора последний можно использовать повторно, что снижает затраты.
зующимся метил- или этилацетатом. В кубе после отгонки остается бесцветный целевой аллиловый эфир, не содержащий вредных примесей.
Предлагаемым способом могут быть получены аллиловые эфиры самых различных карбоновых кислот, например:
аллиловые эфиры таких насыщенных алифатических или циклоалифатических карбоковых кислот, как пропионовая, масляная, изомасляная, валериановая, изовалериановая, пивалиновая, капроновая, 2-метилвалериановая, изокапроновая, диэтилуксусная, диметилэтилуксусная, трег-бутилуксусная кислота; метилизопропилуксусная, энантовая, изопентилуксусная, каприловая, этилбутилуксусная, пеларгоновая, каприновая, ундециловая, лауриновая, тридециловая, миристиновая, пентадециловая, пальмитиновая, маргариновая, стеариновая, щавелевая, малоновая, янтарная, глутаровая, метилянтарная, этилмалоновая, диметилмалоновая, адипиновая, пимелиновая, пробковая, азелаиновая, себациновая, ундекандикарбоновая, додекандикарбоновая, гексагидробензойная, циклогександикарбоновая, эндометилциклогександикарбоновая кислота и т. д.;
аллиловые эфиры замещенных алифатических, циклоалифатических и арилалифатических моно- и поликарбоновых кислот, заместителями у которых могут быть, например, атом галогена, простые эфирные и тиоэфирные группы или арильные остатки, папример фенильный остаток, к подобным кислотам относят следующие: хлоруксусная, дихлоруксусная, трихлоруксусная, бромуксусная, 2-хлорнропионовая, 3-хлорпропионовая, 2хлормасляная, 6-хлоркапроновая, 6-бромкапроновая, а-хлорциклогексанкарбоновая, метоксиуксусная, этоксиуксусная, дигликолевая, тиодигликолевая, фенилуксусная, дифенилуксусная кислота и др.;
аллиловые эфиры таких ненасыщенных алифатических циклоалифатических или арилалифатических моно- и поликарбоновых кислот, как акриловая, метакриловая, кротоновая, винилуксусная, олеиновая, линолевая, сорбиновая, тетрагидробензойная, коричная, малеиновая, фумаровая, метиленянтарная, эндометиленциклогексендикарбоновая, тетрагидрофталевая кислота и др.;
аллиловые эфиры таких ароматических моно- и поликарбоновых кислот, как бензойная, о-толуилкарбоновая, п-толуилкарбоновая, ж-толуилкарбоновая, 4-трег-бутилбензойная, -нафталинкарбоновая, р-нафталинкарбоновая, изофталевая, терефталевая кислота и т. п.;
аллиловые эфиры угольной кислоты.
В качестве катализатора могут быть использованы метилаты лития, натрия, калия, магния, кальция, алюминия, этилат магния, аллилат магния, литиймагнийметилат, литийкальцийметилат, литийборметилат, литийалюминийметилат, натриймагнийметилат, натрийкальцийметилат, натрийборметилаг, натрийалюминийметилат, калиймагнийметилат, калийкальцийметилат, калийборметилат, калийалюминийметилат, кальцийборметилат, кальцийалюминийметилат, магнийборметилат, магнийалюминийметилат и др.
Применяемый в процессе катализатор растворяют или суспендируют в эфирной смеси в количестве 0,1-10 вес. % по отношению к
количеству исходных компонентов. Поскольку катализаторы не растворимы в реакционной смеси при комнатной температуре, то они могут быть отделены от нее после окончания взаимодействия механическим путем и вновь
использованы для новой реакции или же регенерированы после редистилляции аллилового эфира в виде кубового продукта, который без переработки может быть направлен на следующую операцию взаимодействия исходных компонентов.
Этерификацию можно осуществлять периодически или непрерывно. Периодический способ этерификации целесообразно проводить следующим образом. В реакционный сосуд
помещают сложпоэфирпые компоненты и катализатор и реакционную смесь нагревают при перемешивании и температуре кипения. С помощью подсоединенной колонки непрерывно отгоняют метилацетат или этилацетат
по мере того, как он образуется в процессе реакции, причем отгонку ведут до полного превращения всего количества использованного метилового или этилового эфира. Полученный аллиловый эфир карбоновой кислоты
отделяют с помощью простой редистилляции после отгонки не вступивщего в реакцию избыточного количества аллилацетата. В некоторых случаях отгонку ведут после предварительного отделения нерастворимой части катализатора. Катализатор, представляющий собой осадок на фильтре или кубовый остаток, используют снова на следующей стадии этерификации. При осуществлении переэтерификации непрерывным способом взаимодействие компонентов можно производить в каскадно расположенных емкостях или в колонне для дистилляции. Исходную сложноэфирную смесь, содержащую катализатор, непрерывно подводят в подходящее место колонны так, чтобы из головной части ее непрерывно можно было отбирать образующийся при реакции метилацетат или этилацетат, а из нижней части колонны - образующийся аллиловый
эфир, избыточный аллилацетат и катализатор. Отделение аллилацетата, редистилляцня образовавшегося аллилового эфира и отделение катализатора могут быть произведены непрерывно на колонках, подключенных последовательно к колонне для переэтерификации .
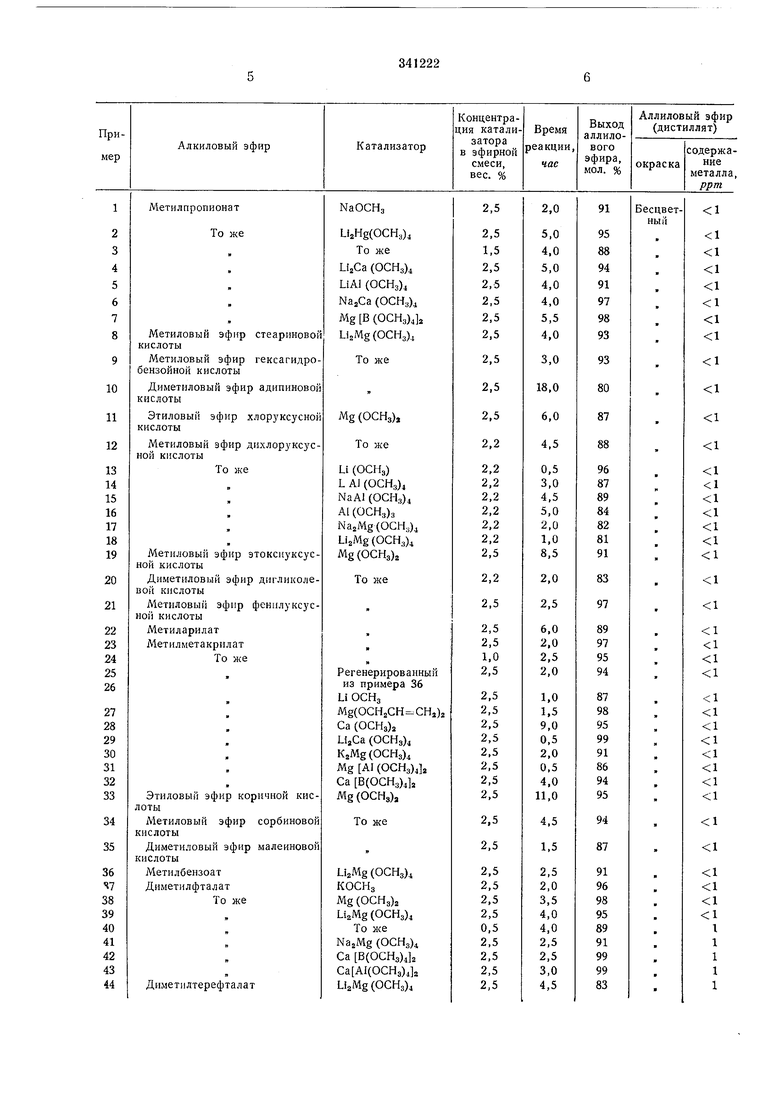
гревающейся колонкой Вигройкса (длина 30 см, ширина просвета 2 см). В реакционный сосуд загружают 1,5 моль аллилацетата и 0,5 моль метилового или этилового эфира монокарбоновой кислоты соответственно 0,25 моль метилового или этилового эфира дикарбоновой кислоты. Соотношение эквивалентов аллилацетата и эфира моно- или дикарбоновой кислоты составляет 3:1. К сложноэфирной смеси добавляют катализатор в количестве, необходимом для получения иужной концентрации (см. таблицу).
Содержимое колбы нагревают до кипения и как только в головной части колонки устанавливается температура кипения метилацетата (57°С) или этилацетата (77°С), отбирают дистиллят в таком количестве, чтобы температура в головной части колонки не превышала 65°С (в случае использования метилового эфира) и 80°С (в случае использования этилового эфира). Для завершения реакции отгонку продолжают до температуры кипения аллилацетата (104°С).
Дистиллят и кубовый остаток анализируют с помошью газовой хроматографии и из полученных данных определяют выход аллилового эфира по отношению к использованному количеству метилацетата или этилацетата. После отгонки избытка аллилацетата выделяют фракцию аллилового эфира карбоновой кислоты в чистом виде (в некоторых случаях в вакууме). Перегнанный эфир исследуют на
содержание в нем металла. Результаты приведены в таблице. Под временем реакции, указанным в таблице, надо понимать время от начала дистилляции до достижения температуры кипения аллилацетата.
Пример 45. Используют в качестве алкилового эфира аллилацетат и диэтиловый эфир угольной кислоты (молярное соотношение 3:1).
В качестве катализатора применяют 2,5 вес. % М§(ОСНз)2, время реакции 9 час. Выход диаллилового эфира угольной кислоты (в расчете на использованное количество эфира угольной кислоты) 89 мол. %. Поеле перегонки получают чистый бесцветный диаллиловый эфир с т. кип. 87°С/40 мм рт. ст., который не содержит следов металла.
Предмет изобретения
Способ получения аллиловых эфиров алифатических, циклоалифатических, ароматических и угольной кислот, отличающийся тем, что, с целью упрощения процесса, аллилацетат подвергают взаимодействию с метиловым или этиловым эфиром соответствующей кислоты при температуре не выше точки кипения реакционной смеси в присутствии алкоголята металла I-III групп периодической системы
или их смеси, или комплексных солей алкоголятов металлов с последующим выделением целевого эфира известными приемами.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АРИЛОВЫХ ЭФИРОВ | 1969 |
|
SU232838A1 |
| СПОСОБ ПОЛУЧЕНИЯ АРИЛОВЫХ ЭФИРОВ | 1968 |
|
SU208569A1 |
| СПОСОБ ПОЛУЧЕНИЯ АРИЛОВЫХ ЭФИРОВ | 1966 |
|
SU186345A1 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНОСИЛАНОВ | 1972 |
|
SU336876A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,2-ДИЗАМЕ1ЦЕННЫХ ЦИКЛОАЛКАН-1,3- | 1973 |
|
SU376933A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЛИЛАЦЕТАТА | 1972 |
|
SU353408A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОИДАНГИДРИДОВ Ы-ЗАМЕЩЕННОЙ АЦИЛКАРБАМИНОВОЙ КИСЛОТЫ | 1971 |
|
SU307566A1 |
| СПОСОБ ПОЛУЧЕНИЯ НЕНАСЫЩЕННЫХ ЭФИРОВ КАРБОНОВЫХ КИСЛОТ | 1972 |
|
SU340157A1 |
| СПОСОБ ПОЛУЧЕНИЯ АНГИДРИДА р-АЦЕТОКСИПИВАЛИНОВОЙ КИСЛОТЫ | 1972 |
|
SU345673A1 |
| СПОСОБ ПОЛУЧЕНИЯ U-ЗАМЕЩЕННЫХ БЕНЗОИНОВи | 1972 |
|
SU334681A1 |


Авторы
Даты
1972-01-01—Публикация