Температура реакции зависит от исходных реагентов и может варьироваться от 20°С до температуры кипения растворителя.
Для получения соединения формулы I, где RI - оксиалкил, целесообразно исходить из соответствующих 1-ацилоксиалкил-,2,3,4,5-тетрагидро-1Н-1,5-бензодиазепин-4-дионов и затем отщеплять при окислении ацильную группу.
Соединения формулы I, где Ri - водород, могут быть алки ированы обычным образом.
Пример 1. 7-Нитро-5-фенил-1Н-1,5-бензодиазепин-2,4-(ЗН, 5Н)-дион.
65 г (0,23 моль 7-питро-5-фенил-2,3,4,5-тетрагидро-1Н-1,5 - бензодиазепин-4-она, т. пл. 24ГС, растворяют или суспендируют в 2000 .ил ацетона. В течение 15 мин по каплям добавляют раствор 120 мл чистого реактива из 40 г СгОз, 38 мл H2SO4 и 150 мл . Нагревающуюся реакционную смесь размешивают 20 мин, декантируют от соли хрома и сгущают приблизительно до 300 мл. Остаток выливают в 500 мл воды, дают еще раз закипеть и оставляют выкристаллизовываться в ледяной бане. Выход 63,5 г (92%); т. пл. 272-274 С (ацетонитрил).
Пример 2. 1-Метил-7-нитро-5-фенил-1Н1,5-бензодиазепин-2,4- (ЗН, 5Н) -дион.
29,7 г (0,1 моль} 1-метил-7-нитро-5-фенил1Н-2,3,4,5-тетрагидро - 1,5-бензодиазепин-4-она, т. пл. 123-125°С, окисляют аиалогично примеру 1. Получают 27,6 г (88%) целевого продукта, т. пл. 178-180°С.
Пример 3. 3-Этил-7-нитро-5-фенил-1П1,5-бензодиазепин-2,4- (ЗП, 5П) -дион.
31,1 г (0,1 моль} 1-этил-7-нитро-5-фенил-1П2,3,4,5 - тетрагидро-1,5 - бензодиазепин-4-она, т. пл. 160-162°С, окисляют аналогично примеру 1. Получают 29,4 г (90%) целевого продукта, т. пл. 257-259°С.
Пример 4. 1-Изопропил-7-нитро-5-фенил1Н-1,5-бензодиазепип-2,4-(ЗН, 5Н)-дион.
32,5 г (0,1 моль} 1-изопропил-7-нитро-5-феНИЛ-1П-2,3,4,5 - тетрагидро-1,5-бензодиазепии4-она, т. пл. 170-171°С, окисляют аналогично примеру 1. Выход 28,0 г (82%), т. пл. 212- .
Пример 5. 1-Аллил-7-нитро-5-фенил-1П1,5-бензодиазепин-2,4- (ЗП, 5П) -дион.
32,3 г (0,1 моль} 1-аллил-7-нитро-5-фенил1Н-2,3,4,5 - тетрагидро-1,5 - бензодиазепин-4она, т. пл. 126-127°С, окисляют аналогично примеру 1. Выход 25,4 е (75%), т. пл. 237- 239°С.
Пример 6. 7-Хлор-1-метил-5-фенил-1П1,5-бензодиазепин-2,4- (ЗН, 5Н) -дион.
79 г (0,276 моль} 7-хлор-1-метил-5-фенил2,3,4,5-тетрагидро - 1Н-1,5-бензодиазепин-4-она, т. пл. 133-139°С, растворяют в 2000 мл ацетона и окисляют, как в примере 1. После упаривания ацетонный раствор обрабатывают метиленхлоридом, промывают водой, высущивают и упаривают до 250-300 мл. Добавляя диизопропиловый эфир, получают 68 г (82%) кристаллизата, т. пл. 179-182°С.
Пример 7. 5-фепил-7-трифторметил-1Н1,5-бензодиазепин-2,4-(ЗН, 5Н)-дион.
34,5 г (0,113 моль} 5-фенил-7-трифторметил2,3,4,5 - тетрагидро- 1Н-1,5 - бензодиазепин - 4она, т. пл. 152-153°С, растворяют или суспендируют в 300 мл ледяной уксусной кислоты и разбавляют 60 мл смеси хромовой и серной кислот. Размешивают 3 час при комнатной температуре и выливают в 3 .д воды.
Выделивщийеся сырой продукт отсасывают, промывают водой и обрабатывают метиленхлоридом. После промывки, сущки и упаривания получают при добавлении изопропилового эфира 30 г (83%) целевого продукта с т. пл.
258-260°С.
Пример 8. 5-Фенил-7-трифторметил-1Н1,5-бензодиазепин-2,4-(ЗН, 51-1)-дион.
6 г (0,02 моль} 5-фенил-7-трифторметил-2,3, 4,5-тетрагидро - 1Н-1,5-бензодиазепин - 4-опа,
т. пл. 152-153°С, растворяют в 100 мл чистого ацетона и после добавления 20 г пермаиганата калия и 30 мл воды кипятят с обратным холодильником 1 час. Отсасывают над кизельгуром, отделяют пиролюзит и упаривают фильтрат. Остаток обрабатывают метиленхлоридом и затем, как в примере 7.
Выход 2 г (32%), т. пл. 258-260°С. Пример 9. 1-Метил-5-фенил-7-трифторметил-1Н-1,5-бензодиазепип-2,4-(ЗП, 5Н)-диои.
5 г (0,016 моль) 1-метил-5-фенил-7-трифторметил-2,3,4,5 - тетрагидро-1Н - 1,5-бензодиазепип-4-она, т. пл. 91-92°С, растворяют в 200 ./ил уксусного эфира и после добавления 15 г активированной двуокиси марганца кипятят с
обратным холодильником 20 час. Отсасывают над кизельгуром, фильтрат упаривают, остаток обрабатывают метиленхлоридом и затем, как описано выще.
Выход 1,5 г (28%), т. пл. 205-206°С.
Пример 10. 1-Метил-7-питро-5-фенил-1Н1,5-бензодиазепин-2,4- (ЗН, 5П) -дион.
5 г (0,017 моль) 1-метил-7-нитро-5-фенил2,3,4,5-тетрагидро - 1Н-1,5-бензодиазепип-4-она, т. пл. 123-125°С, суспендируют в 100 мл тетрагидрофурана и кипятят с обратным холодильником 15 час в присутствии 15 г активированого пиролюзита. Затем смесь отсасывают, фильтрат частично выпаривают в вакууме и обрабатывают, как обычно. Выход 2,1 г
(40%); т. пл. 178-180°С.
Пример 11. 1-р-Ацетоксиэтил-7-хлор-5фенил-1Н-1,5 - бензодиазепин-2,4-(ЗН, 5Н)-дион.
17,9 г (0,05 моль} р-ацетоксиэтил-7-хлор-5фенил-1Н-2,3,4,5 - тетрагидро -1,5 - бензодиазепин-4-она окисляют аналогично примеру 10. Из уксусноэфирного раствора при выпаривании получают бесцветные кристаллы с т. пл. 168-170°С. Их растворяют или суспендируют
в трехкратном количестве 10%-ного метанольно-водпого раствора едкого натра и размешивают 30 мин при комнатной температуре. Затем выливают в воду, встряхивают с метиленхлоридом и получают после выпаривания метиленхлоридной фазы и перекристаллизации
остатка из этанола 5 г (33%) соединения с т. пл. 210°С.
Пример 12. 1-Метил-7-нитро-5-фенил-1Н1,5-бс 130диазепин-2,4-(ЗН, 5Н)-дион.
40 г (0,13 моль} 7-нитро-5-фенил-1Н-1,5-бензодиазепин-2,4-(ЗН, 5Н)-диона суспендируют в 600 мл тетрагидрофурана и после добавления 6,4 г 50%-ной суспензии гидрида натрия получают раствор, в который вводят 8,5 мл метилйодида, размешивают 1 час при 45°С, добавляют 8,5 мл метилйодида и размешивают еще 1 час. В раствор добавляют несколько капель ледяной уксусной кислоты, выпаривают, остаток обрабатывают метиленхлоридом, промывают водой, высушивают метиленхлоридную фазу, выпаривают растворитель и перекристаллизовывают из смеси метиленхлорид-
диизопропиловый эфир. Выход 35 г т. пл. 179-181°С.
Пример 13. 1-Оксиэтил-7-нитро-5-феи 1л1И-1,5-бензодиазепин-2,4-(ЗН, 5Н)-дион.
20 г (0,07 моль 7-нитро-5-фенил-1Н-1,5-бе11зодиазепин-2,4-(3,5Н)-диона суспендируют в 600 мл метанола, добавляют 10 мл воды, 1 м.л тритона В и 50 мл этиленоксида, размешивают при комнатной температуре до образован1 я прозрачного раствора ( час). Раствор упаривают досуха, остаток обрабатывают метпленхлоридом и многократно встряхивают с водой. Органическую фазу высушивают, выпаривают и остаток перекристаллизовывают из этанола. Выход II г, т. пл. 187-188°С.
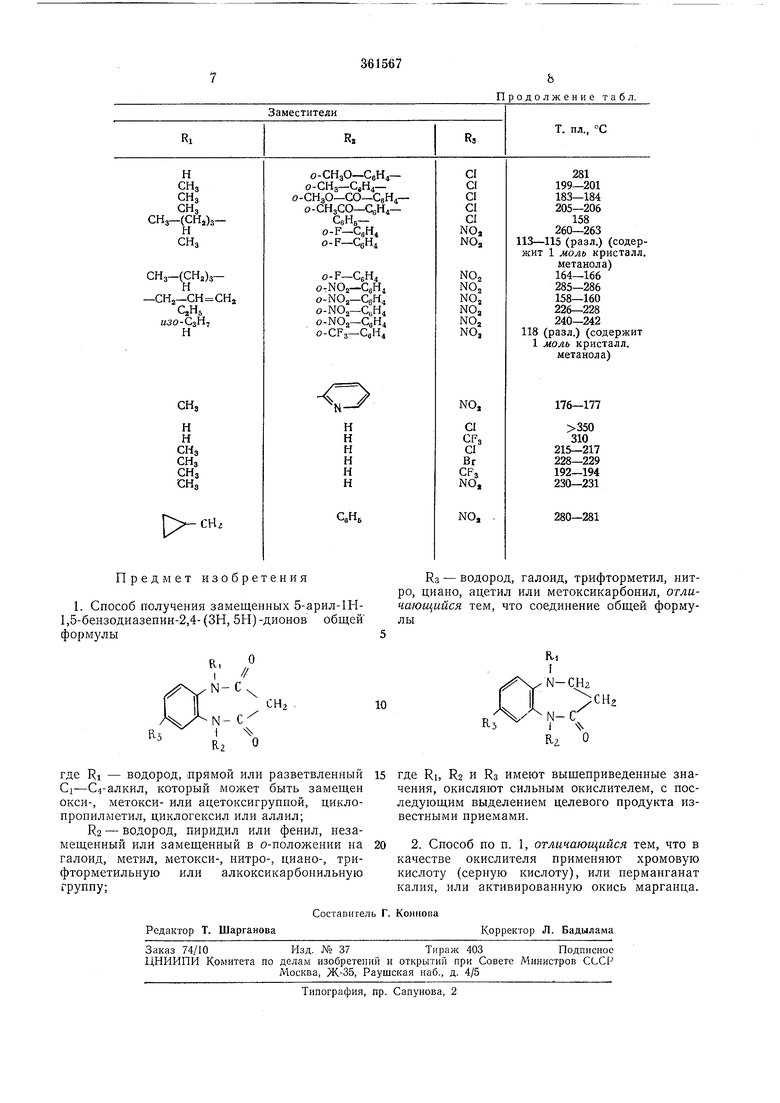
Аналогично методу, приведенпому в примерах 1 -13, получают соединения формулы I, перечисленные в таблице.
Таблица
П р о д о л ж е н и е табл.


| название | год | авторы | номер документа |
|---|---|---|---|
| ВПТБ10Й €51Д;Г.ТГ;!Г?5Т?ЯШ145ИСП511 | 1973 |
|
SU374825A1 |
| Способ получения 5-арил-(или гетероарил)-3-окси 1н-1,5-бензодиазепин-2,4-(3н,5н)-дионов | 1972 |
|
SU460627A3 |
| Способ получения 5-арил-(или гетероарил)-3-окси-1н-1,5-бензодиазепин-2,4(3н,5н)-дионов | 1972 |
|
SU465791A3 |
| Способ получения 5-арил-/или гетероарил/ -3-окси-1н-1,5-бензодиазепин-2,4-/3н,5н/-дионов | 1972 |
|
SU493971A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗОДИАЗЕПИНА | 1973 |
|
SU400100A1 |
| Способ получения производных бензодиазепина | 1969 |
|
SU482947A3 |
| Способ получения /1,2/-аннелированных 7-фенил-1,4-бензодиазепинов или их солей | 1979 |
|
SU904526A3 |
| Способ получения производных 2-амино-дигидро-бензодиазепинона | 1971 |
|
SU437294A1 |
| Способ получения 1,5-бензодиазепинов | 1972 |
|
SU459889A3 |
| Способ получения производных бензодиазепина | 1969 |
|
SU598559A3 |


Авторы
Даты
1973-01-01—Публикация