.ос1
где
X - с - с, -CBjoHioC-,
о / /
BioHjo
заключающийся в том, что дитолильное производное о- пли иг-карборана подвергают окислению хромовым ангидридом в кислой среде с выделением целевого продукта известными приемами.
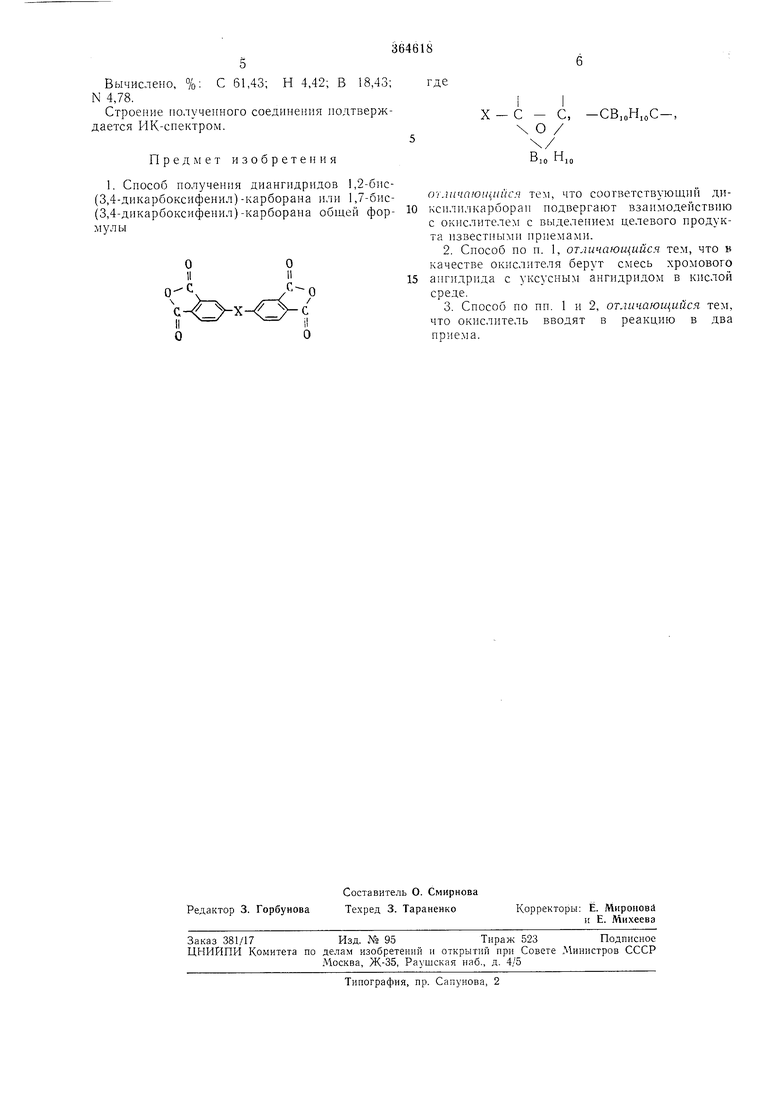
Предлагается способ получения диангидридов 1,2-бис- (3,4-дикарбоксифенил) -карборана
X - С - С, -СВюНщС-,
о /
/
BioHjo
заключающийся в том, что соответствующий диксилилкарборан подвергают взаимодействию с окислителем, преимущественно со
смесью хромового ангидрида с уксусным ангидридом в кислой среде, с выделением целевого продукта известными приемами.
Устойчивость дпксилилкарборанов к данному окислителю и кислотам позволяет применять больщой избыток окислителя, необходимый для полного окисления метильных групп. Окислитель желательно вводить в реакцию в два приема, что вызвано плохой растворимостью исходных диксилилкарборанов в реакционной среде (смесь уксусной и серной кислот), которая препятствует полному окислению. Кроме того, промежуточные продукты окпслепия ск.юппы к комплексообразоваппю с трехпалентпым хромом. Поэтому введение всеIX) избытка окислнте.чя сразу не приводит к гизлиому окие.тенню и затрудняет выделение целевого продукта.
Строение целезы.х продуктов нодтиерждг:но элементарны.-. апалпзо.м, ИК-снектрами, а также синтезом их нроизводпых --- КД -днфепнлдиимидов. По-чученные соедипенни обладают ценными свойствами, которые сделают п. 1- езамеии,мы.м11 в сн ггезе ноли.меров.
Прпмер 1. Получение диангидрпда 1,2бис- (3,4-д,икарбокс 1фенил) -карборана.
В четырехгорлую колбу емкостью 250 мл, снабженную мешалкой, обратным холодильником, капельной воронкой и термометром, загружают 6,6 г (0,02 моль) днкенлилкарборана, 100 мл ледяной уксусиой кислоты и 10 мл концентрнроваппой серпой кислоты. В канельную вороику помещают зарапее приготовленную окислительную смесь 15,8 г (0,16 моль) хромового ангидрида с 80 мл зксусного ангидрида. Затем при переменшваппи прикапывают первую порцию окислительной смесн с такой скоростью, чтобы те.мнература реакционной среды была равна 25-30°С, иосле чего реакционную массу нагревают 1,5 час на кппян,ей водяной бане. Далее реакцноппую смесь охлаждают и сиова добавляют к ней вторую порцию окислительной смеси, состоящей из 8 г хромового ангидрида (0,07 моль) и 50 мл уксусного ангидрида.
Добавив весь окислитель, реакционную массу нагревают еще 2 час на кииящей водяной бане и зате.м, не охлаждая, небольшими иорпиями выливают в большой избыток диетиллироваииой воды (расход воды 15 л на всю реакциониую смесь). Вынавший а.морфньп осадок отфильтровывают (оставлять продукт после осаждепия в воду в этой среде, более чем на 2 час не рекомендуетея, так как ири стоянии аморфный осадок становится смолообразпым, и выделение продукта возможио только экстракцией сериым эфиром), растворяют в 800 мл 1%-цого водиого раство)а едкого кали, иодкисляют концентрироваиной соляной кислотой до выпадеиия белого аморфиого осадка и оставляют па почь в холодильнике для кристаллизации. Осадок отфильтровывают па плотио.м стеклянном фильтре (№ 4), нро.мывают водой до нейтральиой реакции, затем в течение 4 час тщательио сушат в вакууме иад пятиокиеью фосфора при 60-80°С и далее прогревают в вакуу.ме (1 лг.дг рг. ст.), иостеиенно подппмая темиературу до 160°С в течение 2-3 час. Полученный продукт иерекристаллизовЕзТвают из хлорбецзола (4 мл растворителя иа 1 г продукта), отфильтровывают, промывают охлаждеины.м беизолом и сущат в вакуумном шкафу 4 час при 120°С. Высушеипый продукт возгопяют в вакууме (ох:оло мм рт. ст.) п темнерат фе 170-( РЫХОД диапгпдрида после возiOHKH 5,2 г (60% от теории). Продукт представляет собой белый кристаллический порошок, 7. ил. 248-249 С.
Пайдеш), %: С 50,12. 50,02; П 3,97, 3,93; В 24,69, 24,61.
Ci8ni60.iBio.
13ычнслено, %; С 49,51; П 3,67; В 24,80.
Строение по,:|ученпого диапгпдрида подтверждается далшы П1 МК-спектрос1сонии. 11о,1учеп 1с 1,-дифепилднимида 1,2-бис(3,4-днкарбокспфеиил) - дикарбаклозододекаГ1 о р и па.
В ;,вугорлу10 колбу е.мкостью 30 мл, снабженную барботером н газоотводной трубкой, номеи|;ают 0,44 г (0,001 .«оль) возогцаниого диаигидрида, 10 мл сухого иерегианного ацетона п к образовавшемуся раствору добавляют 0,17 мл (0,002 моль) су.хого nepernai ного аннлина. После перемешивания смеси в течение 5---10 .I/HH отгоняют ацетон, а остаток сушат 3 час в вакуумпо.м Н1кафу при 110°С.
IЬлучениый продукт перекристаллизовывают из уксуспого апгндрида (5 мл апгидрида иа 0,5 г прод,укта), отфильтровывают, нро.мывают охлажденной уксусной кислотой, иерекристаллнзо5-;ывают снова из этилового спирта (500 мл. спирта иа 0,5 г продукта) и сушат , вакуумпом шкафу при 100-liO°C. Продукт пре.дставляе1 собой сле1ка желтоватый кристаллический порошок, т. пл. 310-31 °С.
Пайдепо, %: С 60,81, 60,68; П 4,63, 4,48; В 18,29, 18,33, 4,89, 4,91. СзоП..бО.,В,„Х..
Вычисле1ю, %; С 61,43; П 4,42; В 18,43; N 4,78.
14К-сиектра иодтг ерждают строеиие
I1о л у ч е н н о го ди им я д а.
Пример 2. Получение диангидрида 1,7бис- (3,4-дикарбоксифепил) -карборана.
Окислепие 1, - (3,4-д -1карбоксифеиил)карбораиа и выделение иолучеш-юго иродукта осуи.ествляют ио примеру 1. Окисленный нродукт сразу носле в вакууме при 80°С иерекрнсталлизовывают из уксусного аигидрида (5 мл растворителя иа 1 г нродукта) и затем возгопяют в вакуу.ме по примеру 1. Выход целевого продукта 5,7 г (около 65% от теори). Продукт иредставляет собой бе,1ый кристаллический порошок, т. пл. 229- 231°С.
Пайдеио, %: С 49,75, 48,83; П 3,69, 3,72; В 24,74, 24,78. С,цП,йОбВ1о. Вычислено, %: С 49,51; П 3,67; В 24,80.
Строенне полученного диангидрида подтверждаете я ПК-спектром.
К К-днфепил. 1,7-бпс-(3,4 - дикарбокспфенил)-карборана нолучают и очнщают
но примеру 1. Целевой продукт иредставляет
собой белый ме.: кокоисталлический порошок,
т. ил. 247-248 С.
Пайдеио, °/„: С 65,60, 61,38; П 4,66, 4, 58; 15 18,07, 18.18; К 4,59,
C3on9o04B,oN.;. Вычислено, %: С 61,43; Н 4,42; В 18,43; N 4,78. Строение полученного соединения нодтверждается ИК-спектром. Предмет изобретения 1. Снособ нолучения диангидрндов 1,2-бнс(3,4-дикарбоксифенил)-карборана или 1,7-бис(3,4-дикарбоксифенил)-карборана общей формулы10 15 X - С - С, -СВ,оН,(,С о / оглачсчоишпся тем, что соответствующий диксилилкарборан нодвергают взаимодействию с окислителем с выделением целевого продукта известными нриемами. 2.Способ по п. 1, отличающийся тем, что в качестве окислителя берут смесь хромового ангидрида с уксусным ангидридом в кислой среде. 3.Способ по ни. 1 и 2, отличающийся тем, что окислитель вводят в реакцию в два приема.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АЗОТСОДЕРЖАЩИХ ЦИКЛОЦЕПНЫХ ПОЛИМЕРОВ | 1974 |
|
SU401160A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАНГИДРИДА 3,3-БИС-(3,4-ДИКАРБОКСИФЕНИЛ)ФТАЛИДА | 2018 |
|
RU2698914C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИИМИДОВ | 1972 |
|
SU412212A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭПОКСИФЕНОЛЬНЫХ ОЛИГОМЕРОВ | 1973 |
|
SU390116A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАНГИДРИДОВ АРОМАТИЧЕСКИХ ТЕТРАКАРБОНОВЫХ КИСЛОТ | 1972 |
|
SU338092A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-НИТРОНАФТАЛЕВОЙ КИСЛОТЫ | 1973 |
|
SU374287A1 |
| СПОСОБ ПОЛУЧЕНИЯ З'З", 4',4"-ДИФЕНИЛФТАЛИДТЕТРАКАРБОНОВОЙ КИСЛОТЫ | 1970 |
|
SU259073A1 |
| СПОСОБ ПОЛУЧЕНИЯ4,4- | 1967 |
|
SU192791A1 |
| ДИАНГИДРИД 1,7-БИС-{4-[4- (3,4-ДИКАРБОКСИБЕНЗОИЛ)- ФЕНОКСИ]- БЕНЗОИЛ}-КАРБОРАНА В КАЧЕСТВЕ ПЛАСТИФИКАТОРА И УПРОЧНЯЮЩЕГО АГЕНТА ПРЕСС-ИЗДЕЛИЙ ИЗ ПОЛИИМИДОВ | 1991 |
|
RU2050360C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИИМИДОВ | 1970 |
|
SU267893A1 |


Авторы
Даты
1973-01-01—Публикация